胃癌作为全球范围内高发且预后较差的恶性肿瘤之一,其治疗策略的优化一直是临床研究的重点领域。近年来,免疫治疗的兴起为胃癌治疗带来了新的曙光,尤其是在围手术期的应用更是备受瞩目。此前KEYNOTE-585研究未能达到主要终点,在2025年ASCO年会上公布了MATTERHORN研究的阳性结果。尽管两者都探索了免疫治疗在围手术期的应用,但为何机制相似、设计接近的两项研究却呈现出不同的结果?是药物本身的差异使然,还是研究设计中存在关键性的不同?中国人民解放军总医院苟苗苗教授从人群选择、化疗方案、统计设计等多个维度详细解读两项研究的差异,探讨其对胃癌围手术期免疫治疗临床实践的启示与影响,旨在为优化胃癌治疗策略提供循证依据。
日本国立癌研医院 高级访问学者
北京癌症防治学会胃癌防治青年委员会常务委员
CSCO胰腺癌、胆道癌、抗肿瘤药物安全、老年肿瘤防治专委会委员
中国研究型医院学会精准医学与肿瘤MDT专委青年委员、肿瘤外科委员会委员
中国医师协会结直肠肿瘤MDT学组委员、医工融合与智能医学学组委员
中国抗癌协会头颈肿瘤整合康复专委会委员
北京抗癌协会胃癌专业委员会常委
长期以来从事消化道肿瘤的综合治疗,以第一作者发表15余篇SCI论文
多次参与ASCO和ASCO-GI及国内会议交流
CSCO化疗安全管理大赛第一名,个人风采奖
主持一项青年成长课题,参与2项国自然课题和2项重大课题的研究,
撰写中国胆管肿瘤多学科综合治疗专家共识、2023人卫出版社《结肠癌肿瘤学》、中国胃癌肝转移诊断与综合治疗中国专家共识(2024版)
回顾——病理完全缓解率(pCR)的初步成功
在2023年ESMO上公布的数据中,两项研究均显示出免疫治疗联合化疗在提高pCR率方面的显著优势。
KEYNOTE-585研究:帕博利珠单抗联合化疗使pCR率相较于单纯新辅助化疗提升了约10%。在主队列中,pCR率提升了10.9%(12.9% vs 2.0%;95%CI 7.5~14.8;P<0.0001),而在主队列+FLOT队列中,pCR率提升了10.6%(13.0% vs 2.4%;95%CI 7.4~14.0;P<0.0001)。
MATTERHORN研究:度伐利尤单抗组的pCR率通过中央实验室评估显著高于安慰剂组,达到19% vs 7%(OR=3.08,P<0.00001),提升了12%。尽管两者在pCR方面均取得了积极结果,但后续的生存数据却呈现出不同的趋势。
KEYNOTE-585研究的曲折之路
KEYNOTE-585研究在EFS和OS方面的表现,为围手术期PD-1抑制剂的应用蒙上了一层阴影。
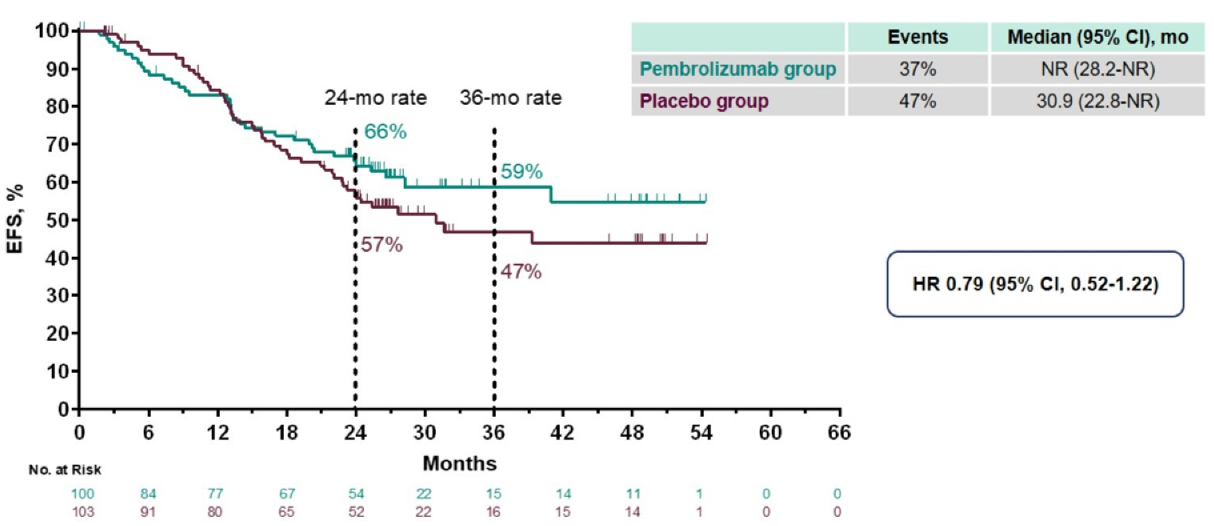
第三次中期分析:帕博利珠单抗组主队列的EFS为44.4个月,化疗组为25.3个月(HR=0.81;95%CI 0.67~0.99;P=0.0198)。尽管有获益趋势,但未能达到预设的统计学差异(预设值P=0.0178)。OS方面,主队列中帕博利珠单抗组中位OS为60.7个月,安慰剂组为58.0个月(HR=0.90),主队列+FLOT队列中,中位OS分别为60.7个月和NR(HR=0.93),两组生存曲线紧密交叉,因EFS未达标而未进行OS的统计学检测。
2024年ESMO GI最终分析:最终分析结果显示,主队列中帕博利珠单抗组和单纯化疗组的中位EFS分别为44.4个月和25.7个月(HR=0.81;95%CI 0.67~0.98)。主队列+FLOT队列中,两组中位EFS分别为47.0个月和26.9个月(HR=0.80;95%CI 0.67~0.95)。OS方面,主队列中联合治疗组和单纯化疗组的中位OS分别为71.8个月和55.7个月(HR=0.86;95%CI 0.71~1.06)。主队列+FLOT队列中,两组中位OS分别为未达到和55.7个月(HR=0.86;95%CI 0.71~1.03)。这些结果表明,尽管EFS有所改善,但在OS方面,帕博利珠单抗的加入并未带来显著优势,且生存曲线的交叉提示长期疗效的复杂性。
MATTERHORN研究的显著突破
MATTERHORN研究在EFS方面取得了突破性进展:
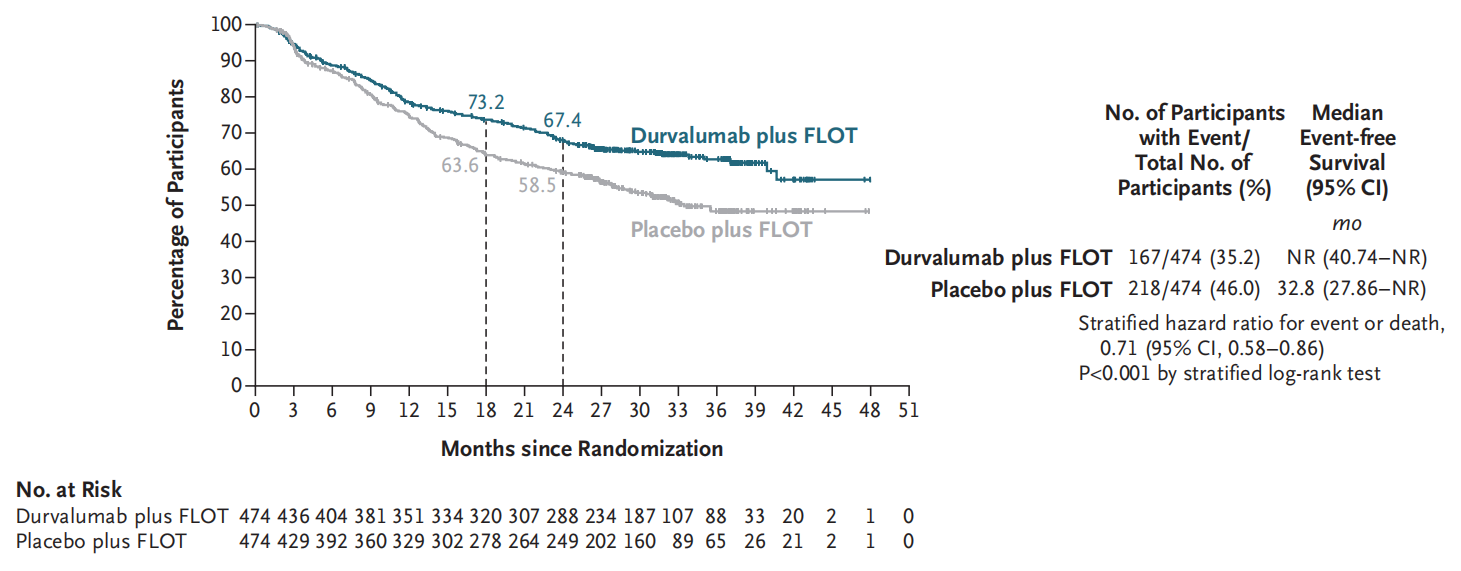
2025年ASCO公布结果:在随访31.5个月后,度伐利尤单抗联合FLOT组的EFS相较于对照组观察到显著的统计学意义改善。度伐利尤单抗联合FLOT组的EFS尚未达到,而对照组为32.8个月(HR=0.71,P<0.001)。18个月EFS率为73% vs 64%,24个月EFS率为67% vs 59%。更重要的是,各亚组均能观察到一致性的获益趋势。
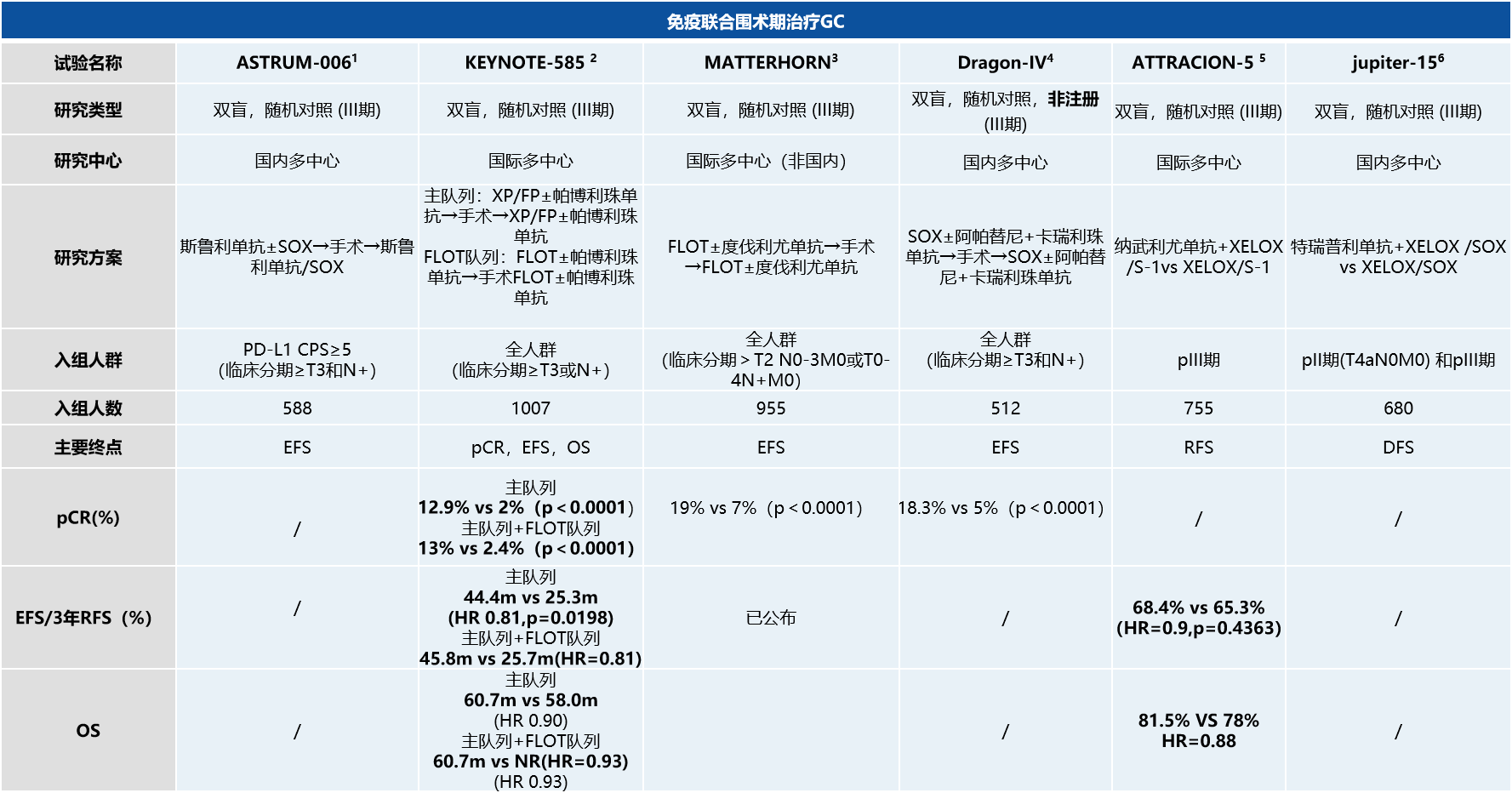
两项研究差异化解读
虽然两者都是PD-1/PD-L1通路抑制剂在围手术期胃癌中的应用,但研究设计上的细微差异可能是导致其不同结果的关键。
人群选择:
KEYNOTE-585:入组1007人,亚洲人群占比39%,PD-L1 CPS≥1的患者占73%,MSI-H占9%,75%为III期患者,GEJ(胃食管结合部)占25%,弥漫型占比40%。
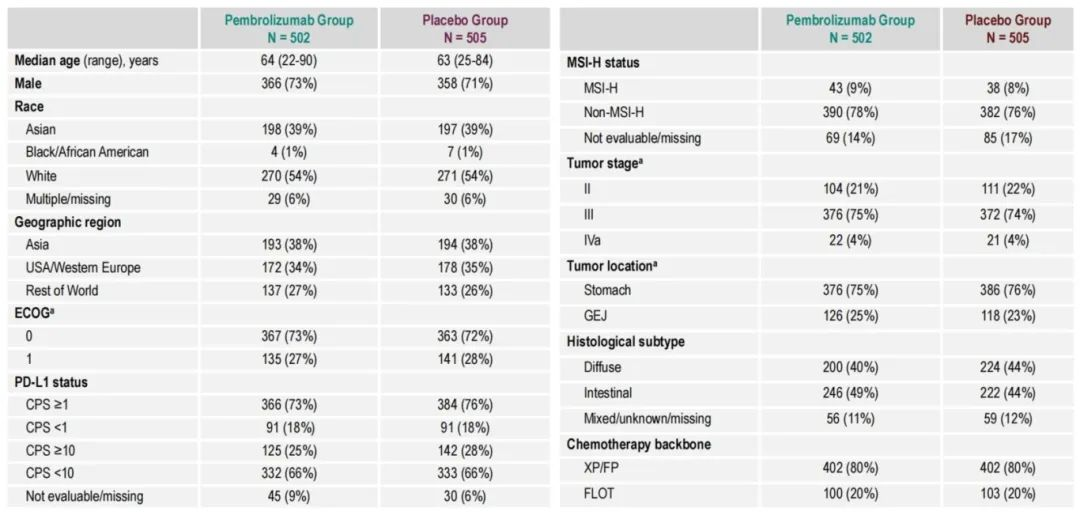
MATTERHORN:纳入948例患者,亚洲患者占比19%,GEJ占32%,PD-L1 TAP>1%占90%,弥漫型占27%。
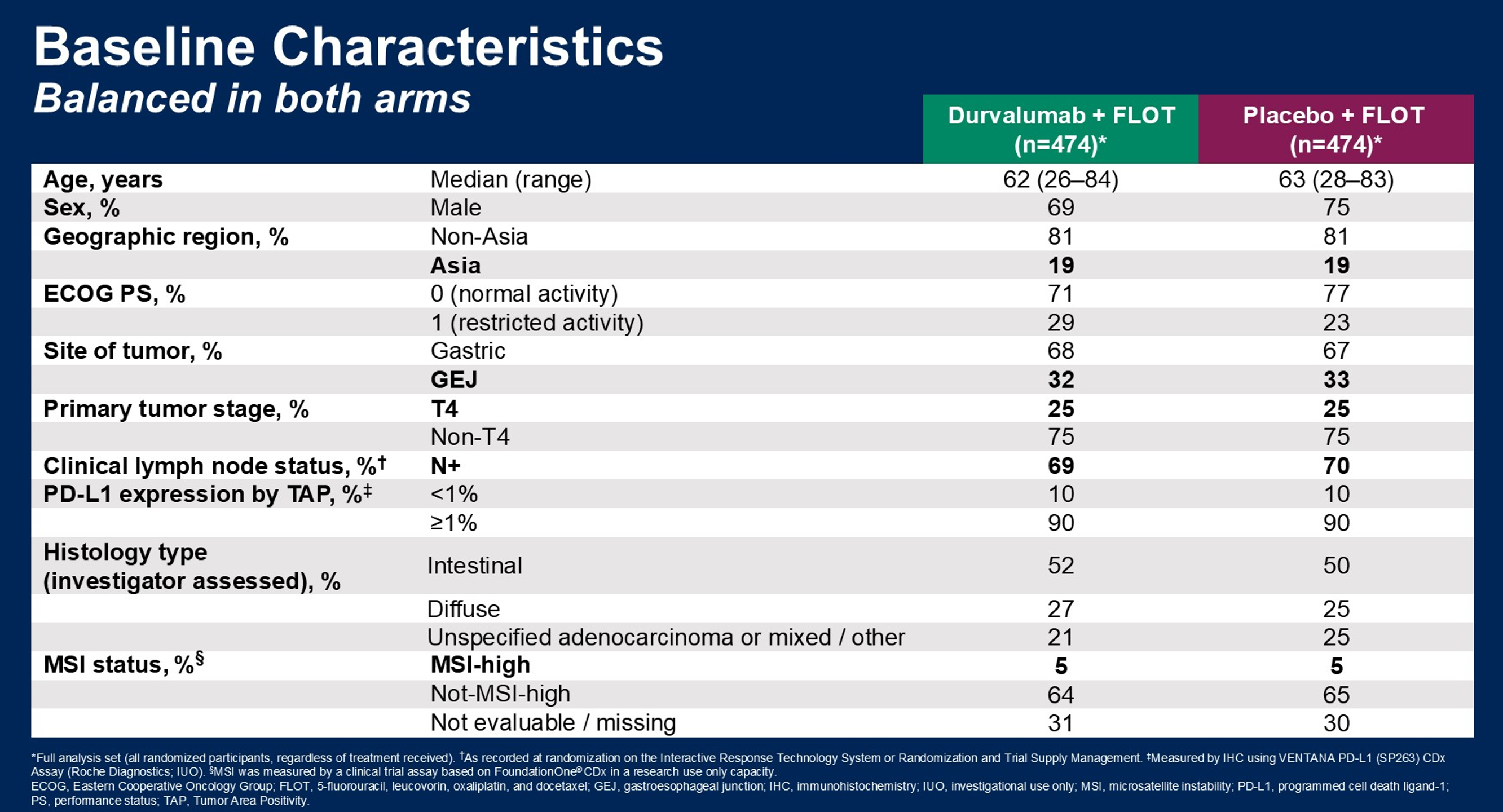
MATTERHORN研究中亚洲人群占比更低,且PD-L1高表达患者比例更高,这可能对结果产生影响。
化疗方案与围手术期管理以及EFS定义:
KEYNOTE-585:80%的患者使用FP或CP方案,20%使用FLOT方案。新辅助治疗3周期化疗(两药化疗)联合免疫后进行手术,术后再行3周期化疗,然后帕博利珠单抗维持最多11个月(33周)。
MATTERHORN:最多4周期FLOT化疗后手术,度伐利尤单抗每4周1次,最多2次。术后再给予4周期FLOT化疗,度伐利尤单抗最多2次,随后度伐利尤单抗维持10个周期(40周)。
MATTERHORN研究采用了更为强化且统一的FLOT方案,并且术后免疫维持时间更长。DANTE和MATTERHORN研究的成功是否完全归因于添加的免疫治疗,还是与化疗方案的协同效应,尤其是FLOT方案中紫杉类药物对免疫原性肿瘤微环境的诱导作用,仍需进一步阐明。
此外,KEYNOTE-585研究将降期失败不能手术等情况被定义为EFS事件,而MATTERHORN研究则将这些情况定义为特定开始时间的删失,EFS事件定义的差异可能影响最终的EFS数据呈现。
亚组分析差异:
KEYNOTE-585研究亚组分析显示,CPS≥1、亚洲人群、胃食管结合部、MSI-H的患者获益趋势不明显。
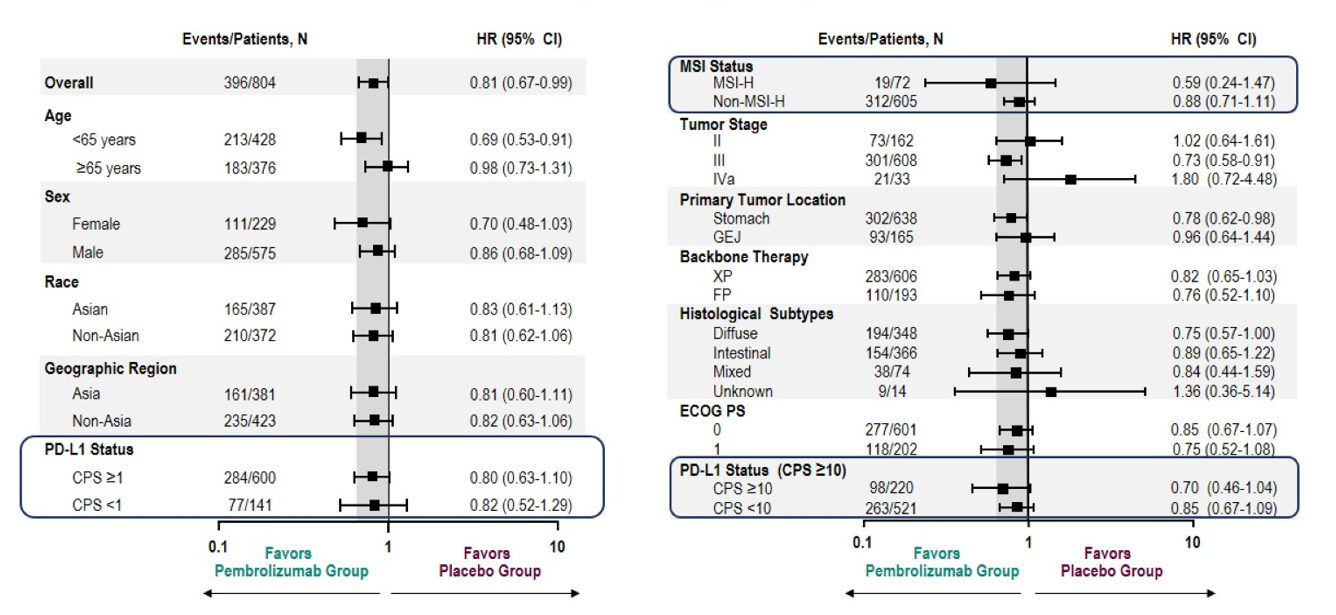
MATTERHORN研究在特定亚组中的获益更为明确,亚组人群中,PD-L1 TAP≥1%、胃食管结合部、肠型、MSI-H患者显示出更显著的获益。
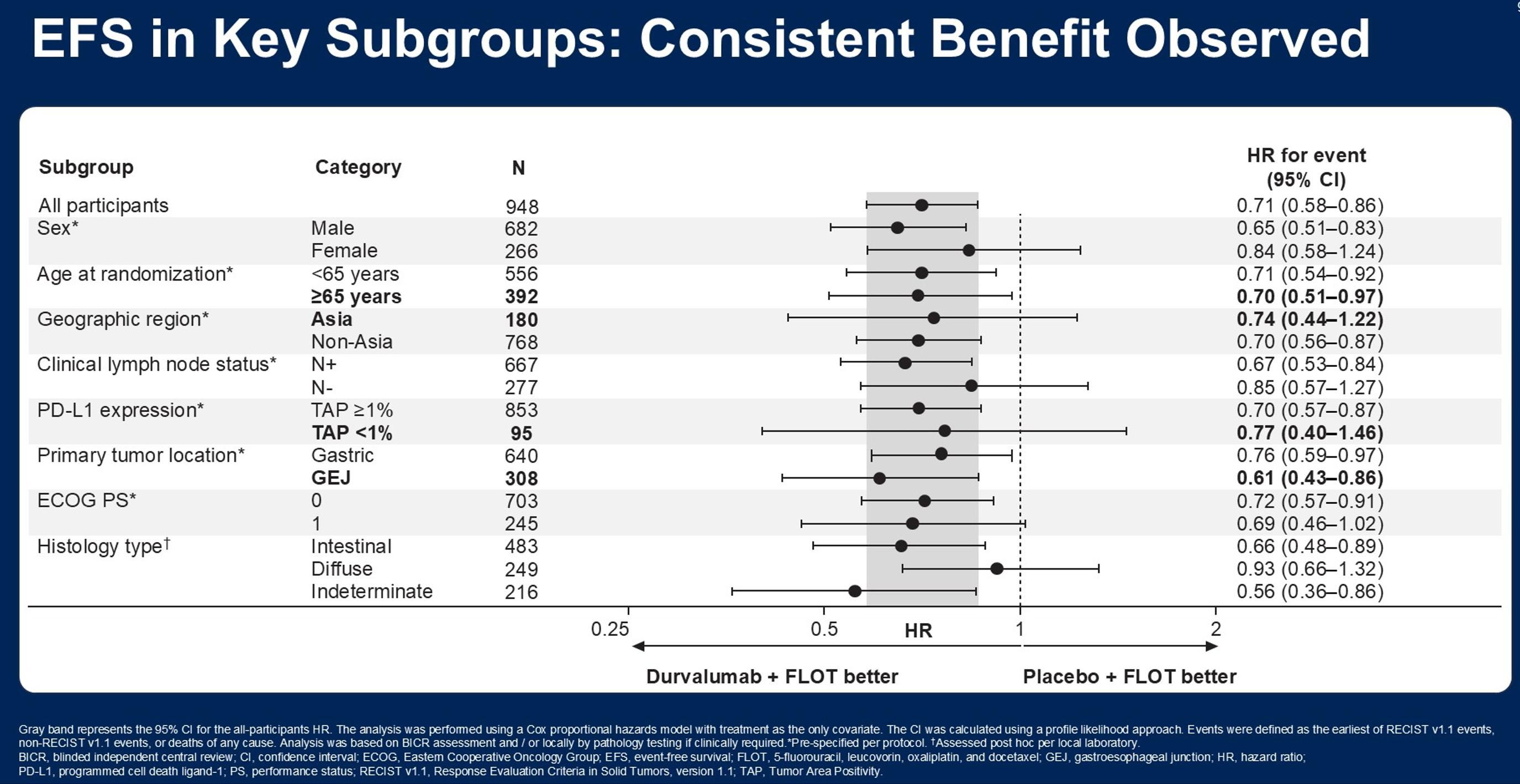
统计设计差异:
两项研究在统计设计上也有显著区别,主要体现在I型错误控制和α值分配策略上。
KEYNOTE-585:采用Maurer和Bretz的图形方法控制总体I型错误,将0.0245分配给EFS,0.0005分配给首次中期分析时的pCR率。在第三次中期分析中,用于检验EFS优越性的单侧P值边界为0.0178。
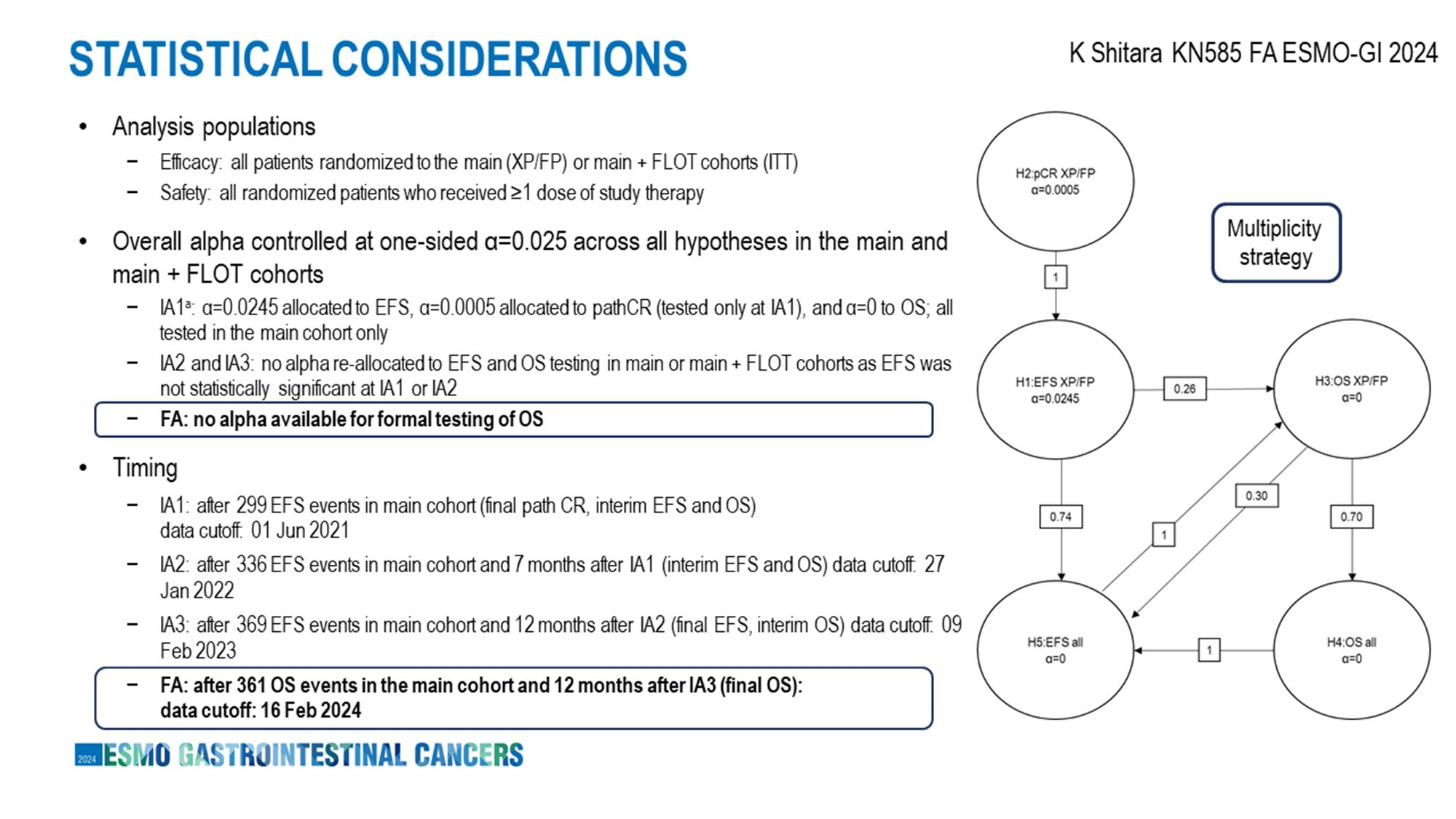
MATTERHORN:总体双侧5%的显著性水平最初分配为pCR分析0.1%,EFS分析4.9%。由于pCR分析结果为阳性,0.1%的α值得以回收,并在EFS分析中使用了Lan-DeMets α值消耗函数来近似O'Brien-Fleming界值,消耗了双侧2.39%的α值。在此次中期时间点,将0.01%的α值分配给总生存期。MATTERHORN研究在pCR结果阳性后,回收了α值,并将其用于EFS分析,这可能使得EFS结果更容易达到统计学显著性。

生存曲线差异:
尽管KEYNOTE-585的FLOT组1年和2年EFS数据与MATTERHORN相似,但OS曲线的差异是关键。MATTERHORN研究的EFS曲线分离更早且更持久,提示更显著的长期获益。
未来展望
尽管KEYNOTE-585的结果给PD-1抑制剂在围手术期胃癌中的应用带来了一些不确定性,但MATTERHORN研究的积极结果无疑为该领域注入了新的希望。未来的研究将进一步探索优化方案,例如联合其他靶向药物。目前国内正在进行的几项研究也值得期待:
DRAGON IV研究:由上海朱正纲教授团队开展,是一项多中心、随机、开放、平行对照的III期临床试验,旨在评估卡瑞利珠单抗联合阿帕替尼和SOX方案在局部进展期胃癌和胃食管结合部腺癌患者中的疗效。早期结果显示,SOXRC组pCR率为18.3%,显著高于SOX组5.0%,OS数据仍在等待中。
ASTRUM006和JUPITER-15研究:这些国内多中心III期研究选择了更具亚洲普适性的SOX或XELOX化疗方案作为骨架,其结果将为亚洲人群的治疗提供重要依据。
结语
总而言之,MATTERHORN研究的成功为围手术期胃癌免疫治疗指明了方向。深入理解两项研究在患者选择、治疗方案、研究设计和统计方法上的差异,对于更好地解读现有数据和指导未来临床实践至关重要。随着更多研究数据的公布,我们期待能够为胃癌患者带来更有效、更精准的治疗选择。
排版编辑:肿瘤资讯-Skye











 苏公网安备32059002004080号
苏公网安备32059002004080号


