三阴性乳腺癌(TNBC)约占所有乳腺癌的15%~20%,且多见于绝经前年轻女性[1,2]。由于其细胞表面缺乏雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER2),TNBC对常规的激素治疗和抗HER2靶向治疗并不敏感,临床治疗手段相对匮乏。复发或转移性TNBC患者的预后往往较差,其5年生存率不足15%,显著低于乳腺癌患者整体的5年生存率(31%)[2]。目前,化疗仍是晚期转移性TNBC的主要治疗手段。本期特别分享一例多次复发的晚期TNBC患者的治疗经历。该患者确诊乳腺癌后,立即接受了手术治疗,并在术后接受了规范的辅助放化疗、内分泌治疗以及强化辅助化疗。然而,16个月后,患者病情复发,再次进行了左乳癌改良根治术。术后,患者继续接受了辅助化疗及强化辅助化疗。不幸的是,在治疗后的第8个月,患者出现了肺部转移。经过手术切除转移灶后,患者开始接受艾立布林治疗。但在治疗过程中,患者出现了手脚麻木等不良反应,因此临床决定换用长春瑞滨软胶囊进行口服治疗。在后续的治疗过程中,患者不良反应较少,耐受性良好。截至目前,患者病情稳定,无进展生存期(PFS)已超过22个月。
病例分享
青海大学附属医院/青海大学附属肿瘤医院 乳腺疾病诊疗中心
青海省抗癌协会中西医整合肿瘤专业委员会秘书
青海省乳腺癌质量控制专家组委员
主要从事乳腺癌的转化及临床研究,在J Clin Oncol,J Hemathol Oncol等期刊发表文章5篇
病例介绍
患者:女,38岁。
主诉:左乳癌肺转移2年半余。
家族史:无特殊。
月经生育史:15岁月经初潮,既往月经规律,末次月经时间:2024年3月20日;21岁结婚,G1P1,育有1子,配偶及儿子均体健。
既往史:既往体健。
治疗过程
2020年8月28日,患者于外院行双乳肿物微创旋切术,术后病理示:(左乳2点)符合乳腺浸润性导管癌(低分化),免疫组化:ER(-),PR(-),HER2(0),Ki67(index 60%),CK5/6(-),E-Cadherin(+)。
2020年9月7日,患者于外院行“左乳癌保乳术+前哨淋巴结活检术”,术后病理示:(左乳肿物扩大切除组织)符合乳腺浸润性导管癌(低分化),脉管内未见明显瘤栓,神经未见肿瘤侵犯,各切缘未见肿瘤组织累及,送检切口窦道周围组织未见肿瘤组织。免疫组化示:ER(-),PR(中阳70%),HER2(1+),AR(-),E-Cadherin(+),P120(膜+);(左侧前哨淋巴结)淋巴结组织显慢性炎(0/4)。后患者行8周期PC-TX方案(顺铂+环磷酸胺*2周期,卡铂+环磷酰胺*2周期序贯白蛋白紫杉醇+卡培他滨1500mg bid d1-14*4周期)辅助化疗,余具体剂量不详。其后,患者继续6个月的卡培他滨(1500mg bid d1-14 q21d)强化辅助化疗。期间行辅助放射治疗(95%PT,50Gy/2Gy/25f,95%PTVtb,60Gy/2Gy/30f)及辅助内分泌治疗(OFS+来曲唑)。
2022年2月8日,复查乳腺核磁提示:左乳(约4点钟)肿块影(大小约2.2cm),BI-RADS分类5类,考虑肿瘤复发。超声引导下左乳腺物穿刺活检病理示:可查见癌细胞,考虑浸润性导管癌。
DFS:16个月
2022年2月15日,于外院行“左乳癌改良根治术”,术后病检示:(左侧乳房)符合乳腺浸润性导管癌(低分化,肿瘤大小:2cm×2cm×2cm),脉管内未见瘤栓,肿瘤侵犯神经;腋窝淋巴结组织显慢性炎(0/16枚)。免疫组化结果显示:ER(-),PR(-),Ki67(index 70%),Her2(0)。其后,患者行4周期AC方案(多柔比星脂质体+环磷酰胺)辅助化疗,后继续卡培他滨(1500mg bid d1-14 q21d,6个月)辅助强化治疗。2022年10月8日,复查胸部CT示:左肺下叶外基底段实性结节(0.9cm),较前新发,转移可能。
DFS:8个月
2022年10月14日,患者于外院行“胸腔镜下左肺下叶结节楔形切除术”,术后病理示:(左肺下叶结节)分化差的癌(肿物大小7mm),伴坏死,结合病史及免疫组化,倾向乳腺癌转移,肺切缘组织未见特殊;免疫组化:ER(-),PR(中阳 80%),HER2(0),Ki67(index30%),GATA3(-)。
2023年1月3日,完善PET-CT示:左乳癌术后+肺转移瘤术后:1、左乳切除后,局部未无明显复发征象。左侧胸壁、肋间肌局部条片影伴代谢增高,术后改变可能性大,建议CT复查;2、左肺下叶术区未见异常高代谢,双肺上叶实性微小结节,不伴高代谢,建议随诊复查。左肺多发索条;3、脑内未见明显异常代谢征象。2023年1月4日,北京某医院病理会诊示:(1)(2020.09.07左乳腺肿物扩大切除标本)病理示:乳腺浸润性导管癌,Ⅲ级,伴灶状坏死及间质纤维化灶形成,免疫组化结果示:ER(-),PR(-),HER2(1+),Ki67(+70%);(2)(2022.02.16左乳改良根治术切除标本)病理示:乳腺浸润性导管癌,III级;伴灶状坏死及间质纤维化灶形成,其余情况请参见原单位病理报告;(3)(2022.10.14左肺下叶楔形切除标本)病理示:转移性乳腺浸润性导管癌,I级,免疫组化结果显示:ER(-),PR(-),HER2(1+),Ki-67(+50%)。
2023年1月9日-2023年7月14日,行8周期艾立布林(1.4mg/m2,2mg,d1、8,q21d)治疗。治疗期间,患者出现不良反应:1级恶心、1级食欲不振、1级乏力,1级手脚麻木。
疗效评价:SD
2023年7月27日至今:口服长春瑞滨胶囊(60mg/m2,d1、8,q21d)治疗。治疗期间,患者出现不良反应:1级恶心、1级食欲不振、1级乏力。近期复查胸部CT、腹部CT、头颅MRI,均未见转移瘤。
疗效评价:SD PFS:22个月
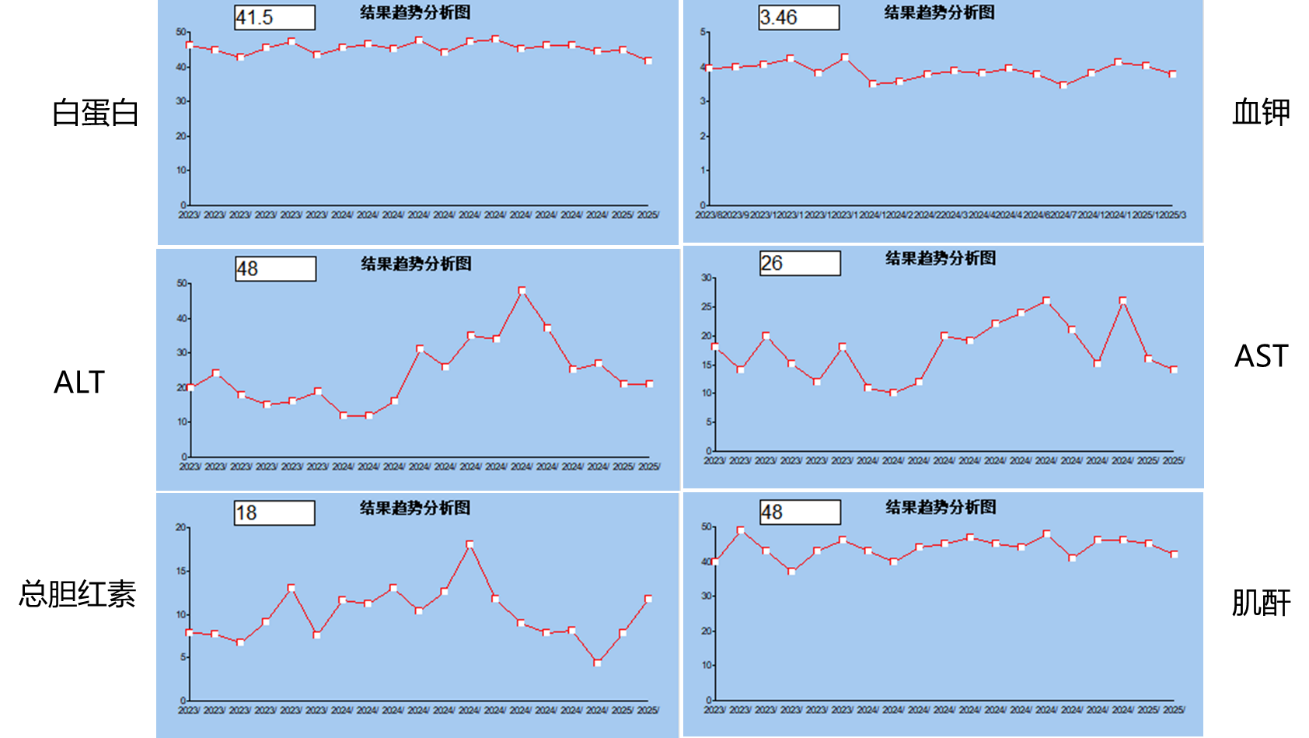
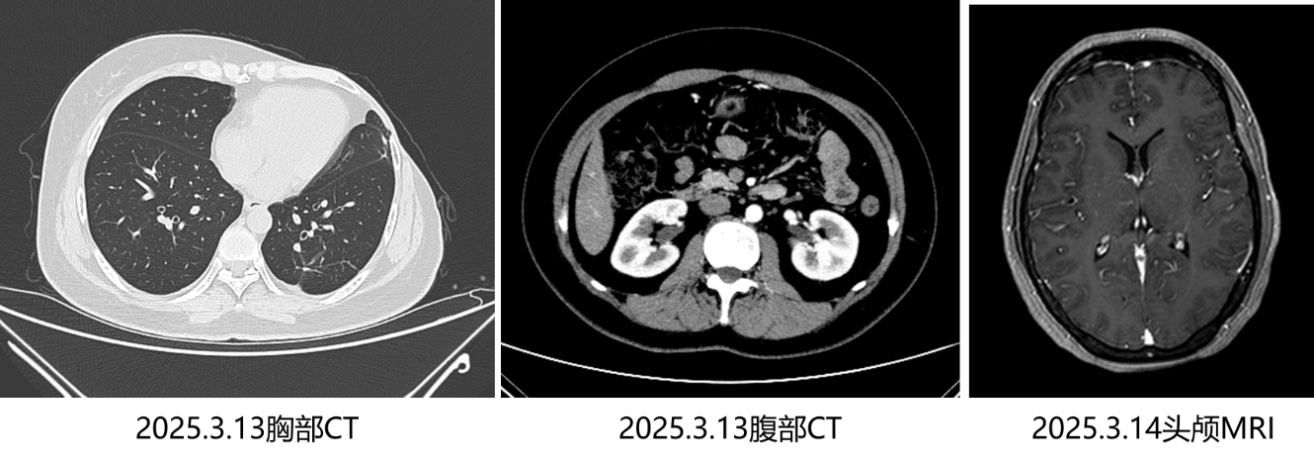 图2.治疗期间检查结果
图2.治疗期间检查结果
专家点评
青海大学附属医院乳腺疾病诊疗中心副主任
国家肿瘤质控中心乳腺癌专家委员会委员
国家卫生健康委卫生发展研究中心乳腺癌单病种分级诊疗专病联盟(项目)专家组成员
全国乳腺癌防控协作组委员
中国老年保健协会乳腺癌专业委员会常务委员
中国抗癌协会乳腺癌专业委员会委员
中国医师协会肿瘤学分会乳腺癌学组委员
中华志愿者协会中西医结合专家志愿者委员会乳腺外科专业组常务委员
青海省抗癌协会中西医整合肿瘤专业委员会主任委员、青海省抗癌协会乳腺癌专业委员会副主任委员
青海省预防医学会乳腺癌专业委员会副主任委员
主持3项国家自然科学基金课题,1项科技部国家科技重大专项子课题。以第一或通讯作者(含共同)在JCO,STTT,JAMA Network Open, Journal of hematology & oncology 和Immunology等杂志发表SCI文章60余篇。Cancer Innovation杂志编委
乳腺癌是全球女性最常见的恶性肿瘤。初次确诊时,3%~10%的乳腺癌患者已处于晚期阶段。即便是早期乳腺癌,经过根治性手术及多学科综合治疗后,仍有30%~40%患者发展为晚期。晚期乳腺癌患者中位生存时间通常为2~3年。虽然晚期乳腺癌难以完全治愈,但通过化疗、内分泌治疗或靶向治疗等手段,可以有效改善患者的生活质量,部分患者甚至能够实现长期带瘤生存[3]。而在乳腺癌的诸多亚型中,TNBC尤其值得关注。其多发于年轻女性群体,具有高度异质性、高侵袭性,疾病进展迅速,易于早期复发转移,且目前缺乏有效治疗靶点,患者的中位总生存期(OS)仅有12~18个月[4]。由于预后极差,TNBC常被形容为“乳腺癌之王”。
化疗一直是晚期转移性TNBC的主要系统治疗手段。目前,临床常用的乳腺癌化疗药物主要包括蒽环类、紫杉类、铂类、卡培他滨、吉西他滨、长春瑞滨、艾立布林以及5-氟尿嘧啶、甲氨蝶呤等。在选择化疗方案时,需根据患者的具体情况进行个体化调整。对于病情进展迅速、症状明显、肿瘤负荷较大或存在内脏危象需要迅速缓解症状、控制疾病进展且耐受性较好的患者,联合化疗通常是首选方案。药物首选以蒽环/紫杉类/铂类为基础的单药或联合方案。这些药物在TNBC治疗中具有明确的疗效和丰富的临床应用经验。而对于既往接受过以蒽环类、紫杉类或铂类为基础的单药或联合方案治疗且已出现治疗失败的患者,应换用其他类别的药物[2],以避免耐药问题的发生,同时为患者提供新的治疗机会,进一步控制疾病,改善预后。
本例患者术后接受了PC-TX方案辅助化疗,随后进行了卡培他滨强化辅助化疗,DFS1为16个月;疾病复发后,患者于术后接受了AC方案辅助化疗,并继续使用卡培他滨强化辅助治疗,DFS2近8个月;肺部转移后,患者术后进行了艾立布林治疗。艾立布林是一种有丝分裂微管动力抑制剂,多项临床研究表明,艾立布林在治疗转移性乳腺癌方面具有优势[3]。我国一项单中心回顾性研究纳入了159例转移性或不可切除TNBC患者。研究结果显示,艾立布林治疗组的中位PFS显著优于紫杉醇治疗组(8.2个月 vs 4.6个月,HR = 0.40,P=0.001)和铂类化疗组(8.2个月 vs 3.3个月,HR = 0.29, P < 0.001)。此外,相较于紫杉醇,艾立布林治疗能够显著延长OS(26.5个月 vs 10.9个月, HR = 0.37, P = 0.015)。安全性方面,艾立布林组的外周神经病变、贫血、恶心呕吐及脱发的发生率均低于紫杉类药物组[5]。另一项对比了艾立布林与卡培他滨在局部晚期或转移性乳腺癌患者中的疗效的研究结果亦显示,在TNBC亚组中,艾立布林组的OS较对照组延长5个月,死亡风险降低29.8%[3]。然而,本例患者在治疗期间出现了恶心、食欲不振、乏力、手脚麻木等不良反应,并拒绝继续艾立布林治疗。在这种情况下,临床更应综合考虑患者的个体差异、耐受性、既往治疗史以及当前病情,制定下一步个体化治疗方案。
长春瑞滨是一种半合成的长春碱类细胞周期特异性抗癌药,能够有效抑制肿瘤细胞的生长和扩散。在NorBreast-231研究中[6],口服长春瑞滨软胶囊显示出了与紫杉醇相似的疗效:两组意向治疗人群(ITT)的疾病控制率(DCR)分别是75.8% vs 75.4%,OS分别为27.6和22.3个月。此外,口服长春瑞滨组的3-4级不良事件发生率与紫杉醇组相似,但在脱发(2% vs 34%)和周围神经病变(0 vs 5%)方面发生率显著更低。一项探索长春瑞滨联合铂类方案在既往接受过蒽环类药物治疗的晚期TNBC中的疗效与安全性的研究结果显示[7],在可评价疗效的31例患者中,总有效率达45.2%,全组中位肿瘤进展时间(TTP)为7.9个月;在安全性方面,血液学不良反应可耐受,其他不良反应发生率低。另一项来自中国的真实世界回顾性研究中[8],中位随访时间为17.0个月,194例接受口服长春瑞滨软胶囊(单药或联合方案)治疗的转移性乳腺癌患者中,首次评估时部分缓解(PR)53例,106例患者疾病稳定(SD),客观缓解率(ORR)为27.3%,临床获益率(CBR)为60.8%,中位PFS为6.2个月。可见,长春瑞滨软胶囊具有较好的疗效及安全性。此外,研究表明[9,10],在疗效相当的情况下,大多数患者对口服化疗药物的接受度更高,口服药物治疗的不良反应更少,且因其便利性,可以减轻患者的患病感受,使其更好地融入日常生活与工作中。
基于此,在与患者充分沟通后,临床决定换用长春瑞滨软胶囊口服治疗。目前,患者仍在坚持治疗中,病情稳定,不良反应轻微且可耐受,PFS已超22个月。可见,长春瑞滨软胶囊不仅丰富了晚期乳腺癌,尤其是TNBC的治疗选择,而且为患者带来了重要的生存获益与生活质量保障。
[1] Brown M, Tsodikov A, Bauer KR, Parise CA, Caggiano V. The role of human epidermal growth factor receptor 2 in the survival of women with estrogen and progesterone receptor-negative, invasive breast cancer: the California Cancer Registry, 1999-2004. Cancer. 2008;112(4):737-747.
[2]中国抗癌协会乳腺癌专业委员会, 中国抗癌协会国际医疗交流分会, 中国医师协会肿瘤医师分会乳腺癌学组. 中国晚期三阴性乳腺癌临床诊疗指南(2024版)[J]. 中华肿瘤杂志, 2024, 46(6):471-480. DOI: 10.3760/cma.j.cn112152-20240118-00034.
[3]桑蝶, 宋丽华, 邸立军, 等. 艾立布林治疗晚期乳腺癌疗效和安全性的多中心真实世界研究[J]. 中华肿瘤杂志, 2022, 44(4):364-369.DOI: 10.3760/cma.j.cn112152-20210226-00173.
[4]李彬,张桂芳.晚期三阴性乳腺癌诊疗进展及未来治疗方向[J].河南医学研究, 2023, 32(19):3636-3644.DOI:10.3969/j.issn.1004-437X.2023.19.044.
[5] Huang, W., Wang, C., et al. (2024). Feasibility and tolerability of eribulin-based chemotherapy versus other chemotherapy regimens for patients with metastatic triple-negative breast cancer: A single-centre retrospective study. Frontiers in Cell and Developmental Biology, 12, 1313610.
[6] Aapro M, et al. Randomized phase II study evaluating weekly oral vinorelbine versus weekly paclitaxel in estrogen receptor-positive, HER2-negative patients with advanced breast cancer (NorBreast-231 trial)[J]. Breast. 2019;45:7-14.
[7] 施秀青,徐兵河,李青,等.长春瑞滨联合铂类一线治疗晚期三阴性乳腺癌[J].中国肿瘤临床与康复,2013,20(04):324-328.DOI:10.13455/j.cnki.cjcor.2013.04.009.
[8] Huang J, et al. A Real-World Study on Oral Vinorelbine for the Treatment of Metastatic Breast Cancer. Oncologie. 2022;24(1):131-145.
[9] Sarah Schott, Andreas Schneeweiss, Judith Reinhardt, et al. Acceptance of oral chemotherapy in breast cancer patients - a survey study[J]. BMC Cancer. 2011 Apr 12:11:129.doi: 10.1186/1471-2407-11-129.
[10] Maria Rosa Strada, Raffaella Palumbo, Antonio Bernardo, et al. Intravenous or oral vinorelbine plus capecitabine as first-line treatment in HER2- metastatic breast cancer: joint analysis of 2 consecutive prospective phase II trials[J]. Clin Breast Cancer. 2012 Feb;12(1):30-9. doi: 10.1016/j.clbc.2011.11.001. Epub 2011 Dec 6.
排版编辑:TanRongbing











 苏公网安备32059002004080号
苏公网安备32059002004080号


