胆道肿瘤,以其高度异质性、复杂的分子机制及普遍较差的预后,长久以来一直是肿瘤学领域亟待攻克的难题。这类肿瘤往往隐匿起病,进展迅速,加之早期诊断标志物的匮乏与有效治疗手段的缺失,使得多数患者在确诊时已步入疾病晚期,五年生存率堪忧。然而,随着下一代测序技术的飞速发展与基础、临床转化研究的不断深入,胆道肿瘤的分子病理机制逐渐被揭开神秘面纱,临床分型日益精细,治疗策略亦迎来革命性变革。在此背景下,特邀复旦大学附属中山医院施国明教授,基于当前最前沿的研究成果,系统解读胆道肿瘤的一线和二线治疗、分子特征、靶向药物的最新进展,以期为临床医生提供科学、全面的治疗决策依据,进一步改善患者预后,推动胆道肿瘤治疗领域迈向新的高度。
专家简介
肝脏外科教授,主任医师,博士生导师
中山医院科研处处长,中山医院临床医学研究院执行院长
复旦大学长寿与衰老研究所副所长
哈佛医学院高级访问学者,上海市优秀学术带头人
中国医师协会外科医师分会胆道外科专家工作组副组长
国家肝癌早筛专委会委员
上海市医药协会产学研医创新转化专委会常务副主委
上海市抗癌协会转化医学专业委员会常委
CSCO临床研究专委会委员
CSCO肝癌专委会委员
晚期胆道癌患者的生活质量评估
KEYNOTE-966研究
Health-related quality of life in participants with advanced biliary tract cancer from the randomized phase III KEYNOTE-966 study1
KEYNOTE-966研究显示,帕博利珠单抗+吉西他滨联合顺铂一线治疗,中位OS为12.7个月,对照组为10.9个月,显著延长患者的总生存期。本研究还关注了患者健康相关生活质量(HRQoL)的变化,为评估该联合治疗方案的全面影响提供了重要依据。
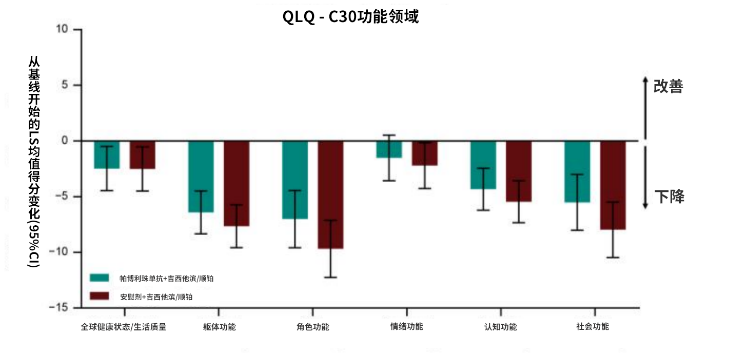
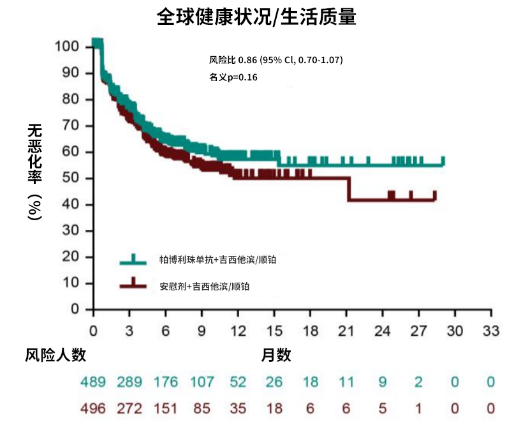
本研究采用了三种经过验证的问卷——欧洲癌症研究与治疗组织生活质量核心问卷(EORTC QLQ)-C30、EORTC QLQ-BIL21和EQ-5D-5L——来评估患者的生活质量。共随机分配了1069例参与者进入研究(帕博利珠单抗组533例,安慰剂组536例)。结果显示,两组在所有预设领域的基线到第18周的均值变化相似。其中,全球健康状况/生活质量(GHS/QoL)在帕博利珠单抗组中位数未达到,安慰剂组为21.2个月(HR 0.86,95%CI 0.70-1.07),黄疸和疼痛的中位数恶化时间在两组中均未达到。研究提示,在吉西他滨和顺铂联合帕博利珠单抗后,HRQoL得以维持。
晚期胆道癌一线治疗
仑伐替尼/贝伐珠单抗联合免疫化疗的疗效与安全性
Analysis of the effectiveness and safety of lenvatinib/bevacizumab combined with PD-1/PD-L1 inhibitors and GEMOX in the first-line treatment of advanced biliary tract carcinoma2
靶免化联合是目前的研究热点,有望颠覆胆道肿瘤的治疗格局。2019年复旦大学附属中山医院周俭教授团队开展了一项特瑞普利单抗+仑伐替尼+GEMOX一线治疗晚期肝内胆管癌(ICC)的研究。该研究结果于2023年在线发表在Signal Transduction and Targeted Therapy(STTT, IF=38)杂志。2022年,该方案被纳入CSCO《胆道恶性肿瘤诊疗指南》晚期BTC的一线治疗推荐。本研究在真实世界中针对晚期胆道恶性肿瘤,回顾性地评估了仑伐替尼/贝伐珠单抗联合PD-1/PD-L1抑制剂(信迪利单抗或卡瑞利珠单抗)和吉西他滨/奥沙利铂(GEMOX)作为一线治疗的疗效和安全性。研究共纳入172例患者,分为四组:A组接受GEMOX联合PD-1抑制剂和仑伐替尼;B组接受GEMOX、PD-1抑制剂和贝伐珠单抗;C组接受GEMOX和PD-1抑制剂;D组单独接受GEMOX。
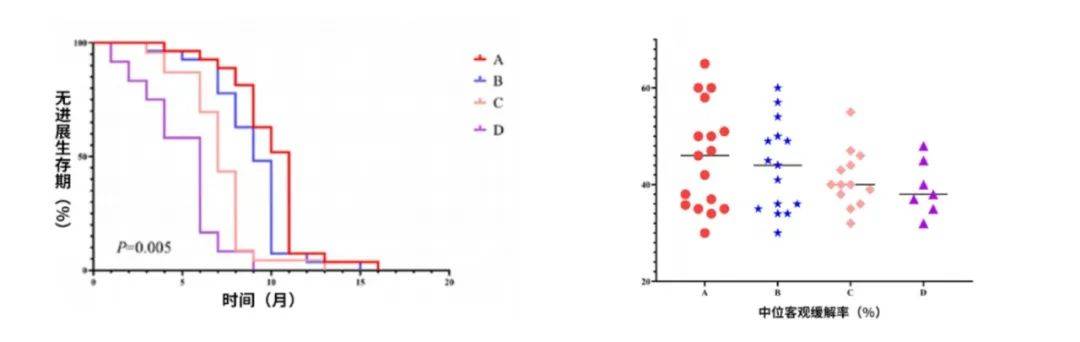
研究结果显示,A组患者的中位PFS达到12.42个月,显著优于其他三组(B组11.05个月,C组8.89个月,D组6.02个月,95%CI 11.31-13.53,P<0.01)。ORR在A、B、C、D组分别为45.00%、34.78%、16.67%、17.86%。回归分析显示,患者的转移部位、中性粒细胞与淋巴细胞比值(NLR)是否小于2.3,以及是否通过肝动脉栓塞进行化疗是影响中位OS和PFS的独立预后因素。几乎所有患者均经历了不同程度的治疗相关不良事件,但大多数为1-2级。
胆道癌二线治疗
伊立替康脂质体联合方案的疗效与安全性
Liposomal irinotecan for previously treated patients with biliary tract cancer: A pooled analysis of NIFTY and NALIRICC trials3
在韩国的NIFTY和德国的NALIRICC试验中,伊立替康脂质体(nal-IRI)+5-氟尿嘧啶(5-FU)和亚叶酸钙(LV)作为吉西他滨治疗进展后晚期胆道癌的二线治疗方案,结果存在差异。NIFTY达到主要终点,但NALIRICC研究主要终点为阴性结果。本研究对上述两个研究进行全面的汇总分析,来评估nal-IRI联合5-FU/LV方案相较于单纯5-FU/LV方案的疗效和安全性。
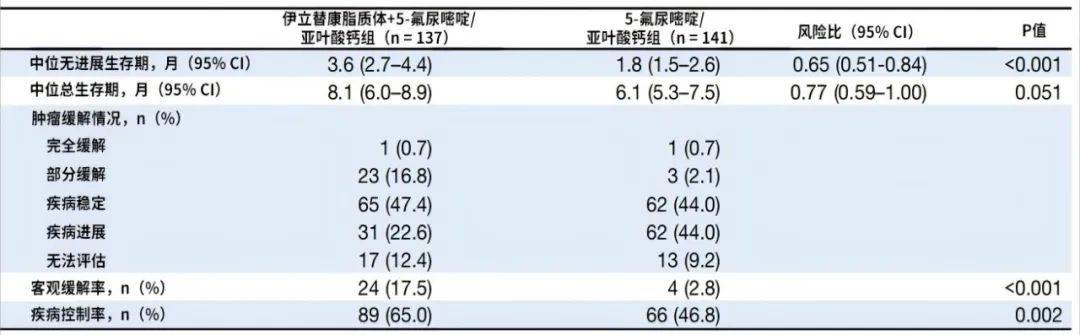
本研究从NIFTY和NALIRICC试验的意向治疗人群中汇总了个体患者数据,主要终点为PFS,次要终点包括OS、客观反应率(ORR)和安全性。共有278例患者被纳入研究,其中137例分配至nal-IRI联合5-FU/LV组,141例分配至5-FU/LV组。结果显示,nal-IRI联合5-FU/LV组的中位PFS显著延长,分别为3.6个月(95%CI 2.7-4.4)对比1.8个月(95%CI 1.5-2.6)(HR 0.65,P<0.001)。中位OS分别为8.1个月(95%CI 6.0-8.9)和6.1个月(95%CI 5.3-7.5)(HR 0.77,P=0.051)。ORR在nal-IRI联合5-FU/LV组中更高(17.5%对比2.8%;P<0.001)。在nal-IRI联合5-FU/LV组和5-FU/LV组中,分别有4例(2.9%)和21例(15.3%)患者接受了后续的伊立替康治疗。在安全性方面,不良事件的发生率在不同种族间存在差异,德国患者中胃肠道毒性更为常见,而韩国患者中中性粒细胞减少症更为普遍。剂量调整方面,韩国人群中nal-IRI剂量降低的频率更高(67.0% vs 33.3%;P<0.001),而德国人群因不良事件或患者意愿更常停用nal-IRI(31.3% vs 8.0%;P<0.001)。
胆道肿瘤的分子检测与靶向治疗进展
Molecular Testing and Targeted Therapies in Hepatobiliary Cancers: A Review4
胆道肿瘤具有高度异质性,且分子机制复杂,患者预后普遍较差。分子检测可为患者提供重要的预测和预后信息,并为晚期患者指导治疗。胆道恶性肿瘤(BTCs)中存在大量可作用的靶点。对ICC患者,特别是不可切除/转移性的ICC患者而言,全面的生物标志物检测有助于确定个体化治疗方案。我国《肝内胆管癌精准检测专家共识(2024版)》推荐ICC患者、特别是不可切除/转移性ICC患者进行分子检测,筛选获益人群(证据级别:高,推荐级别:强)。美国国家综合癌症网络(NCCN)指南包含了针对胆管癌分子检测的建议:
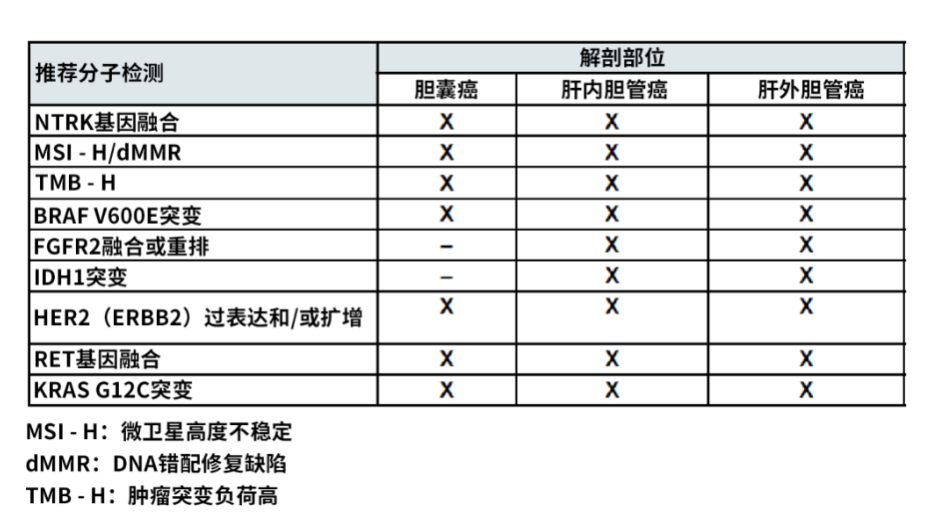
有证据表明,多达50%的BTCs患者可能存在可治疗的基因改变。肝内胆管癌常见的基因改变包括IDH1突变(15%-20%)和FGFR2融合或重排(10%-15%)。在肝内胆管癌中,IDH1突变是一个重要的可靶向分子改变。ICC患者、特别是小胆管型ICC患者进行IDH1突变检测具有重要临床意义。下一代测序(NGS)可同时检出多种形式的IDH1突变位点。若NGS不可及,可采用Sanger法,但灵敏度有限。针对IDH1突变的靶向治疗药物艾伏尼布已获得FDA批准,用于治疗先前接受过治疗的IDH1突变型胆管癌患者。这一批准基于ClarIDHy试验的结果,该试验显示,与安慰剂相比,艾伏尼布显著延长了患者的无进展生存期(PFS),中位PFS分别为2.7个月和1.4个月(HR 0.37,95%CI 0.25-0.54),艾伏尼布治疗组患者的中位总生存期(OS)为10.3个月,而安慰剂组为5.1个月(HR 0.49,95%CI 0.34-0.70)。
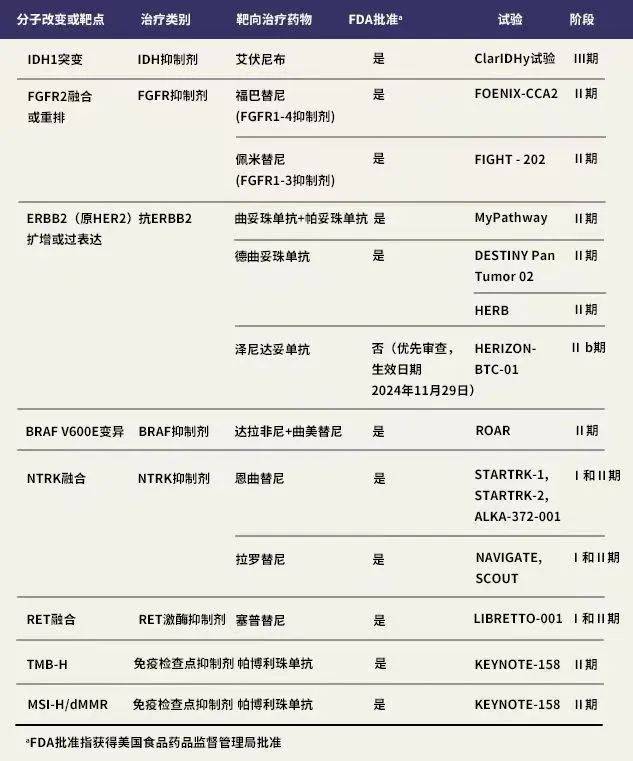
此外,针对多种实体瘤的泛肿瘤疾病疗法也已获批,包括针对NTRK融合的拉罗替尼、恩曲替尼,针对RET融合的塞普替尼,针对BRAF V600E突变的达拉非尼和曲美替尼联合疗法,针对微卫星不稳定肿瘤的dostarlimab或帕博利珠单抗等,凸显了在各类肿瘤中进行NGS检测以及ERBB2免疫组织化学(IHC)检测的必要性。下表中列出了BTCs患者可检测的变异及针对性靶向疗法。
专家点评
KEYNOTE-966的研究结果使得帕博利珠单抗+吉西他滨+顺铂作为晚期胆道恶性肿瘤一线治疗被给予1A推荐。这项健康相关生活质量分析表明,在帕博利珠单抗联合吉西他滨和顺铂的治疗方案中,患者的HRQoL得到了维持,进一步支持了该方案作为一线治疗的合理性。该研究是目前针对晚期BTC患者的HRQoL进行的最大且最全面的分析。研究表明在提高患者生存率的同时,该联合治疗方案不影响患者的生活质量,这对于改善晚期BTCs患者的预后具有重要意义。
仑伐替尼/贝伐珠单抗联合PD-1/PD-L1抑制剂及GEMOX这种“三联四药”的组合方案在晚期BTCs一线治疗中的探索,为临床实践提供了新的思路。本篇收录的回顾性研究结果显示,该方案在延长PFS和提高ORR方面表现出色,尤其是在与GEMOX联合时,疗效更为显著。该研究进一步在真实世界中验证了复旦大学附属中山医院团队先前在该联合方案的研究结果。尽管这种联合治疗方案在提高疗效的同时也带来了更多的不良事件,但大多数为1-2级,可通过剂量调整和支持治疗进行有效管理。这一研究结果为BTCs的一线治疗提供了新的选择,尤其是在传统化疗方案疗效有限的情况下。需要注意的是,该研究为单中心回顾性研究,样本量较小,仍需更大规模的前瞻性研究来进一步验证其疗效和安全性。目前复旦大学附属中山医院领衔的ToLegend Ⅲ期研究已完成入组,期待该研究结果的发布。
BTCs的二线治疗一直是临床实践中的难点。通过对NIFTY和NALIRICC两项试验的汇总分析可以看出,与单独使用5-FU/LV相比,联合nal-IRI显著延长了PFS,并提高了ORR。这一发现为BTCs的二线治疗提供了新的选择,尤其是在亚洲患者中,nal-IRI联合方案可能具有更好的耐受性和疗效。然而,需要注意的是,不同种族患者之间的不良事件发生率存在差异,提示在临床应用中需要根据患者的种族背景进行个体化的剂量调整和毒性管理。这项研究为BTC的二线治疗提供了有价值的参考,但仍需进一步的随机对照试验来验证其长期疗效和安全性。
基于胆道肿瘤的分子检测和靶向治疗进展,精准医学在这一领域显示出广阔的应用前景。随着NGS技术的发展,胆道肿瘤的分子特征得到了更深入的揭示,为靶向治疗提供了更多机会。BTCs中常见的IDH1和FGFR2等突变为精准治疗提供了靶点。因此,对于不可切除或转移性BTC且适合全身治疗的患者,建议进行基因组检测,优先检测肿瘤标本,也可以考虑检测游离DNA作为补充。我国的临床专家也在近期发布了《肝内胆管癌精准检测专家共识(2024版)》,制定中国的分子检测标准。未来的治疗策略需要更加注重个体化,通过综合分析患者的基因组特征、免疫微环境和临床特征,制定更适合患者的治疗方案。
1. Yoo C, Ueno M, Klümpen HJ, et al. Health-related quality of life in participants with advanced biliary tract cancer from the randomized phase III KEYNOTE-966 study. J Hepatol. 2025 Mar 26:S0168-8278(25)00207-7.
2. Zhao L, Zhang Z, Wang D, et al. Analysis of the effectiveness and safety of lenvatinib/bevacizumab combined with PD-1/PD-L1 inhibitors and GEMOX in the first-line treatment of advanced biliary tract carcinoma. Clin Exp Med. 2025 Mar 19;25(1):87.
3. Yoo C, Saborowski A, Hyung J, et al. Liposomal irinotecan for previously treated patients with biliary tract cancer: A pooled analysis of NIFTY and NALIRICC trials. J Hepatol. 2025 Mar 25:S0168-8278(25)00169-2.
4. Tsilimigras DI, Kurzrock R, Pawlik TM. Molecular Testing and Targeted Therapies in Hepatobiliary Cancers: A Review. JAMA Surg. 2025 Mar 19.
排版编辑:肿瘤资讯-展思懿











 苏公网安备32059002004080号
苏公网安备32059002004080号


