肺癌远距离转移是导致肺癌患者死亡的主要原因,其中骨骼是肺癌最常见的转移部位之一,肺癌骨转移患者大多数为溶骨性转移。骨转移会导致病理性骨折、脊髓压迫和高钙血症等严重的骨相关事件(SREs)的发生,并常常预示着患者生活质量的下降和生存期的缩短[1]。鉴于肺癌骨转移的严重性,了解其发生过程、诊断方法及治疗策略至关重要。同济大学医学院附属上海肺科医院何雅億教授于Translational Lung Cancer Research发表了一篇综述文章[2],系统阐述了肺癌骨转移的过程、可能的机制、诊断方法和当前的治疗手段。【肿瘤资讯】特此整理,以飨读者。
肺癌骨转移的过程
肺癌骨转移过程可分为三步:肿瘤侵袭、肿瘤细胞迁移和在骨组织侵袭(图1)。
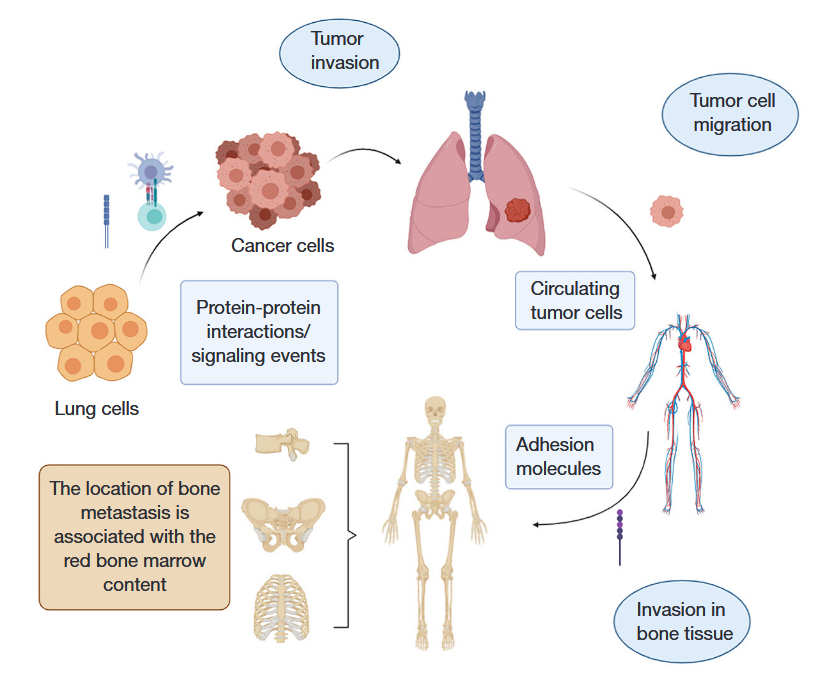
1. 肿瘤侵袭:
最初,在蛋白质相互作用和信号传导事件等因素的影响下,特别是E-钙粘蛋白的减少和基质金属蛋白酶(MMPs)等蛋白酶的作用下,肺癌细胞的状态发生改变,细胞间的粘附和交联减少,导致肿瘤细胞发生侵袭并呈现迁移趋势。
2. 肿瘤细胞迁移:
随后,肺癌细胞进入循环系统,被称为循环肿瘤细胞(CTCs)。骨转移的位置与红骨髓(RBM)的含量有关。常见的转移部位包括脊柱、骨盆和肋骨等。
3. 骨组织侵袭:
当肿瘤细胞到达骨骼表面时,它们开始侵入。某些粘附分子,如血管细胞粘附蛋白-1,在此过程中发挥重要作用。这些分子促进肺癌细胞与骨细胞结合,并开始改变骨微环境。
肺癌骨转移的类型
骨的动态平衡由成骨细胞和破骨细胞共同调节,在正常情况下两者功能相反但维持相对平衡。肿瘤细胞的侵入会打破这种平衡,干扰骨重建过程。肺癌的骨转移有两种不同的类型:溶骨性转移和成骨性转移,其中溶骨性转移占肺癌的骨转移70%。
溶骨性转移 (Osteolytic Metastasis)
肺癌细胞不能直接通过向局部组织分泌蛋白水解酶来直接导致骨溶解。相反,肺癌细胞与骨组织之间的微环境通过激活破骨细胞发挥了重要作用。被激活的破骨细胞会破坏骨骼,导致溶骨性病变的形成。由肺癌细胞产生的循环miR-21可促进单核细胞向破骨细胞分化。并且肺癌细胞产生的IL-7可以上调T细胞来源的细胞因子,如RANKL和TNF-α,从而促进破骨细胞的生成。肝细胞生长因子(HGF)-MET信号通路能激活骨微环境中的RANKL/RANK信号通路,诱导破骨细胞活化,最终导致溶骨性转移的发生。
成骨性转移 (Osteogenic Metastasis)
与溶骨性转移相比,肺癌的成骨性转移较为罕见,其是否存在独特的机制尚不清楚。
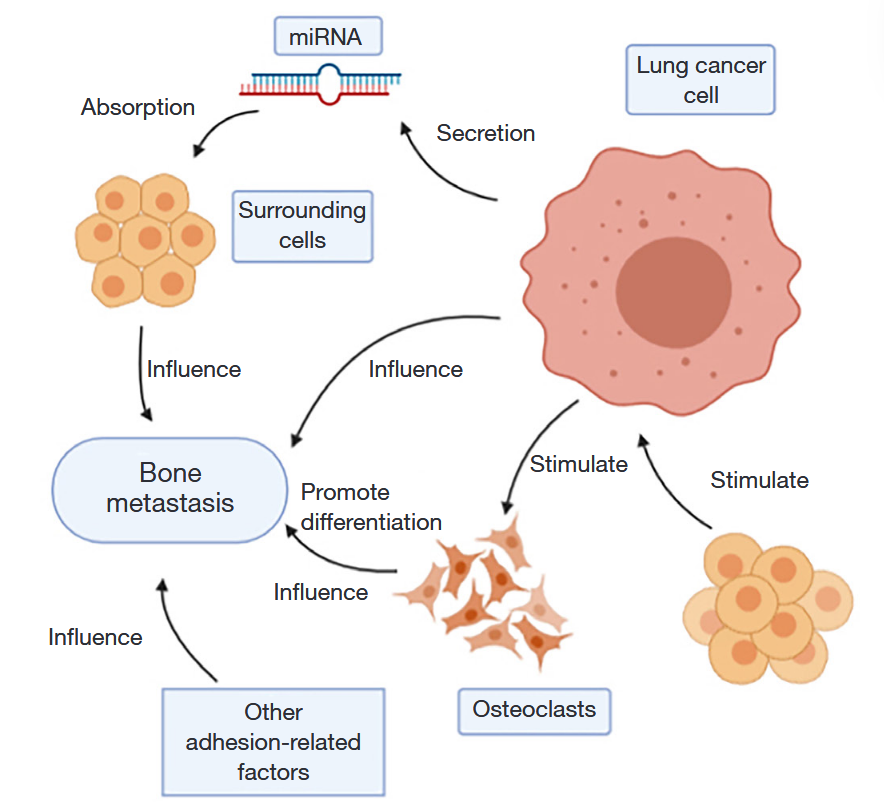
遗传因素
癌细胞分泌的miRNA能以胞外囊泡的形式被周围细胞吸收并发挥作用。例如,在肺癌细胞中过表达的miR-192可通过外泌体靶向血管内皮细胞,抑制血管生成,从而降低骨转移的能力。miR-192-5p通过靶向TRIM44抑制肺癌骨转移。相反,来自缺氧骨髓间充质干细胞(BMSCs)的外泌体miRNA可通过STAT3诱导的上皮-间充质转化(EMT)促进肺癌细胞的转移。
此外,DNA和mRNA也在其中发挥重要作用。例如,在肺癌患者中,EGFR信号通路的激活会上调VEGF-A等血管生成因子,诱导肿瘤血管形成,促进肿瘤细胞的侵袭和转移。
微环境
骨微环境中多种细胞、因子和信号通路在肺癌骨转移中起到了关键作用。BMSCs被引导至肿瘤细胞处,帮助形成癌症微环境。肥大细胞释放的类胰蛋白酶可通过胞外体促进肿瘤细胞转移。RANKL/RANK通路是介导肺癌溶骨性骨破坏的重要环节。甲状旁腺激素相关蛋白(PTHrP)被认为是肺癌溶骨性骨转移过程中的主要调节因子之一。肺癌细胞分泌的PTHrP与成骨细胞表面的PTH/PTHrP受体结合,增强了成骨细胞表面RANKL基因的表达,同时减少了骨保护素(OPG)的合成。这促进了破骨细胞的分化和成熟,加剧了溶骨性骨破坏。在骨溶解过程中,大量从骨基质中释放的TGF-β会刺激播散性肿瘤细胞(DTCs)产生更多的PTHrP,进一步加剧溶骨性转移的形成。
其他粘附相关因子
任何粘附相关因子的变化都可能影响肺癌的骨转移。例如,肺癌细胞中lumican的高表达通过自分泌机制促进骨转移。
诊断方法
影像学检查:
目前多种技术或方法都可用于诊断肺癌骨转移。放射性核素骨扫描(ECT)和正电子发射断层扫描(PET)/计算机断层扫描(CT)是筛查骨转移的主要影像学手段。其中,ECT是目前筛查骨转移的首选方法。18F-FDG PET/CT对溶骨性和骨髓转移最为敏感,可作为不明原因骨转移患者的首选影像学检查。此外,CT和MRI也是常用的影像学检查方法。
实验室检查:
除了上述影像学检查外,生化检查也具有重要意义。骨转移患者的循环游离DNA(cfDNA)浓度通常较高,且与较差的生存预后相关。因此,检测cfDNA浓度可以为患者的临床预后管理提供重要参考。此外,尿液标志物的检测也具有价值,例如循环肿瘤DNA(ctDNA)水平的降低通常预示着更好的总体生存结果。血清学标志物,如糖链抗原125(CA 125)、癌胚抗原(CEA)、神经元特异性烯醇化酶(NSE)、鳞状细胞癌抗原(SCCA)以及血清I型胶原羧基末端肽(ICTP)等,也可用于肺癌骨转移的诊断。
病理学检查:
病理检查是诊断肺癌骨转移的金标准。通常,临床医生需要综合影像学检查、实验室检查和病理检查来确诊肺癌骨转移。
当前治疗方法
手术:
对于临床N0-1期且伴有同步骨转移的NSCLC患者,进行原发性肺肿瘤切除术可能会获得更长的生存期。
靶向治疗:
分子靶向治疗是一种新型的生物治疗模式,通过在分子水平上阻断肿瘤信号通路来抑制肿瘤细胞生长。对于携带EGFR基因敏感突变的NSCLC骨转移患者,EGFR-TKI可作为一线治疗选择,并能延长患者生存期。对于EGFR-TKI治疗后进展且T790M阳性的患者,推荐使用奥希替尼。Buparlisib是一种磷酸肌醇3激酶(PI3K)抑制剂,可抑制破骨细胞的形成,具有抗肿瘤活性,因此靶向PI3K通路可能是一种潜在的治疗策略。他汀类药物可以通过阻断RhoA和Ras的翻译后修饰直接抑制破骨细胞生成和癌细胞的增殖。因此,他汀类药物如氟伐他汀可以抑制肿瘤进展,大大降低肿瘤细胞迁移和侵袭的能力。地舒单抗是一种针对RANKL的单克隆抗体,可以显著提高无骨转移生存率。卡博替尼是一种口服的MET和VEGFR2多靶点小分子抑制剂,临床活性表现为改善无进展生存期(PFS)。
表1 肺癌常用的靶向药物

双膦酸盐:
一些双膦酸盐具有直接的抗肿瘤作用,可用于治疗肺癌骨转移,减少SREs并改善疼痛症状。含氮双膦酸盐(如唑来膦酸)通过抑制破骨细胞介导的骨破坏来延缓骨肿瘤的生长。
放射治疗:
放射治疗是治疗肺癌骨转移的有效方法之一,包括体外放射治疗和放射性核素治疗,通过这种治疗可以减轻或消除一系列症状,减轻病理性骨折,减轻脊髓压迫,提高患者生活质量,并且延长其生存期。
化学治疗:
化疗广泛用于治疗肺癌骨转移,可有效缓解患者疼痛。但常规化疗药物存在毒性反应和骨髓抑制等副作用,因此临床应用时应谨慎选择。
总结
肺癌骨转移是肿瘤细胞经侵袭、迁移、侵入骨组织并定植的过程,受到遗传、微环境和粘附因子的共同影响。目前,影像学检查、生化检查和病理检查是诊断肺癌骨转移的主要手段,其中病理检查为诊断的金标准。手术、放疗、靶向治疗以及双膦酸盐治疗是目前临床常用的治疗方法。
尽管现有的诊断和治疗手段已取得一定进展,但仍有许多问题亟待解决。首先,肺癌骨转移涉及的机制非常广泛,任何一个环节的改变都可能加速转移进程。特别是罕见的成骨性转移,其是否存在及其独特机制仍需进一步确认。其次,目前用于预防和延缓SREs发生的药物(如双膦酸盐和地舒单抗)主要靶向破骨细胞,长期使用会增加患者发生骨质疏松和骨折的风险 。这些药物本身也可能引发颌骨坏死等副作用。如何有效预防药物导致的骨折,是肺癌骨转移治疗中亟待解决的难题之一 。
[1] Zhang L, Gong Z. Clinical Characteristics and Prognostic Factors in Bone Metastases from Lung Cancer. Med Sci Monit 2017;23:4087-94.
[2] Wu S, Pan Y, Mao Y, Chen Y, He Y. Current progress and mechanisms of bone metastasis in lung cancer: a narrative review. Transl Lung Cancer Res. 2021 Jan;10(1):439-451.
排版编辑:肿瘤资讯-IRIS











 苏公网安备32059002004080号
苏公网安备32059002004080号


