肺癌是中国发病率和死亡率最高的恶性肿瘤,可分为非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)。NSCLC占全部肺癌的80%~85%。在NSCLC患者中,ALK融合基因阳性的发生率为5%,中国NSCLC患者为3%~11%1。针对这一靶点,ALK酪氨酸激酶抑制剂(TKI)的研发显著改善了晚期患者的预后,当前国内已经有三代共八种ALK-TKI获批,使晚期ALK阳性NSCLC逐步慢性化。
近年来,ALK-TKI的应用场景正从晚期向早期拓展。ALINA研究2的公布标志着ALK-TKI成为ALK阳性NSCLC患者术后辅助治疗的标准选择,目前也已有一些病例报告及小样本临床研究探讨ALK-TKI新辅助治疗的有效性及安全性。布格替尼作为第二代ALK-TKI,一线治疗晚期ALK阳性NSCLC患者中位无进展生存期(mPFS)达24个月,系统疗效、脑转移控制、安全性方面均展现优势,为晚期患者提供了一线治疗优选3。然而,针对局部晚期不可切除患者的转化治疗证据仍显不足。
在此背景下,西安交通大学第一附属医院肿瘤内科傅潇博士分享了一例IIIB期ALK融合突变NSCLC患者的诊疗经历,该患者通过布格替尼转化治疗后成功实现手术切除,这一病例不仅为局部晚期不可切除患者的治疗提供了新的思路和参考,还丰富了布格替尼在转化治疗领域的临床证据,有助于推动该领域相关研究的进一步开展。同时,我们也邀请到了西安交通大学第一附属医院肿瘤内科的姚煜教授和胸外科的张广健教授,从内外科角度点评本次布格替尼临床病例。
病例介绍
病例分享
西安交通大学第一附属医院肿瘤内科
全国卫生产业企业管理协会精准医疗分会委员
中国抗癌协会肿瘤标志物委员会外泌体技术专家委员会委员
陕西省预防医学会肿瘤预防专业委员会委员
陕西省抗癌协会老年肿瘤专业委员会委员
陕西省抗癌协会中西整合肿瘤专业委员会委员
西安医学会精准医学分会委员
主持国家自然科学基金1项、陕西省自然基金1项、西安市科技计划项目1项
患者基本情况及基线特征
该患者为男性,44岁,因“体检发现肺结节1周”于2024年8月就诊。患者有长期吸烟史(约24年,平均40支/日)和饮酒史(约24年,平均250克酒精量/次,2 - 3次/周),无特殊既往史和家族史。
2024-08患者体检发现右肺中叶结节,同时无发热,盗汗,咳嗽,咳痰,胸闷,气短,乏力及胸背部疼痛不适。遂就诊于我科复查胸部增强,检查结果显示:1.右肺中叶内侧段有不均匀强化结节影;右肺门区、纵隔多发增大不均匀强化淋巴结影;呈恶性病变征象。2.右侧锁骨上区稍大淋巴结影;双肺多发实性小结节影;建议随上述病变复查(图1)。
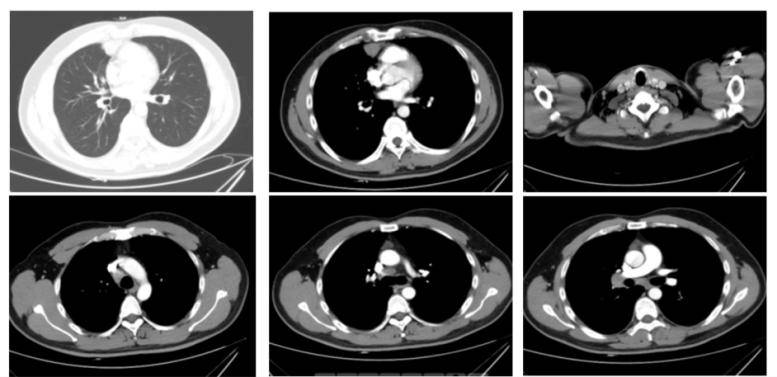
体格检查:T36.1℃,P94次/分,R 20次/分,Bp 126/ 94mmHg,身高170cm,体重58kg。发育良好,营养良好,正常面容,神志清醒,自主体位,查体合作。ECOG 0分。
心肺查体未见明显异常。
辅助检查:血气分析、血常规、肝肾功、电解质、凝血、肌钙蛋白T、肌钙蛋白I、ProBNP未见异常。
头颅MRI、全身骨显像未见明显异常。
初步诊断
患者肺占位性病变 肺癌?
锁骨上淋巴结和纵隔淋巴结肿大 转移?
诊断经过
2024-8-29在局部浸润麻醉下行CT引导下肺穿刺活检术。“右肺中叶结节穿刺活检”病理检测结果显示为非小细胞癌伴坏死,结合免组染色提示低分化腺癌。CK7(+)、TTF-1(+)、NapsinA(+)、p40(-)、p63(-)、CK5/6(部分+)、PD-L1(TPS:+20%)、ALK(D5F3)(+)、Ki67(70%)(图2)。
基因检测:ALK-EML4融合突变(图3)。因此,结合病理及基因检测,修正诊断为右肺腺癌 cT1N3M0,IIIB期不可切ALK融合突变。

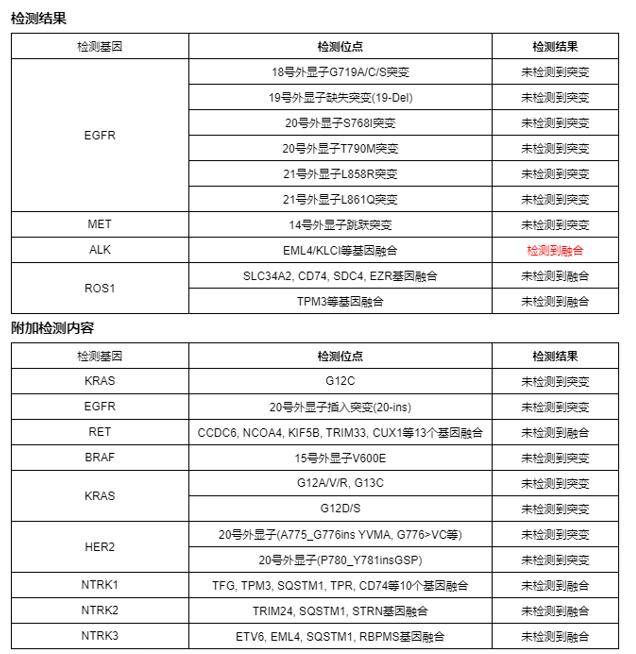
治疗方案及疗效评估
2024-09患者开始布格替尼靶向治疗。2024-10行2周期培美曲塞+顺铂化疗。疗效评价PR。
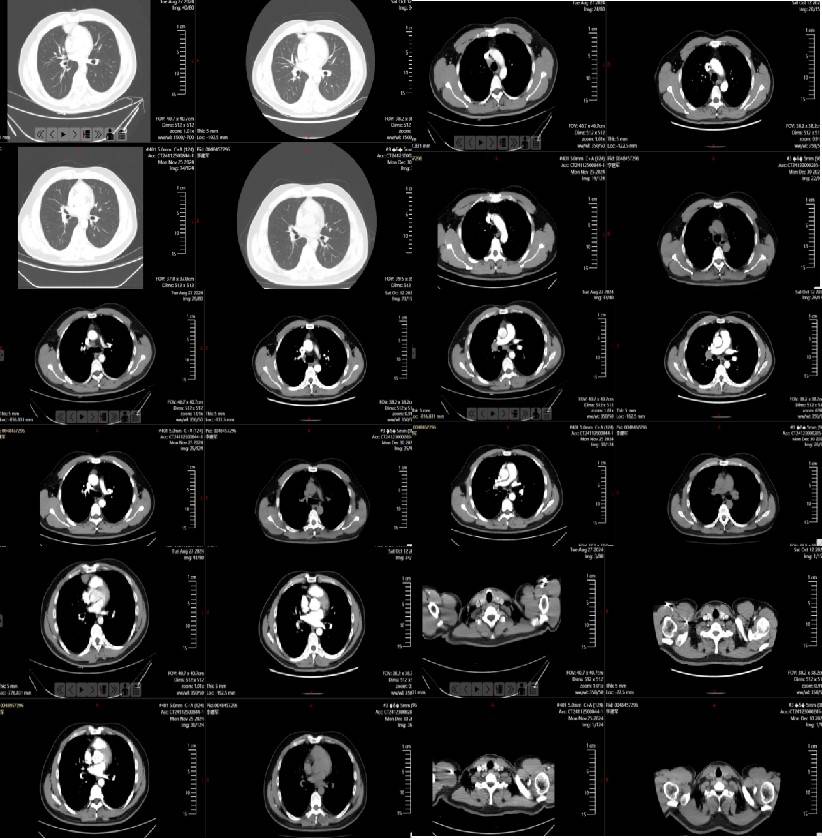
经医院胸外科专家和肿瘤内科团队对该病例患者MDT会诊,评估后制定相应手术方案,并于2025-01对该患者行胸腔镜下右肺中叶癌根治术+纵隔肿物切除术+右肺下叶背段切除术。
术后送检标本信息如下:肉眼所见:送检“右中叶”肺切除标本,肺叶体积10cmx6cmx3cm,肺膜灰红色,尚光滑,带支气管长1cm,直径1.3cm,距支气管切缘3cm处可见一挂线,于挂线下方见一结节,直径1.2cm,灰白色,质硬,与周围肺组织界限不清,距肺膜0.1cm,余肺组织灰红色,质软;肺门检见淋巴结2个,直径0.3-0.6cm。另送“右下叶背段”肺切除标本,肺叶体积7cmx4.5cmx3cm,肺膜灰红色,尚光滑,带支气管长0.5cm,直径2cm,未见明显肿物,余肺组织灰红色,质软;肺门检见淋巴结1个,直径0.4cm。另送“纵隔肿物”囊壁样组织,面积3cmx1cm,两侧面均灰白色,尚光滑,壁厚0.1cm。另送“2、4组”淋巴结2个,“7组”淋巴结2个,“10组”淋巴结2个,“11组”淋巴结1个,“12组”淋巴结1个,直径0.6-1cm。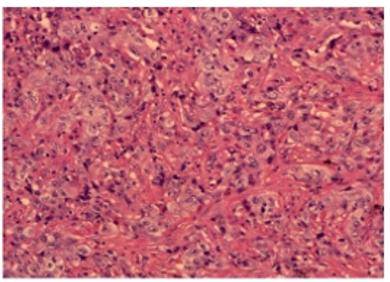
术后病理诊断
“右中叶”肺周围型低分化癌(具体类型待补充报告)伴治疗反应,未侵及肺膜(治疗后评估:残存活肿瘤细胞约占50%,间质约占50%),支气管切缘未见癌组织,肺门(2个)淋巴结未见癌转移,“纵隔肿物”胸腺囊肿“2、4组”(2个)、“7组”(2个)、“10组”(2个)、“11组”(1个)、“12组”(1个)淋巴结未见癌转移,“右下叶背段”肺组织慢性炎伴局部间质纤维组织增生、炭末沉积,支气管切缘未见病变组织,肺门(1个)淋巴结反应性增生。
术后诊断评估
右肺腺癌 ypT1bN0M0,IA2期ALK融合突变。
同时,患者术后复查PET-CT未见明显异常。2025-02继续布格替尼靶向治疗。
专家点评
西安交通大学第一附属医院肿瘤内科主任
中国临床肿瘤学会(CSCO)理事
中华肿瘤学会姑息治疗学组副组长
国家肿瘤质控中心肺癌质控专委会委员
国家肿瘤质控中心抗肿瘤监测专委会委员
中国健康促进基金会肺癌专委会主任委员
中国老年学和老年医学学会肿瘤心理学分会副主委
中国医药教育协会肿瘤化疗专委会副主委
中国医药教育协会肿瘤转移专委会副主委
CACA黑色素瘤专委会副主任委员
CSCO肺癌专业委员会常委
陕西省抗癌协会常务理事
陕西省抗癌协会化疗专业委员会主任委员
西安市医学会肿瘤学分会主任委员
陕西医学会肿瘤内科专业委员会常委
JCO中文编委
本病例为一例44岁男性患者,因体检发现右肺中叶结节就诊,最终诊断为右肺腺癌cT1N3M0,IIIB期,携带ALK-EML4融合突变。患者接受了布格替尼联合化疗转化治疗及胸腔镜手术切除,术后病理显示ypT1bN0M0,IA2期,预后良好。
III期NSCLC的治疗一直是临床中的难点。这类患者通常处于局部晚期,肿瘤较大或伴有淋巴结转移,但尚未发生远处转移。传统治疗手段包括手术、放疗和化疗,但对于ALK阳性患者,传统化疗的疗效有限,手术切除率低,且预后不佳。许多III期NSCLC患者在确诊时已失去手术机会,即使能够手术,术后复发率也较高。因此,探索新的治疗策略对于改善患者的预后至关重要。
近年来,一些研究已经显示出ALK-TKI在术前治疗中的潜力。例如,ALNEO4和NAUTIKA15等研究的初步结果令人鼓舞,表明ALK-TKI在术前治疗中能够显著缩小肿瘤体积,部分患者在手术后的病理检查中显示出肿瘤负荷的显著降低。这些研究结果为ALK-TKI在术前的应用提供了重要的理论基础。
布格替尼作为第二代ALK-TKI,在晚期ALK阳性NSCLC治疗中展现出色疗效。ALTA-1L研究显示,布格替尼治疗初治ALK阳性晚期NSCLC患者, BIRC确认的mPFS显著优于克唑替尼,达到24个月,而克唑替尼为11.1个月(HR=0.48,P<0.0001)3。这些数据证实了布格替尼强大的抗肿瘤活性和良好的安全性。
基于布格替尼在晚期ALK阳性NSCLC中的出色疗效及ALK-TKI在局晚期患者中的应用潜力,经MDT讨论后,治疗团队决定给予本病例布格替尼转化治疗方案。治疗过程中,患者先接受布格替尼靶向治疗,随后进行化疗,最终通过胸腔镜手术成功切除肿瘤,术后病理显示患者达到ypT1bN0M0,IA2期。通过这种治疗策略,患者的肿瘤负荷显著降低,手术切除率提高,预后得到改善。术后,患者继续接受布格替尼靶向治疗,以进一步降低复发风险并巩固治疗效果。
该病例的成功为局部晚期不可切除患者的治疗提供了创新思路和临床参考,还为布格替尼在转化治疗领域的应用积累了宝贵的临床数据支持。未来需进一步探索布格替尼等ALK-TKI在不同阶段NSCLC中的应用价值,尤其是在转化治疗中的最佳用药时长、联合方案及疗效预测标志物,以优化个体化治疗策略。此外,还需要开展更多前瞻性、多中心的临床研究,以验证其在提高手术切除率和长期生存率方面的潜在价值。随着对ALK阳性NSCLC生物学行为的深入了解和新治疗策略的不断探索,布格替尼有望为更多患者带来长生存的希望。
西安交通大学第一附属医院 胸外科主任
陕西省中西医结合加速康复重点研究室主任
三秦英才特支计划—科技创新领军人才
中华医学会器官移植分会肺移植学组、质控学组委员
中国康复医学会外科快速康复专委会副主委
中国医药教育协会胸外科专委会常委
中国抗癌协会肺部肿瘤整合康复专委会常委
中国老年保健协会肺癌专业委员会常委
中国健康促进基金会肺癌专业委员会副主委
陕西省医师协会肿瘤多学科专委会副主委
第十八届陕西省青年五四青年奖章
第十三届陕西省青年科技奖
局部晚期NSCLC的手术可行性高度依赖MDT团队对肿瘤生物学行为及治疗反应的精准评估。本例患者经布格替尼联合化疗转化治疗后,原发灶及转移淋巴结显著退缩,纵隔肿物术后病理证实为胸腺囊肿,淋巴结未见癌转移,最终实现R0切除。这一结果凸显了布格替尼转化治疗在降低肿瘤分期、改善手术结局中的关键作用。
术后送检标本病理诊断显示,治疗后残存活肿瘤细胞占比50%,提示肿瘤对布格替尼治疗敏感。转化治疗显著降低了肿瘤负荷,原发灶体积缩小及淋巴结转移灶的消退,为微创手术提供了有利条件。术中未见明显粘连或组织纤维化,手术难度、手术时长未因前期治疗增加。术中结合胸腔镜技术,通过高分辨率影像实时导航,精准定位原发灶及淋巴结清扫范围,既确保了肿瘤的根治性切除,又最大限度保留了正常肺组织功能。术后病理证实支气管切缘及淋巴结均无癌残留,进一步验证了转化治疗联合精准外科技术的协同效应。此外,术后复查PET-CT未见异常代谢灶,提示当前治疗策略有效控制了局部及潜在微转移风险。
总体而言,本病例成功体现了多学科协作下转化治疗与微创外科的深度融合,为局部晚期ALK阳性NSCLC的个体化治疗提供了重要参考。此外,推动更多前瞻性研究验证转化治疗对手术切除率及长期生存的影响,将有助于完善局部晚期ALK阳性NSCLC的诊疗规范。

1.中国医疗保健国际交流促进会肿瘤内科学分会, 中国医师协会肿瘤医师分会. Ⅳ期原发性肺癌中国治疗指南(2024版)[J]. 中华肿瘤杂志, 2024, 46(7):595-636. DOI:10.3760/cma.j.cn112152-20240311-00104.
2. Alectinib in Resected ALK-Positive Non-Small-Cell Lung Cancer. N Engl J Med. 2024;390(14):1265-1276. doi:10.1056/NEJMoa2310532.
3. Camidge DR, et al. Brigatinib versus Crizotinib in ALK-Positive NSCLC: Final Results of ALTA-1L. J Thorac Oncol. 2021;16(12):2091-2108.
4. Alessandro Leonetti, et al. Neoadjuvant Alectinib in Potentially Resectable Stage III ALK-positive NSCLC: Interim Analysis of ALNEO-GOIRC-01-2020 Phase II Trial. MA01.03, 2024 WCLC.
5. Jay M. Lee, et al. NAUTIKA1 Study Preliminary Efficacy and Safety Data with Neoadjuvant Alectinib in Patients with Stage IB-III ALK+ NSCLC. 2023 WCLC Poster no. 1795.
审批编号:VV-MEDMAT-122959
审批日期:2025年6月
仅供医疗卫生专业人士使用
排版编辑:肿瘤资讯-LWT











 苏公网安备32059002004080号
苏公网安备32059002004080号


