2025 年 5 月 刊的《 The Lancet Oncology 》杂志,在线发表了题为《 Outcomes based on risk-adapted adjuvant therapy in postmenopausal women with early breast cancer: a nationwide, prospective cohort study by the Danish Breast Cancer Group 》( 基于风险调整辅助治疗的绝经后早期乳腺癌患者的结局 :丹麦乳腺癌协作组的一项全国性前瞻性队列研究 )。

研究主要内容
本研究通过丹麦全国性队列( 2013 年 8 月 -2018 年 12 月,纳入 8,921 例患者)首次在真实世界验证了预后标准死亡率指数( PSI )对 ER+/HER2- 早期乳腺癌辅助化疗决策的指导价值。结果显示:
1. 低危组( PSI 1 ,占 75% ): 仅接受内分泌治疗的 5 年标准死亡率比( SMR=0.89 )与普通人群无差异,证实豁免化疗的可行性 ;
2. 中高危组( PSI 2-4 ):完成化疗联合内分泌治疗的患者 5 年复发风险显著降低( PSI 2 组 SMR=1.71 , PSI 3-4 组 SMR=2.39 ),但高危人群仍需探索新疗法(如 CDK4/6 抑制剂);
3. 依从性影响: 未完成内分泌治疗者死亡风险升高 62% ( HR=1.62 ),提示需优化患者管理。该研究为 ER+ 乳腺癌个体化治疗提供了基于临床病理特征的低成本分层框架。
研究背景
本研究聚焦于雌激素受体阳性( ER+ ) /HER2 阴性( HER2- )早期乳腺癌患者术后辅助治疗的个体化决策问题。丹麦乳腺癌协作组( DBCG )开发了一种 基于临床病理特征的预后标准死亡率指数( Prognostic Standard Mortality Rate Index, PSI ),旨在通过整合患者年龄、肿瘤特征(如大小、淋巴结状态、组织学分级等)和合并症等因素,预测仅接受内分泌治疗的 5 年超额死亡率。
前期研究基础
PSI 的起源与验证
PSI 的开发基于 1996-2004 年丹麦 6,259 例绝经后患者的回顾性队列数据。该模型通过多变量分数多项式( multivariable fractional polynomials )将 肿瘤大小、淋巴结状态、组织学分级、淋巴管浸润和 ER 表达水平等参数与年龄相关的竞争性死亡风险相结合,将患者分为 4 个风险组( PSI 1-4 ) 。原始研究显示, PSI 1 组(低危)仅需内分泌治疗即可获得与非乳腺癌人群相似的生存率,而 PSI 3-4 组(高危)即使完成内分泌治疗仍存在显著超额死亡风险 ( HR=3.3 )。
2. 临床指南的演变
2013 年 8 月, DBCG 将 PSI 纳入国家指南,取代了传统的 St. Gallen 标准,用于指导 ER+/HER2- 早期乳腺癌的辅助化疗决策。 PSI 1 组推荐单纯内分泌治疗, PSI 2-4 组推荐化疗联合内分泌治疗。 这一决策基于早期研究显示,化疗对中高危患者的生存获益显著( 10 年绝对获益约 5-10% ),但对低危患者可能带来不必要的毒性。
3. 国际研究的对比
PREDICT 模型: 英国广泛使用的预后工具,基于临床病理参数预测生存率,但未整合竞争性死亡风险,可能高估老年患者的化疗获益。
TAILOR-X 与 MINDACT 试验: 证实 21 基因检测( Oncotype DX )和 70 基因检测( MammaPrint )可识别化疗不敏感的低危人群,但这些基因检测在丹麦未常规应用。
EBCTCG 荟萃分析: 支持化疗在淋巴结阳性或高风险淋巴结阴性患者中的生存获益,但缺乏针对老年人群的数据。
未解决的临床问题
1. 老年患者与合并症人群的代表性不足: 临床试验常排除≥ 70 岁或有合并症患者,导致指南在这些人群中的外推证据薄弱。
2. 治疗依从性的影响: 内分泌治疗完成率在真实世界中仅为 50-70% ,远低于临床试验的 85% ,但 PSI 模型未纳入依从性因素。
3. 化疗方案的选择: 丹麦指南推荐 EC-T 方案 (表柔比星 + 环磷酰胺序贯紫杉类),但剂量密集方案或含铂方案可能更优,需进一步验证。
研究方法
设计:全国性前瞻性队列研究( 2013 年 8 月 -2018 年 12 月),纳入绝经后(≥ 50 岁) ER+/HER2- 早期乳腺癌患者,术后接受 PSI 指导的辅助治疗。数据来源:丹麦乳腺癌临床数据库( DBCG ),覆盖全国 95% 以上的乳腺癌病例,通过丹麦民事登记系统链接生存数据。
纳入标准:术后病理确诊为 ER+ (≥ 10% 染色)且 HER2- ( IHC 0/1+ 或 2+ 且 FISH 阴性);满足以下任一条件:
1. 1-3 枚阳性淋巴结;2. 淋巴结阴性且年龄 <60 岁;3. 淋巴结阴性、年龄≥ 60 岁且肿瘤 >10mm 或中 / 高分级。排除标准:转移性乳腺癌、双侧乳腺癌、既往恶性肿瘤史、未按指南接受手术。
PSI 分类与治疗推荐
PSI 算法: 基于年龄、肿瘤大小、淋巴结状态、组织学类型、分级、淋巴管浸润和 ER 表达水平自动计算,分为 4 组:
PSI 1 (低危):推荐 5 年内分泌治疗( AI 或 AI+ 他莫昔芬序贯);
PSI 2-4 (中高危):推荐化疗( EC-T 方案)联合内分泌治疗。
2017 年更新: PSI 2 组增加 PAM50 基因分型, Luminal A 亚型豁免化疗 (本研究排除该亚组)。
终点指标
1. 主要终点:标准死亡率比( Standard Mortality Ratio, SMR ):观察死亡数 / 预期死亡数(基于丹麦一般人群死亡率)。
2. 次要终点:总生存期( OS ):手术至全因死亡;无复发生存期( RFS ):手术至局部 / 远处复发或对侧乳腺癌;治疗依从性:内分泌治疗完成(≥ 4.5 年)或化疗完成(≥ 4 周期)。
研究结果
患者基线特征(表 1 ):人群分布: 共纳入 8,921 例, PSI 1 组占 75% ( 6,704 例), PSI 2-4 组分别占 15% ( 1,300 例)、 8% ( 745 例)和 2% ( 172 例) 。
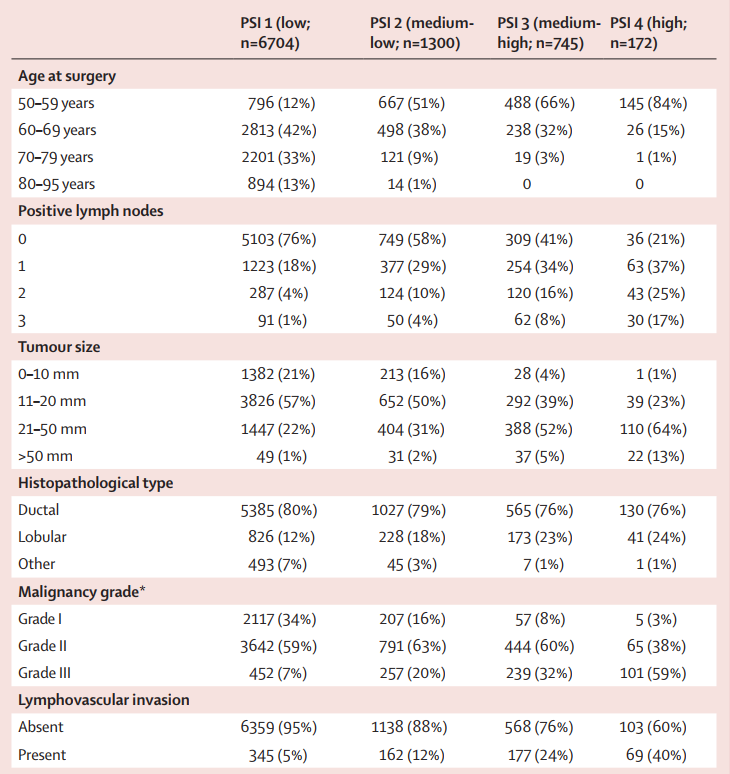

年龄与肿瘤特征:PSI 1 组中位年龄 68 岁( IQR 63-75 ), PSI 4 组中位年龄 58 岁( IQR 54-62 );淋巴结阳性比例随 PSI 升高显著增加 ( PSI 1 组 24% vs. PSI 4 组 79% );肿瘤 >50mm 在 PSI 4 组占 13% ,而 PSI 1 组仅 1% 。合并症: PSI 1 组 Charlson 指数≥ 3 者占 12% ,与年龄分布相关( p=0.48 )。
治疗依从性(表 2 ):内分泌治疗:PSI 1 组完成率 65% ( 4,358/6,704 ),未完成原因包括早期停药( 10% )和未启动( 4% );PSI 2-4 组完成率 70% ( 905/1,300 )、 67% ( 500/745 )和 70% ( 120/172 )。
化疗:PSI 2 组 66% ( 854/1,300 )完成化疗, PSI 3-4 组完成率 83% ( 618/745 )和 85% ( 146/172 );剂量强度:表柔比星( 96.6% )、多西他赛( 84.3% )、紫杉醇( 82.9% )。

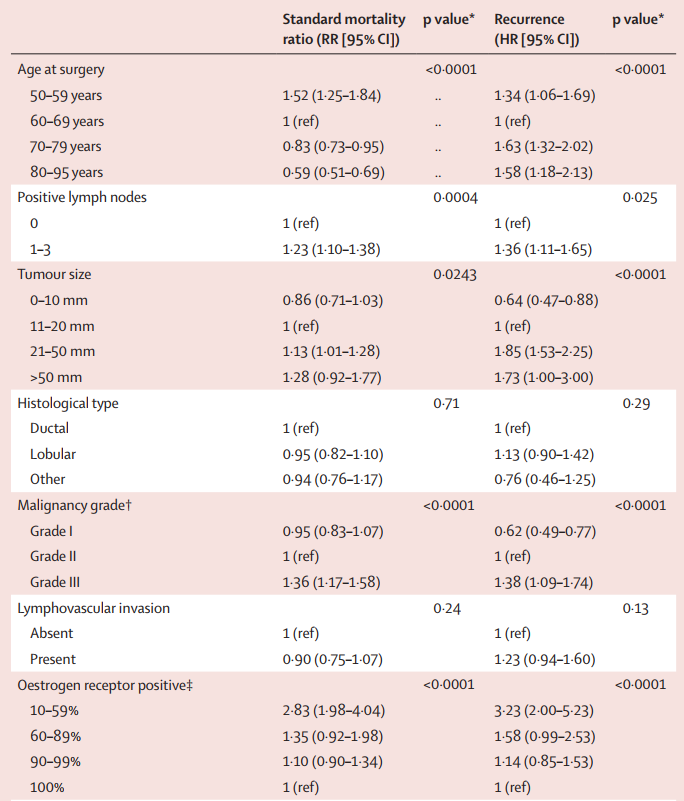
生存结局 (表 3 ,图 2 ):PSI 1 组 SMR=0.89 ( 95% CI 0.85-0.95 ),表明无超额死亡;PSI 2 组 SMR=1.71 ( 1.47-1.97 ), PSI 3-4 组 SMR=2.39 ( 1.99-2.88 );未完成治疗者死亡风险显著升高( HR=1.62 , p<0.0001 )。
复发风险:5 年累积复发率: PSI 1 组 3.8% vs. PSI 3-4 组 7.7% ;未完成内分泌治疗者复发风险升高 3.79 倍( 95% CI 3.19-4.50 )。


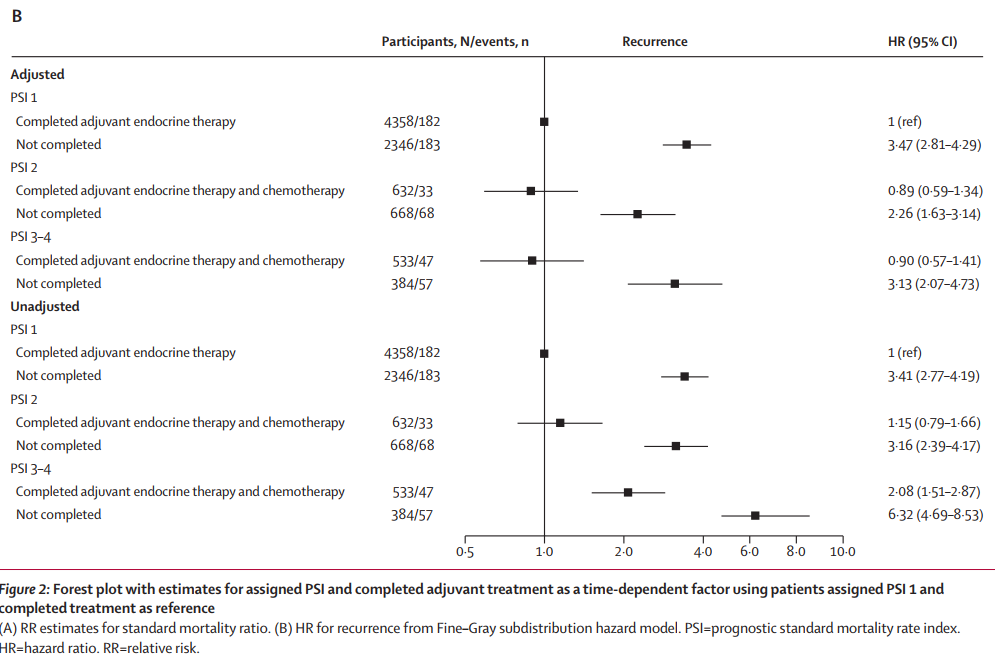
分层分析 (图 2 ):PSI 2 组完成化疗 + 内分泌治疗者 SMR=0.90 ( 0.66-1.22 ), 与 PSI 1 组相当 ;PSI 3-4 组即使完成治疗, SMR 仍达 2.31 ( 1.74-3.05 )。
研究讨论与结论
本研究首次在真实世界验证了 PSI 作为辅助治疗决策工具的实用性:
1. 低危人群( PSI 1 ):仅内分泌治疗的 5 年 SMR 为 0.89 ,与一般人群无差异,支持豁免化疗的可行性。
2. 中危人群( PSI 2 ):完成化疗 + 内分泌治疗的 SMR=1.71 , 10 年复发率 11.4% ,提示现行方案有效但需关注依从性(完成率仅 49% )。
3. 高危人群( PSI 3-4 ):即使完成治疗, SMR 仍高达 2.39 ,提示需探索 CDK4/6 抑制剂或强化化疗方案。
与现有证据的对比:
PREDICT 模型:本研究显示 PSI 在整合竞争性死亡风险(尤其是老年患者)方面更具优势, PREDICT 可能高估化疗获益。
TAILOR-X 试验: 21 基因检测可将化疗豁免人群扩大至中危组,但 PSI 通过临床参数实现了相似分层,成本效益更高。
EBCTCG 数据:本研究验证了化疗在 PSI 2-4 组的生存获益( HR=0.76 ),与 EBCTCG 的 10 年绝对获益 5% 一致。
局限性
选择偏倚:排除 PAM50 分型的 PSI 2 亚组可能低估基因检测的价值。
化疗方案: EC-T 方案非剂量密集型,可能弱化高危组疗效(对比 CALGB 9741 的密集方案)。
随访时间:中位随访 7 年,尚未捕获全部晚期复发事件。
未来方向
整合多基因检测: PAM50 或 Oncotype DX 可能优化 PSI 2-4 组的分层。
新型治疗策略:CDK4/6 抑制剂(如阿贝西利)在 monarchE 试验中显示高危患者 DFS 获益( HR=0.66 );免疫检查点抑制剂( KEYNOTE-756 )在 NeoALTTO 试验中病理完全缓解率( pCR )提升。
老年患者管理:需开发简化风险评估工具(如简化 PSI )以指导合并症患者的治疗强度。
结论
PSI 为 ER+/HER2- 早期乳腺癌提供了高效、低成本的个体化治疗决策框架。其临床实用性不仅体现在避免低危患者过度治疗,更重要的是识别出需要创新疗法的高危人群。未来需结合基因组学与新型系统性治疗,进一步提升分层精准度。











 苏公网安备32059002004080号
苏公网安备32059002004080号


