随着免疫治疗在肝癌领域取得突破性进展,肝癌治疗已进入免疫治疗时代。嵌合抗原受体修饰的T细胞(CAR-T)治疗作为免疫治疗的一种方式,其在晚期肝癌治疗中的潜力正被积极探索,相关临床研究正在开展。然而,需要注意的是CAR-T治疗会引发一些不良反应,例如抗肿瘤治疗所致血小板减少症(CTIT)。CTIT可导致抗肿瘤治疗延迟、减量甚至中止,并增加出血及严重并发症风险,危害患者生存和生活质量。因此,积极防治CTIT是包括肝癌在内恶性肿瘤全程管理的重要内容。
本期特邀同济大学附属上海市第十人民医院杨静主治医师分享一例晚期肝癌病例诊治经过。治疗团队对该患者探索性开展CAR-T治疗临床研究,收到一定疗效,但过程中出现了血小板减少症,重组人血小板生成素(rhTPO)不能有效升板,及时联用海曲泊帕后疗效显著,保障了后续抗肿瘤治疗的顺利进行。同时,本期特邀同济大学附属上海市第十人民医院许青教授对病例给予精彩点评,分享CTIT全程管理经验。
同济大学附属上海市第十人民医院肿瘤科主治医师
肿瘤学博士
长期从事恶性肿瘤的诊治工作,擅长结直肠癌、胃癌等疾病诊治
主持“国家自然科学基金青年项目”1项。第一作者发表SCI论文5篇
病例介绍
1病历资料:
患者,女,35岁。
初次就诊日期:2023年1月29日。
主诉:肝癌首次术后4年半,复发术后近4年。
现病史:患者于2018年7月15日因反复上腹部胀痛不适就诊于当地医院,完善检查示:甲胎蛋白(AFP)升高(具体不详),腹部MRI提示肝右叶(VI-VII段)占位性病变,考虑肝癌可能性大;肝炎指标提示乙肝小三阳。2018年7月21日行肝癌切除+肠粘连松解术+肠排列术,右后叶切除,确诊肝细胞癌pT2N0M0 II期,Child-Pugh A,术后行经导管动脉化疗栓塞术(TACE)。患者分别于2019年2月、2021年3月、2021年6月出现多次病情进展,先后进行手术治疗、TACE、晚期一线、二线治疗等治疗后,病情再次进展。2023年1月29日,患者为求进一步诊治来院就诊,并于2023年6月入组临床研究。
既往史、个人史、婚育史、家族史:无特殊。
辅助检查:上腹部增强MRI:肝恶性肿瘤术后改变,肝脏多发转移瘤,左叶为著,直径约1.0~3.7cm不等。
肿瘤指标:AFP 973ng/ml。
临床诊断:原发性肝细胞癌(BCLC分期C期)
2诊疗经过:
(1)抗肿瘤治疗经过
2023-02至2023-05
三线治疗行“信迪利单抗200mg d1+贝伐珠单抗 500mg d1 q3w方案”治疗3周期,疗效评价为疾病进展(PD)。
2023-06起
患者入组一项“靶向磷脂酰肌醇蛋白多糖-3(GPC3)嵌合抗原受体修饰的T细胞(CAR-T)治疗晚期肝癌的开放、单臂的临床研究”,接受CAR-T治疗。2023年6月9日起,行清淋预处理:环磷酰胺(CTX)460mg(300mg/m2)d1~3。2023年6月13日,行CAR-T细胞回输(1.75×107 cells/kg,总量1×109cell)。疗效评价为部分缓解(PR)。
2023-06-16至2023-06-28
CAR-T治疗期间出现血小板减少,予rhTPO升板治疗,疗效欠佳,后联用海曲泊帕及输注血小板治疗。
(2)CTIT治疗经过
2023-06-15至2023-06-18
CAR-T治疗期间,患者出现CTIT。6月16日血小板降至74x109/L,加用rhTPO治疗(15000U,qd),但不能有效升板,6月18日血小板降至22x109/L(4级CTIT)且患者四肢、躯干皮肤出现散在出血点。
2023-06-18至2023-06-24
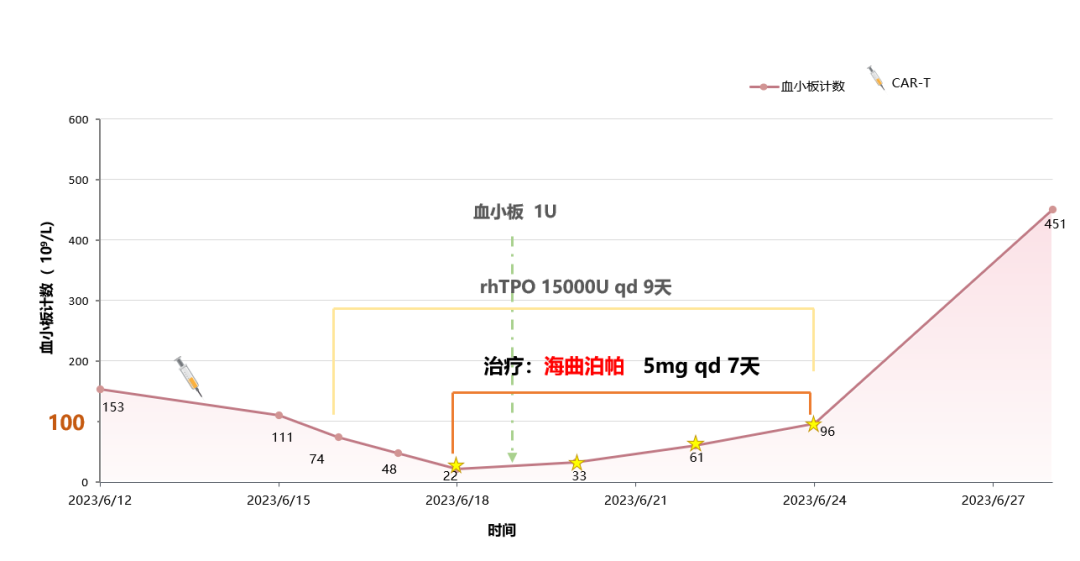
为减少脏器进一步出血风险,6月18日起予以rhTPO联合促血小板生成素受体激动剂(TPO-RA)海曲泊帕(5mg,qd,口服)进行升板治疗7天。6月19日予以血小板1U输注。6月24日血小板恢复至96×109/L,停止海曲泊帕治疗后血小板依然持续升高,6月28日升至451×109/L,无不良反应。
部分升板治疗过程:
诊疗思考
本例为一例转移性肝细胞癌患者。5年前,患者确诊肝癌并行肝癌切除术及TACE治疗;术后7个月后首次复发,进行肝II段肿瘤切除术及TACE治疗;25个月后,患者第二次复发,一线治疗选择了特瑞普利单抗+安罗替尼、TACE,再次出现疾病进展后二线治疗采用替雷利珠单抗+仑伐替尼、TACE+肝脏消融术,但疾病控制不佳。
进入本院后,患者采用信迪利单抗+贝伐珠单抗进行三线治疗,随后依然出现疾病进展。患者自2023年6月起开始CAR-T细胞治疗,治疗进行不久后发生CTIT,血小板计数一度降至仅22×109/L,且rhTPO不能有效升板。故6月18日起,治疗团队及时给予患者加用海曲泊帕,期间还辅以单次血小板输注。治疗后血小板计数有效提升,升至451×109/L,并在从患者用药经过来看,海曲泊帕升板快速、有效且安全性良好,口服给药十分便利,患者依从性良好。海曲泊帕的多重优势保障了患者CTIT的高质量全程管理。
回顾整个治疗经过,CTIT问题在CAR-T治疗启动后不久即出现,患者血小板计数一度跌到十分危险的地步,进展为重度CTIT。及时联用海曲泊帕是化险为夷的关键,海曲泊帕充分展现了作为新一代TPO-RA以及1类新药的疗效优势,与rhTPO、人源血小板联合使用,起到了协同增效的作用,从而使患者迅速转危为安。
总的来说,这是一例典型的使用海曲泊帕进行升板治疗、全程护航患者抗肿瘤综合治疗的成功病例,可供同行参考。
病例点评
Q1:该患者接受CAR-T治疗后出现重度血小板减少,您认为可能原因是什么?临床实践中,接受CAR-T治疗的患者出现血小板减少症的发生率如何?
许青教授:CTIT的发生的原因及机制相对复杂,与含外因与内因在内的多重因素综合作用相关。内因则包括患者自身因素和肿瘤因素等;外因包括抗肿瘤治疗的类型、剂量和周期,例如化疗、放疗、靶向治疗和免疫治疗等均有可能引起CTIT [1]。
患者自身因素方面,尽管本病例为年轻女性,但由于其原发肿瘤在肝脏,且多次复发,肿瘤负荷较重,体力状态较差。需知,血小板生成素(TPO)主要合成部位便是肝脏,肝脏损伤可导致TPO合成相对不足,增加CTIT的发生率[2]。
外因方面,可能与CAR-T细胞治疗有关。有研究显示,血液系统毒性是CAR-T细胞输注后常见的≥3级不良反应[3],可见在CAR-T治疗中血液毒性较为常见。另有一项研究数据进一步揭示了CAR-T治疗的血液毒性相关不良事件发生情况:在该研究中,几乎所有接受CAR-T治疗的患者都发生了血液毒性相关不良反应,分别有96%、81%、79%、62%、53%患者出现中性粒细胞减少症、贫血、血小板减少症、白细胞减少症、淋巴细胞减少症[4]。
总的来说,这些内部因素及外部因素的叠加使得这例患者处于CTIT高风险的状态。对于这类患者,临床团队须在CAR-T治疗全程保持高度警惕,全程监测并准备应对可能发生的CTIT风险。
Q2:您如何看待本患者的升板经过?对于接受CAR-T治疗导致血小板减少症的患者,您一般如何进行管理?
许青教授:本例患者出现CTIT后,首先使用rhTPO进行升板治疗,是符合指南推荐的[1,2]。但患者单用rhTPO仍无法逆转局势,血小板计数持续降低并一度降低到十分危险的22×109/L,属于是重度的CTIT减少,此时患者有着极高的出血风险,亟需升级升板治疗方案。
输注血小板是严重血小板减少症患者的最快最有效的治疗方法之一,然而外源性血小板的寿命通常仅能维持3天左右,为避免患者血小板计数过低危及生命,因此有必要使用促血小板生长因子如海曲泊帕等TPO-RA类药物共同帮助患者升板。
海曲泊帕作为我国首个自主研发1类新药,用于治疗CTIT在多项研究中表现出升板速度快、应答高等特征[5~7],基于其临床价值,海曲泊帕被2023版《中国临床肿瘤学会(CSCO)肿瘤治疗所致血小板减少症诊疗指南》[1]列为Ⅱ级推荐用于CTIT治疗。并且,海曲泊帕不仅可单药应用,也被推荐可联合rhTPO使用,可用于各等级CTIT患者治疗。该例患者出现4级CTIT后,治疗团队给予海曲泊帕与rhTPO联用,是有证可依的。在海曲泊帕联合方案的治疗下,患者血小板数量迅速上升至正常水平,避免了严重出血等严重并发症的出现,确保了后续抗肿瘤治疗的顺利进行。
同时还需注意到,血液毒性是CAR-T最常见的≥3级不良反应,患者出现血液毒性后并非只表现为血小板降低,三系同时降低也较为多见[3,4]。有研究发现[8],海曲泊帕不仅可提升血小板,还可起到 “三系同升”的作用,即对血红蛋白和中性粒细胞同样有升高作用[8]。因此,针对接受CAR-T治疗的患者,海曲泊帕可作为升板治疗主要优选药物,在一定程度上改善患者三系降低的问题。
Q3:从本病例出发,请您谈谈以海曲泊帕为代表的新型升板药物在抗肿瘤治疗相关血小板减少症的患者中的应用前景。
许青教授:肿瘤患者在治疗中出现CTIT将对患者造成严重影响,可能会被迫中断抗肿瘤治疗从而影响生存预后。重症CTIT甚至可能在短期内引起严重的出血,甚至导致患者死亡。对于重度CTIT患者,需要尽快开展能强效提升血小板计数的手段。海曲泊帕为代表的新型升板药物进入临床实践,为临床实践中无法从rhTPO单药治疗中获益人群以及重度CTIT人群带来新选择。
一项回顾性研究[6]分析了血小板计数<50×109/L的重度CTIT患者使用“海曲泊帕+rhTPO”联合疗法的有效性和安全性,其研究结果显示:与单用rhTPO组相比,海曲泊帕+rhTPO组中位治疗时间明显缩短(9.5天 vs 6.5天);并且75%海曲泊帕+rhTPO组患者在治疗7天内获得应答,而rhTPO组仅为30%;整个治疗过程中,海曲泊帕+rhTPO组未发生出血事件,而rhTPO组有1例患者发生出血。在这项回顾性研究中,“海曲泊帕+rhTPO”联合疗法表现出了更快且更有效地提升血小板水平,而不增加安全性顾虑的优势。对于无法从rhTPO单药治疗中获益的患者群体以及重度血小板减少性出血(CTIT)患者群体,这一联合疗法有着非常好的应用前景。
同时,在近期召开的2023年欧洲临床肿瘤学会年会(ESMO 2023)上公布的一项研究结果[7]显示,“海曲泊帕+rhIL-11”联合治疗方案可为重度CTIT患者带来临床获益,且不增加不良事件发生率。“海曲泊帕+”的联合治疗模式为临床治疗重度CTIT提供了新的思路,值得进一步探索。
值得一提的是,海曲泊帕在单药治疗和预防CTIT中也表现出同样出彩的疗效和安全性。在一项评估海曲泊帕治疗CTIT疗效和安全性II期临床研究[5] 结果显示,与安慰剂相比,海曲泊帕单药治疗可显著提高CTIT患者的治疗有效率,更快恢复血小板水平,保障抗肿瘤治疗的顺利进行,且整体的给药安全性和耐受性良好。凭借此项研究成果,海曲泊帕成为首个取得CTIT随机双盲多中心II期注册临床研究阳性结果的口服TPO-RA类药物。近期另有一项研究[7]支持这一结论,其研究结果证实:海曲泊帕单药治疗为轻度CTIT患者提供了一种有效、安全且便利的手段。在CTIT预防领域,一项前瞻性真实世界研究[9]证实,单用海曲泊帕可使所有受试者均可得到有效预防,治疗整体安全性可控。
总而言之,海曲泊帕已在CTIT领域积累起丰富的循证医学证据,兼具有效、安全、口服用药便利等多重优势,贴合CTIT院内外防治实际需求,有望在未来指南推荐和临床实际预防用药中受到进一步推荐。
[1] 中国临床肿瘤学会(CSCO)肿瘤治疗所致血小板减少症诊疗指南2023.
[2] Kuter DJ. Semin Hematol, 2010, 47(3):243‑248.
[3] 2023 ASCO, Abstract 8025.
[4] Lancet. 2021 Jul 24;398(10297):314-324.
[5] Jun Ma, et al. 2023 European Congress of Internal Medicine, Abstract 2360.
[6] 2022 ASH poster 3772.
[7] 2023 ESMO, Abstract FPN2100P.
[8] Fengkui Zhang, et al. Blood 2020; 136 (Supplement 1): 3-4.[9] 2022 ESMO Asia poster 563.
排版编辑:肿瘤资讯-展思懿
版权声明











 苏公网安备32059002004080号
苏公网安备32059002004080号


