病理完全缓解(pCR)被认为是评估新辅助治疗疗效的重要指标,并与患者的长期生存密切相关。然而,尽管pCR与良好的预后相关,但局部晚期人表皮生长因子受体2(HER2)阳性乳腺癌患者即使在达到pCR后,仍面临着较高的复发风险。因此,针对这类患者,采用奈拉替尼等强化辅助治疗策略以进一步降低复发风险显得尤为重要。本文特别分享一例新辅助治疗后达到pCR的HER2阳性乳腺癌患者的治疗经历。该患者在接受6周期的TCbHP方案新辅助治疗后,进行了左乳腺癌改良根治术。术后病理结果显示pCR。为了进一步巩固治疗效果,预防疾病复发,术后在完成11周期的HP双靶辅助治疗联合辅助放疗后,临床继续采用奈拉替尼强化辅助治疗1年。目前,患者的病情保持稳定,整体状况良好。
病例分享
重庆大学附属肿瘤医院,乳腺肿瘤中心,副主任医师,医学博士
毕业于中国医学科学院肿瘤医院 肿瘤学专业
中国抗癌协会第十届乳腺癌专业委员会青年专家
中国医药教育协会肿瘤临床科研创新发展专业委员会委员
中国医疗保健国际交流促进会国际教育培训分会委员
中国医师协会科普分会乳腺学组委员
北京慢性病防治与健康教育研究会肿瘤免疫治疗专业委员会第一届委员会 委员
重庆市医学会肿瘤学专业委员会乳腺学组委员
重庆市外科学委员会甲状腺乳腺癌学组委员会委员
主持国家自然科学基金青年项目及重庆市各项基金项目6项
以第一作/通讯作者在Breast Cancer Research等杂志发表SCI文章12篇,中文核心期刊论文2篇,研究成果在ESMO、KSMO及CSCO等国内外专业领域学术会议上以壁报的形式展示和交流
参编/译肿瘤学专著3部,副主编乳腺癌科普图书1部
《中国肿瘤临床与康复》杂志编委,《中国肿瘤临床》杂志的外审专家
一般情况:
患者:女,年龄47岁。
主诉:确诊“左乳腺癌”半月。
家族史:无特殊。
既往史:既往健康。
个人史:无特殊。
现病史:半月前患者无意间扪及左乳肿块,遂于外院就诊,2023-7-8左乳肿物穿刺活检病理示:左乳浸润性癌,III级。免疫组化:ER(-),PR(-),HER-2(3+),Ki-67(+)20%。左腋窝淋巴结穿刺活检病理示:符合乳腺癌转移,免疫组化:ER(-),PR(-),HER-2(3+),Ki-67(+)15%。为求进一步治疗入院。
入院查体:左乳外上象限可触及大小约4×3.5cm的肿物,质硬,边界欠清,活动度欠佳,局部皮肤无红肿、无破溃无波动感,皮温不高,基底与胸壁有粘连,左腋窝扪及多枚淋巴结肿大,最大约2×2cm,质硬,多个融合,固定;右乳、右腋窝及双锁骨上未及明显肿大淋巴结。
辅助检查:
(1)实验室检查:
血常规、血生化、心肺功能均未见异常。肿瘤指标CA199升高:41.84U/mL(正常范围0-34U/mL)和细胞角蛋白19片段升高:3.84ng/ml(正常范围0-2.03ng/mL)。
(2)影像学检查:
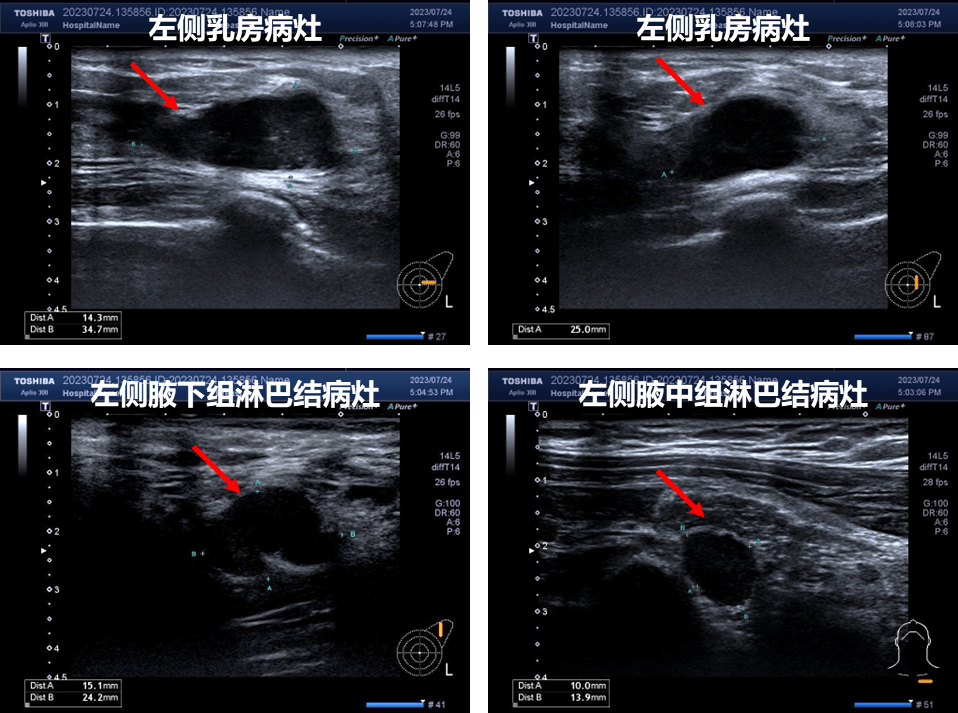
乳腺超声(2023-7-24)示(图1):1、双颈、双颌下淋巴结肿大:反应性?2、左乳异常回声,性质待定(较大位于2点半,大小约14×35×25mm):结合病史考虑乳Ca?(BI-RADS分类6类)。3、左侧腋下组(含腋窝)淋巴结肿大(大小约15×24mm),性质待定:结合病史考虑淋巴M?4、左锁骨上(较大约11×25mm)、左侧腋上组、左侧腋中组(较大约10×14mm)淋巴结肿大,性质待定:淋巴M?建议超声引导下穿刺活检以进一步鉴别其性质。5、右乳异常回声,性质待定:增生结节?囊肿(囊液浑浊)?(BI-RADS分类3类)。6、右锁骨上淋巴结,性质待定:反应性增生?随诊;右侧腋下组(含腋窝)淋巴结肿大:反应性?
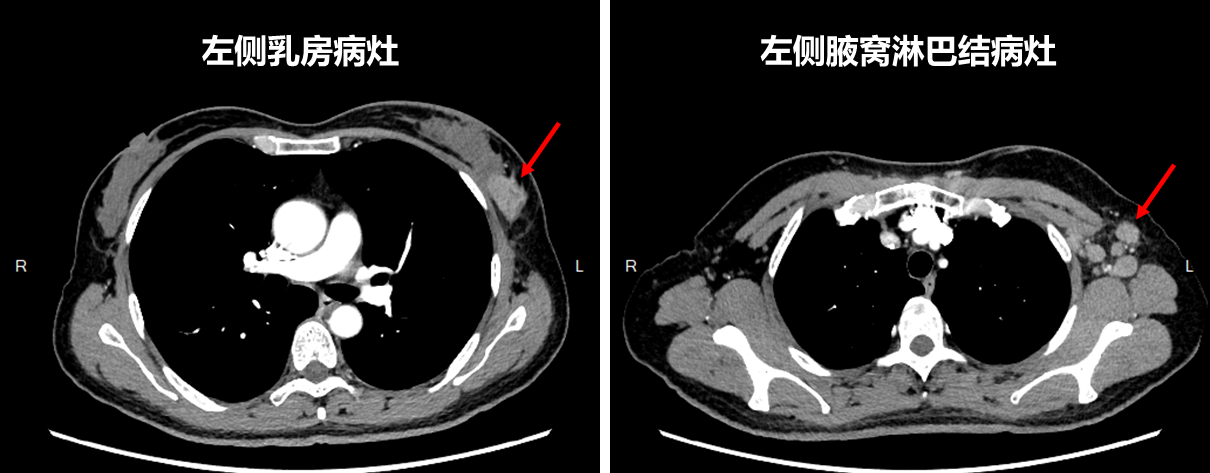
胸部CT(2023-7-24)示(图2):1、左乳外份后部异常强化肿块(2.7cm×1.8cm),请结合MR检查;2、左侧腋窝及胸肌间隙多发淋巴结、部分肿大(大者短径约1.5cm),转移可能;3、双肺多发结节,右肺上叶尖段结节,性质待定,建议随诊;4、右肺中叶内侧段少许慢性炎症;5、左锁骨上区淋巴结显示。
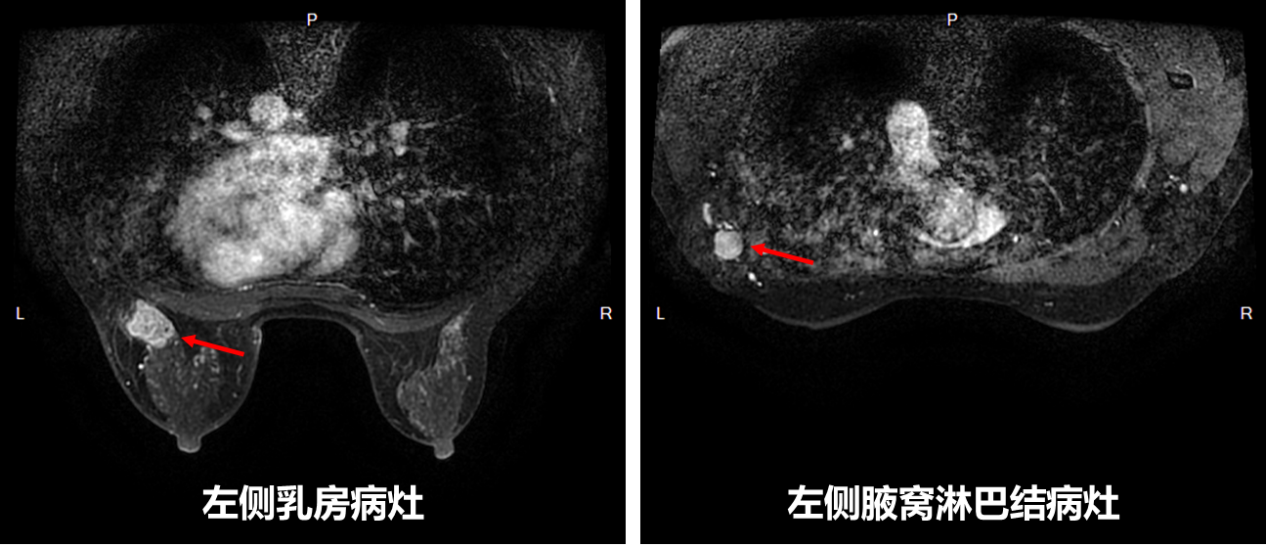
乳腺MRI(2023-7-25)示(图3):1、左乳外份后部肿块(2.6cm×1.5cm×2.4cm),考虑乳腺癌,胸大肌可疑受侵,BI-RADS 6类;2、双乳多发斑点、结节状强化影,BI-RADS 3类,随诊;3、左侧腋窝多发淋巴结肿大(大者短径约1.5cm),考虑转移;4、左侧胸大肌内结节,性质待定,转移待排,随诊。
(3)病理检查:
我院疑难病理会诊(2023-7-25)示:1、“左乳肿物穿刺”:浸润性癌,非特殊类型(III级8分)。2、“左腋窝肿物穿刺”:淋巴结转移癌,符合乳腺癌转移。免疫组化结果示:左乳肿物:ER(-),PR(-),Her-2(3+),ki-67(+)25%。左腋窝肿物:ER(-),PR(-),Her-2(3+),Ki67(+)20%。
超声引导下左锁骨上淋巴结针吸物液基制片(2023-7-27)查见腺癌细胞。病理结果示(左锁骨上淋巴结,2023-7-31):转移性癌,结合临床及免疫组化,符合乳腺癌转移。免疫组化结果示:ER(-),PR(-),Her-2(3+),Ki67(+)15%。
腹部CT、脑MRI以及骨扫描均未见转移征象。
诊断:左乳癌 cT2N3M0 IIIC期 HER2阳性型
治疗经过:
(1)新辅助治疗:
2023年7月28日-2023年11月17日,行6周期TCbHP方案新辅助治疗,具体药物为:多西他赛(110mg)+卡铂(400mg)+曲妥珠单抗(首次432mg,后续320mg)+帕妥珠单抗(首次840mg,后续420mg)。新辅助治疗过程顺利,患者耐受可。2周期治疗后乳腺MRI检查提示左乳外份后部肿块,较前强化程度减轻,范围较前缩小;左侧腋窝多发淋巴结,较前减少,缩小;左侧胸大肌内结节消失。根据实体瘤疗效评价标准RECIST V1.1评估治疗效果,2、4、6周期疗效评估均为部分缓解(PR)。6周期治疗后即术前的乳腺MRI图像见图4。
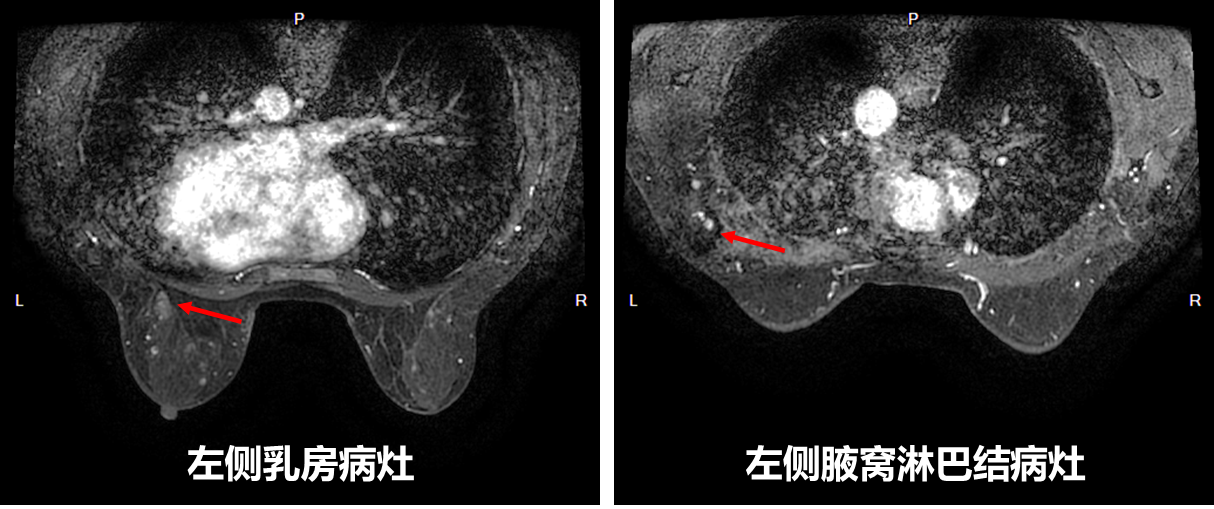
(2)手术治疗:
2023年12月11日,患者于全麻下行左乳腺癌改良根治术(姑息性)。
术后病理示:1、(左乳及基底)乳腺组织经象限全部取材示腺病伴导管扩张,间质胶原化伴淋巴细胞、浆细胞及大量泡沫样组织细胞浸润,未见明确癌残留,治疗后Miller-Payne评估系统:5级,乳头及基底切缘未见癌累及;2、淋巴结未见转移癌:0/19(左腋窝LN 0/17,左锁骨下LN 0/2)。
术后诊断:左乳癌 ypT0N0M0。
(3)辅助治疗+强化辅助治疗:
2023年12月17日-2024年7月14日,行HP双靶方案辅助治疗(曲妥珠单抗+帕妥珠单抗,第7-17周期)。
辅助靶向治疗期间(2024年1月24日-2024年3月6日)行左侧胸壁+锁骨上下淋巴结引流区放疗,累计50GY/25F,锁骨上下淋巴结引流区局部加量(10GY/5F)。
2024年8月5日,开始奈拉替尼强化辅助治疗,计划1年。
专家点评
重庆大学附属肿瘤医院乳腺肿瘤中心主任、主任医师
医学博士、博士后、博士研究生导师
中国抗癌协会乳腺癌专业委员会常务委员
中华医学会肿瘤学分会乳腺癌学组委员
国家肿瘤质控中心乳腺癌专家委员会委员
中国医师协会肿瘤医师分会乳腺癌学组委员
中国研究型医院学会乳腺专业委员会常务委员
国家癌症中心《中国乳腺癌筛查与早诊早治指南》成员
中国医师协会外科医师分会乳腺外科专家工作组专家委员
国家卫健委卫生发展研究中心乳腺癌单病种分级诊疗专病联盟专家组成员
重庆市医药生物技术协会副理事长
重庆市中西医结合学会乳腺疾病专业委员会主任委员
重庆市医药生物技术协会乳腺癌防治专业委员会主任委员
重庆市肿瘤医疗质量控制中心乳腺癌诊疗专家组组长
重庆大学附属肿瘤医院乳腺癌MDT多学科联合诊治组首席专家
国务院政府特殊津贴专家
重庆五一劳动奖章、重庆英才·创新领军人才
第四批重庆市有突出贡献的中青年专家、重庆市卫生健康系统先进个人
《重庆医学杂志》、《实用癌症杂志》、《中国癌症防治杂志》编委会编委
警惕不懈——pCR患者仍存在较高复发风险
乳腺癌是全球女性群体中发病率最高的恶性肿瘤之一。而在中国等东亚国家,乳腺癌的中位发病年龄较西方提前约10年,为45~49岁[1]。在众多乳腺癌亚型中,HER2阳性乳腺癌占全部乳腺癌的20%~25%[2]。HER2阳性乳腺癌是一种侵袭性较强的乳腺癌亚型,具有较高的复发和转移风险,并且对内分泌治疗和标准化疗的反应通常不佳,导致患者预后较差。近年来,随着抗HER2靶向治疗的不断发展,HER2阳性乳腺癌患者的预后得到了显著改善。
新辅助治疗是乳腺癌综合治疗中非常重要的组成部分,新辅助治疗后50%-65%的患者可以达到pCR[3]。相比未达到pCR的患者,pCR患者往往具有更好的预后结果。一项评估曲帕双靶新辅助治疗疗效的研究结果显示[4],中位随访3.2年后,pCR组的3年无病生存(DFS)率显著高于non-pCR组(95% vs 91%,p=0.03),总生存期(OS)亦呈现出相同趋势。然而,仍有5%-10%的pCR患者术后3年内会出现疾病复发[3]。除此之外,淋巴结阳性、肿瘤较大、激素受体阴性、组织学分级2-3级、诊断时年龄较小等也与HER2阳性乳腺癌复发风险增加相关[5]。
本例患者经临床诊断为左乳癌,cT2N3M0 IIIC期,HER2阳性。患者在接受6周期的TCbHP新辅助治疗后,顺利完成了左乳癌改良根治术。虽然术后病理显示达到pCR,但患者确诊时肿瘤较大,且已出现了多发淋巴结转移,具有较高的复发风险,临床需进一步探索强化辅助治疗策略[5,6],以降低复发风险并改善患者的长期生存。
强化治疗——奈拉替尼为患者长生存保驾护航
奈拉替尼是一种不可逆的泛HER酪氨酸激酶抑制剂,能够有效抑制HER1、HER2和HER4的信号传导。与曲妥珠单抗不同,奈拉替尼可以阻断HER2受体的所有二聚化形式,从而实现对HER2信号通路的全面抑制。这一独特机制使得奈拉替尼在HER2阳性乳腺癌的治疗中具有显著优势。
ExteNET研究结果显示,在接受曲妥珠单抗辅助治疗后,继续使用奈拉替尼进行强化治疗可以显著降低患者的复发风险:意向性治疗(ITT)人群的2年、5年疾病复发风险分别降低了33%和27%[6,7]。此外,对于新辅助达到pCR的患者,奈拉替尼治疗同样具有获益趋势。其5年无浸润性疾病生存率(iDFS)绝对获益为 9.8%(HR 0.44; 95% CI 0.06-1.89),8年OS绝对获益为19.6%(HR 0.40; 95% CI 0.06-1.88)。多项真实世界研究数据亦表明,辅助治疗后使用奈拉替尼进行强化治疗的安全性良好,且不良反应可管理。根据多国家、前瞻性、非干预性研究——ELEANOR研究[8]期中分析,该研究纳入300例患者,其中231例患者接受新辅助治疗,114例患者达到pCR,占49.4%。临床选择使用奈拉替尼强化辅助治疗最常见的原因为疗效(61.5%),其他原因还有安全性(14.7%)、医生偏好(12.9%)、患者偏好(6.3%)、生活质量(3.8%)等。NER-Tree研究[9]则探索了奈拉替尼强化辅助治疗在中国真实世界中的应用。该研究纳入了中国30个中心500例完成曲妥珠单抗辅助治疗并计划接受1年奈拉替尼延长辅助治疗的HER2阳性早期乳腺癌患者,患者将接受12个月的奈拉替尼延长辅助治疗和12个月随访。2024年ESMO BC上发表的数据显示,在已入组的250例患者中,33.6%(84例)的患者接受了新辅助治疗,其中39.3%的(33例)患者为pCR;在辅助治疗中,88%(220例)的患者接受了曲帕双靶治疗,10.4%(26例)的患者接受曲妥珠单抗治疗,1.6%(4例)的患者接受了T-DM1治疗,这可能与T-DM1当时尚未被纳入国家医保药品目录有关。该研究将为中国临床提供更大样本的数据支持,目前该研究尚未结束,让我们共同期待其疗效数据的公布。基于以上研究数据,本例患者在完成术后HP双靶辅助治疗后,临床继续给予1年奈拉替尼强化辅助治疗。截至目前,患者病情稳定,一般状况良好。
总之,尽管pCR与良好的预后密切相关,但乳腺癌新辅助治疗后的pCR并不能完全代表患者的最终预后。新辅助治疗后的优化策略需要对复发风险进行全面的综合分析,这不仅包括初诊肿瘤的临床分期,还应结合组织学和循环生物标志物等多维度因素,充分考虑奈拉替尼强化治疗的必要性。通过这种综合评估,才能为患者制定更为精准的个体化治疗方案,从而为患者带来全面且持久的获益。
[1]中国临床肿瘤学会乳腺癌专家委员会 中国抗癌协会乳腺癌专业委员会 中华医学会外科学分会乳腺外科学组. 中国年轻乳腺癌诊疗专家共识(2022)[J], 中华医学杂志, 2022年第103卷第6期:387-403页.
[2]罗师萍,张捷,俞育帅等. HER2阳性乳腺癌的靶向治疗进展[J]. 中国临床药理学与治疗学. 2023;28(08):876-886.
[3]Valenza C, Trapani D, Loibl S, Chia SKL, Burstein HJ, Curigliano G. Optimizing Postneoadjuvant Treatment in Patients With Early Breast Cancer Achieving Pathologic Complete Response. J Clin Oncol. 2024 Jul 10;42(20):2372-2376.
[4]Emanuela Ferraro, Jasmeet Singh, Sujata Patil,et al. Incidence of brain metastases in patients with early HER2-positive breast cancer receiving neoadjuvant chemotherapy with trastuzumab and pertuzumab[J]. NPJ Breast Cancer. 2022 Mar 22;8(1):37. doi: 10.1038/s41523-022-00380-7.
[5]中国抗癌协会乳腺癌专业委员会, 中华医学会肿瘤分会乳腺肿瘤学组. 中国抗癌协会乳腺癌与中华医学会肿瘤学分会乳腺癌诊治指南与规范(2025年版精要本).
[6]Chan A, Delaloge S, Holmes FA, et al. Neratinib after trastuzumab-based adjuvant therapy in patients with HER2-positive breast cancer (ExteNET): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2016;17(3):367-377.
[7]Martin M, Holmes FA, Ejlertsen B, et al. Neratinib after trastuzumab-based adjuvant therapy in HER2-positive breast cancer (ExteNET): 5-year analysis of a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2017;18(12):1688-1700.
[8]Bartsch R, Harbeck N, Wrobel D, et al. Interim analysis of 300 patients with HER2+/HR+ early breast cancer enrolled in the multi-national, prospective, observational, non-interventional study ELEANOR treated with extended adjuvant neratinib in clinical routine. 2024ESMO BC,116p.
[9]Zhang J, Liu H, Liu X, et al. A multicenter, prospective, non-interventional study to investigate the treatment patterns of neratinibin Human Epidermal Factor Receptor 2 positive (HER2+) early breast cancer in China: NER-Tree study .An interim analysis on patient characteristics and pretreatment patterns. Annals of Oncology.2024ESMO BC,118p.
责任编辑:Annie
排版编辑:Zika











 苏公网安备32059002004080号
苏公网安备32059002004080号


