布鲁顿酪氨酸激酶抑制剂(BTKi)是治疗B细胞恶性肿瘤的重要手段,改变了B细胞淋巴瘤患者的治疗模式与预后。奥布替尼是新型BTKi(Ⅰ类创新药),于2020年12月25日在中国获批上市。目前奥布替尼已被批准用于既往至少接受过1种治疗的成年人慢性淋巴细胞白血病/小淋巴细胞淋巴瘤、套细胞淋巴瘤、边缘区淋巴瘤。近年来,奥布替尼在其他B细胞淋巴瘤领域亦获得了良好的疗效和安全性。为满足当前临床需求,规范奥布替尼临床用药,专家组成员结合最新的研究进展,在2021年版奥布替尼治疗B细胞淋巴瘤中国专家推荐临床应用指导原则的基础上,讨论并制定了该共识。
2013年全球首个布鲁顿酪氨酸激酶抑制剂(BTKi)伊布替尼问世,开启了小分子靶向药物治疗B细胞淋巴瘤的新时代,然而传统BTKi存在生物利用度低、激酶选择性差、脱靶效应导致的不良反应发生率高等问题。作为新一代BTKi,奥布替尼通过优化分子结构,具有更小的空间夹角、更少的铰链区H键结合位点,去除了手性中心,提高了激酶选择性,对布鲁顿酪氨酸激酶(BTK)以外的靶点作用极低。临床研究中,奥布替尼未发生≥3级心房颤动、≥3级出血和腹泻等因脱靶效应导致的不良反应,耐受性好,因不良反应导致剂量降低的发生率仅6.6%。奥布替尼对患者外周血单个核细胞(PBMC)BTK靶点24 h内接近100%持续抑制,BTK靶点占有率个体差异小,有效避免了由靶点占有率个体差异导致的部分患者疗效不佳现象。目前奥布替尼已被批准用于治疗既往至少接受过1种治疗的成年人慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)、套细胞淋巴瘤(MCL)、边缘区淋巴瘤(MZL)。为进一步规范奥布替尼治疗B细胞淋巴瘤的临床用药,专家组成员根据国内外最新指南和循证医学证据,讨论并制定本共识。
1 奥布替尼简介
1.1 奥布替尼药物结构
作为新型不可逆共价结合的BTKi,奥布替尼在第1代BTKi基础上进行了结构优化( 图1 ),这保证了奥布替尼具有最佳激酶选择性,有助于降低脱靶效应,使奥布替尼拥有更好的疗效和安全性。KINOMEscan平台测定显示,奥布替尼靶区更集中,对其他非目标靶点抑制作用小,拥有最佳激酶选择性。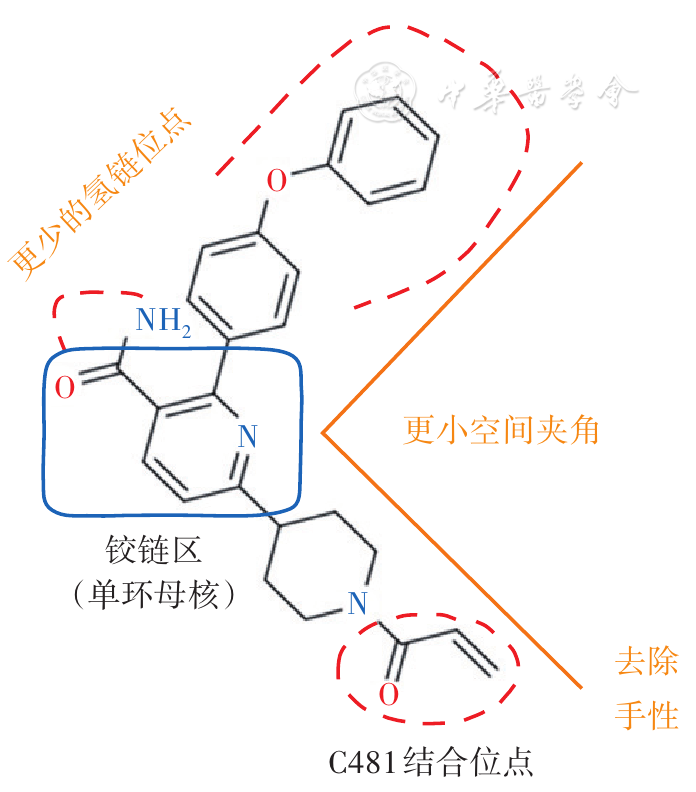
1.2 奥布替尼联合治疗的临床前研究
既往体外试验表明,奥布替尼在多种肿瘤的细胞株中均不会抑制ITK激酶,因此不影响抗体依赖的细胞介导的细胞毒作用(ADCC)。研究显示,奥布替尼联合利妥昔单抗可增加B细胞淋巴瘤的细胞凋亡,两者具有协同作用。另一项细胞实验亦显示,奥布替尼较伊布替尼能更好地协同坦昔妥单抗和来那度胺发挥ADCC效应,为临床研究中联合用药提供了科学依据。
2 奥布替尼在CLL/SLL、MCL和MZL中的相关临床研究
2.1 在CLL/SLL中的主要研究与建议
2.1.1 在复发难治CLL/SLL中开展的注册研究
一项开放性、多中心Ⅱ期关键性临床研究评估了奥布替尼治疗复发难治CLL/SLL患者的效果和安全性。共纳入80例患者,截至2021年8月10日,中位随访32.3个月,研究者评估的总有效率(ORR)达93.8%,完全缓解(CR)/伴骨髓恢复不完全的完全缓解(CRi)率达26.3%,部分缓解(PR)率达56.3%。其相似随访时间内的CR/CRi率较其他BTKi更高(CR率是其他BTKi的2~7倍),不同细胞遗传学高危亚组患者具有高ORR:del(17p)患者达100.0%,TP53突变患者达100.0%,del(11q)患者为94.7%,免疫球蛋白重链可变区基因(IGHV)未突变患者为93.9%。达到CR/CRi患者的无进展生存(PFS)、缓解持续时间(DOR)均优于PR/伴淋巴细胞增多的部分缓解(PR-L)患者。
2.1.2 在CLL/SLL中开展的探索性研究
国内一项多中心、真实世界研究探索了奥布替尼一线治疗CLL/SLL的效果。共纳入53例患者,中位年龄68岁,69%的患者合并疾病,其中35.7%合并心脑血管疾病。中位治疗持续时间(DOT)15.2个月。治疗期间无患者出现进展,中位PFS时间未达到。
一项Ⅱ期多中心CWCLL-001研究探索了奥布替尼+氟达拉滨+环磷酰胺+奥妥珠单抗(OFCG)方案一线治疗CLL患者[不受IGHV和del(17p)/TP53突变状态的限制]的安全性和有效性,共纳入25例患者,中位年龄为49岁。分别有56.5%、16.0%和24.0%的患者为IGHV未突变、TP53突变/del(17p)和del(11q)。研究结果显示,外周血微小残留病(PB-MRD)阴性率和骨髓微小残留病(BM-MRD)阴性率随给药周期延长而提高;6个周期治疗后,PB-MRD和BM-MRD阴性率分别为95.2%、86.4%,CR/CRi为59.1%;15例患者完成了12个周期治疗,PB-MRD和BM-MRD阴性率均为100%,CR/CRi率为80.0%。该15例患者在第12个周期治疗后因BM-MRD阴性停用奥布替尼。该研究提示,奥布替尼联合免疫化疗为患者带来了快速且持久的缓解。
一项临床Ⅱ期研究评估了奥布替尼治疗既往BTKi不耐受的经治B细胞恶性肿瘤患者的安全性。结果显示,既往伊布替尼或泽布替尼不耐受的患者转为奥布替尼治疗后,51例(46%)不良反应消失,20例(18%)不良反应缓解,缓解的主要不良反应为高血压(12/15)、心脏事件(9/11)、感染事件(2/2)、皮下出血(1/1)。提示既往对其他BTKi不耐受的惰性淋巴瘤患者在换用奥布替尼后安全性得到明显提升。
2.1.3 针对CLL/SLL的治疗建议
(1)对于复发难治CLL/SLL患者,奥布替尼表现出优异的高CR率,TP53突变/del(17p)患者也可获得100%的ORR。(2)对于初治CLL患者,有合并疾病者也适合接受奥布替尼治疗。(3)基于CWCLL-001研究,对于年轻且体健的初治CLL患者,无论是否有IGHV突变、TP53突变,奥布替尼+氟达拉滨+环磷酰胺+奥妥珠单抗(OFCG)有限期治疗方案能带来更快更深的缓解及停药可能。(4)奥布替尼可改善既往对其他BTKi不耐受的不良反应,尤其是脱靶相关不良反应,因而对伊布替尼或泽布替尼不耐受的患者可尝试应用奥布替尼。
2.2 在MCL中的主要研究与建议
2.2.1 在复发难治MCL中开展的注册研究
一项开放性、多中心Ⅱ期关键性临床研究探索了奥布替尼治疗复发难治MCL患者的效果和安全性。共纳入106例患者,中位随访23.8个月时研究者评估ORR为82.1%,CR率为34.9%,中位DOR和中位PFS时间分别为22.9、22.0个月,24个月总生存(OS)率为74.3%。CR患者有更高的24个月PFS率和OS率。
2.2.2 在MCL一线治疗中开展的探索性研究
一项前瞻性、多中心、Ⅱ期研究(POLARIS)评估了奥布替尼+来那度胺+利妥昔单抗(OLR)方案治疗初治MCL的效果和安全性,共入组29例初治MCL患者,中位年龄61岁,其中28例患者完成6个周期的诱导治疗且疗效可评估,ORR为85.8%,CR率为67.9%。该研究提示OLR方案在未经治疗的MCL患者中具有较好的抗肿瘤活性,为此类患者提供了一个新的无化疗方案的治疗选择。
2.2.3 针对MCL的治疗建议
(1)对于复发难治MCL患者,奥布替尼注册研究中未观察到≥3级心房颤动、出血发生,无治疗相关死亡病例,是一个安全有效的选择。(2)基于POLARIS研究,初治MCL患者可考虑OLR方案。
2.3 在MZL中的主要研究与建议
2.3.1 在复发难治MZL中开展的注册研究
一项Ⅱ期注册研究评估了奥布替尼治疗复发难治MZL患者的效果和安全性,共入组90例患者,中位随访24.3个月,独立评审委员会(IRC)评估的ORR为58.9%,10例(11.1%)患者达到CR,PR率为47.8%。2年PFS率为75.8%,2年OS率为86.8%。中位DOR为34.3个月,2年DOR率为88.5%。在按性别、年龄、美国东部肿瘤协作组(ECOG)评分、抗CD20单抗难治、既往治疗线数和肿瘤负荷指标分层的亚组中,ORR差异均无统计学意义。最常见的不良反应为血液学不良反应,患者整体耐受性良好。
基于上述研究,奥布替尼被批准用于既往至少接受过1种治疗的MZL患者,成为目前我国唯一获批MZL适应证的BTKi。2024版《CSCO淋巴瘤诊疗指南》将奥布替尼纳入MZL二线治疗的Ⅰ级推荐 。基于奥布替尼在单臂研究中表现出的显著疗效,一项评价奥布替尼联合来那度胺和利妥昔单抗治疗复发难治MZL患者有效性和安全性的Ⅲ期临床研究(NCT06082102)正在开展,以期为MZL患者提供更多治疗选择。
2.3.2 在MZL一线治疗中开展的探索性研究
一项回顾性研究评估了奥布替尼联合利妥昔单抗治疗初治MZL的效果和安全性。共纳入10例患者,包括4例黏膜相关淋巴组织淋巴瘤(MALT),1例脾边缘区淋巴瘤(SMZL),2例淋巴结边缘区淋巴瘤(NMZL),3例未知亚型。中位随访13个月,最佳ORR为90%,CR率为30%。6个月PFS率为100%。整体耐受性良好,未报告心房颤动、腹泻和大出血等脱靶相关不良反应。另一项前瞻性研究探索了奥布替尼联合奥妥珠单抗系统治疗初治MZL的效果和安全性。符合入组条件的患者接受6个周期奥布替尼联合奥妥珠单抗诱导治疗,而后应答的患者接受1年奥布替尼单药维持治疗。截至2024年4月11日,共入组19例患者,其中13例接受至少1次疗效评估,中位随访6.8个月,ORR为100%,CR率为53.8%。常见不良反应为1~2级血液学不良反应,整体耐受性良好。前瞻性和回顾性研究的初步结果表明,奥布替尼联合抗CD20单抗可为初治MZL患者提供安全有效的无化疗新选择。
2.3.3 针对MZL的治疗建议
(1)对于复发难治MZL患者,基于Ⅱ期注册研究,推荐选择奥布替尼单药持续治疗,亦可选择奥布替尼联合其他免疫治疗或免疫调节剂或免疫化疗(如BR、R-CHOP、R-CVP方案等)。(2)基于奥布替尼在初治MZL中的研究数据,对于有治疗指征且需系统治疗的初治MZL患者可考虑尝试奥布替尼联合抗CD20单抗方案。
3 奥布替尼在其他B细胞淋巴瘤中的临床研究
目前上市的抗肿瘤药物尚不能完全满足肿瘤患者的用药需求,药品说明书也往往滞后于临床实践。特殊情况下抗肿瘤药物的使用权应当仅限于三级医院授权的具有高级专业技术职称的医师,并充分遵循患者知情同意的原则,同时应当做好用药监测和跟踪观察。为更好地满足患者临床用药需求,正在开展以下奥布替尼相关临床研究,以积累临床用药经验。
3.1 奥布替尼在弥漫大B细胞淋巴瘤(DLBCL)中的临床研究
3.1.1 在原发结外和双表达DLBCL中开展的探索性研究
一项前瞻性、单臂临床研究评估了奥布替尼联合R-CHOP方案治疗初治非生发中心B细胞(non-GCB)型DLBCL伴原发结外受累患者的效果和安全性。共纳入22例患者,ORR为86.4%,CR率达77.3%,中位PFS时间未达到,5个月PFS率为90.9%。
另一项单中心真实世界研究评估了含BTKi(奥布替尼或泽布替尼)方案治疗23例MYD88突变和(或)CD79B突变初治DLBCL患者的效果和安全性。研究显示,BTKi+R-CHOP方案组的最佳ORR、CR率和1年PFS率分别为100%、94.4%和88.9%,均高于R-CHOP方案组,且含奥布替尼方案组的CR率(100%比87.5%)和1年PFS率(100%比75%, P=0.028)均优于含泽布替尼方案组。此外,一项奥布替尼联合R-CHOP方案治疗23例初治MCD亚型患者的真实世界研究也进一步丰富了相关治疗数据。
ORIENT研究前瞻性探索了奥布替尼联合R-CHOP样方案对于短期接受奥布替尼+利妥昔单抗(OR)方案诱导治疗应答的初治non-GCB型DLBCL患者的疗效和安全性。22例患者完成诱导治疗并可疗效评估,疗效应答率(mRR)为95.5%[CR率27.3%,PR率63.6%,miniR(定义为CT评估病灶缩小25%~50%)率4.5%],16例在第6个周期结束时达到CR。除以上临床研究外,针对MCD亚型、双表达、TP53突变、老年、复发难治等DLBCL患者均有奥布替尼联合方案的前瞻性或回顾性探索研究,研究内容见 表1 。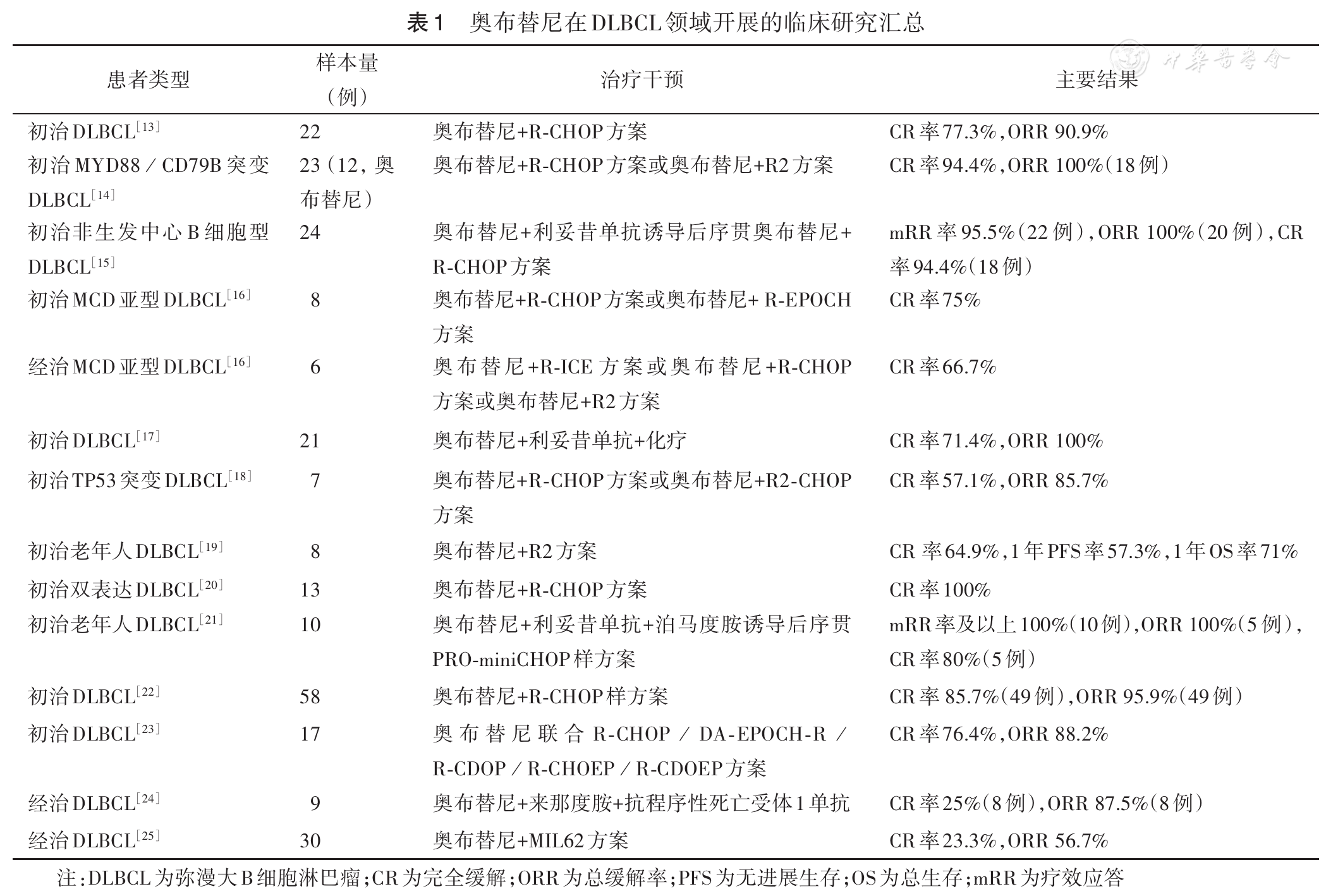
3.1.2 针对DLBCL的治疗建议
对于non-GCB、双表达、结外受累及MCD样基因分型等预后不良的DLBCL患者,可以考虑使用含奥布替尼的方案。与R-CHOP等标准治疗方案联合时,推荐奥布替尼剂量为150 mg/d,治疗过程中重点关注中性粒细胞减少、贫血、血小板减少等血液学不良反应,必要时需要使用粒细胞集落刺激因子(G-CSF)等进行相应的预防和治疗。
3.2 奥布替尼在原发中枢神经系统淋巴瘤(PCNSL)中的临床研究
一项单中心、回顾性研究评价了奥布替尼联合利妥昔单抗与甲氨蝶呤治疗新诊断PCNSL的效果、安全性和生物标志物。纳入34例患者,其中18例完成6个周期治疗,ORR为94.4%(17/18),CR率为88.9%(16/18)。中位PFS、OS时间均未达到,6个月PFS率为97%。5例患者连续用药15 d后2 h采集血浆和脑脊液样本,奥布替尼脑脊液中位浓度为21.6 ng/ml,中位血脑屏障透过率58.6%。另一项奥布替尼联合程序性死亡受体1(PD-1)的临床研究中检测了4例患者在给药后的血浆和脑脊液样本,奥布替尼的中位脑脊液浓度为28.7 ng/ml(范围:11.8~52.7 ng/ml),中位脑脊液与血浆游离比为59.8%(范围:46.09%~86.67%)。
一项Ⅰ期临床研究探索了奥布替尼联合高剂量甲氨蝶呤(HD-MTX)、利妥昔单抗和地塞米松(ORMD)方案在新诊断PCNSL患者中的安全性和有效性。研究显示,200 mg+5 g/m 2剂量组合为Ⅱ期推荐剂量(RP2D),未发生4级不良反应。ORR和CR/不确定的完全缓解(CRu)率均为83.3%,1年PFS率和OS率分别为56.6%和100%。所有缓解患者均达到CR/CRu,深度缓解率高可能与奥布替尼的加入有关。
3.3 针对PCNSL的奥布替尼治疗建议
对于可以耐受HD-MTX治疗的患者,在HD-MTX为基础的化疗方案基础上加用奥布替尼的多项研究均显示缓解率较高。尽管在甲氨蝶呤5 g/m 2、奥布替尼200 mg的剂量组合中验证了其安全性,但考虑真实诊疗环境与临床研究的差别,甲氨蝶呤的推荐剂量为3.5~5 mg/m 2,奥布替尼的推荐剂量为150 mg/d。临床研究中规定需在HD-MTX给药后72 h或清除后(血药浓度降至安全水平)再给予奥布替尼,实际临床中可根据患者情况适当调整用药时间。
对于无法耐受高强度化疗的患者,含奥布替尼的无化疗方案疗效、耐受性均较好,可以考虑使用。
3.4 奥布替尼在华氏巨球蛋白血症(WM)中的临床研究
3.4.1 在WM中开展的探索性研究
一项单臂、多中心、开放标签、Ⅱ期研究(NCT04440059)评估了奥布替尼治疗复发难治WM的效果和安全性,共入组47例患者。中位随访31.9个月,IRC评估的主要反应率(MRR)为80.9%,ORR为91.5%。IRC评价中位PFS时间未达到,3年PFS率为72.1%。MYD88和CRCR4双突变或单突变基因型患者的PFS差异无统计学意义( P=0.69)。提示不管基因状态如何,都可从奥布替尼治疗中获益。
3.4.2 针对WM的治疗建议
2024年第2版美国国立综合癌症网络(NCCN)指南和2022年淋巴浆细胞淋巴瘤(LPL)/WM诊断与治疗中国指南均推荐BTKi单药或联合利妥昔单抗用于WM的一线治疗。(1)对于复发难治WM患者,与Ⅱ期注册研究一致,无论MYD88和CXCR4基因状态如何,推荐奥布替尼单药持续治疗;(2)对于初治WM患者,可考虑奥布替尼单药或联合利妥昔单抗治疗方案。
4 奥布替尼的临床应用推荐
4.1 奥布替尼的剂量与使用方法
奥布替尼在我国已被获批用于治疗既往至少接受过1种治疗的成年人CLL/SLL、既往至少接受过1种治疗的成年人MCL,以及既往至少接受过1种治疗的成年人MZL。可在饭前或饭后口服奥布替尼,推荐剂量为150 mg/次(50 mg/片,3片),1次/d,直至疾病进展或出现不可耐受的不良反应。
奥布替尼在人体内主要由细胞色素P450 3A(CYP3A)代谢。与CYP3A抑制剂联用时会增加本品的暴露量,应避免与强效或中效CYP3A抑制剂联用( 表2 )。柚子中含有的活性成分呋喃香豆素类化合物属于一种不可逆的CYP3A4抑制剂,可能导致奥布替尼体内暴露量增加,因此服用奥布替尼期间应避免食用含CYP3A4抑制剂或诱导剂的食物(如柚子)。
心血管疾病是淋巴瘤患者常见合并疾病和死亡原因之一,如患者需使用血管紧张素转化酶抑制剂类药物治疗,与奥布替尼联用时需谨慎,可能会增加室性心动过速和心源性猝死的风险;高血压患者可选择血管紧张素受体拮抗剂类或β受体阻滞剂类药物进行治疗,不会与BTKi产生相互作用。抗凝药物尽量选择直接口服抗凝药物(阿哌沙班、利伐沙班、艾多沙班、达比加群酯),避免使用华法林等维生素K拮抗剂。
4.2 奥布替尼在特殊人群中的用药
肝功能不全人群:轻度肝功能不全患者不建议进行剂量调整,中度肝功能不全患者需在医师指导下慎用本品并严密监测肝功能及相关不良反应,重度肝功能不全患者禁用。肾功能不全人群:轻、中度肾功能不全患者不建议进行剂量调整,重度肾功能不全患者必须在医师指导下慎用本品并监测不良反应。老年患者无需进行剂量调整。奥布替尼在儿童患者中的安全性和有效性尚未进行研究。
4.3 奥布替尼的不良反应及处理
6项奥布替尼单药治疗B细胞恶性肿瘤的临床试验共纳入440例患者,接受奥布替尼150 mg/d及以上剂量连续给药。中位治疗时间为14.0个月(范围:0.1~40.3个月)。常见的不良反应(发生率≥10%)为中性粒细胞减少症、血小板减少症、白细胞减少症、血尿、贫血、上呼吸道感染、皮疹、出血、感染性肺炎、肺部炎症、丙氨酸氨基转移酶升高和血胆红素升高。未观察到≥3级心房颤动、心房扑动及其他心律失常。绝大多数不良反应通过对应的支持治疗均可恢复,仅3.2%的患者因不良反应永久终止治疗。
5 结语
传统BTKi激酶选择性差,脱靶相关不良反应发生率高。奥布替尼具有更高的激酶选择性,可减少脱靶相关不良反应。同时,奥布替尼与抗CD20单抗联用时不影响其ADCC效应,能更好发挥联合抗肿瘤作用。奥布替尼在CLL/SLL、MCL、MZL及WM等惰性淋巴瘤治疗中展示了显著的疗效,在non-GCB、双表达、结外受累(含中枢神经系统)及MCD样基因分型的DLBCL中亦展现了较好的疗效。而既往BTKi不耐受的经治B细胞恶性肿瘤患者仍可从奥布替尼中获益,尤其是脱靶相关不良反应的改善。随着临床研究数据的不断公布,本共识的更新将促进奥布替尼更好地用于B细胞淋巴瘤的治疗,提高患者临床获益,也期待更广泛、更长随访时间的奥布替尼研究数据公布,以更好地指导临床实践。
中国临床肿瘤学会(CSCO)淋巴瘤专家委员会. 奥布替尼治疗B细胞淋巴瘤临床应用专家共识(2024年版)[J]. 白血病·淋巴瘤,2025,34(01):1-7. DOI:10.3760/cma.j.cn115356-20241023-00158.











 苏公网安备32059002004080号
苏公网安备32059002004080号


