

余静, 杨康, 程亚杰, 等. 局限期小细胞肺癌诱导化疗的缓解深度对预后的影响[J]. 中华肿瘤杂志, 2023, 45(7):621-626. DOI:10.3760/cma.j.cn112152-20220107-00019.
目的
探讨诱导化疗的肿瘤缓解深度对局限期小细胞肺癌整体预后的影响。
方法
研究为回顾性研究,选取2013年1月至2021年6月于武汉大学中南医院接受规范化治疗且影像资料完整的局限期小细胞肺癌患者,通过影像系统勾画肿瘤在诱导化疗前与化疗后的体积,并以此计算诱导化疗的缓解深度。通过时间依赖受试者工作特征(timeROC)曲线评价局限期小细胞肺癌最佳的预后评估指标及其预测结果,多因素分析采用Cox风险比例模型。
结果
104例患者的中位无进展生存时间和总生存时间分别为13.7和20.9个月。timeROC结果显示,诱导化疗后肿瘤残存体积是患者1年无进展生存[曲线下面积(AUC)=0.86,95% CI:0.78~0.94]和2年总生存(AUC=0.76,95% CI:0.65~0.87)的最佳预测指标。多因素分析显示,诱导化疗后残存肿瘤体积的绝对值是影响局限期小细胞肺癌无进展生存( HR=1.006,95 CI:1.003~1.009)和总生存( HR=1.009,95% CI:1.005~1.012)的独立因素(均 P<0.001)。诱导化疗后肿瘤退缩至10 cm 3以下者,无论其初始的肿瘤负荷,均能够获得较好的长期预后。
结论
局限期小细胞肺癌诱导化疗的缓解深度能够预测其远期疗效,并且能够为患者提供个体化的治疗指导。
【关键词】肺肿瘤;局限期小细胞癌;诱导化疗;肿瘤缓解深度
小细胞肺癌占全部肺癌的15%~20%。初诊时病变处于局限期小细胞肺癌的患者约占全部小细胞肺癌患者人群的1/3。通过药物治疗和放射治疗,局限期小细胞肺癌5年生存率可达20%。局限期小细胞肺癌是放化疗敏感的肿瘤,其预后却具有很大的异质性,即使在标准的治疗模式下,一部分患者仍然会在治疗后的1年内发生复发和转移。根据CONVERT研究的报道,对于计划接受每日单次放疗和每日2次放疗的局限期小细胞肺癌患者,1年内发生局部进展的比例分别为34.8%(94/270)和27.8%(76/273),1年内即发生远处转移的比例分别可达41.1%(111/270)和31.9%(87/273)。
近年来,多项研究显示,肿瘤早期治疗的缓解程度与长期预后关系密切。例如,对于临床Ⅱ~Ⅲ期的乳腺癌,新辅助化疗能够获得病理完全缓解者预后优于新辅助化疗肿瘤消退不佳者。同样,对于局部晚期的直肠癌,新辅助放化疗后肿瘤消退的病理分级也已被证明是其独立的预后因素。小细胞肺癌是化疗敏感的肿瘤,相对于乳腺癌和直肠癌等实体肿瘤,其更加容易复发转移。既往研究显示,局限期小细胞肺癌的TNM分期、诱导化疗后根治性放疗的介入时机以及放疗分割模式的选择是影响其预后的重要因素,而在标准的治疗模式下,诱导化疗后的肿瘤缓解深度与其远期预后的关系还鲜有研究报道。因此,本研究中我们通过分析局限期小细胞肺癌诱导化疗后肿瘤缓解深度与预后的关系来探索其对长期预后的预测价值。


一、临床资料
选取2013年1月至2021年6月间就诊于武汉大学中南医院、病理确诊为局限期小细胞肺癌的患者。患者须具有完整且可调阅的治疗前、中、后的胸部CT和头部MRI影像资料,所有患者均接受至少4个周期的系统性化疗和胸部放疗。
二、治疗
1 .系统性化疗:
所有患者均采取依托泊苷联合铂类为基础的化疗方案,其中EP方案(依托泊苷+顺铂)具体剂量:依托泊苷100 mg/m 2 第1~3天给药,顺铂80 mg/m 2 第1天给药;EC方案(依托泊苷+卡铂)具体处方剂量:依托泊苷100 mg/m 2 第1~3天给药,卡铂曲线下面积(area under curve, AUC)按1~3进行计算,第1天给药。依托泊苷联合奈达铂方案的具体剂量为依托泊苷100 mg/m 2 第1~3天给药,奈达铂80 mg/m 2 第1天给药。
2 .胸部放疗:
采用直线加速器进行治疗,所有患者均采用调强放疗,要求按照95%的计划靶区(planning target volume, PTV)接受处方剂量,每周一至周五连续治疗,中位处方剂量为60 Gy/分30次完成(54 Gy/分27次完成~66 Gy/分33次完成)。我们将胸部放疗介入的时机位于2周期诱导化疗内开始者(含2周期)定义为早放疗组,而介入时机在2周期诱导化疗后者定义为晚放疗组。
3 .全脑预防放疗:
对于完成足疗程系统性化疗和原发灶区根治性放疗的患者,若能获得疾病的完全缓解或部分缓解,我们推荐患者进行全脑预防放疗。采取三维适形放疗或调强放疗的方式来进行全脑预防放疗,每周一至周五连续治疗,处方剂量统一为95%PTV为25 Gy/分10次完成。
三、诱导化疗缓解深度的评价
我们将每例患者治疗前、诱导化疗2周期后的CT影像资料导入Varian放疗计划系统,在1名高年资(工作时间>10年)影像科医师的指导下对每例患者所有CT层面上的肿瘤进行靶区勾画,重建后计算肿瘤残存体积(包括原发肿瘤以及转移的淋巴结)。评价诱导化疗前后肿瘤体积变化差、诱导化疗后与诱导化疗前肿瘤体积的退缩比以及诱导化疗后肿瘤残存的绝对体积等参数对预后的预测价值。
四、随访及研究终点
采取电话、门诊及住院复查等方式进行随访。无进展生存时间(progression-free survival, PFS)定义为患者从疾病诊断至出现肿瘤复发或死亡的时间。总生存时间(overall survival, OS)定义为患者从诊断开始至患者因任何原因死亡的时间。随访截至2021年12月15日,全组患者的随访时间为20.4~47.9个月,中位随诊时间为34.2个月。全组患者均获得随访。
五、统计学方法
采用SPSS 22.0软件进行统计学分析。生存分析采用Kaplan-Meier法计算OS及PFS,采用时间依赖受试者工作特征(time receiver operating characteristic, timeROC)曲线来评价诱导化疗的肿瘤缓解程度对长期预后的预测价值,单因素分析采用Log rank检验,多因素分析采用Cox风险比例模型。检验水准α=0.05。


1 .临床病理特征:
本研究纳入104例局限期小细胞肺癌患者,年龄为30~80岁,中位年龄为61岁。全组患者中,<65岁患者占全组患者的71.2%(74/104),男性患者占比(89.4%,93/104)高于女性患者(10.6%,11/104)。同时,>80%的患者接受了胸部区域早放疗,60.6%(63/104)的患者接受了计划性全脑预防性放疗。全组患者的临床特征见 表1 。

2 .预后:
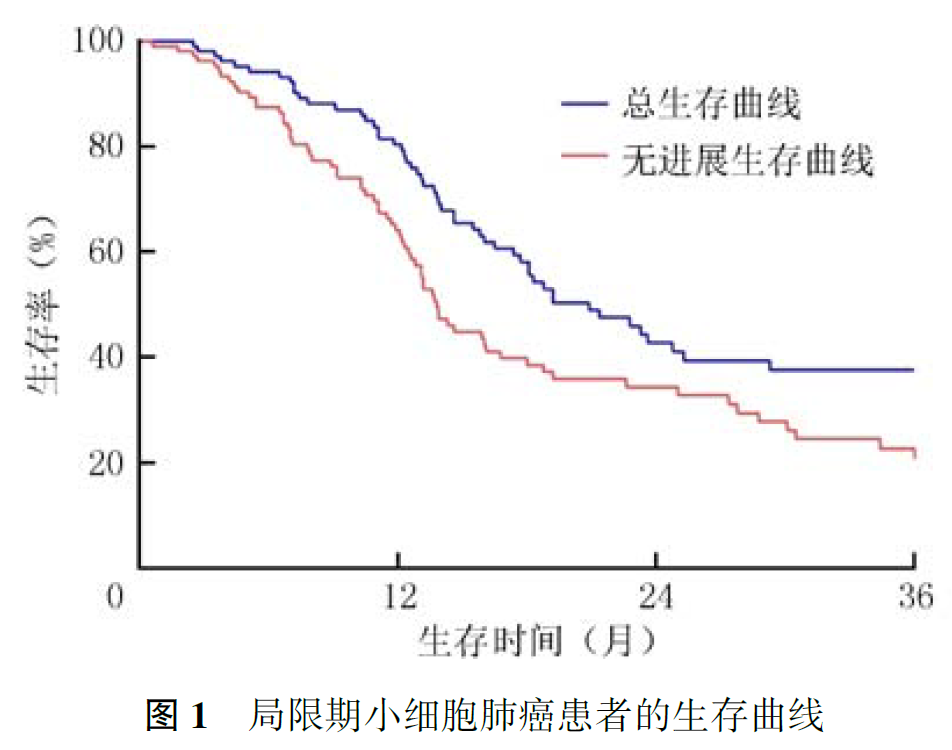
全组患者的中位PFS为13.7个月(95% CI :12.1~15.3个月),中位OS为20.9个月(95% CI :15.9~25.9个月),详见 图1 。全组患者1年和2年无疾病进展生存率分别为63.1%和34.5%,1年和2年总生存率分别为80.4%和42.8%。
3 .肿瘤缓解深度对预后的预测价值:
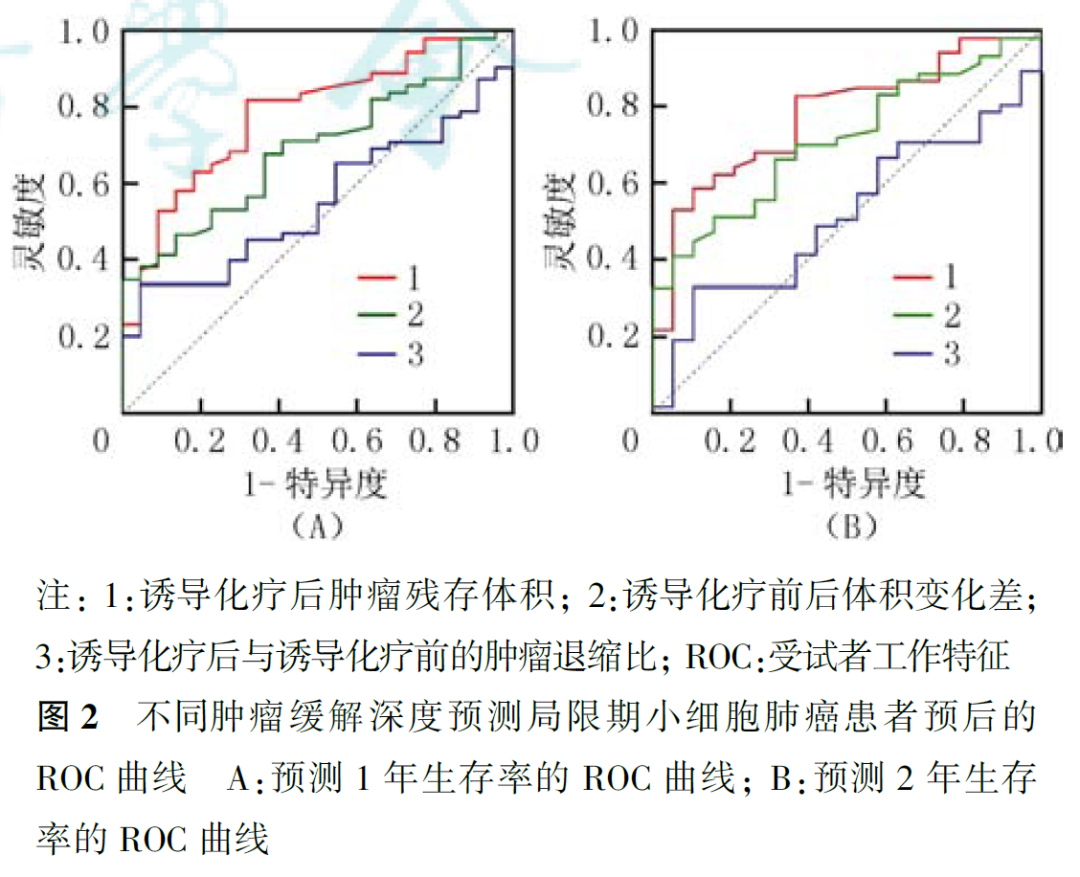
全组患者在治疗前和2周期诱导化疗后的肿瘤残存体积分别为130.4 cm 3 (78.5,218.3 cm 3 )和20.0 cm 3 (9.0,87.5 cm 3 )。timeROC结果显示,诱导化疗后残存肿瘤体积的绝对值较诱导化疗前后的体积变化差以及诱导化疗后与诱导化疗前的肿瘤退缩比具有更优的PFS和OS的预测效力( 图2 )。诱导化疗后残存肿瘤体积的绝对值预测患者1年生存率的AUC为0.86(95% CI :0.78~0.94),预测2年生存率的AUC为0.76(95% CI :0.65~0.87);诱导化疗前后的体积变化差预测患者1年生存率的AUC为0.82(95% CI :0.71~0.89),预测2年生存率的AUC为0.72(95% CI :0.61~0.84);诱导化疗后与诱导化疗前的肿瘤退缩比预测患者1年生存率的AUC为0.47(95% CI :0.34~0.60),预测2年生存率的AUC为0.49(95% CI :0.35~0.61)。
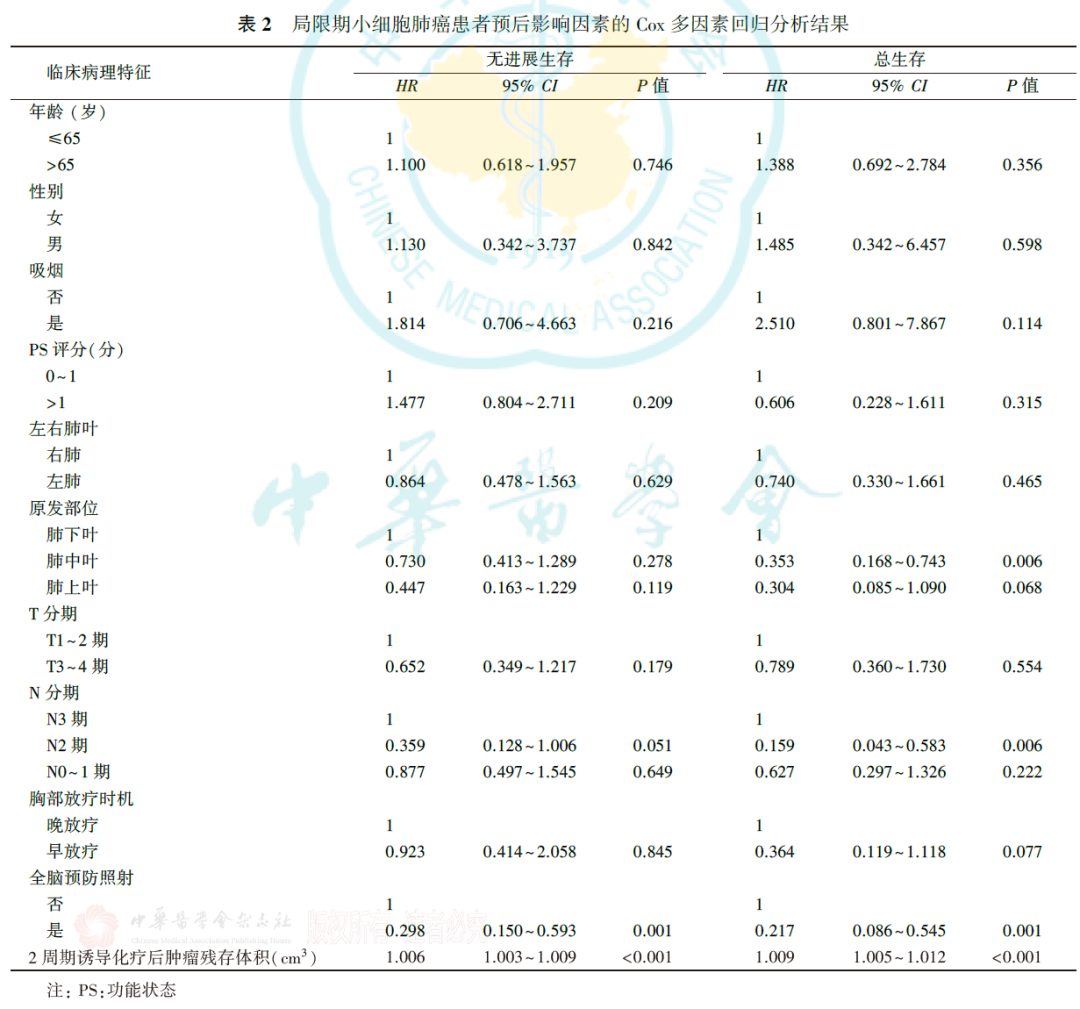
多因素分析显示,诱导化疗后肿瘤残存体积的绝对值是影响局限期小细胞肺癌PFS( HR =1.006,95% CI :1.003~1.009, P <0.001)和OS( HR =1.009,95% CI :1.005~1.012, P <0.001)的独立危险因素( 表2 )。此外,全脑预防放疗的应用也是患者PFS( HR =0.298,95% CI :0.150~0.593, P <0.001)和OS( HR =0.217,95% CI :0.086~0.545, P <0.001)的独立危险因素( 表2 )。
4 .不同肿瘤缓解深度对预后的影响:
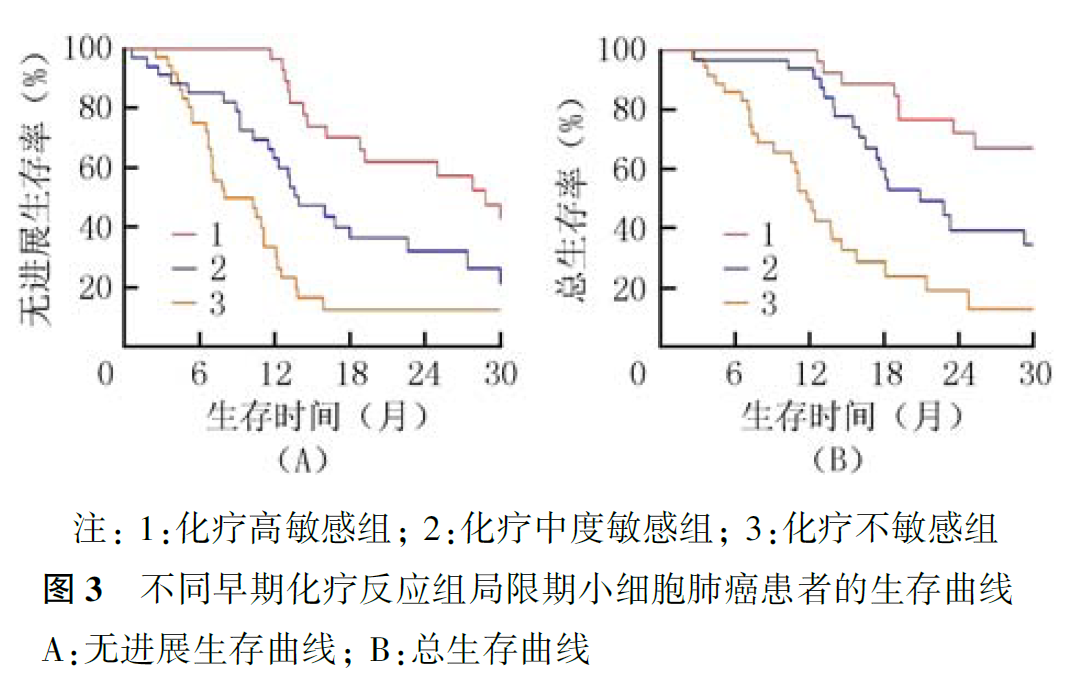
将全组患者诱导化疗后残存肿瘤体积的绝对值进行分组,将残存体积<10 cm 3 者定义为化疗高敏感组,体积10~50 cm 3 的患者定义为化疗中度敏感组,体积>50 cm 3 者定义为化疗不敏感组。亚组分析显示,无论患者治疗前的肿瘤分期,诱导化疗高敏感组患者无论是PFS还是OS均优于化疗中度敏感或不敏感组患者。高敏感组患者1年PFS和2年的OS分别可达96.4%和72.2%( 图3 )。


根据初始累及的范围,小细胞肺癌可分为局限期和广泛期,其中,局限期小细胞肺癌是指病变仅累及胸腔内结构,无远处转移。相对于广泛期小细胞肺癌,局限期小细胞肺癌具有标准的治疗流程。根据美国国立综合癌症网络和中国临床肿瘤协会的治疗指南,局限期小细胞肺癌的推荐治疗模式为以铂类联合依托泊苷为基础的4~6个周期的系统性化疗,在完成第一阶段2周期的诱导化疗后,尽早针对胸部病变实施同期放化疗,全部化疗完成后,若肿瘤能够达到完全缓解或部分缓解,后续推荐实施全脑预防放疗。然而,局限期小细胞肺癌存在很大程度的疗效异质性,即使接受同样强度的放化疗方案,仍有一部分患者会发生治疗抵抗,在短期内或是疗程中就发生远处转移,从而治疗失败。本研究中,我们发现局限期小细胞肺癌无论其初始分期如何,诱导化疗的肿瘤缓解深度是预测PFS和OS的独立影响因素,通过评估诱导化疗后肿瘤残存体积的绝对值,我们可以较好地预测患者的长期预后。
肿瘤药物的发展和技术的革新大幅提高了肿瘤治疗的整体水平。近年来有研究显示,肿瘤早期治疗的缓解深度是其长期预后的独立预测因素。对于转移性肾癌患者,在一线接受靶向治疗后,病变缓解超过60%的患者,其中位生存时间将超过4年。而对于胃黏膜相关淋巴瘤患者,在接受抗幽门螺杆菌治疗后能够达到影像学完全和部分缓解的患者,其中位PFS将远优于影像学疗效判断为疾病稳定的患者。上述这些研究预示着肿瘤的早期治疗反应可能与其长期的疗效密切相关,并可能指导患者后续的治疗决策。
本研究中我们发现局限期小细胞肺癌也具有类似的特征。诱导化疗后肿瘤残存体积的绝对值是预测其长期预后的独立因素。我们将化疗后肿瘤残存的体积进行分类,发现对诱导化疗高敏感的患者(肿瘤残存体积<10 cm 3 ),无论其初始的肿瘤分期,其1年的无进展生存率和2年生存率可达到96.4%和72.2%,这一结果与Ⅰ期小细胞肺癌手术治疗的生存水平已大致相当。
我们认为肿瘤治疗的缓解比包括客观缓解率或疾病控制率可以从一定程度上代表肿瘤治疗的敏感性,缓解比的高低往往与肿瘤的长期预后有关。然而,计算肿瘤治疗的缓解比会受到肿瘤初始体积绝对值的影响,以肿瘤退缩至10 cm 3 以内为例,初始体积为100 cm 3 与200 cm 3 的肿瘤患者所计算出的肿瘤缓解比竟相差1倍。但是,就结果而言,若肿瘤能够退缩至10 cm 3 以内,无论其初始体积大小,均可获得较好的长期生存。因此,本研究中,肿瘤残存体积的绝对值显示出较肿瘤缓解比更好的PFS与OS的预测效力。
在本研究中,我们还发现全脑预防放疗是降低复发和死亡风险的独立预后因素。因此我们建议,对于诱导化疗敏感的患者,应积极推荐实施全脑预防放疗。此外,对于局限期小细胞肺癌,在诱导化疗后尽早的介入实施胸部放疗能够提高患者的总生存。在本研究中>80%的患者接受了胸部病变的早放疗,而不足20%的患者是在2周期诱导化疗后才实施的胸部放疗,两种治疗模式下患者样本量不匹配是本研究中放疗介入时机不是OS的独立影响因素的重要原因之一。在临床实践中,对于一部分肿瘤负荷较大的患者,在接受2周期的诱导化疗后肿瘤尚未到达实施胸部同步放化疗的最佳时机,此时,我们会适当地增加诱导化疗的周期数,在第3或4周期后再实施胸部放疗,以确保最大的治疗获益比。本研究中,为了保证研究设计的一致性,我们统一将缓解深度的测量时机定义为2周期诱导化疗后。
本研究为回顾性分析,纳入患者的时间跨度较长,但是,我们在进行病例资料收集时纳入了所有符合条件的患者,并尽可能做到信息详实,最大限度避免选择性偏倚。同时,相对于其他小细胞肺癌的队列研究,我们具有较长的随访信息,能够保证预后信息的准确性。另外,基因表达差异是影响小细胞肺癌化疗敏感性的另一个重要因素,还需要我们后续的进一步研究。
总之,我们认为,通过评估局限期小细胞肺癌诱导化疗的肿瘤缓解深度能够准确地预测其远期生存并指导患者的整体治疗决策。
参考文献略。











 苏公网安备32059002004080号
苏公网安备32059002004080号


