第 60 届 ASCO 年会已于 2024 年 5 月 31 日至 6 月 4 日在美国芝加哥盛大召开。作为全球肿瘤学界的顶级盛会,ASCO常吸引来自世界各地的肿瘤学专家、学者和医务工作者齐聚一堂。
中山大学肿瘤防治中心徐瑞华教授作为消化道肿瘤治疗领域的领军人物,其团队已成功开展了多项重磅III期临床研究,助力革新消化道肿瘤临床治疗格局。继其主导的全球多中心III期临床研究RATIONALE-305研究5月28日见刊于《The BMJ》之后,FRUTIGA 研究又紧随其后,在本次ASCO年会上亮相并同步见刊国际权威期刊《Nature Medicine》,令人振奋!
在此次ASCO大会上,其团队共入选11项研究(口头报告5项,壁报6项)。表现亮眼,奏出了消化领域中国强音!
 图:RATIONAL-305研究发表于国际顶刊《 The BMJ》
图:RATIONAL-305研究发表于国际顶刊《 The BMJ》

入选的5项口头报告中,IBI310L301研究为II/III期dMMR/MSI-H结肠癌患者提供了更有效的围手术期治疗可能;KYM901研究的CMG901则有望在未来成为Claudin 18.2高表达胃癌患者的治疗新选择。FRUTIGA 研究数据的更新,再一次为一线化疗失败的晚期胃或胃食管结合部腺癌治疗带来信心。此外,该团队研究还证明了HQP1351治疗的潜在益处,为未来研究SDH缺陷GIST提供了重要参考。HX008/MRG003-C001研究,则为EGFR阳性实体瘤患者,尤其是PD-1治疗失败的NPC患者带来更多希望!硕果累累,无一不展示了中国学者的科研实力和学术影响力。
在此,【肿瘤资讯】特将其团队入选ASCO 的11项研究精心整理,以飨读者。


徐瑞华教授团队
研究一:IBI310(抗CTLA-4抗体)+信迪利单抗(抗PD-1抗体)新辅助治疗微卫星不稳定性高/错配修复缺陷结直肠癌:一项随机、开放标签、Ib期研究结果

摘要号:3505
汇报人:徐瑞华 教授
IBI310L301是一项随机、开放标签、Ib期临床研究(NCT05890742),评估了抗CTLA-4抗体IBI310联合PD-1抑制剂信迪利单抗新辅助治疗微卫星高度不稳定(MSI-H)/错配修复缺陷(dMMR)局部晚期结直肠癌(CRC)患者的疗效。本次ASCO大会上,徐瑞华教授报道了该研究的疗效及安全性结果。
该研究共纳入101例可切除的IIB-III期的MSI-H或dMMR结肠癌受试者分别接受IBI310联合信迪利单抗新辅助治疗(n=52)和信迪利单抗新辅助治疗 (n=49)。主要疗效终点方面,IBI310联合信迪利单抗组病理完全缓解(pCR)率显著高于信迪利单抗单药组(80.0% vs 47.7%,p=0.0007)。安全性方面,IBI310联合信迪利单抗组对比信迪利单抗单药组未增加额外的安全性风险,并且未对后续手术造成显著影响。
该研究结果显示,与单独使用信迪利单抗相比,IBI310联合信迪利单抗新辅助治疗显著提高了MSI-H/dMMR CRC患者的pCR率,两种治疗方案的安全性相当且可控。基于该研究的III期多中心随机对照研究(Neoshot)正在进行。
研究二:Claudin 18.2抗体偶联药物CMG901治疗晚期胃癌/胃食管结合部腺癌患者中的I期临床研究

摘要号:434420
汇报人:徐瑞华 教授
Claudin 18.2作为一种在胃癌中高表达的治疗靶点,近年来引起了广泛关注。康诺亚生物医药科技有限公司在研新药CMG901(AZD0901)是一款潜在同类首创、靶向Claudin 18.2的抗体偶联药物,通过链接体与单甲基奥瑞他汀E(MMAE)偶联而形成。徐瑞华教授团队为探索CMG901在治疗Claudin 18.2高表达的晚期胃癌患者疗效与安全性开展了此研究。
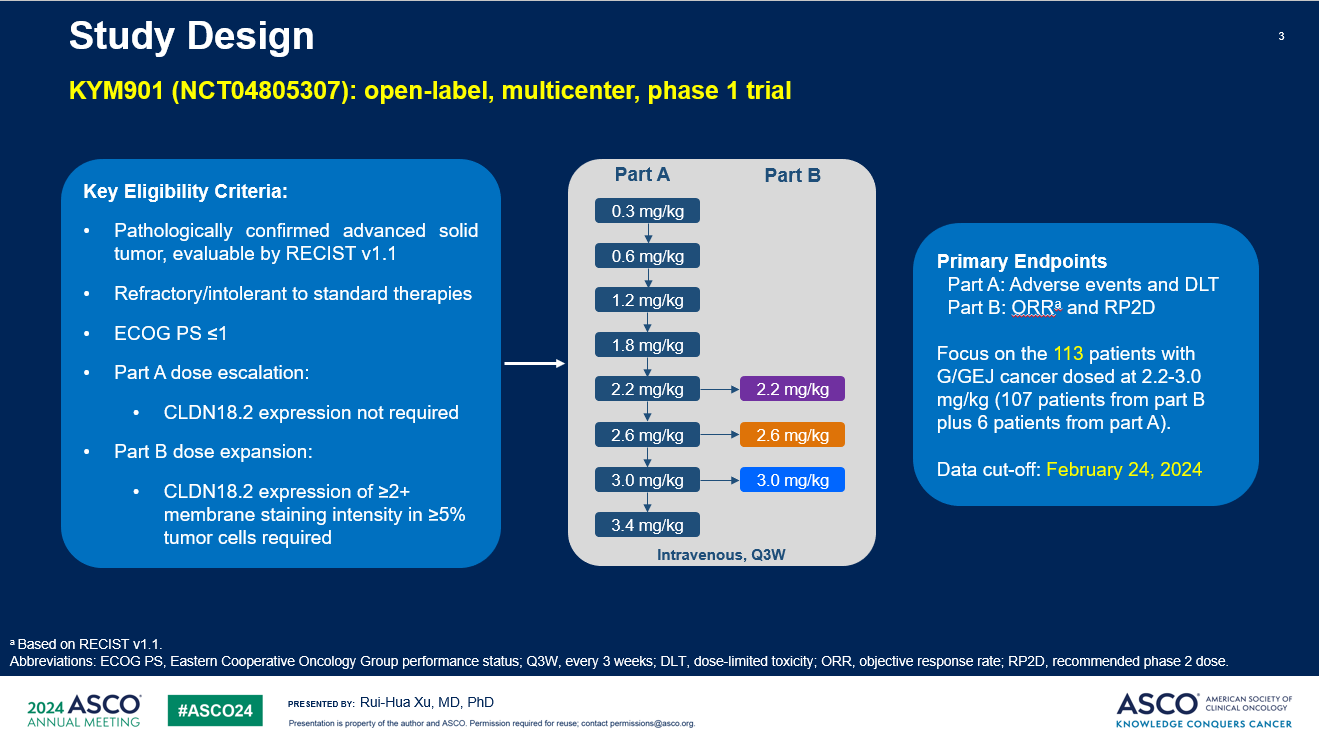
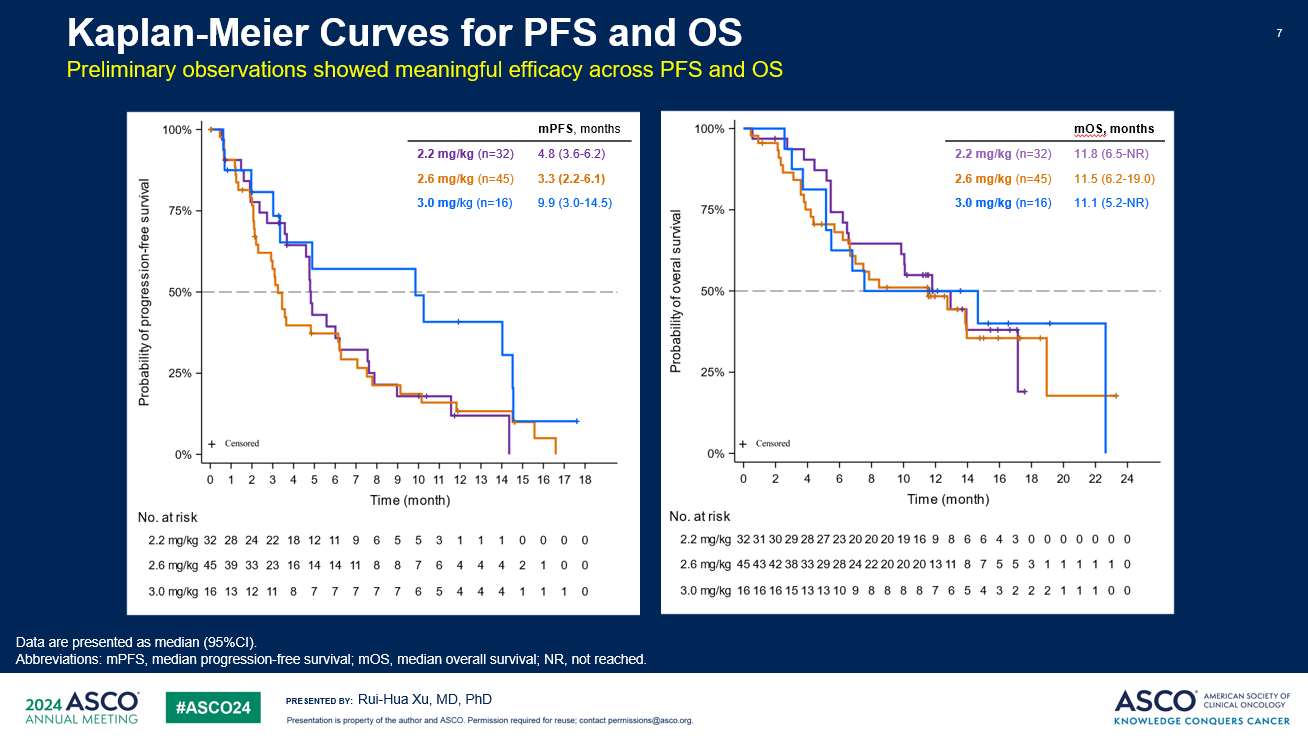
KYM901研究共纳入113例胃癌/胃食管结合部腺癌受试者,其中,89例可评估的Claudin 18.2高表达受试者在三个剂量组的确认的ORR为35%,确认的疾病控制率(DCR)为70%。2.2 mg/kg剂量组确认的ORR为48%。所有93例Claudin 18.2高表达受试者的中位无进展生存期(mPFS)为4.8个月,中位总生存期(mOS)为11.8个月。
安全性方面,113例受试者中,最常见的治疗期不良事件包括贫血(63%)、呕吐(58%)和低白蛋白血症(58%)。受试者最常见的≥3级治疗不良事件是中性粒细胞计数下降(19%)和贫血(13%)。
该研究结果显示,CMG901在治疗晚期抗Claudin 18.2高表达胃癌/胃食管结合部腺癌患者中表现出了优秀的疗效及良好的安全性和耐受性,提示CMG901有望在未来成为Claudin 18.2高表达胃癌患者的治疗新选择。
研究三:呋喹替尼联合紫杉醇二线治疗晚期胃癌或胃食管结合部腺癌III期研究(FRUTIGA)的数据结果更新

摘要号:438730
汇报人:王峰 教授
研究团队开展的FRUTIGA研究是一项基于中国患者的随机双盲III期临床试验,其主要目的是评估呋喹替尼联合紫杉醇对比紫杉醇单药二线治疗晚期胃癌或胃食管结合部腺癌患者的疗效和安全性。
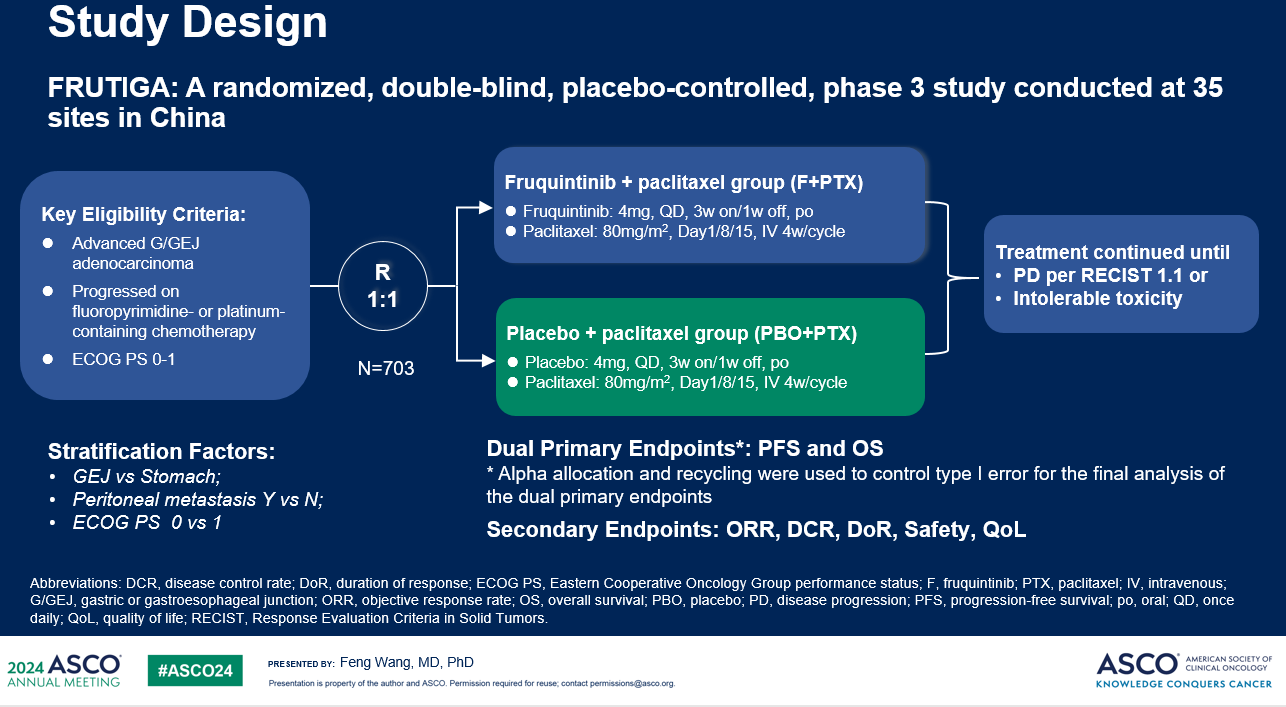
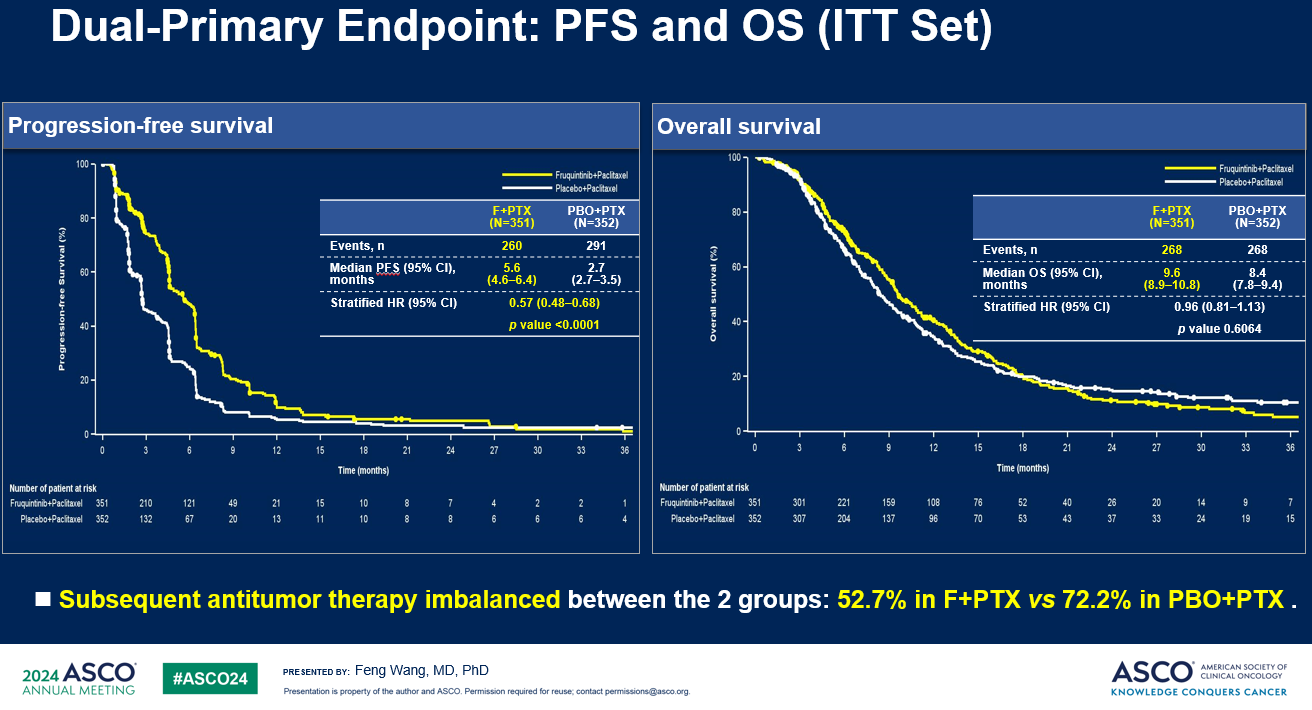
该研究取得了方案预设的阳性结果,与紫杉醇单药相比,呋喹替尼组联合紫杉醇显著延长疾病无进展生存期 (PFS),显著降低了疾病进展或死亡风险 43%(中位PFS: 5.6 vs 2.7个月,HR= 0.57,p<0.0001),呋喹替尼联合紫杉醇对比安慰剂联合紫杉醇,中位PFS达到了5.6个月(95% CI: 4.6-6.4)对比2.7个月(95% CI: 2.7-3.5),HR 0.57(95% CI: 0.48-0.68),P<0.0001。森林图显示在所有亚组中都具有一致性的PFS获益。
OS的分析中发现,本研究在后续抗肿瘤治疗高比例应用(50% vs 70%)且两组间比例严重不均衡的情况下(紫杉醇单药组后续抗肿瘤治疗比例比联合用药组高20%),仍观察到联合用药组总生存期的获益趋势(mOS 9.6 vs 8.4个月,HR= 0.96,p=0.6064)。相对于紫杉醇单药,联合用药组中位OS有1.2个月的延长。通过统计模型校正了两组后续抗肿瘤治疗的不均衡和基线因素等混杂因素后,两组的OS治疗效应HR在0.73-0.91之间,显示联合用药组有名义统计学差异的OS获益。值得注意的是,研究也观察到了在中国胃癌二线治疗III期临床研究中最长的中位总生存期。
此次更新数据中还探索了基于呋喹替尼作用机制和病理分析的亚组分析,在伴有淋巴转移的非弥散型胃癌的亚组中呋喹替尼联合治疗组显示了 PFS(6.1 vs 2.7个月), OS(9.6 vs 2.9个月), ORR(47.4% vs 23.6%), DCR(80% vs52.9%)等疗效的更优获益。
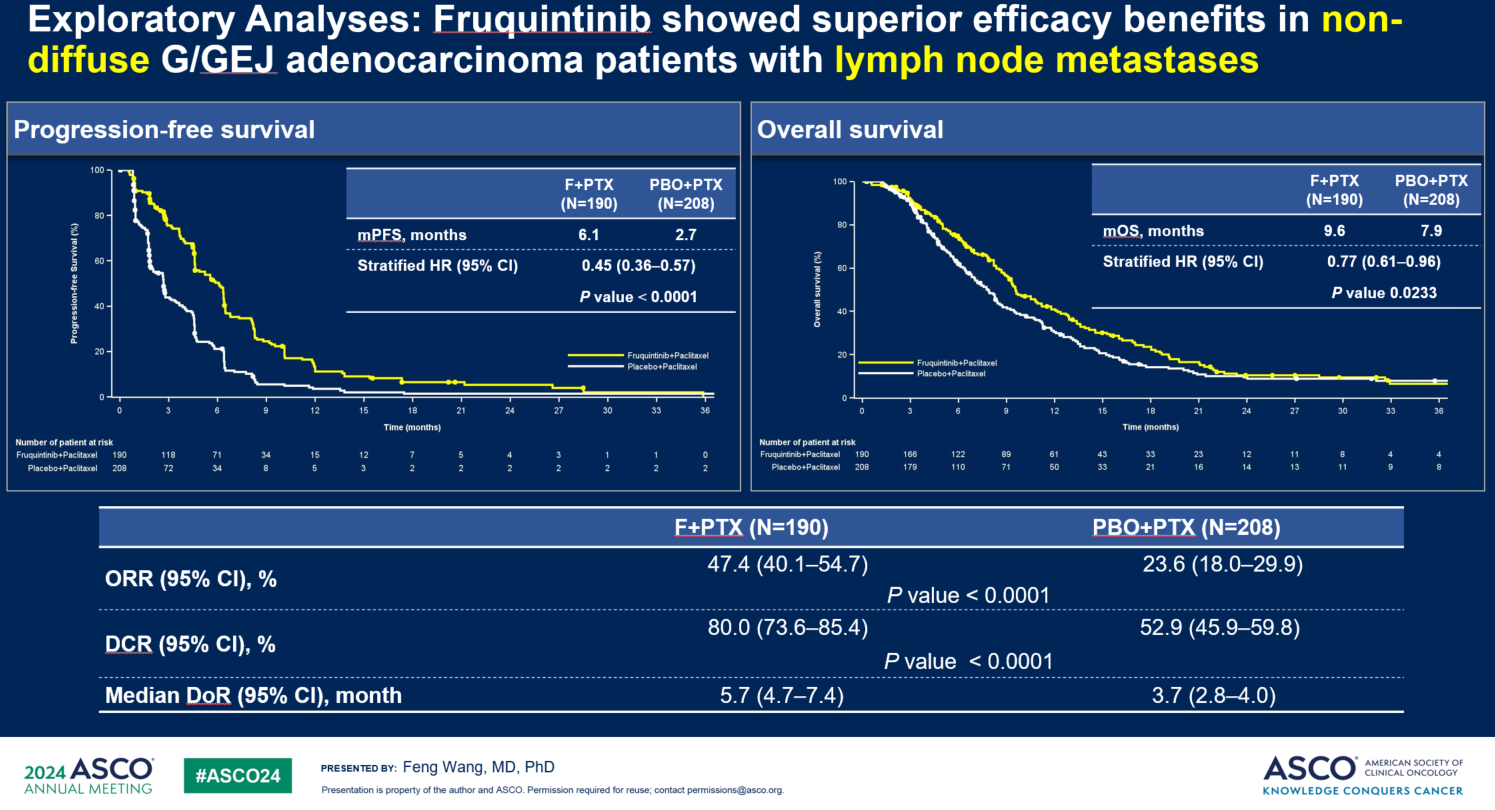
总体上,呋喹替尼联合紫杉醇在一线化疗失败的晚期胃或胃食管结合部腺癌患者中耐受性良好、安全性可控,希望未来能够为此类患者提供另一种新的治疗选择。
研究四:olverembatinib(HQP1351)用于酪氨酸激酶抑制剂(TKI)耐药的琥珀酸脱氢酶(SDH)缺陷型胃肠间质瘤(GIST)和副神经节瘤的疗效结果更新

摘要号:11502
汇报人:邱海波 教授
Olverembatinib(HQP1351)在中国被批准用于治疗慢性髓细胞白血病患者,在SDH缺陷GIST中显示出良好的临床疗效。在此报告了SDH缺陷GIST的最新疗效数据和副神经节瘤的初步疗效数据,副神经节瘤是一种与SDH缺陷相关的肿瘤。
本研究旨在评估Olverembatinib在TIK耐药的SDH缺陷GIST和其他实体瘤患者中的安全性和有效性(per RECIST v1.1)。Olverembatinib每隔一天口服一次(QOD),每28天为一周期。
研究结果显示,26例患者中6例达部分缓解(PR),为最佳缓解。另有18例患者疾病稳定(SD)≥4周期。临床获益率为92.3%,最长治疗时间为40个月。中位随访17.0个月后,中位无进展生存期(PFS)为25.7个月。不良事件发生情况与先前报道一致,未观察到新的安全性问题。
本研究证实Olverembatinib耐受性良好。CBR超过90%,中位PFS显著延长,证明了这种治疗的潜在益处,并为未来研究这种罕见的GIST亚型提供了重要参考。
研究五:评估普特利单抗联合表皮生长因子受体-ADC (EGFR-ADC)药物MRG003治疗EGFR阳性实体瘤患者安全性和有效性的I/II期研究初步结果

摘要号:6013
汇报人:阮丹云 教授
在这项I/II期剂量递增和扩展研究中,符合条件的患者接受3.0 mg/kg HX008联合每3周一次的MRG003治疗,剂量从1.5 mg/kg递增至2.3 mg/kg。主要终点是最大耐受剂量(MTD)、推荐的II期剂量(RP2D)以及客观缓解率(ORR)。次要终点包括缓解持续时间(DOR)、疾病控制率(DCR)和无进展生存期(PFS)。
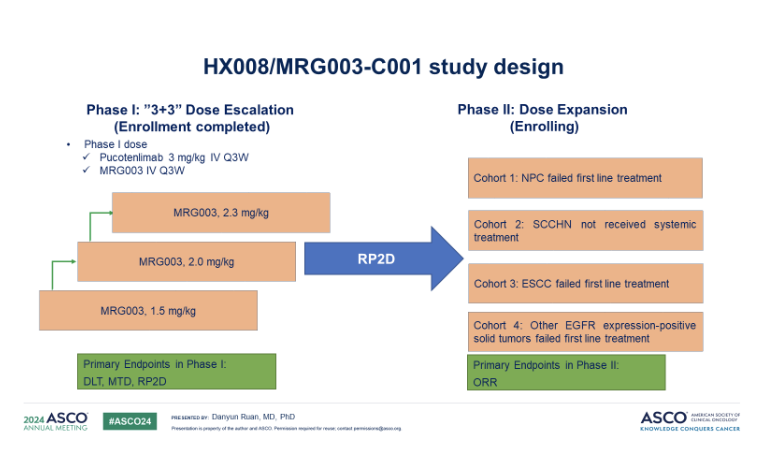
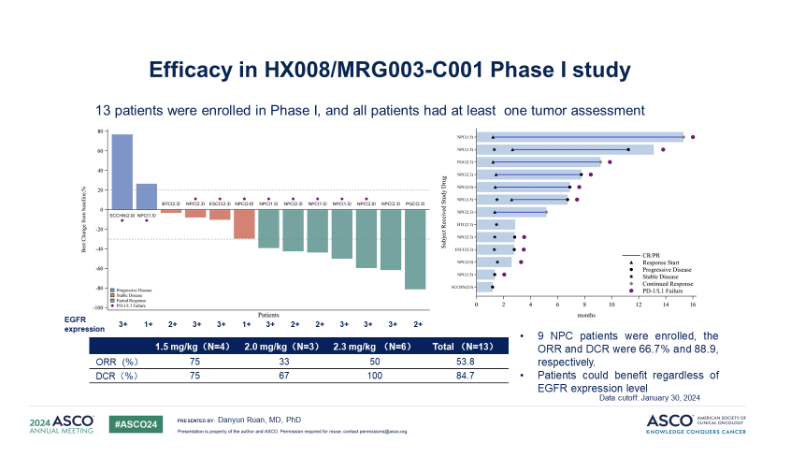
唯一的剂量限制性毒性(DLT)事件发生在2.3mg/kg剂量组,未达到MTD,MRG003的RP2D由安全监测委员会(SMC)确定为2.0mg/kg。在27名可评估的患者中,17名患者达到部分缓解(PR),7名患者病情稳定(SD),因此ORR和DCR分别为63.0%(95%CI: 42.4, 80.6)和88.9%(95%CI: 70.8, 97.7)。
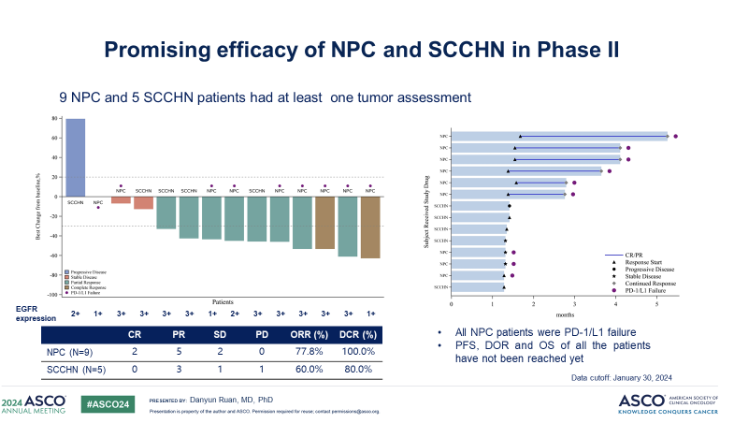
II期研究部分,9名可评估的EGFR阳性NPC患者在接受一线治疗(PD-1抑制剂联合铂类化疗)后进展,在这些患者中观察到2例完全缓解(CR)、5例PR和2例SD,ORR和DCR分别为77.8%(95%CI:40.0, 97.2)和100%(95%CI:66.4, 100)。5名可评估的初治的EGFR阳性SCCHN患者,其中3例PR和1例SD,ORR和DCR分别为60%(95%CI:14.7, 94.7)和80%(95%CI:28.4, 99.5)。研究中的DOR和PFS尚未成熟。治疗时间最长的患者DOR已超过17个月,仍在持续。
安全性方面,最常报告的治疗相关不良事件(TRAEs)包括瘙痒(46%)、皮疹(33%)、AST升高(30%)、贫血(30%)。3-4级TRAEs出现在4名患者(12%)中,主要是白细胞计数减少(9%)和低钾血症(6%)。
I/II期研究结果提示,接受HX008联合MRG003治疗的患者显示出良好的耐受性和在NPC和SCCHN中令人鼓舞的抗肿瘤活性,特别是在PD-1治疗失败的NPC患者中。
研究六:基于cfDNA甲基化标志物的多癌早筛研究

摘要号:3043
汇报人:骆卉妍 教授
本研究基于最新研发的GM-seq技术,针对外周血cfDNA进行甲基化检测,建立了多癌早期检测(MCED)和癌症信号起源(CSO)模型,以实现食管癌、胃癌、结直肠癌、胰腺癌、肝癌、肺癌、乳腺癌和卵巢癌的早期筛查。
研究共纳入1407名受试者(包括癌症757例,健康人群650例)随机分为训练集(989例)和验证集(418例)。在训练集中,多癌早筛技术可以检出71.9%的癌症患者,综合特异性高达99.1%,Top1(首要溯源器官)和Top2(首要和次要溯源器官)的预测准确率高达92.1%和95.3%。验证集中,在99.0%的综合特异性下,本技术仍可检出74.9%的癌症患者,Top1和Top2的预测准确率高达88.2%和92.9%。此外,在训练集和验证集中,I-IV期敏感性分别可达到46.6%、68.5%、76.6%、94.1%和51.8%、66.7%、83.6%、91.1%。
研究证实基于cfDNA的多癌早筛技术在八种癌症的早期检测中具有优异性能,有望成为现有癌症筛查手段的有力补充。
研究七:随机III期ESCORT-1st试验最终分析结果:卡瑞利珠单抗联合化疗一线治疗晚期或转移性食管鳞癌

摘要号:4055
汇报人:骆卉妍 教授
ESCORT-1st研究是一项随机、双盲、安慰剂对照的III期研究,旨在评估卡瑞利珠单抗联合化疗对比安慰剂联合化疗一线治疗晚期或转移性食管鳞癌(ESCC)患者中的疗效与安全性。
该研究的最终分析结果显示,卡瑞利珠单抗联合化疗组一线治疗晚期ESCC的中位总生存期(OS)和无进展生存期(PFS)均显著优于安慰剂联合化疗组,3年总生存率分别为25.6% vs 12.8%;并且亚组分析表明,在PD-L1 TPS<1%的患者中,3年总生存率从14.2%提升到24.4%;在PD-L1 TPS≥1%的患者中,3年总生存率从11.4%跃升至25.9%,再次证实无论PD-L1 TPS的表达水平如何,卡瑞利珠单抗联合化疗一线治疗晚期ESCC均能显著提升3年总生存率,并且安全性可控。
本次公布数据进一步支持了卡瑞利珠单抗联合化疗作为晚期ESCC标准治疗的稳固地位。
研究八:斯鲁利单抗联合HLX04和XELOX vs 安慰剂联合贝伐珠单抗和XELOX一线治疗转移性结直肠癌:一项2/3期研究
摘要号:3569
汇报人:王峰 教授
ASTRUM-015是一项随机、双盲、多中心的II/III期研究,旨在评估斯鲁利单抗联合HLX04(贝伐单抗生物类似药)和XELOX(奥沙利铂+卡培他滨)对比安慰剂联合贝伐珠单抗和XELOX一线治疗转移性结直肠癌(mCRC)的疗效和安全性。
随访时间增至24.2个月的分析结果显示,斯鲁利单抗联合HLX04和XELOX组一线治疗mCRC的主要终点无进展生存期(PFS)对比安慰剂联合XELOX组有着明显的改善:中位PFS为16.8 vs 10.7个月(风险比(HR)=0.58),疾病进展和死亡风险降低42%。微卫星稳定(MSS)(16.8 vs. 10.1个月,HR=0.60)等各亚组中均观察到斯鲁利单抗带来的PFS获益。次要终点总生存期(OS)分析结果显示,斯鲁利单组较安慰剂组OS有明显的改变趋势:中位OS为尚未达到vs 21.2个月(HR=0.74),各亚组中也观察到类似的获益趋势。斯鲁利组的中位持续缓解时间(DOR)也优于安慰剂组:19.4 vs. 11.3个月(HR=0.31)。随着随访时间的延长,联合斯鲁利单抗一线治疗mCRC给患者带来了持续的生存获益,且安全性可控。
这些结果支持斯鲁利单抗联合HLX04和XELOX作为一种非常有前景的转移性结直肠癌一线治疗方案,值得进一步研究。
研究九:射频消融(RFA)联合瑞戈非尼和特瑞普利单抗治疗结直肠癌肝转移的II期临床结果
摘要号:3566
汇报人:王志强 教授
该研究是一项非随机、单臂II期研究,旨在探讨射频消融联合瑞戈非尼和特瑞普利单抗后线治疗微卫星稳定(MSS)结肠直肠癌多发肝转移患者的疗效与安全性。研究采用Simon’s二阶段设计,第一阶段纳入10位患者。90%的患者为同时性肝转移,80%的患者同时出现肝内和肝外转移;其中 60% 的患者至少接受了两个周期的治疗。RFA针对单个肝脏病灶进行,其他病灶被指定为靶病灶。瑞戈非尼和特瑞普利单抗的治疗在RFA后一周开始,每4周为一个周期。特瑞普利单抗每两周静脉注射一次,瑞戈非尼每日口服剂量为80毫克(服药3周,停药1周)。
该研究的最终分析结果显示,中位无进展生存期(PFS)为3.3个月,中位总生存期(OS)为11.3个月,50%患者病情稳定(SD)。遗憾的是,无一患者确认为部分或完全缓解,未能进入研究第二阶段。不良事件(AEs)包括手足综合征、肝功能异常、疲劳、腹胀和血小板减少。最常见的不良反应是手足综合征,发生率为50%。可能与治疗有关的严重不良反应(≥3 级)包括手足综合征和高胆红素血症,发生率均为10%,不良反应大多可控,值得注意的是,一名患者在治疗期间出现了超进展。
射频消融与瑞戈非尼和特瑞普利单抗的联合疗法在MSS 结直肠癌肝转移患者中未显示出令人鼓舞的有效率,但中位生存时间较长并且安全性可控。
研究十:比较结直肠癌肺寡转移患者消融与手术的长期结果:一项回顾性队列研究
摘要号:3581
汇报人:张天奇 教授
这一项回顾性队列研究旨在评估消融治疗或外科切除结直肠癌肺寡转移患者的长期生存随访。
该研究共纳入96例患者(2012.01-2018.10),41例患者(75个病灶)接受消融治疗,55例患者(59个病灶)接受手术治疗,中位随访时间为58.3个月(IQR:38.6-73.7)。最终结果显示两组的中位总生存期(mOS)以及3年和5年生存率无显著统计学差异(消融 vs. 手术,mOS:73.3个月 vs. 70.4个月,P=0.64;3年生存率:82.6% vs. 79.8%;5年生存率:59.9% vs. 58.7%)。消融组和手术组的中位无进展生存期(mPFS)分别为12.1个月和11.5个月,无显著差异(P=0.48)。病灶的局部复发率分别为26.7%和22.0%(P=0.68),也未见显著统计学差异。
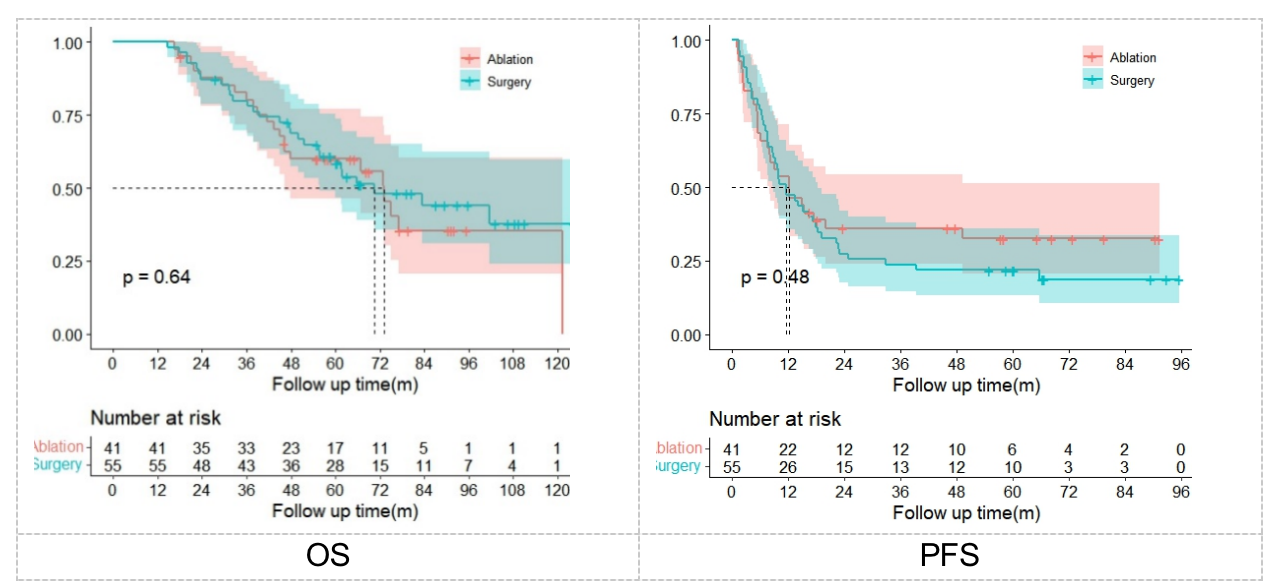
这是目前结直肠癌肺寡转移纳入病例最多,随访时间最长的研究,为消融治疗肠癌肺寡转移提供科学依据。
研究十一:局部晚期胃食管结合部癌的围手术期PD-1抗体替雷利珠单抗联合化疗:一项前瞻性、非随机、开放标签、II期临床试验
摘要号:4083
汇报人:聂润聪 教授
NEOSUMMIT-03是一项前瞻性、非随机、开放标签的II期试验,以评估在局部晚期可切除的食管胃结合部(GEJ)癌患者围手术期化疗中添加PD-1抗体替雷利珠单抗的有效性以及安全性。
在2022年10月至2023年6月期间,32例患者纳入本研究。该研究成果显示,所有患者都接受了至少一个周期的术前治疗,96.9%(31/32)的患者完成了三个周期的术前替雷利珠单抗联合SOX治疗。R0切除率为96.9% (31/32)。MPR率为50.5% (16/32,95% CI: 31.9% ~ 68.1%), pCR率为28.1% (9/32,95% CI: 13.7% ~ 46.7%)。手术发生率为15.6%(5/32),无30天死亡率。术前和术后治疗期间,与治疗相关的3-4级不良事件发生率为31.2%(10/32)。
本次公布数据初步提示围手术期化疗联合替雷利珠单抗可提高进展期GEJ腺癌患者的病理反应。
排版编辑:肿瘤资讯-tcz











 苏公网安备32059002004080号
苏公网安备32059002004080号


