在HER2异常的非小细胞肺癌(NSCLC)患者的治疗中,此前大分子单抗或小分子酪氨酸激酶抑制剂(TKI)的临床探索未能取得理想结果。德曲妥珠单抗(T-DXd,DS-8201)是一种靶向HER2突变的新型抗体偶联药物(ADC),凭借在DESTINY-Lung系列研究中的优异表现,目前已获得美国FDA加速批准,适用于既往接受过系统治疗的HER2突变阳性的晚期NSCLC患者的治疗,成为了首个获批适用于HER2突变NSCLC的靶向药物。2023年,DESTINY-Lung系列研究持续更新,包括在中国开展的DESTINY-Lung05研究以及探索在一线应用的DESTINY-Lung04研究,这些研究也将为T-DXd在国内的临床实践应用提供重要的指导价值。【肿瘤资讯】诚邀江苏省肿瘤医院史美祺教授参与分享,共同探讨HER2突变晚期NSCLC的治疗模式,展望ADC药物临床前景。
专家介绍
江苏省肿瘤医院/江苏省肿瘤防治研究所肿瘤内科肺癌亚专业
中国医疗保健国际交流促进会肿瘤内科学分会常务委员
中国医疗保健国际交流促进会胸部肿瘤学分会常务委员
中国初级卫生保健基金会胸部肿瘤精准治疗专业委员会常务委员
中国临床肿瘤学会(CSCO)非小细胞和小细胞肺癌专家委员会委员
中国抗癌协会肿瘤药物临床研究专业委员会委员
中国抗癌协会肺癌专中国初级卫生保健基金会胸部肿瘤精准治疗专业委员会常务委员
泛长三角胸部肿瘤联盟专业委员会副主席
中国抗癌协会肿瘤标志物专业委员会肺小结节分子标志物协作组常务委员
江苏省研究型医院学会肺结节与肺癌MDT委员会副主任委员
江苏省抗癌协会肺癌专业委员会常务委员
江苏省康复医学会呼吸康复专业委员会常务委员
江苏省医学会肿瘤学分会肺癌学组副组长
国际肺癌协会会员,ASCO会员
专业特长:晚期肿瘤治疗,擅长肺癌的内科治疗,参与过近80项国际国内多中心肺癌临床新药研究试验,发表论文100余篇,以第一作者发表的SCI论文影响因子最高分32.976分。获省卫生厅新技术引进二等奖二项。
ADC在HER2突变NSCLC中取得亮眼表现,FDA批准T-DXd适用于后线患者治疗
史美祺教授:HER2突变在非小细胞肺癌中是一类少见突变。既往对于HER2突变的NSCLC,在一线治疗中通常按驱动基因阴性进行治疗,即采取免疫+化疗为主的治疗方案。近年来,随着研究进展,一些TKI类药物在后线治疗中取得了一定成果,包括阿法替尼、来那替尼、吡咯替尼等,但疗效数据难以令人满意,例如吡咯替尼在治疗铂类化疗后的HER2突变型晚期肺腺癌患者的II期临床研究中,经独立评审委员会(IRC)评估的客观缓解率(ORR)约30.0%,中位无进展生存期(PFS)约半年[1],目前也暂未有TKI类药物获批。
近年来,ADC类药物在治疗HER2突变阳性晚期NSCLC患者的临床研究中取得了令人瞩目的表现。其中,德曲妥珠单抗(T-DXd,DS-8201)在DESTINY-Lung系列研究中取得了优异的疗效数据。此前,DESTINY-Lung01研究曾发表于NEJM[2],这项多中心、开放标签的Ⅱ期研究中,T-DXd 6.4mg/kg治疗经治的HER2突变NSCLC患者,ORR达到55%,中位缓解持续时间(DoR)达到9.3个月,中位PFS达到8.2个月,中位OS则为17.8个月。后续的DESTINY-Lung02研究进一步探索了5.4mg/kg和6.4mg/kg不同剂量水平下的疗效和安全性差异。基于这一系列研究中的表现,2022年8月,FDA正式批准T-DXd作为HER2突变NSCLC患者的后线治疗,这也是首个获批适用于HER2突变晚期NSCLC的靶向治疗药物。目前,在NCCN指南、ESMO指南和CSCO指南中,T-DXd都获得了推荐,当然由于在国内尚未获批,因此在2023版CSCO指南中T-DXd仅获得了III级推荐[3-5]。相信在今年下半年,T-DXd在HER2突变阳性晚期NSCLC患者中的后线适应症将有望在国内获批,其未来临床表现值得期待。
精准检测是治疗的前提,推荐治疗前优先行NGS检测
史美祺教授:精准诊断是精准治疗的前提,基因检测是肺癌治疗前重要的诊断手段。自EGFR靶点问世以来,越来越多肺癌靶点成药,基因检测作为治疗前的重要诊断手段其重要性也逐渐提高。对于类似HER2的少见靶点,通过基因检测指导治疗方案的开展,是其精准治疗的重中之重。HER2基因变异常见的形式为HER2突变、HER2扩增和HER2过表达,在肺癌中的发生率分别约为2-4%、2.4%和6%~35%[6-8]。其中我们今天讨论的HER2突变,多见于酪氨酸激酶域的18~21号外显子,最常见的突变形式是20号外显子插入。肺癌中HER2突变被视为预后不良因素,多数为腺癌、女性、不吸烟的年轻患者[9-11]。
目前,对于HER2突变的检测,临床常用的检测方法包括RT-PCR和NGS。由于肺癌中驱动基因众多,对于HER2的检测推荐采取NGS,在检测同时也可以一并检测包括EGFR、ALK在内的其他驱动基因,有条件的患者可以采取更大的Panel,以便更为精细地检测峰度更低的罕见靶点。在2023版《CSCO非小细胞肺癌诊疗指南》中,II级推荐采取单基因检测技术或NGS检测HER2突变。我国专家牵头制定的HER2变异检测共识也应该尽早检测,推荐用NGS作为HER2突变的优选检测手段[12]。
总之,HER2基因作为一个重要的驱动基因,应该作为晚期非小细胞肺癌的常规检测靶点,优先在晚期一线治疗前,使用NGS 对大panel进行检测,从而帮助患者选择最适合的治疗方案,最大化患者的生存获益。
DESTINY-Lung系列研究剖析,安全保障疗效出色
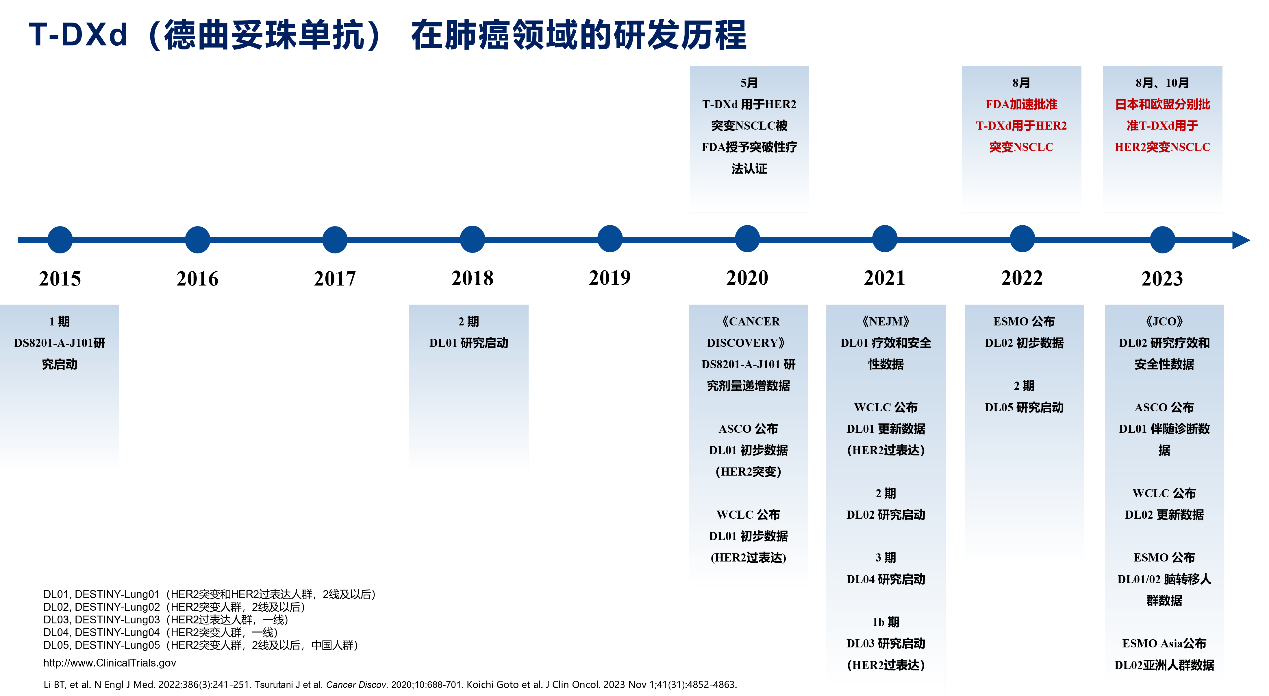
图1. DESTINY-Lung系列研究历程
史美祺教授:DESTINY-Lung02研究是目前在HER2突变的NSCLC中非常重要的一项研究,旨在探索不同剂量的T-DXd在HER2突变的NSCLC后线治疗中的应用,该研究此前多次登上顶尖学术舞台,包括WCLC、ESMO ASIA等等。
这是一项随机双盲、多中心、双队列II期临床研究,该研究共纳入152例既往接受过一种系统性治疗的不可切除或转移性HER2突变NSCLC患者,以2:1的比例随机接受5.4mg/kg和6.4mg/kg剂量的德曲妥珠单抗治疗。主要研究终点是独立评审委员会评估的ORR。2023 WCLC大会上公布的主要研究结果显示[13],截至2022年12月23日,研究共纳入152例患者,其中5.4mg/kg组纳入102例患者,6.4mg/kg组纳入了50例患者。中位随访时间分别为11.5个月和11.8个月。其中,5.4mg/kg组患者经BICR评估的cORR达到了49.0%,中位DoR为16.8个月,中位PFS为9.9个月,中位OS 为19.5个月。从疗效方面评估,6.4mg/kg剂量组和5.4mg/kg剂量组都成功到达预设目标。
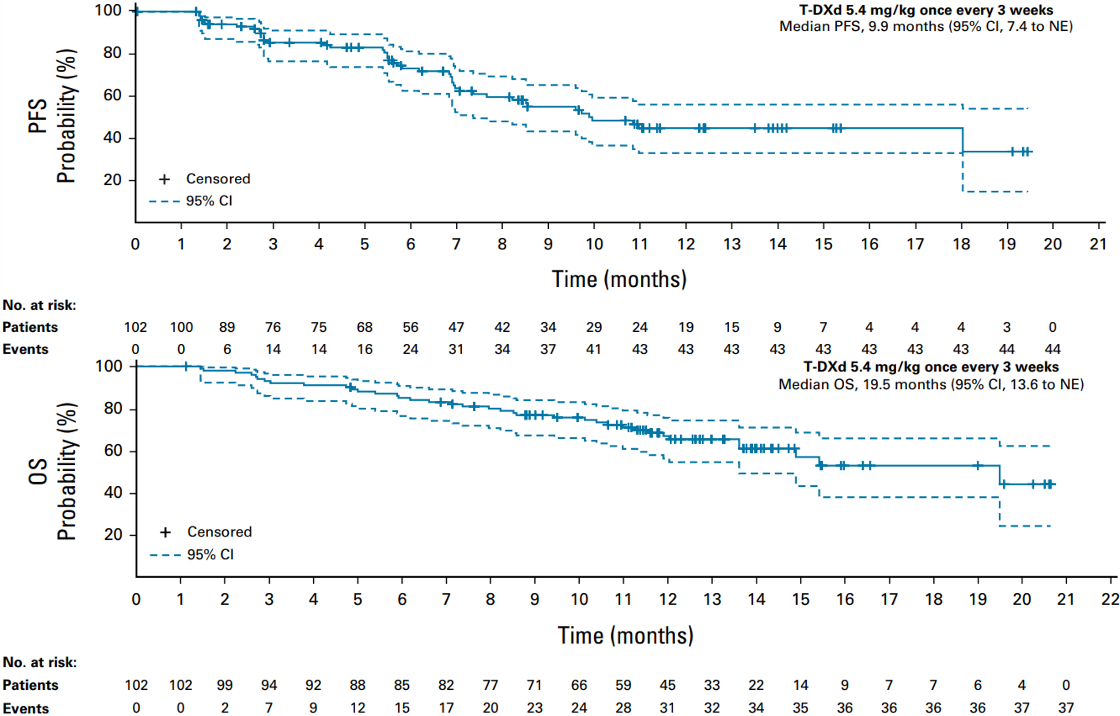
图2. DESTINY-Lung02研究中5.4mg/kg组的PFS、OS曲线
临床实践中,除疗效外,安全性也是重要考量因素。5.4mg/kg组和6.4mg/kg组最常见≥3级不良事件包括中性粒细胞减少(18.8%和36.0%)和贫血(10.9%和16.0%)。两组患者发生药物相关性间质性肺病(ILD)/非感染性肺炎的发生率分别为12.9%和28.0%,主要为1和2级。5.4mg/kg组相比6.4mg/kg组观察到更优的安全性。基于该研究,FDA最终批准5.4mg/kg 剂量的T-DXd作为HER2突变的NSCLC患者的后线治疗。
2023年ESMO大会中更新的DESTINY-Lung01和DESTINY-Lung02中针对脑转移患者的汇总分析希望探索ADC对于脑转移是否可带来获益,该研究受到全球研究者的高度重视[14]。此次报告数据显示,T-DXd 5.4 mg/kg对于脑转移和无脑转移患者的cORR分别达到46.9%和50.0%,DCR分别为90.6%和94.3%,中位PFS分别为7.1个月和18.0个月,中位OS分别为13.6个月和19.5个月。而对于基线有可测量脑转移病灶的患者,颅内cORR为50%,颅内DCR为92.9%,颅内中位DoR为9.5个月。这也显示了T-DXd对于HER2突变患者脑转移的出色疗效。
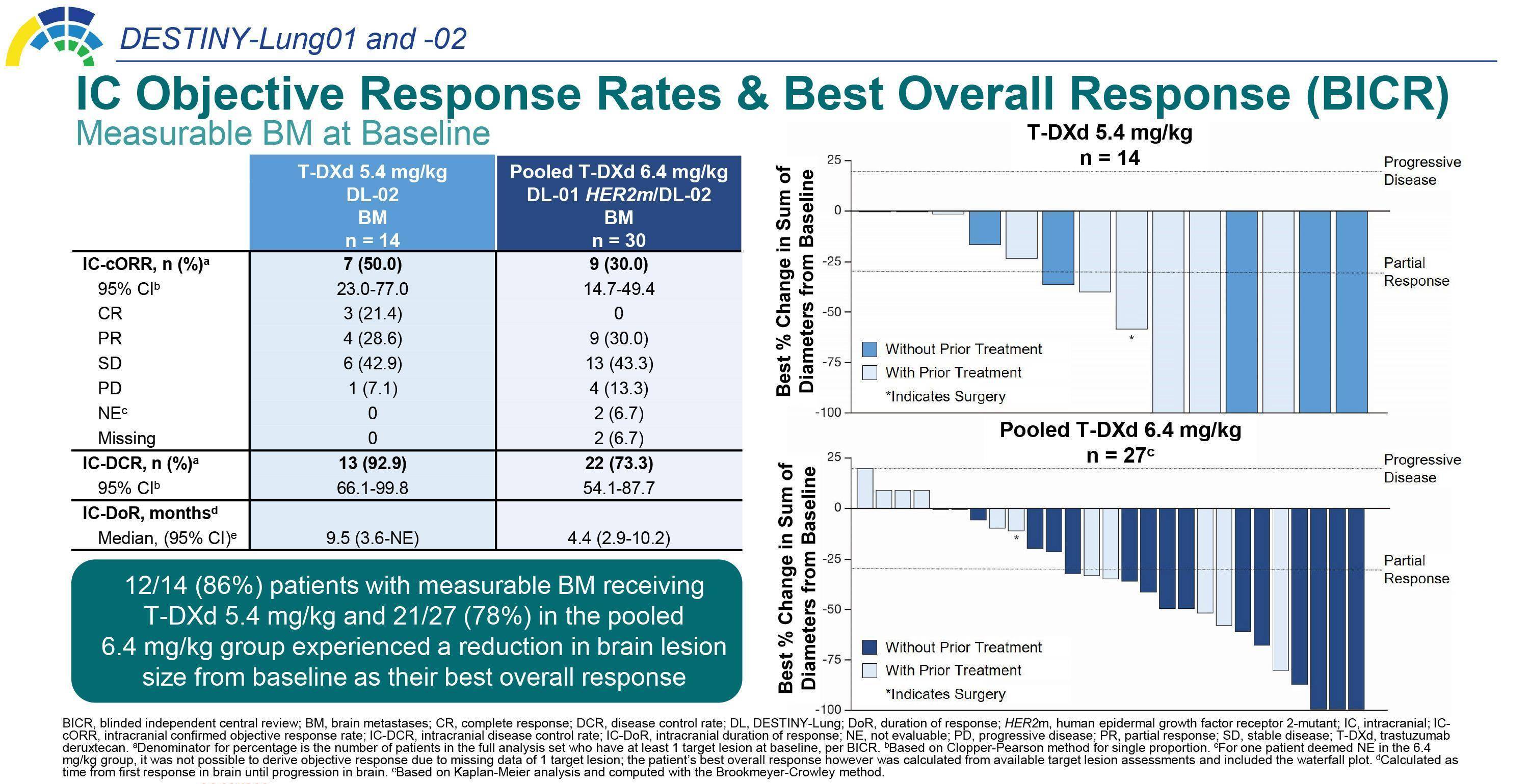
图3. DESTINY-Lung01和02中的IC-ORR与ORR数据
除全球人群外,对于亚裔人群,2023年ESMO ASIA更新的亚裔(日本、韩国和中国台湾地区)亚组数据显示[15],截至2022年12月23日,研究总计纳入了93例亚洲患者,其中5.4mg/kg组63例,6.4mg/kg组共30例。5.4mg/kg组的cORR达到了50.8%,中位DoR为16.8个月,中位PFS为10.8个月,中位OS为19.5个月。亚裔亚组数据提示,亚洲患者的疗效结果与总体人群一致。安全性方面,两组分别有41.9%和63.3%的患者观察到药物相关≥3级TEAE;与6.4mg/kg组相比,5.4mg/kg组导致停用、剂量降低和治疗中断等药物相关TEAEs的发生率更低,且与总体人群一致。
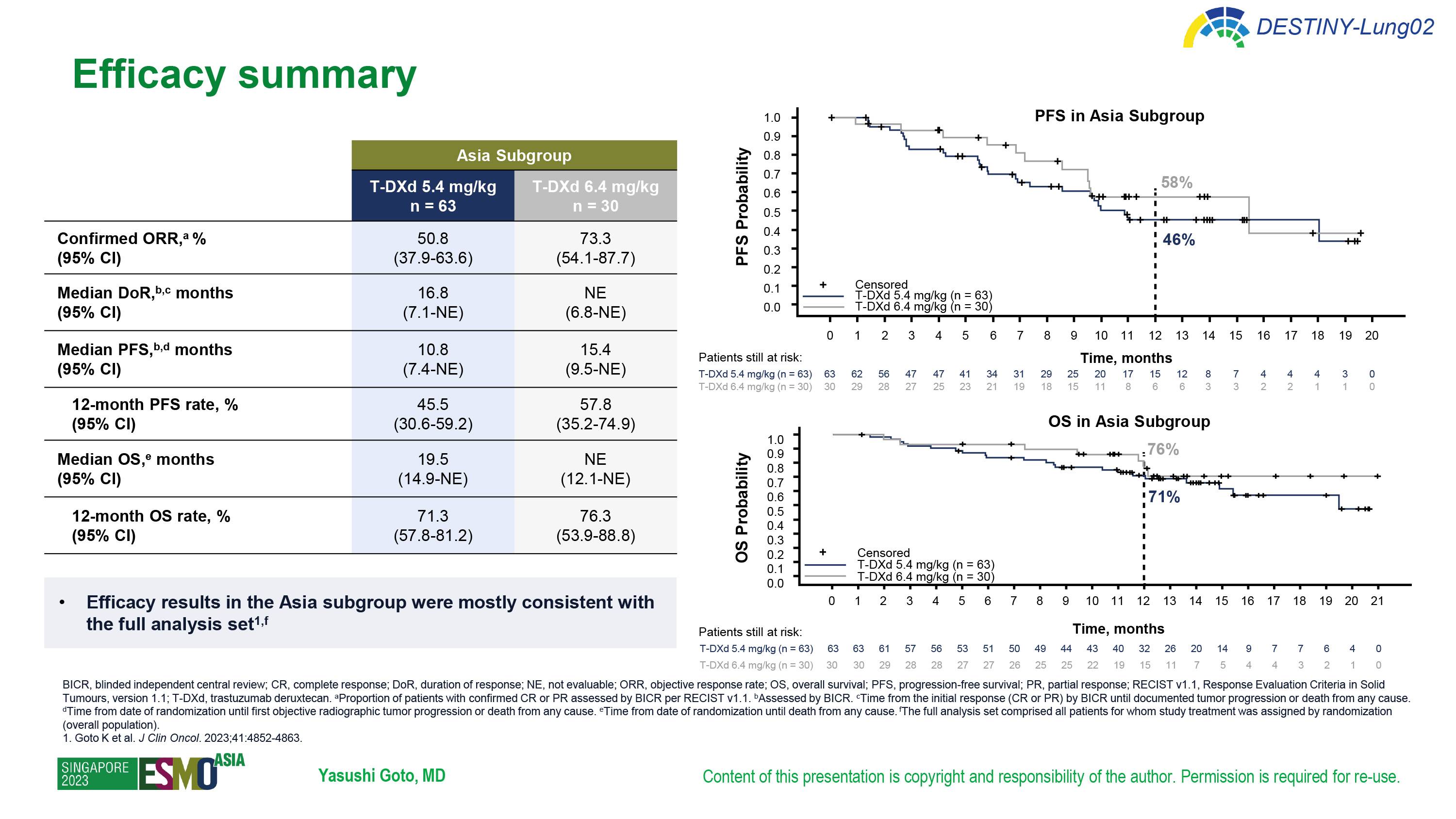
图4. DESTINY-Lung02研究中亚洲亚组数据
总之,DESTINY-Lung02研究的结果提示了5.4mg/kg剂量的T-DXd在经治的HER2突变晚期NSCLC患者中展示出令人鼓舞的疗效和可控的安全性,总体人群cORR达到了49.0%,中位PFS达到了9.9个月,亚洲人群中的获益也保持一致,这样的表现增强了临床医生将其应用于临床实践的信心。我很期待未来更大规模的研究的开展,并期待它尽早在国内获批相关适应症,也期待未来通过更多临床研究探索在一线治疗或联合治疗中的应用。
HER2靶向治疗百花齐放,期待T-DXd向前线更进一步探索
史美祺教授:目前ADC主要在后线治疗中取得了突破,T-DXd目前针对中国患者后线治疗的DESTINY-Lung05研究已经开展,预计将于不久后的AACR公布结果,该研究将为中国临床实践提供更加有力的指导,并有望获得NMPA批准,对此我抱有信心。
通常创新药在肿瘤治疗中的探索路径是由晚期后线至一线,再进一步尝试前移至局晚期。T-DXd在后线立足后,在一线治疗中的临床探索也已经如火如荼地开展,III期DESTINY-Lung04研究便尝试在一线治疗中使用T-DXd头对头对比驱动基因阴性患者的标准一线免疫联合化疗方案,研究设计体现了研究者的信心,我们也期待研究取得成功,为HER2突变NSCLC的治疗建立新的里程碑。除了T-DXd外,其他的ADC如SHR-A1811,新型HER2-TKI如BI 1810631的未来探索也值得期待。
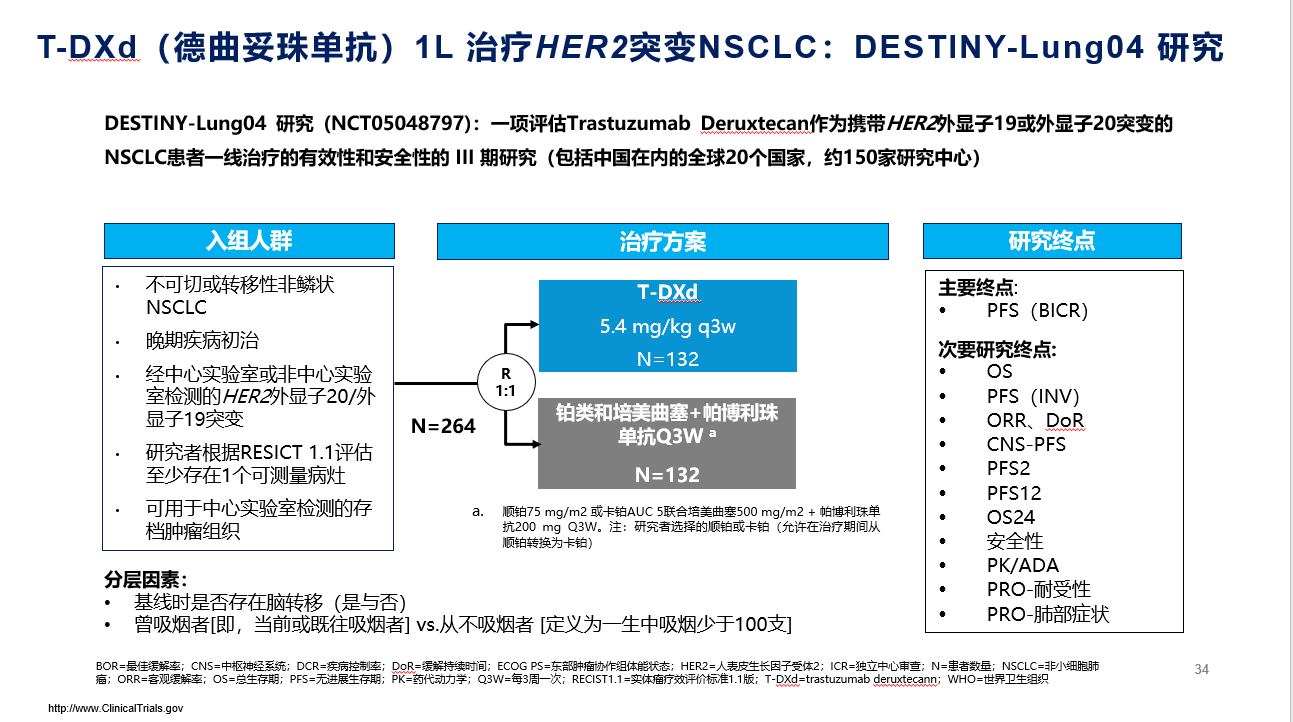
图5. DESTINY-Lung04研究设计图
HER2突变之外,在其他的HER2变异形式如HER2过表达中,T-DXd也有所布局,例如DESTINY-Lung03研究和U106研究,两项研究都探索了T-DXd联合ICI±化疗治疗HER2过表达患者的疗效和安全性,期待这类联合模式为我们带来好消息。如果这类研究取得成功,将提示除HER2突变外的更多HER2变异阳性患者,也将从新型靶向治疗中获益,进一步拓展获益患者群体。
总结
采访临近尾声,史美祺教授结合临床经验整体总结了对于HER2突变晚期NSCLC诊疗的看法,自EGFR靶点问世以来,越来越多的靶点拥有可及的药物,使得基因检测成为了当下非常重要的诊断手段。近年来,随着靶向HER2的治疗方案取得突破,也更加强调了HER2突变检测的重要性,包括CSCO指南在内的多部权威指南都强调了肺癌HER2突变检测的重要价值。
如今,HER2突变作为肺癌中的治疗靶点,临床价值也在逐渐提高,以T-DXd为代表的ADC药物在临床研究中取得突破,尽管药物暂时仍不可及,但相关研究结果已经提示了其重要的应用价值。考虑到T-DXd已经在国内获批了乳腺癌的适应症,相信肺癌适应症的获批或也将不再遥远。
未来,除在后线治疗中进一步拓展应用之外,我们也很关注T-DXd在一线治疗中,在更早期肺癌患者的围术期治疗中,或以联合治疗方式使用等其他治疗模式中的应用。我们将继续深入探索T-DXd在肺癌中的更多可能,为HER2变异肺癌带来治疗希望。
[1] WANG Y, JIANG T, QIN Z, et al. HER2 exon 20 insertions in non-small-cell lung cancer are sensitive to the irreversible pan-HER receptor tyrosine kinase inhibitor pyrotinib [J]. Ann Oncol, 2019, 30(3): 447-455.
[2] Li BT, Smit EF, Goto Y, Nakagawa K, Udagawa H, Mazières J, et al. Trastuzumab Deruxtecan in HER2-Mutant Non-Small-Cell Lung Cancer. N Engl J Med 2022; 386(3):241-251.
[3] CSCO非小细胞肺癌诊疗指南(2023版)
[4] Hendriks L E, Kerr K M, Menis J, et al. Oncogene-addicted metastatic non-small-cell lung cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up☆[J]. Annals of Oncology, 2023, 34(4): 339-357.
[5] NCCN Guidelines:NSCLC 2024 v3.
[6] JING C W, MAO X H, WANG Z, et al. Next generation sequencing based detection of EGFR, KRAS, BRAF, NRAS, PIK3CA, Her2 and TP53 mutations in patients with non small cell lung cancer [J]. Mol Med Report, 2018: 2191-2197. DOI: 10.3892/mmr.2018.9210.
[7] PILLAI R N, BEHERA M, BERRY L D, et al. HER2 mutations in lung adenocarcinomas: a report from the Lung Cancer Mutation Consortium [J]. Cancer, 2017, 123(21): 4099-4105. DOI: 10.1002/cncr.30869.
[8] HIRSCH F R, VARELLA-GARCIA M, FRANKLIN W A, et al. Evaluation of HER-2/neu gene amplification and protein expression in non-small cell lung carcinomas [J]. Br J Cancer, 2002, 86(9): 1449-1456. DOI: 10.1038/sj.bjc.6600286.
[9] Mazières J,Peters S,Lepage B,et al. Lung cancer that harbors an HER2 mutation:epidemiologic characteristics and therapeutic perspectives [J]. J Clin Oncol,2013,31 (16):1997-2003.
[10] Arcila M,Chaft J,Nafa K,et al. Prevalence,clinicopathologic associations,and molecular spectrum of ERBB2 (HER2) tyrosine kinase mutations in lung adenocarcinomas[J]. Clin Cancer Res, 2012, 18(18): 4910-4918.
[11] Liu S,Li S,Hai J,et al. Targeting HER2 aberrations in non-small cell lung cancer with osimertinib[J]. Clin Cancer Res,2018,24(11):2594-2604.
[12] Chinese expert consensus on the diagnosis and treatment of HER2-altered non-small cell lung cancer. Thorac Cancer. 2023 Jan;14(1):91-104. doi: 10.1111/1759-7714.14743. Epub 2022 Nov 28. PMID: 36444143; PMCID: PMC9807451.
[13] Goto K, Goto Y, Kubo T, et al. Trastuzumab Deruxtecan in Patients With HER2-Mutant Metastatic Non-Small-Cell Lung Cancer: Primary Results From the Randomized, Phase II DESTINY-Lung02 Trial. J Clin Oncol. 2023;41(31):4852-4863. doi:10.1200/JCO.23.01361
[14] Li BT, Planchard D, Goto K, et al. Trastuzumab deruxtecan (T-DXd) in patients (pts) with HER2(ERBB2)-mutant (HER2m) metastatic nonesmall cell lung cancer (NSCLC) with and without brain metastases (BMs):Pooled analyses from DESTINY-Lung01 and DESTINYLung02. 2023 ESMO 1321MO.
[15] Goto Y, Goto K, Kubo T, et al. 510MO Trastuzumab deruxtecan (T-DXd) in Asian patients (Pts) with human epidermal growth factor receptor 2 (HER2; ERBB2)-mutant (HER2m) metastatic non-small cell lung cancer (mNSCLC): Subgroup analysis of DESTINY–Lung02 (DL-02). Annals of Oncology, 2023, 34: S1666-S1667. doi:10.1016/j.annonc.2023.10.589
排版编辑:Crystal











 苏公网安备32059002004080号
苏公网安备32059002004080号


