EML4-ALK重排,也称为ALK阳性变体,是非小细胞肺癌(NSCLC)的重要驱动突变之一,约占NSCLC的5%[1-3]。在过去十年中,ALK酪氨酸激酶抑制剂(ALK-TKI)靶向治疗ALK阳性肺癌取得了进展。阿来替尼是一种高选择性ALK抑制剂,目前用作晚期ALK阳性NSCLC的一线或二线治疗[4,5]。然而,尽管阿来替尼在治疗晚期ALK阳性NSCLC方面具有良好的疗效和耐受性,但其作为新辅助治疗在可切除ALK阳性NSCLC中的活性仍有待研究。
一篇关于阿来替尼新辅助治疗EML4-ALK重排的肺腺癌患者的文献发布于Frontiers in Oncology,文中报告了2例现有阿来替尼新辅助治疗病例,并回顾了7例既往报告的病例[6]。
研究背景
既往ALK阳性患者的新辅助治疗大多是小样本的临床研究或病例报告[7,8]。正在进行的II期ALNEO试验评估了新辅助阿来替尼(口服8周)治疗在可能可切除的III期ALK阳性NSCLC(任何T分期伴N2或T4 N 0 -1)中的活性[9]。另一项正在进行的NAUTIKA1研究是一项在可切除的II-III期NSCLC患者中进行的多队列围手术期试验,研究ALK阳性队列中的新辅助和辅助阿来替尼治疗[10]。
尽管之前有几项研究报道了接受阿来替尼新辅助治疗的病例[9,11],但鉴于目前尚未有针对接受阿来替尼新辅助治疗的患者进行严格设计和实施的大型试验的公开结果,因此对阿来替尼的术前方案和治疗时机尚未进行深入研究。此外,还没有关于阿来替尼新辅助治疗长疗程的病例报道或研究。
研究方法
我们的报告涉及2例早期NSCLC病例,他们在适应症外长期新辅助阿来替尼治疗获得病理完全缓解(pCR)。在PubMed、Web of Science和Cochrane Library中全面检索ALK阳性可切除的新辅助阿来替尼病例。论文的选择遵循 PRISMA建议。我们首先报道了2例可切除的ALK阳性肺腺癌患者,他们接受了超过6个月的阿来替尼新辅助治疗,随后接受了根治性手术切除以获得病理完全缓解。随后,我们系统回顾了之前报道的阿来替尼新辅助治疗病例。
病例展示
2例IIB期(cT3N0M0)EML4-ALK肺腺癌患者接受了长期(超过30周)新辅助阿来替尼治疗,随后进行了R0肺叶切除术,获得了完全病理学缓解。
病例1
51岁男性,重度吸烟,诊断为肺腺癌。免疫组化证实ALK阳性(图2)。此外,采用60基因组二代测序,在肿瘤标本中检测到EML4(外显子13)-ALK(外显子20)融合蛋白(变体1)。
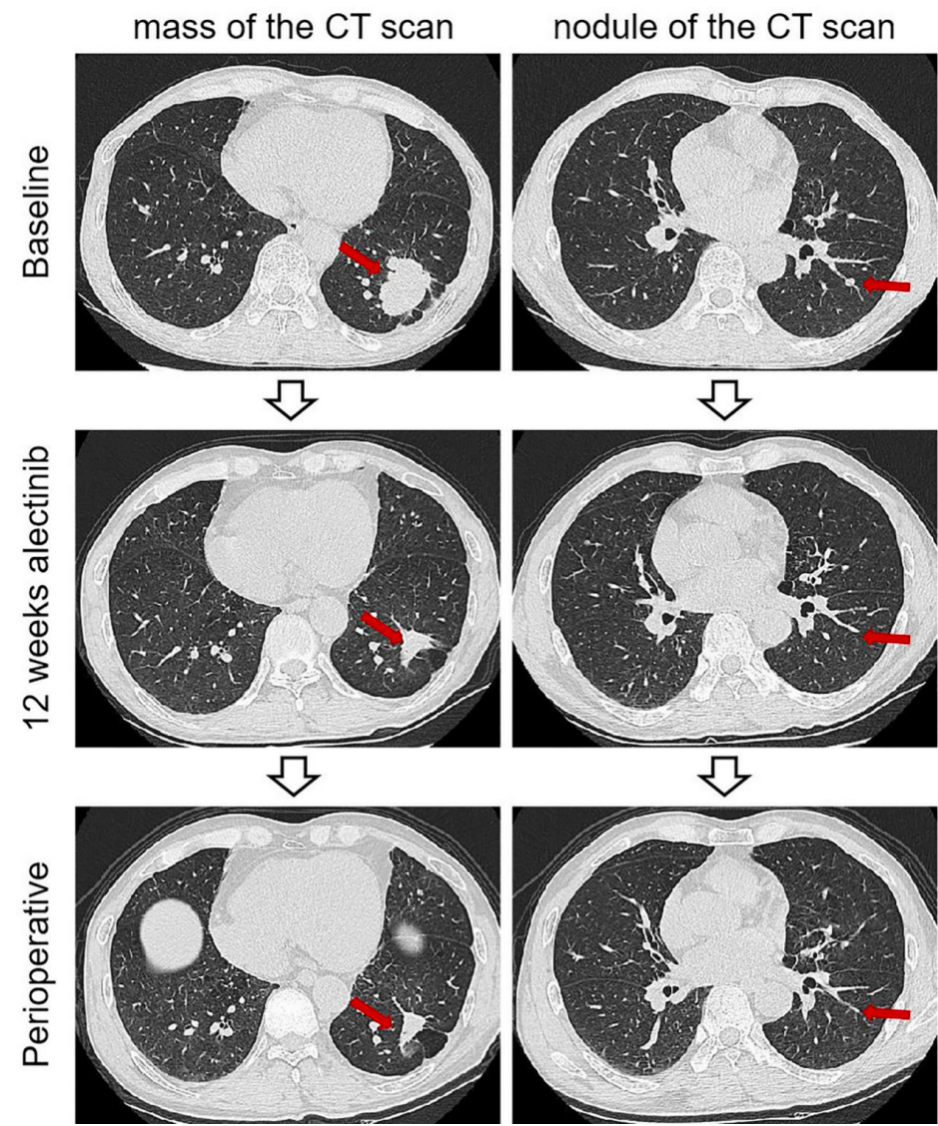 图1. 病例1的影像学表现,阿来替尼新辅助治疗前后的CT
图1. 病例1的影像学表现,阿来替尼新辅助治疗前后的CT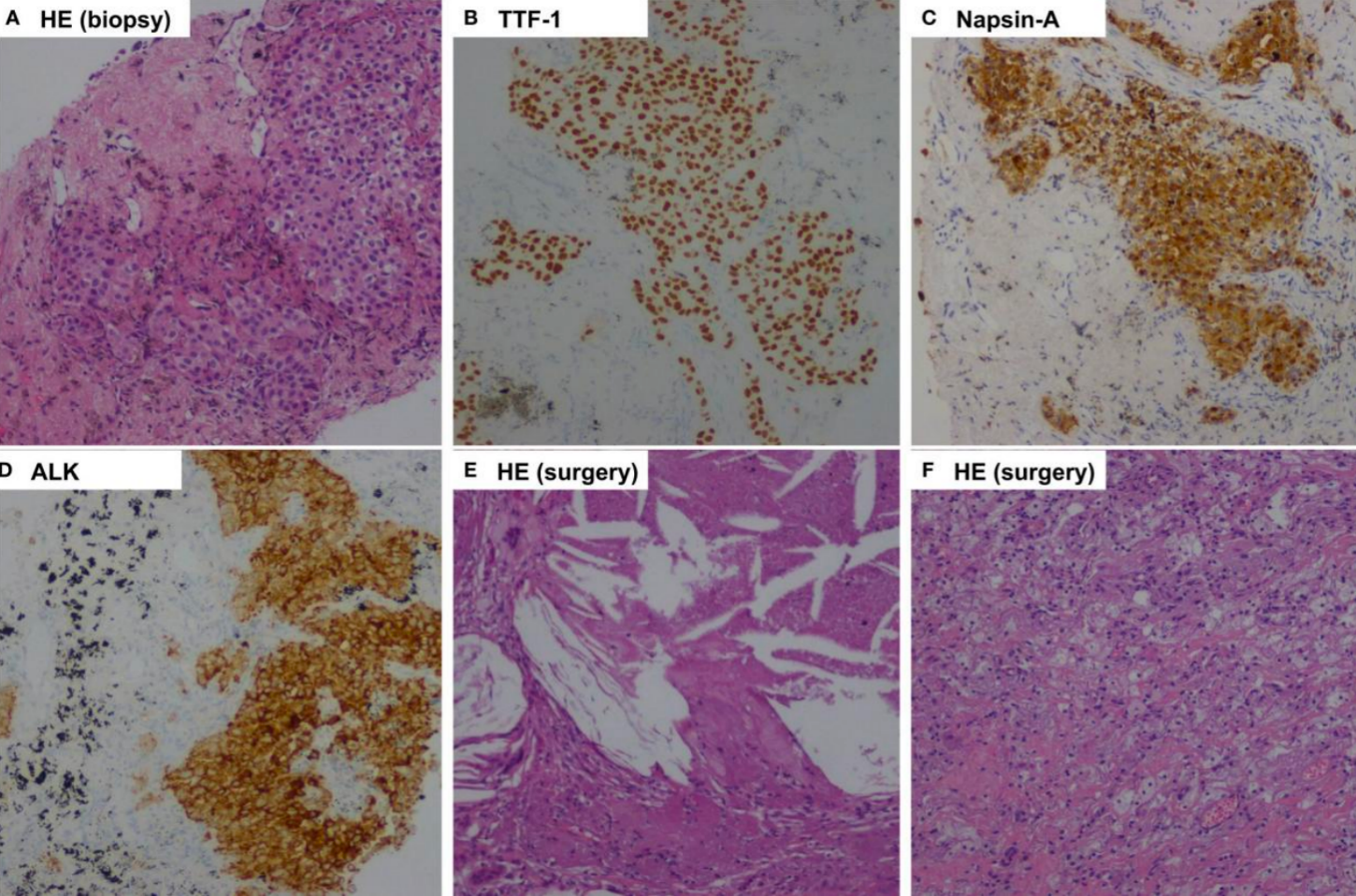 图2. 病例1的病理结果
图2. 病例1的病理结果
2021年7月15日起给予阿来替尼600 mg,每日2次,共3个周期(12周)。影像学疗效评价显示部分缓解,建议患者考虑接受手术治疗,但患者拒绝手术,继续口服阿来替尼治疗,患者肿块持续缩小。治疗30周后,进行CT扫描以评估新辅助治疗的疗效。新辅助治疗后获得部分缓解,肿块缩小66%(18 mm×15 mm),左下叶孤立性结节消失(图1)。反复系列血清CEA结果显示CEA逐渐下降。在新辅助治疗期间仅观察到1级贫血。2022年3月1日,在电视辅助胸腔镜下成功进行了左下叶肺叶切除术和全身淋巴结切除术。手术过程中,发现轻度组织粘连,未检测到明显的肺门纤维化或明显的淋巴结粘连。手术持续时间为153分钟,术中出血100 ml,未输血。术后病理显示肺组织慢性炎症、更多组织细胞浸润、多核巨细胞反应和胆固醇结晶。根据新辅助治疗后肺癌切除标本病理学评估的IASLC多学科建议,原发性肿瘤床的组成为0%存活肿瘤、10%坏死和90%间质,与pCR一致(图2)。此外,在4L、5L、7、8、10L和11L站切除的任何淋巴结(共9个淋巴结)中均未观察到转移癌。术后病理TNM分期降至ypT0N0M0。患者出院后继续接受阿来替尼治疗,13个月随访时(直至2023年4月)未报告任何特定不适。CT扫描显示,在手术后的最后一次随访中,癌症没有复发。反复检查患者的CEA水平,显示在正常范围内。
病例2
48岁男性,无吸烟史,支气管镜活检病理学提示肺腺癌,包含腺泡亚型成分。肿瘤细胞的TTF-1和Napsin-A免疫组化呈阳性(图4)。采用单克隆抗体(D5F3,Ventana-Roche Diagnostics,曼海姆,德国)进行免疫组化和采用60个基因组(Novogene Bioinformatics Technology,中国北京)进行二代测序,ALK融合状态为阳性。NGS发现了EML4-ALK融合(变体3)。没有发现远处转移。
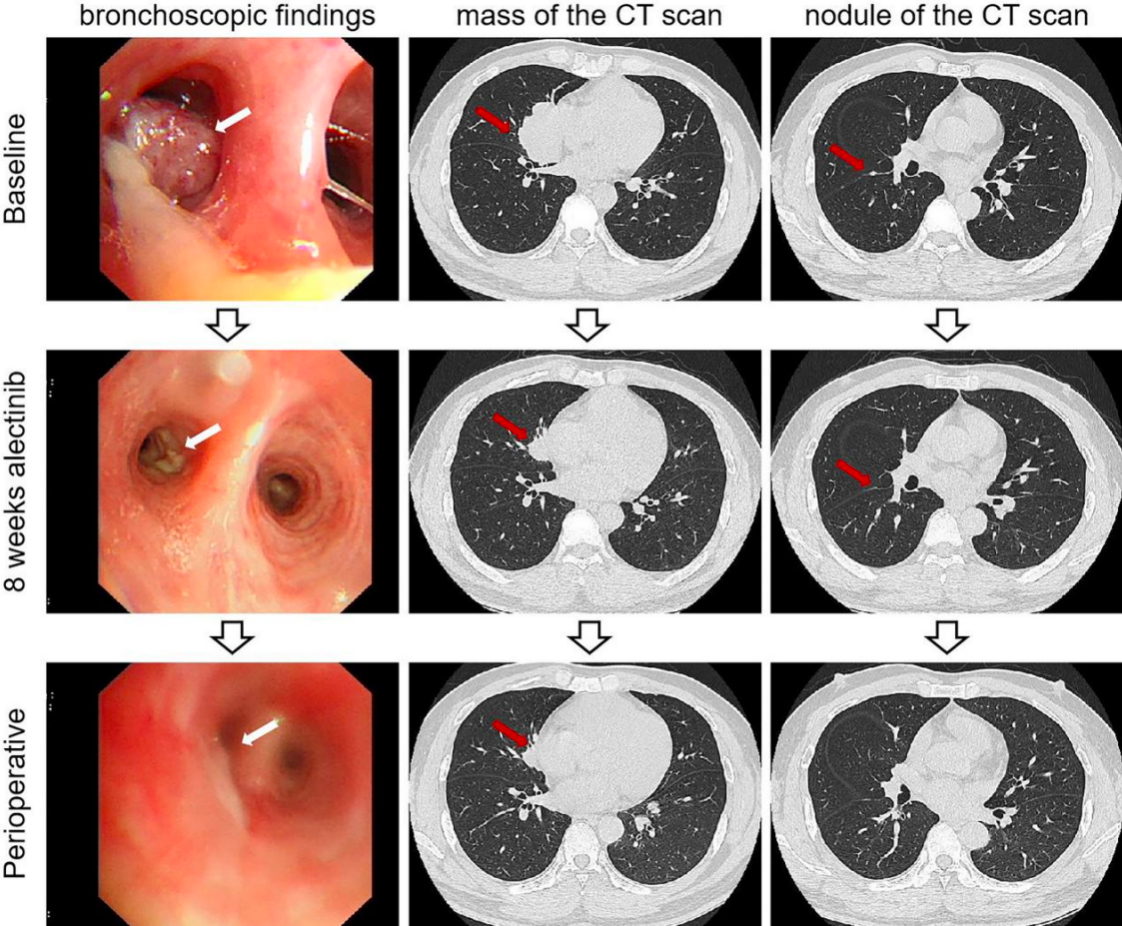 图3.病例2的影像学表现。基线和新辅助阿来替尼治疗后的支气管镜检查结果和CT
图3.病例2的影像学表现。基线和新辅助阿来替尼治疗后的支气管镜检查结果和CT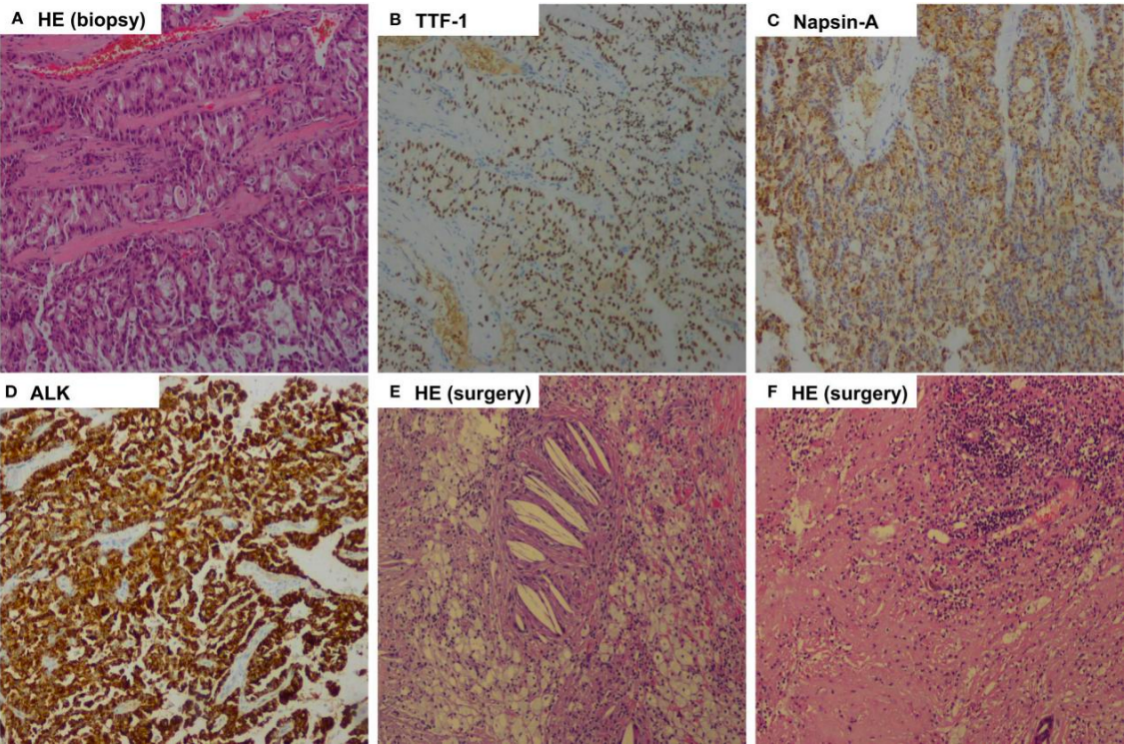 图4. 病例2的病理结果
图4. 病例2的病理结果
接受新辅助阿来替尼治疗,剂量为600 mg,每日两次。接受阿来替尼治疗8周后,根据实体瘤疗效评价标准(RECIST)第1.1版,该患者被评价为部分缓解(PR)。
阿来替尼治疗32周后,再评价显示右中叶肿瘤缩小70%,未检测到胸膜结节(图3)。此外,患者耐受性良好,仅发生1级转氨酶升高。在阿来替尼末次给药后1周,在电视辅助胸腔镜下进行了R0右中叶切除术和全身淋巴结切除术。手术期间,分离血管和支气管时发现中度组织粘连。术后病理示切除肺组织慢性炎症,纤维组织增生,多核巨细胞、淋巴细胞浸润,泡沫细胞增多,坏死,胆固醇结晶。 根据IASLC 2020方法,原发性肿瘤床的组成为0%存活肿瘤、25%坏死和75%基质。在2R、4R、7R、8R、10R、11R、12R和13R站切除的淋巴结(共18个淋巴结)中未发现转移癌。此外,右中叶右叶间胸膜切除结节的病理学提示纤维结缔组织慢性炎症。术后组织学检查显示完全病理学缓解(图4)。建议患者在术后再服用阿来替尼两年,在12个月的随访期间(直至2023年4月)未复发。
研究结果
在我们的系统综述中,有74项研究被纳入原始检索。应用筛选标准后,有18篇文章被认为符合全文阅读条件。在应用排除标准后,从6篇论文中筛选出7个病例纳入最终分析,并纳入系统综述。这些研究均未纳入定量分析。
在既往报告的7例接受新辅助阿来替尼治疗的病例中,4例为非吸烟者,3例为既往吸烟者。此外,5例患者临床分期为cIIIA期,2例临床分期为cIIIB期。关于新辅助阿来替尼治疗的持续时间,2例患者治疗6周,3例患者治疗8周,2例患者治疗12周,平均8.6周。 新辅助靶向治疗后,6例患者的最佳影像学结局为PR,1例患者达到CR。
表1. ALK阳性肺腺癌中接受新辅助阿来替尼治疗的报告病例总结
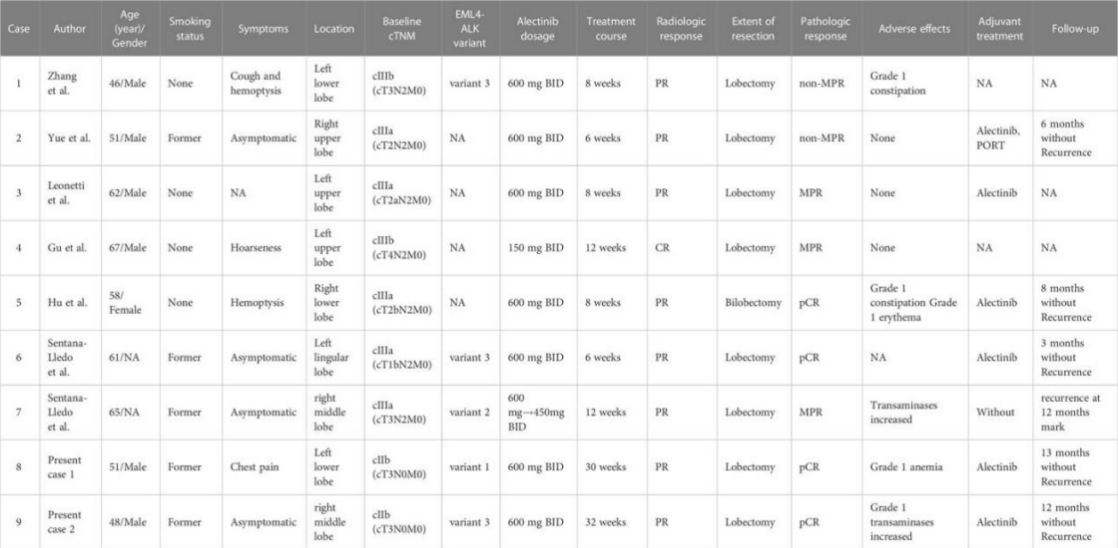
所有患者均行肺叶切除联合纵隔淋巴结清扫术,并行R0切除术。术后病理结果显示pCR 2例(28.6%),MPR 3例(42.9%),非MPR 2例(28.6%)。
研究结论
我们报告了2例ALK阳性可切除肺腺癌患者,他们通过长期新辅助阿来替尼治疗获得了pCR。我们的病例和对文献的系统性综述支持新辅助阿来替尼治疗 NSCLC的可行性。然而,未来必须开展大型临床试验,以确定新辅助阿来替尼模式的疗程和疗效。
1.Soda M, Choi YL, Enomoto M, et al. Identification of the transforming EML4-ALK fusion gene in non-small-cell lung cancer. Nature (2007) 448:561–66. doi: 10.1038/nature05945.
2. Inamura K, Takeuchi K, Togashi Y, et al. EML4-ALK fusion is linked to histological characteristics in a subset of lung cancers. J Thorac Oncol (2008) 3:13–7. doi: 10.1097/JTO.0b013e31815e8b60.
3. Paik JH, Choe G, Kim H, et al. Screening of anaplastic lymphoma kinase rearrangement by immunohistochemistry in non-small cell lung cancer: correlation with fluorescence in situ hybridization. J Thorac Oncol (2011) 6:466–72. doi: 10.1097/JTO.0b013e31820b82e8.
4. Solomon BJ, Mok T, Kim DW, et al. First-line crizotinib versus chemotherapy in ALK-positive lung cancer. N Engl J Med (2014) 371:2167–77. doi: 10.1056/NEJMoa1408440.
5. Shaw AT, Kim DW, Nakagawa K, et al. Crizotinib versus chemotherapy in advanced ALK-positive lung cancer. N Engl J Med (2013) 368:2385–94. doi: 10.1056/NEJMoa1214886.
6. Shi L, Gao S, Tong L, et al. Pathological complete response to long-course neoadjuvant alectinib in lung adenocarcinoma with EML4-ALK rearrangement: report of two cases and systematic review of case reports. Front Oncol. 2023 Jun 20;13:1120511. doi: 10.3389/fonc.2023.1120511.
7. Zhang C, Li SL, Nie Q, et al. Neoadjuvant crizotinib in resectable locally advanced non-small cell lung cancer with ALK rearrangement. J Thorac Oncol (2019) 14:726–31. doi: 10.1016/j.jtho.2018.10.161.
8. Bing Z, Jia Z, Wang Y, et al. Pathological complete response to neoadjuvant ceritinib of a crizotinib-resistant, stage IIIB non-small cell lung cancer with ALK rearrangement: a case report. Thorac Cancer (2021) 12:2130–33. doi: 10.1111/1759-7714.14045.
9. Leonetti A, Minari R, Boni L,et al. Open-label, single-arm, multicenter study to assess the activity and safety of alectinib as neoadjuvant treatment in surgically resectable stage III ALK-positive NSCLC: ALNEO trial. Clin Lung Cancer (2021) 22:473–77. doi: 10.1016/j.cllc.2021.02.014.
10. Lee JM, Sepesi B, Toloza EM, et al. EP02.04-005 phase II NAUTIKA1 study of targeted therapies in stage II-III NSCLC: preliminary data of neoadjuvant alectinib for ALK+ NSCLC. J Thorac Oncol (2022) 17:S233–34. doi: 10.1016/j.jtho.2022.07.390.
11. Zhang C, Yan L, Jiang B, et al. Feasibility and safety of neoadjuvant alectinib in a patient with ALK-positive locally advanced NSCLC. J Thorac Oncol (2020) 15:e95–99. doi: 10.1016/j.jtho.2019.12.133.
排版编辑:肿瘤资讯-olivia











 苏公网安备32059002004080号
苏公网安备32059002004080号


