PACIFIC-6研究的最终分析结果公布,为高龄、合并症较多的Ⅲ期NSCLC患者提供序贯替代方案。
2023年欧洲肿瘤内科学会(ESMO)大会将于当地时间10月20日~10月24日在西班牙马德里盛大召开。ESMO大会涵盖基础研究、转化研究以及最新临床研究进展,将为临床实践交流、多学科讨论等提供广阔、卓越的学术平台。继PACIFIC研究开启Ⅲ期NSCLC免疫治疗时代以来,更多研究如PACIFIC-2、PACIFIC-6等研究仍在探索更多治疗可能。本次ESMO大会公布了PACIFIC-6研究的最终分析结果[1],进一步证实了Ⅲ期肺癌患者,在同步放化疗不可耐受的情况下,接受序贯放化疗后度伐利尤单抗巩固治疗的可行性。【肿瘤资讯】诚邀河南省肿瘤医院葛红教授剖析该最终分析结果及其对于临床实践的意义。
博士,二级教授/主任医师 ,博士生导师 中原名医
第八届国家卫建委突出贡献中青年专家
享受国务院政府津贴专家
河南省肿瘤医院放疗科主任&河南省放射治疗中心主任
河南省肿瘤医院放射治疗科住规培基地主任
中国医师协会放射肿瘤委员会副会长
中国医师协会多学科诊疗专委会常委
河南省肿瘤诊疗质控中心放疗专家委员会主任委员
河南省医学会放疗分会候任主任委员
中华医学会放射治疗学分会委员
中华放射肿瘤学杂志编委
中国抗癌协会多学科诊疗专委会常委
中国抗癌协会放射防护专委会常委
中国抗癌协会放疗专业委员会委员
国家肿瘤质控中心肺癌质控专家委员会委
中国北方放疗协作组副组长
研究背景
在所有肺癌患者中,非小细胞肺癌(NSCLC)占80%~85%,其中约30%的NSCLC患者在就诊时已达到Ⅲ期,且大部分失去了手术切除的机会[2]。Ⅲ期NSCLC具有高度临床和病理异质性,这决定了其治疗的复杂性。在预后方面,Ⅲ期NSCLC患者的生存预后不佳,ⅢA期、ⅢB期和ⅢC期NSCLC的5年生存率分别为36%、26%和13%[3]。
回顾Ⅲ期NSCLC标准治疗模式的转变历程,首先为1980年代的单纯放疗,1980年RTOG 7301研究[4]结果发布,确定了Ⅲ期NSCLC的最佳放疗剂量。随后,CALGB 8433研究[5]通过比较序贯放化疗与单纯放疗,确立了联合放化疗在Ⅲ期NSCLC治疗中的作用。放疗和化疗的联用模式有两种,分别为序贯放化疗和同步放化疗。20世纪末RTOG 9410研究[6]证实同步放化疗由于更好的局部控制效果,与序贯放化疗相比,改善患者总生存期(OS)更多,同步放化疗成为不可切除Ⅲ期NSCLC主要治疗手段。
为进一步提高不可切除Ⅲ期NSCLC患者的临床获益,人们基于同步放化疗进行了一系列尝试,直到2017年PACIFIC研究公布结果[7],不可切除Ⅲ期NSCLC治疗迎来了革命性的突破。PACIFIC研究率先成功探索了同步放化疗+免疫治疗在不可切除Ⅲ期NSCLC的临床价值,首次证实了同步放化疗后加入免疫巩固治疗可显著提高不可切除Ⅲ期NSCLC患者的生存获益。基于PACIFIC研究结果,对于PS评分为0~1分的不可切除Ⅲ期NSCLC,2023年V3版美国国家综合癌症网络(NCCN)NSCLC指南、2023版中国临床肿瘤学会(CSCO)NSCLC诊疗指南、中华医学会肺癌临床诊疗指南(2022版)等国内外肺癌领域权威指南一致最高级别推荐,同步放化疗后度伐利尤单抗免疫巩固治疗作为标准疗法[8-10]。
然而,并非所有患者都符合同步放化疗的条件,尤其是年龄较大、PS评分较差、合并症较多的患者,这类患者的功能状态可能无法耐受同步放化疗,这一问题成为临床关注的焦点。2022年,《J Thorac Oncol》杂志公布的PACIFIC-6研究[11]评估了不耐受同步放化疗的患者,接受序贯放化疗后度伐利尤单抗巩固治疗的安全性和耐受性。在进一步随访后,本次ESMO公布了PACIFIC-6研究的最终分析结果。
研究结果
PACIFIC-6研究[1]纳入体力状况(PS)评分≤2、序贯放化疗后无进展的不可切除III期NSCLC患者,接受度伐利尤单抗巩固治疗,度伐利尤单抗的剂量为1500mg,每4周一次,治疗时间为24个月,或直至疾病进展、或出现不可耐受的不良反应。主要研究终点为6个月内出现的3/4级治疗相关不良反应(PRAEs),次要研究终点包括研究者评估的无进展生存期(PFS)和总生存期(OS)。
截至2023年3月20日,共117例患者入组试验。59.8%的患者PS评分为1/2,65.8%的患者年龄≥65岁,63.2%的患者为ⅢB/ⅢC期。几乎所有患者在过去或现在存在合并症(98.3%),主要为血管(59.0%)、呼吸(53.0%)和代谢(51.3%)疾病。
在生存疗效方面,中位治疗持续时间为41.0周。中位随访时间为32.6个月,中位PFS为13.1个月,中位OS为39.0个月,3年OS率为56.5%。
在安全性方面,4.3%的患者在6个月内出现3/4级PRAEs,6.0%的患者在整个研究期间出现3/4级PRAEs。整体安全性可控,与其他研究不良反应表现一致。
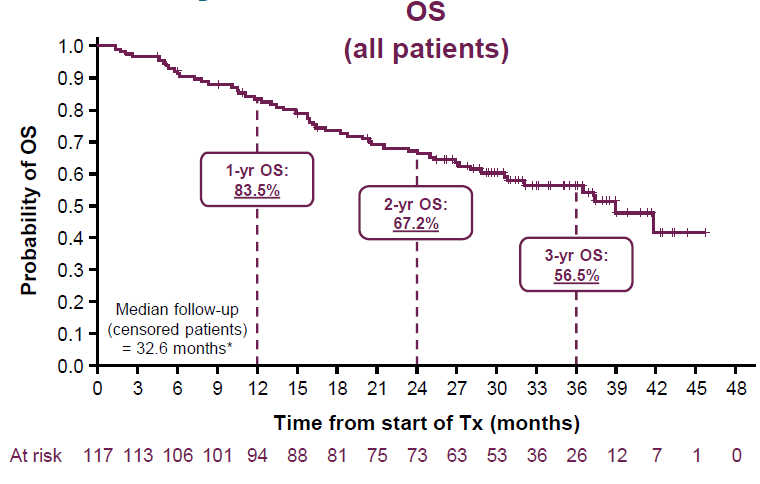
图 中位随访时间32.6个月时,PACIFIC-6研究OS生存曲线
研究结论
PACIFIC-6研究结果显示,针对高龄、合并症较多的不耐受同步放化疗的III期NSCLC 患者,接受序贯放化疗后度伐利尤单抗巩固治疗,仍显示出令人鼓舞的疗效获益,并且与PACIFIC研究中同步放化疗后度伐利尤单抗巩固治疗方案具有相当的安全性。本研究结果表明,对于被认为不适合进行同步放化疗的患者,序贯放化疗后度伐利尤单抗巩固治疗可能成为替代治疗策略。
2017年PACIFIC研究以“海啸”之势席卷而来,掀开了不可切除III期NSCLC免疫治疗的新时代。随访5年的更新数据[12]显示,同步放化疗后度伐利尤单抗免疫巩固治疗的生存获益显著,5年PFS率和5年OS率分别为33.1%和42.9%,近一半患者实现5年“临床治愈”,“PACIFIC模式”为更多不可切除III期NSCLC患者带来了临床治愈的希望。但在临床实践中,部分不可切除III期NSCLC患者因年老、虚弱、合并症等原因无法耐受同步放化疗,而PACIFIC-6研究采用序贯放化疗后度伐利尤单抗巩固治疗,为这一部分患者提供替代方案。PACIFIC-6研究[11]是一项国际多中心、开放标签、单臂、II期临床研究,相较于PACIFIC研究,PACIFIC-6研究入组人群相对体弱,PS评分1/2、年龄≥65岁以及IIIB/IIIC期的患者比例更高,但依然显示出与PACIFIC相当的安全性,以及良好的初步抗肿瘤活性,为该治疗模式的临床应用带来了令人振奋的数据。
其实PACIFIC-6研究中令人鼓舞的结果与早前PACIFIC-R研究中的结果相互映证。PACIFIC-R研究是一项全球多中心大型真实世界研究,评估了放化疗(同步/序贯)后度伐利尤单抗巩固治疗方案在真实世界的疗效与安全性。PACIFIC-R研究对象是2017年9月至2018年12月期间EAP中接受度伐利尤单抗治疗的不可切除Ⅲ期NSCLC患者,主要终点是研究者评估的真实世界无进展生存期(rwPFS)和总生存期(rwOS),截至2021年11月30日,分析集共纳入来自10个国家的1154名患者。总体而言,2年和3年OS率分别为72.3%和63.2%;更新的中位rwPFS为24.1个月,2年和3年rwPFS率分别为50.1%和42.2%。
就不同放化疗模式而言,虽然同步放化疗亚组的OS率和PFS率在数值上更高,但序贯放化疗亚组也观察到良好的生存获益。序贯放化疗亚组患者的2年和3年OS率分别为67.8%和57.9%,2年和3年rwPFS率分别为48.8%和38.9%,中位PFS为23.2个月。
结合PACIFIC-6研究和PACIFIC-R研究序贯放化疗亚组数据可见,无论是临床试验中还是真实世界中,序贯放化疗后度伐利尤单抗巩固治疗具有令人鼓舞的疗效和可控的安全性。对于不适合同步放化疗的不可切除III期NSCLC患者,序贯放化疗后度伐利尤单抗免疫巩固治疗有望成为替代治疗策略,为患者带来更好的生存获益。因此,III期患者异质性较大,但仍有治愈机会,在临床实践中,临床医生应根据患者的具体情况,为其选择合适的放化疗顺序和免疫巩固治疗方案,以确保患者最大程度获益。
[1] Garassino MC, Mazieres J, Reck M, et al. Durvalumab (durva) after sequential chemoradiotherapy(CRT) in patients (pts) with unresectable stage III NSCLC: Final analysis from PACIFIC-6. 2023 ESMO LBA61.
[2] 中国抗癌协会肺癌专业委员会, 中华医学会肿瘤学分会肺癌学组. Ⅲ期非小细胞肺癌多学科诊疗专家共识( 2019版)[J]. 中华肿瘤杂志, 2019, 41(12):10.
[3] Goldstraw P, Chansky K, Crowley J, et al. The IASLC Lung Cancer Staging Project: Proposals for Revision of the TNM Stage Groupings in the Forthcoming (Eighth) Edition of the TNM Classification for Lung Cancer[J]. J Thorac Oncol. 2016;11(1):39-51.
[4] Patel M, Bruno D, Grubb W, et al. The changing landscape of stage III lung cancer: a literature review. Expert Rev Anticancer Ther. 2020 Aug;20(8):675-686.
[5] Dillman RO, Herndon J, Seagren SL, et al. Improved survival in stage III non-small-cell lung cancer: seven-year follow-up of cancer and leukemia group B (CALGB) 8433 trial. J Natl Cancer Inst. 1996 Sep 4;88(17):1210-5.
[6] Curran WJ Jr, Paulus R, Langer CJ, et al. Sequential vs. concurrent chemoradiation for stage III non-small cell lung cancer: randomized phase III trial RTOG 9410. J Natl Cancer Inst. 2011 Oct 5;103(19):1452-60. Erratum in: J Natl Cancer Inst. 2012 Jan 4;104(1):79.
[7] Antonia SJ, Villegas A, Daniel D, et al. Durvalumab after Chemoradiotherapy in Stage III Non-Small-Cell Lung Cancer[J]. N Engl J Med. 2017 Nov 16;377(20):1919-1929.
[8] 中华医学会肿瘤学分会, 中华医学会杂志社. 中华医学会肺癌临床诊疗指南(2022版)[J]. 中华医学杂志, 2022, 102(23):35.
[9] 中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南(2023).
[10] NCCN Clinical Practice Guidelines in Oncology: Non-Small Cell Lung Cancer. Version 3. 2023.
[11] Garassino MC, Mazieres J, Reck M, et al. Durvalumab After Sequential Chemoradiotherapy in Stage III, Unresectable NSCLC: The Phase 2 PACIFIC-6 Trial. J Thorac Oncol. 2022;17(12):1415-1427.
[12] Spigel DR, Faivre-Finn C, Gray JE, et al. Five-Year Survival Outcomes From the PACIFIC Trial: Durvalumab After Chemoradiotherapy in Stage III Non-Small-Cell Lung Cancer. J Clin Oncol. 2022 Apr 20;40(12):1301-1311.
排版编辑:Alin











 苏公网安备 32059002004080号
苏公网安备 32059002004080号


