2023年欧洲肿瘤内科学会(ESMO)年会于10月20日-24日在西班牙马德里隆重召开,新一代ROS1/NTRK抑制剂瑞普替尼(Repotrectinib)在此次大会报道了TRIDENT-1研究的最新数据,为NTRK融合阳性晚期实体瘤这一罕见靶点领域带来了全新选择。本期特邀湖南省肿瘤医院的杨农教授、张永昌教授解读并点评瑞普替尼TRIDENT-1研究的最新数据。
中南大学湘雅医学院附属肿瘤医院/湖南省肿瘤医院
肺胃肠肿瘤内科主任,主任医师,博导
第六届 国之名医·优秀风范
国家科技重大专项首席专家
国家肿瘤质控中心肺癌质控专委会委员
湖南省呼吸肿瘤临床医学研究中心主任
肺癌精准诊疗湖南省重点实验室主任
湖南省卫生健康高层次人才
中国医药教育协会肿瘤免疫治疗专委会副主任委员
中国医药教育协会肿瘤临床科研创新发展专委会副主任委员
中国医药教育协会肺部肿瘤专委会常委
中国临床肿瘤学会理事及肿瘤免疫治疗专委会、非小细胞肺癌专委会、药物研发专委会委员
中国抗癌协会青委会、抗肿瘤药物专委会常委、肺癌专委会委员
中国医师协会结直肠肿瘤专委会委员
中国老年医学会肿瘤学分会委员
CTONG主要研究者
湖南省抗癌协会肿瘤精准医学专委会主任委员、化疗专委会候任主委
湖南省老年医学学会临床肿瘤学分会主任委员
肺胃肠内科/ECTC 副主任
国家优青
湖南省科技创新领军人才、中华医学会青年科技奖
十一届湖南省青年科学家奖、湖南省青年五四奖章
省委组织部“湖湘青年英才”、长沙市十大杰出青年
湖南省人才托举工程“年轻优秀科技人才”
中国抗癌协会肿瘤呼吸病学专委会委员
中国抗癌协会肿瘤精准治疗专委会委员
湖南省抗癌协会肿瘤精准医学专业委员会青委会主委
湖南省医学会肿瘤内科专业委员会青委会副主委
围绕肺癌靶向及免疫耐药的临床与转化医学研究,在J Thorac Oncol. J Natl Cancer Inst. Innovation, Oncogene, Eur J Cancer, JAMA Network Open, BMC Med. NPJ Precis Oncol. J Clin Oncol, Lancet Oncol发表多篇学术成果。
张永昌教授:
靶向治疗时代,NTRK融合阳性实体瘤仍需新药满足临床需求
神经营养因子受体酪氨酸激酶(neurotrophic tyrosine receptor kinase, NTRK)基因包括NTRK1、NTRK2和NTRK3,分别编码TRKA、TRKB和TRKC蛋白。NTRK融合(以下简写为NTRK+)是多种实体瘤的已知驱动因素,在罕见癌症中发生率较高,在常见癌症中发生率普遍较低,其在肺癌的发生率不到1%。尽管如此,结合肺癌的高发病例数,NTRK+肺癌仍是一个庞大的人群,这些患者的治疗需求值得高度重视。既往NTRK+肺癌患者参考驱动基因阴性治疗方案进行治疗,预后不佳。恩曲替尼、拉罗替尼率先发力,在NTRK+实体瘤患者中展现了良好的临床疗效,ORR约62%-66%,mPFS 约15.7-30.8个月,基于这些数据,NTRK+肺癌患者也终于迎来靶向治疗时代。
然而,由于受到获得性耐药突变的限制,部分患者接受恩曲替尼或拉罗替尼后肿瘤缓解无法持续,最终出现疾病进展。获得性耐药突变是TRK-TKI耐药的主要因素之一,包括TRKAG595R、TRKBG639R等溶剂前沿突变,TRKAF589L、TRKBF623L等守门员突变以及xDFG突变等。对于TRK-TKI经治的患者,因其主要涉及on-target耐药机制,在治疗选择上我们仍将希望寄托于靶向NTRK的治疗,但目前尚且面临空白。新一代NTRK抑制剂是否有望填补这一治疗领域的空白?让我们来看瑞普替尼TRIDENT-1研究在2023年ESMO报道的最新数据:
瑞普替尼初治数据稳健,另辟蹊径克服耐药
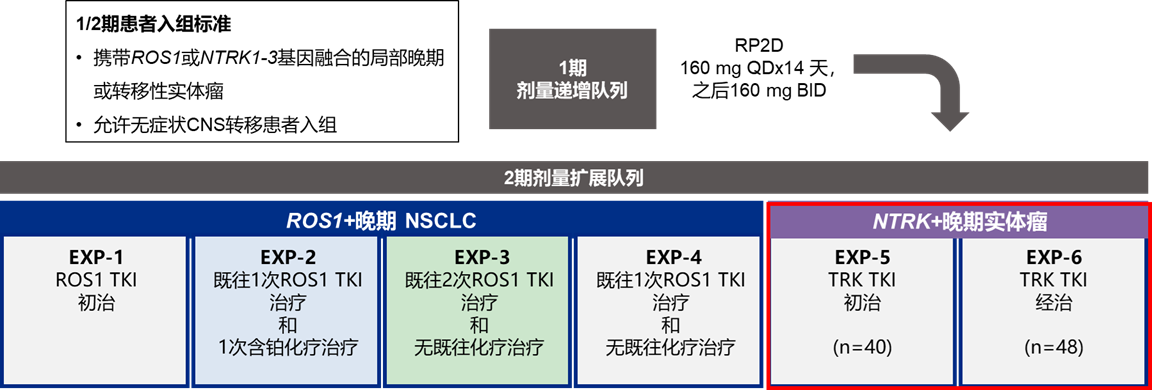 图1.TRIDENT-1试验设计总览
图1.TRIDENT-1试验设计总览
TRIDENT-1研究中,TRK-TKI初治和经治队列分别纳入了40例和48例患者,基线资料如表1所示。值得留意的是,TRK-TKI经治队列有50%患者既往接受过恩曲替尼治疗,52%的患者检测到溶剂前沿突变。
表1.人口统计学特征和基线资料
TRK-TKI初治队列包含11种肿瘤类型,其中NSCLC是最常见的类型,占52%,其次为甲状腺癌(12%),唾液腺癌(8%)和软组织肉瘤(8%);TRK-TKI经治队列包含13种肿瘤类型,NSCLC占29%,其次为甲状腺癌(17%)和软组织肉瘤(12%)。
有效性-TRK TKI初治队列
TRK-TKI初治队列中位随访时间为17.8个月,cORR为58% (95% CI, 41‑73)(图2)。虽然中位无进展生存期尚未达到,但从客观缓解率这一指标上来看,瑞普替尼与恩曲替尼、拉罗替尼在初治人群中的疗效是可比较的。
 图2. TRK-TKI初治队列肿瘤负荷变化(A)、缓解持续时间(B)和无进展生存曲线(C)
图2. TRK-TKI初治队列肿瘤负荷变化(A)、缓解持续时间(B)和无进展生存曲线(C)
有效性-TRK TKI经治队列
TRK-TKI经治队列中位随访时间为20.1个月,cORR为50% (95% CI, 35‑65),12个月DOR率为39%,12个月PFS率为22%(图3)。
 图3. TRK-TKI经治队列肿瘤负荷变化(A)、缓解持续时间(B)和无进展生存曲线(C)
图3. TRK-TKI经治队列肿瘤负荷变化(A)、缓解持续时间(B)和无进展生存曲线(C)
尤其值得注意的是,对于其中TRK-TKI治疗后伴有溶剂前沿突变的25例患者,cORR为60%(95% CI,39-79),12个月DOR率为33%,12个月PFS率为21%(图4),这是瑞普替尼对溶剂前沿耐药突变患者具有抗肿瘤活性在临床研究中取得的再次验证。在临床前研究中,瑞普替尼显示出了相比现有TRK抑制剂更强的细胞毒性,对TRK非耐药突变和TRK守门员突变的IC50值均<0.2,对TRKA-C溶剂前沿突变的IC50均值在0.2-2.6范围内(表2)。临床前和临床研究结果相互印证,共同说明了瑞普替尼对溶剂前沿耐药突变的疗效,而这与瑞普替尼具有紧凑三维大环结构,分子量小(MW=355.37)的药物设计不无关系。这些特性使其不受耐药突变空间结构冲突的影响,能够顺利进入ATP结合口袋从而发挥疗效(图5)。
 图4. TRK-TKI经治队列伴溶剂前沿突变的肿瘤负荷变化(A)、缓解持续时间(B)和无进展生存曲线(C)
图4. TRK-TKI经治队列伴溶剂前沿突变的肿瘤负荷变化(A)、缓解持续时间(B)和无进展生存曲线(C)
 图5. 瑞普替尼在ATP口袋中的示意图
图5. 瑞普替尼在ATP口袋中的示意图
表2. TRK-TKI抑制TRK融合Ba/F3细胞增殖的IC50
此外,TRIDENT-1研究中5例(初治队列2例,经治队列3例)基线伴有脑转移患者的icORR为100%,均为PR,初步验证了瑞普替尼良好的入脑能力。
有效性-NSCLC队列
在TKI初治的NTRK+NSCLC中,cORR为62%;在TKI经治的NTRK+NSCLC中,cORR为43%,这些数据表明瑞普替尼在NTRK+NSCLC患者中的疗效与整体队列基本一致(表3)。
表3. NTRK+NSCLC队列有效性数据
瑞普替尼安全性良好
接受RP2D治疗的NTRK+实体瘤患者(n=104)与所有接受RP2D治疗的患者(包括ROS1+队列和NTRK+队列,n=426)安全性结果相似,最常见的TEAE是头晕,在接受RP2D治疗的所有患者中发生率为62%,绝大多数为低级别,仅3%的患者≥3级,并且没有因头晕导致的停药。导致剂量调整和治疗中断的研究期间发生的不良事件(TEAEs)和治疗相关不良事件(TRAEs)见表4。
表4. 接受RP2D治疗的患者安全性数据
总之,瑞普替尼在TRIDENT-1研究中针对NTRK+局部晚期/转移性实体瘤(包括NSCLC)展现出了可持续的临床活性,对于无论是TRK-TKI初治还是经治的患者,cORR达50-58%,中位生存期仍在长期随访中,尤其对于既往无计可施的TRK-TKI耐药患者亦能实现60%的ORR,且安全性可控,与之前所报道的基本一致。基于TRIDENT-1研究结果,FDA对瑞普替尼治疗既往接受过一或二个前线TRK-TKI治疗的NTRK+晚期实体瘤授予了突破性疗法认定(Breakthrough Therapy Designation,BTD),认可瑞普替尼填补了NTRK+患者耐药后治疗领域的空白。
杨农教授点评:
瑞普替尼具有紧凑大环结构,为ROS1和NTRK阳性NSCLC带来卓越疗效
区别于传统ROS1/TRK抑制剂的链式分子结构,瑞普替尼作为新一代ROS1/TRK抑制剂,具有紧凑三维大环结构,分子量小(MW=355.37),不与溶剂前沿突变或守门员突变产生空间结构冲突,能够顺利且精准铆合在ATP结合口袋从而发挥疗效,对ROS1/TRK融合均具有抗肿瘤活性。实际上,TRIDENT-1(1/2期)研究2期扩展队列除了此次2023年ESMO报道的NTRK+队列的结果之外,在一个月前的世界肺癌大会(WCLC)上也报道了瑞普替尼在既往未接受过ROS1-TKI治疗的EXP-1队列的疗效和安全性数据:经过2年的中位随访时间,ROS1-TKI初治患者(n=71)ORR为79%;mDOR达34.1个月; mPFS长达35.7个月;mOS尚未达到。(图6)
 图6. 瑞普替尼对ROS-TKI初治ROS1+NSCLC患者的疗效
图6. 瑞普替尼对ROS-TKI初治ROS1+NSCLC患者的疗效
对瑞普替尼治疗后进展的14例患者进一步分析提示,这些患者均未出现G2032R等ROS1-TKI耐药突变,而耐药突变正是限制以克唑替尼为代表的传统ROS1-TKI疗效的关键因素,延缓ROS1耐药突变的出现是瑞普替尼带来长PFS获益的机制之一。
兼顾系统性和颅内疗效,瑞普替尼成为ROS1/NTRK+新选择
此外,基线伴有脑转移的ROS1-TKI初治患者颅内ORR 89%,基线无脑转移的ROS1-TKI初治患者12个月颅内PFS率为91%(图7)。在NTRK+队列也观察到了相似的瑞普替尼颅内活性,5例基线伴有脑转移的NTRK+实体瘤患者均实现了PR,icORR为100%。这些数据证明瑞普替尼具有强大的CNS活性,为预后不良的脑转移患者提供了新的治疗机会。
 图7. 瑞普替尼在初治ROS1+NSCLC人群中的颅内疗效
图7. 瑞普替尼在初治ROS1+NSCLC人群中的颅内疗效
对于ROS1+晚期NSCLC,目前的标准治疗方案下,一线使用克唑替尼和恩曲替尼的中位PFS在15.9-19.3个月范围内,二线化疗中位PFS为3.6-5个月左右,而瑞普替尼治疗ROS1-TKI初治患者的中位PFS长达35.7个月,FDA和国家药监局药品审评中心(CDE)因而都对瑞普替尼用于治疗未接受过ROS1-TKI治疗的ROS1阳性转移性非小细胞肺癌患者授予了突破性治疗认定。优化ROS1+治疗策略,将瑞普替尼作为一线治疗的优先选择,有望更好地实现ROS1+NSCLC患者的长期生存。
而对于NTRK+晚期NSCLC,正如张永昌教授所言,靶向治疗已然成为一线首选治疗方案,但耐药后的靶向治疗选择仍十分有限。瑞普替尼在溶剂前沿耐药突变患者中显示出了良好的抗肿瘤活性,cORR达60%,填补了NTRK+患者耐药后治疗领域的空白,为NTRK+靶向治疗续航。
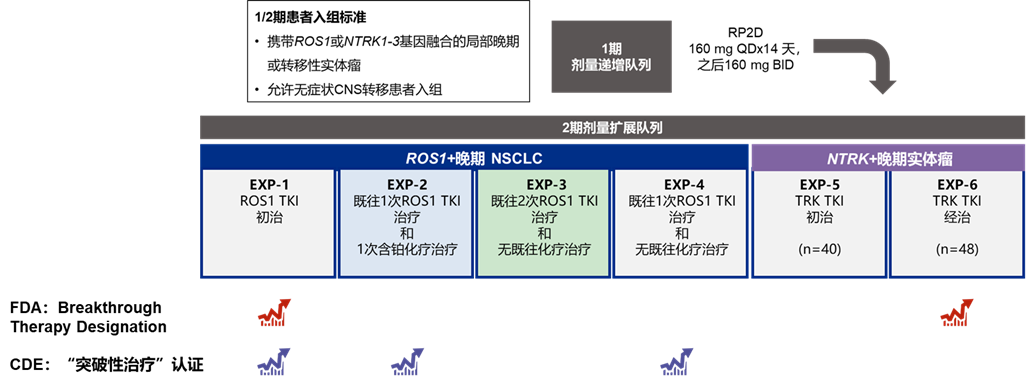 图8. 瑞普替尼获FDA/CDE认定情况概览
图8. 瑞普替尼获FDA/CDE认定情况概览
优化检测,让更多ROS1/NTRK+患者获得长生存机会
综上可见,ROS1+ NSCLC以及NTRK+实体瘤领域迎来了瑞普替尼这一新的有力武器。如何识别和筛选最佳获益人群对指导临床用药、延长驱动基因阳性患者生存期有重要意义。然而,融合突变的检测复杂程度高,尤其NTRK涉及NTRK1-3三种基因及多种潜在融合伴侣,目前尚缺乏精准的检测方法,可能存在ROS1+/NTRK+患者因漏检、误检而错失从靶向治疗中获益的机会。未来,如何优化融合突变的检测策略,提高ROS1/NTRK融合检出率,使这些驱动基因阳性的患者及时进入有效的靶向治疗,是值得进一步探索的问题。
总之,瑞普替尼作为新一代ROS1/NTRK抑制剂,为ROS1+ NSCLC患者以及NTRK+实体瘤患者带来了新的希望。2023年6月,瑞普替尼用于ROS1+局部晚期或转移性NSCLC新药上市申请已获得CDE受理且纳入优先审评,让我们共同期待其早日上市,惠及更多中国患者。
1. Benjamin Solomon, et al. 2023 ESMO Poster 1372P.
2. Cocco E, et al. Nat Rev Clin Oncol 2018;15:731‑747.
3. Amatu A, et al. Ann Oncol 2019;30:viii5‑viii15.
4. National Comprehensive Cancer Network Clinical Practice Guidelines in Oncology (NCCN Guidelines®) for Non‑Small Cell Lung Cancer. V.3.2023. https:/ /www.nccn.org/professionals/physician_gls/pdf/nscl. pdf. Accessed July 24, 2023.
5. Drilon A, et al. New Engl J Med 2018;378:731‑739.
6. Doebele RC, et al. Lancet Oncol 2020;21:271‑282.
7. Drilon A, et al. Cancer Discov 2018;8:1227‑1236.
8. Besse B, et al. Poster presentation at the EORTC‑NCI‑AACR (ENA) Symposium; October 26‑28, 2022; Barcelona, Spain. Abstract 209
9.Shaw AT et al., Ann. Oncol. 2019, 30, 1121–1126.
10. Wu YL et al., J Clin Oncol 2018;36:1405-11.
11. Zhang L, et al. Oncotarget. 2016 Nov 15;7(46):75145-75154.
12. DOEBELE RC,DRILON A, PAZ-ARES L, et al. Entrectinib in patients with advanced or metastatic NTRK fusion-positive solid tumours: integrated analysis of three phase 1-2 trials. Lancet Oncol, 2020, 21 (2): 271-282.
13. DRILON A, L AETSCH TW, KUMMAR S, et al. Efficacy of Larotrectinib in TRK Fusion–Positive Cancers in Adults and Children. N Engl J Med,2018,378 (8): 731-739.
14. S. Lu, et al. 2023 ESMO Poster 666P
15. DRILON A, et al. 2023 ESMO Poster 668P
*仅供医疗卫生专业人士学术参考之用
ZMCNNP20231025002 Expire Date 2024/10/25
排版编辑:肿瘤资讯-CYX











 苏公网安备32059002004080号
苏公网安备32059002004080号


