2023年7月23日,由君实生物主办的“THE NEW TORCH中外对话第二期NSCLC围术期免疫治疗新纪元”线上论坛成功举办。Neotorch研究是全球首个PD-1单抗用于非小细胞肺癌(NSCLC)围术期治疗达到无事件生存期(EFS)阳性结果的Ⅲ期研究,开创了“3+1+13”的围术期免疫治疗新模式,具有里程碑式的重大意义。本期会议聚焦Neotorch研究数据展开深度解析,北京大学人民医院杨帆教授担任主席,肺癌领域多位知名内外科专家共同参与,并特别邀请到了英国皇家布朗普顿医院Eric Kian Saik Lim教授出席,中外专家云端相聚,共话NSCLC围术期免疫治疗最新进展,共议临床实践新探索新挑战。本文整理会议精要如下,与读者共享前沿。
“拓”领域新章,“启”新生希望
“Neotorch”不负使命

会议伊始,大会主席杨帆教授介绍了Eric Lim教授等与会特邀嘉宾并作开场致辞,杨帆教授指出,新辅助免疫治疗已经成为驱动基因阴性非小细胞肺癌患者标准治疗模式,虽然对于具体的患者筛选、治疗周期、术后是否需要辅助治疗等问题仍存在争议。今年ASCO大会上 Neotorch研究 以“新辅助+手术+辅助”夹心饼的围术期免疫治疗模式报告了不俗成绩,毫无疑问围术期免疫治疗已逐渐成为最新趋势。本次会议邀请Eric Lim教授与多位国内专家聚焦围术期免疫治疗进行深度研讨,期待在学术交流中共同加深友情。

Eric教授在致辞中首先进行了自我介绍,回顾了过往在肺癌领域及间皮瘤中的研究历程,并表示很荣幸参与此次围术期免疫治疗的中外对话,特瑞普利单抗在Neotorch研究中取得了令人惊艳的成绩,期待与中国专家们围绕肺癌围术期免疫治疗进行更深入的学术交流。
主题报告:开创新模式,引领新标准
 本篇章由上海交通大学医学院附属胸科医院储天晴教授主持
本篇章由上海交通大学医学院附属胸科医院储天晴教授主持

辽宁省肿瘤医院孙楠教授深度解析了Neotorch研究数据。匠心独运的研究设计(图1)奠定了Neotorch研究卓越的临床指导价值。Neotorch研究首创的“3+1+13”围术期治疗模式(特瑞普利单抗联合化疗新辅助治疗3周期+特瑞普利单抗联合化疗辅助治疗1周期+特瑞普利单抗巩固治疗13周期),巧妙地将免疫治疗贯穿全程管理,不仅优于Keynote-671研究中4周期新辅助治疗的耐受性和完成率,也拥有优于Checkmate-816模式3周期新辅助治疗的标准化疗强度,带来了更大的临床获益。从基线特征可以看到,从组织学类型到疾病分期,都高度符合中国临床实践,具有很好的真实世界代表性。
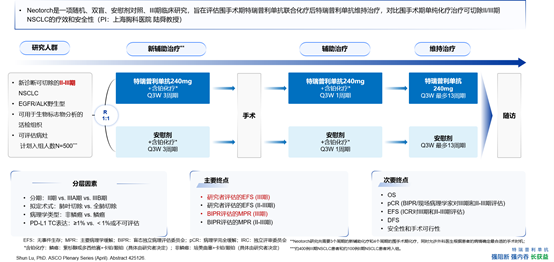 图1 Neotorch研究设计方案
图1 Neotorch研究设计方案
手术结局方面,与单独化疗组相比,特瑞普利单抗联合化疗组有更多患者接受了手术、达到了R0切除,潜在增加了生存获益机会,且未增加全肺切除风险,保障了患者生活质量。
研究者评估的ITT人群EFS数据显示,特瑞普利单抗联合化疗围术期治疗显著延长了中位EFS[尚未成熟(NE)vs15.1个月,风险比(HR)=0.40,P<0.0001],疾病复发、进展或死亡风险降低高达60%,疗效惊艳。亚组分析显示,无论患者PD-L1表达水平、无论鳞癌或非鳞癌,特瑞普利单抗联合化疗组EFS均获益。同时,特瑞普利单抗联合化疗组的主要病理学缓解(MPR)率和病理学完全缓解(pCR)率均大幅提升(48.5% vs 8.4%, 24.8% vs1.0%,P<0.0001),且MPR和pCR均与更好的EFS相关(图3、图4),总生存期(OS)也显示出明显的获益趋势。
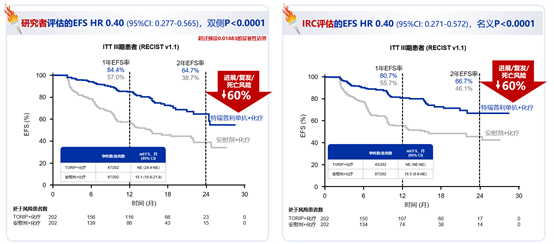 图2 Neotorch研究中Ⅲ期患者EFS结果
图2 Neotorch研究中Ⅲ期患者EFS结果
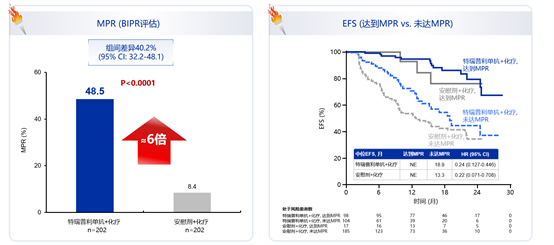 图3 Neotorch研究中Ⅲ期患者的MPR结果
图3 Neotorch研究中Ⅲ期患者的MPR结果
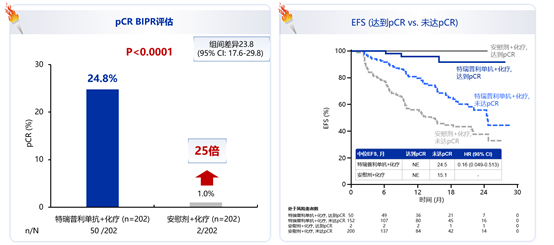 图4 Neotorch研究中Ⅲ期患者的pCR结果
图4 Neotorch研究中Ⅲ期患者的pCR结果
安全性方面,特瑞普利单抗联合化疗不仅未影响手术安全性,且总体安全可控、耐受性良好,无新的安全信号。可以预见,Neotorch研究结果将进一步改变Ⅲ期NSCLC围术期治疗标准。
巅峰对话:全方位优选,最大化获益
 本篇章由空军军医大学唐都医院闫小龙教授主持
本篇章由空军军医大学唐都医院闫小龙教授主持
在闫小龙教授的主持下,中南大学湘雅医院李敏教授、北京大学人民医院燕翔教授与杨帆教授、Eric Lim教授、孙楠教授围绕NSCLC围术期免疫治疗相关研究数据、结合实践体会,探讨了模式选择、获益人群筛选、安全性等热点问题。
围术期免疫治疗最佳模式的选择
近期,Neotorch、KN-671、AEGEAN及NADIM II等围术期免疫治疗研究相继公布最新结果,对于围术期免疫治疗模式的选择带来新的挑战。Eric Lim教授表示,西方国家与中国对于围术期免疫治疗模式的选择存在差异,西方国家更依赖指南,如今Neotorch研究带来了新辅助+辅助的围术期全程治疗模式,有望改变指南。
李敏教授表示赞同,指出“三明治式”围术期免疫治疗地位已随着多项研究的发布得到巩固,但其中也仍存在一些争议,例如术后是否需要后续辅助治疗,哪些人群更适应等。
孙楠教授肯定了Eric Lim教授关于临床用药选择需依据权威指南指导的原则,表示此前辅助免疫治疗的地位很快便获得指南肯定,但II期及更早期患者的围术期治疗还有待进一步探索。
燕翔教授同样对于“夹心饼式”围术期免疫治疗模式给予肯定,表示该模式将毫无疑问为临床实践带来改变,但具体适应人群还需要更进一步探索。
杨帆教授在讨论的最后对专家们的意见进行了总结,表示目前对于分期较晚的驱动基因阴性患者,接受免疫联合化疗的新辅助治疗已经达成共识,但对于偏早期患者的新辅助治疗选择还有待商榷。针对non-pCR患者辅助治疗的选择目前循证医学证据较少,未来还需在可能获益与风险间进行权衡。
对于不同分期患者的治疗策略抉择
而对于不同分期患者的治疗策略,以及新辅助治疗阶段达到pCR的患者是否应进行辅助治疗,专家们也进行了深入研讨。
李敏教授和孙楠教授都表示,对于术前新辅助治疗达到pCR患者的术后辅助治疗选择,现有循证医学证据很难给出准确答案。李敏教授还指出临床研究与真实世界的pCR判断标准也需要慎重考虑,可能需要对所有患者采取新辅助+辅助全程治疗模式以保障获益。
孙楠教授也同样指出现有循证医学证据中,即便达到pCR的患者未来也可能出现复发、转移,提示对于该类患者体内可能仍存在MRD。术后的辅助治疗选择则要充分考虑药物安全性与患者依从性。
燕翔教授对于前述专家的讨论给予肯定,并指出,如今针对医疗方案的思考已经上升至对患者的深度人文关怀层面,长期治疗中需充分考虑治疗对患者生活质量、经济条件的影响。
杨帆教授一针见血地指出,本次讨论体现了东西方临床实践中的差别,西方国家按照临床指南进行治疗方案抉择,我国则考虑依据患者个体化情况进行选择,但两种方法并无优劣之分。新辅助治疗后达pCR的患者是否需要进行辅助治疗,期待中国研究者通过更多的临床研究予以解答。
围术期免疫治疗的未来探索
 针对未来围术期免疫治疗的发展方向,讨论专家皆肯定了生物标志物的探索价值。
针对未来围术期免疫治疗的发展方向,讨论专家皆肯定了生物标志物的探索价值。
Eric Lim教授还指出,治疗介入时机、治疗成本的选择、患者基因突变等都值得探索。英国的临床条件难以获得足够的患者数量,期待中国研究者开展更多探索性研究。
李敏教授与燕翔教授则主要围绕驱动基因阳性患者的治疗选择发表了看法,表示Checkmate-816研究与Neotorch研究都排除了驱动基因阳性患者,对于这部分患者的围术期治疗需要分层讨论。
最后,杨帆教授肯定了专家们提出的探索方向,并表示,除现有探索方向外,新靶点的探索、新治疗方案的组合也值得期待。对于新辅助靶向治疗,其pCR是否可以转化为患者的OS获益还尚不确定。
奋进新征程,开启新实践

会议尾声,杨帆教授对大会内容进行总结,并对于本次中外对话给予了高度评价,指出各位讨论者的精彩发言体现了专业的学术思想与对未来医学的瑰丽想象,杨帆教授向所有与会嘉宾的参与表示了感谢,并表示期待未来开展更多的高水平学术交流。
扫描海报下方二维码即可观看会议回放

排版编辑:肿瘤资讯-LY











 苏公网安备 32059002004080号
苏公网安备 32059002004080号


