近日,一年一度的全球肿瘤学盛会——美国临床肿瘤学会(ASCO)年会在芝加哥盛大召开,一如既往云集了全球肿瘤学领域最前沿的进展、带来了新的获益希望。膀胱癌是泌尿系统最常见的恶性肿瘤之一,高危非肌层浸润性膀胱癌(HR-NMIBC)患者比例不容小觑,甚至患者往往需进行膀胱切除,因此对这部分患者而言,临床尚存在明显的未被满足的需求。维迪西妥单抗(爱地希®)是由荣昌生物自主研发的中国首个原创抗体药物偶联物(ADC),目前已获批晚期胃癌、尿路上皮癌适应证且均已纳入国家医保药品目录。2023 ASCO中,天津医科大学第二医院胡海龙教授团队开展的一项真实世界研究入选摘要展示(摘要号:e16616),维迪西妥单抗用于HR-NMIBC治疗展现了良好疗效和安全性,为临床实践带来了诸多有益的启示,为维迪西妥单抗的应用时机向早期前移探索奠定了基石。【肿瘤资讯】特邀胡海龙教授介绍和解读该研究数据,展望未来探索方向。
【研究简介】
研究背景
维迪西妥单抗是一种靶向HER2的新型ADC药物,在晚期尿路上皮癌中显示了良好疗效。早期尿路上皮癌尚存在明显的未被满足的治疗需求,维迪西妥单抗的潜力值得进一步挖掘。
回顾性收集接受维迪西妥单抗治疗的HER2过表达(IHC 2/3+)的HR-NMIBC患者临床资料,这些患者无法完全切除肿瘤或无法耐受手术,分析病理学完全缓解(CR)率、部分缓解(PR)率、疾病稳定(SD)率、客观缓解率(ORR)、缓解持续时间(DoR)、保膀胱生存期 (CFS)、无事件生存期 (EFS) 、安全性等指标。
研究结果
(1)基线特征:共纳入19例患者,中位年龄69岁(58~81岁);其中7例(36.8%)采用维迪西妥单抗单药治疗,12例(63.2%)采用维迪西妥单抗联合PD-1抑制剂替雷利珠单抗治疗。
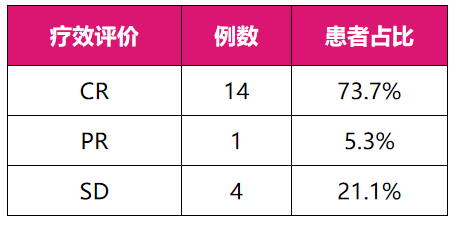
(2)总体疗效:14例[73.7%, 95%可信区间(CI): 48.6%~89.9%]患者达到CR,1例(5.3%, 95% CI: 0.3%~8.1%)为PR,4例(21.1%, 95% CI: 7.0%~46.1%)为SD状态。ORR为78.9% (95%CI: 53.9%~93.0%),DoR率为92.9% (95% CI: 80.3%~100.0%),12个月 DoR率为61.9% (95% CI: 27.4%~100.0%)。
(3)分层分析:14例(73.7%)患者HER2表达为IHC 3+,其中12例获得缓解,ORR为85.7% (95% CI: 56.2%~97.5%);5例HER2 IHC 2+患者中, 3例获得缓解, ORR为60.0% (95% CI: 17.0%~92.7%)。此外,有5例患者为既往PD-1抑制剂治疗失败,接受以维迪西妥单抗为基础的方案治疗后,ORR达60.0% (95% CI: 17.0%~92.7%), 且有2例(40.0%, 95% CI: 7.3%~83.0%)达到CR。
(4)生存结局:1例患者因非治疗相关原因死亡。12个月CFS率为84.2% (95% CI: 69.3%~100.0%), 中位CFS尚未达到。12个月EFS率为75.8% (95% CI: 48.3%~100.0%), 中位EFS尚未达到。
(5)安全性:最常见的1~2级治疗相关不良事件(TRAEs)为脱发(36.8%)、皮疹(36.8%)、瘙痒(36.8%)、厌食(31.6%)和疲乏(26.3%)。3例(6.3%)患者发生了3~4级TRAEs,包括皮疹、瘙痒、白细胞减少和中性粒细胞减少。无治疗相关死亡病例。
研究结论
维迪西妥单抗单药以及联合PD-1抑制剂治疗HR-NMIBC均显示了良好疗效,ORR高且安全性可控可管理,为这类患者提供了新的有效治疗策略。基于此,研究者团队已经启动了一项维迪西妥单抗联合PD-1抑制剂治疗HR-NMIBC的前瞻性研究,以期为临床应用提供更多证据。
【研究者说】
医学博士泌尿外科专家
天津市中西医结合泌尿外科分会青委会副主任委员
中国中西医结合泌尿外科分会青委会副主任委员
天津市泌尿外科研究所基因工程实验室副主任
天津医科大学硕士研究生导师
天津医科大学第二医院泌尿外科主任医师
2013年作为访问学者在美国梅奥诊所、罗切斯特大学学习4个月
作为主持人及主要参与人参与国家级,省部级局级课题10项
参编专著5部,发表论文被SCI收录8篇

胡海龙教授在ASCO现场
着眼未尽之需,深挖新药潜力
膀胱尿路上皮癌根据肿瘤是否浸润膀胱肌层分为NMIBC和肌层浸润性膀胱癌(MIBC),其中NMIBC占比达75%,包括Ta期(70%~75%)、Tis期(原位癌,5%~10%)及T1期(20%~25%)[1]。根据复发风险及预后特征,NMIBC 分为低危、中危、高危和极高危4组。高危定义为满足以下任何1项条件:T1期肿瘤;G3(高级别)肿瘤;原位癌(CIS);多发、复发、直径>3cm的TaG1G2(低级别)肿瘤[2]。可见,高危患者比例不容小觑,其标准治疗首选经尿道膀胱肿瘤电切术(TURBt)、术后采用膀胱灌注化疗+膀胱灌注卡介苗(BCG)辅助治疗,但部分患者不能耐受手术或无法完全切除肿瘤甚至拒绝手术。如何为这部分HR-NMIBC患者找到一种安全有效且能够保障生活质量的替代治疗方式或是缩瘤后为完全切除肿瘤创造机会,是亟待满足的临床需求。
维迪西妥单抗的应用已覆盖晚期尿路上皮癌全线治疗,维迪西妥单抗+PD-1抑制剂是一线和二线治疗的推荐方案,维迪西妥单抗单药被推荐用于二线及三线治疗[2]。指南的这些推荐主要是基于维迪西妥单抗在相应临床研究中展现出的良好疗效和可靠安全性,有效率高且带来了明显生存获益[3-5]。鉴于其作为新型ADC药物的独特结构、药学优势和出色临床表现,我们对其前移至早期尿路上皮癌寄予厚望,希望能够填补当前未尽的需求。此项回顾性研究是一次成功的“投石问路”,为后续的前瞻性研究奠定了重要基础。
深度持久缓解,高质量生存获益
本研究共纳入了19例无法完全切除肿瘤或无法耐受手术的HR-NMIBC患者,7例为维迪西妥单抗单药治疗,12例为维迪西妥单抗联合PD-1抑制剂治疗。无论深度缓解率还是疗效持久性都令人鼓舞,73.7%的患者达到了CR,1例获得PR,60%以上的患者DoR超过了1年,且无论HER2表达水平如何(IHC 3+或2+),均可获得高缓解率,得益于维迪西妥单抗可有效克服HER2表达异质性的疗效优势,这与其在晚期尿路上皮癌中的研究结果也是一致的。值得注意的是,既往PD-1抑制剂治疗失败的患者对维迪西妥单抗方案应答良好,5例患者的ORR达60.0%, 且有2例获得了CR。全组人群中位CFS和中位EFS均未达到,12个月CFS率和12个月EFS率分别高达84.2%和75.8%,生活质量和生存期都明显获益。

安全性方面,绝大多数TRAEs为1~2级,包括脱发、皮疹、瘙痒、厌食、疲乏等,易于控制和管理,基本不影响治疗的持续性。3~4级TRAEs发生率仅为6.3%,经对症处理后均有效缓解。本组患者中位年龄69岁,年龄最大者81岁,老年、高龄患者均可安全耐受维迪西妥单抗单药或联合治疗,这是临床实践的重要保障。
创新治疗模式,追求更多治愈
我国膀胱癌患者基数庞大,提高早期诊断率、创新综合治疗模式、改善患者生活质量是膀胱癌临床诊疗和科研实践的三大目标。除了本研究所探索的不可手术HR-NMIBC患者,术后膀胱灌注治疗后复发率仍较高、BCG灌注治疗不可耐受/无应答/失败等都是HR-NMIBC患者亟待解决的临床问题。复发后一旦出现高级别肿瘤或MIBC,目前指南推荐行根治性膀胱切除术,患者生活质量将受到巨大影响。因此,寻找能够进一步降低复发风险、克服BCG灌注治疗局限性的新型治疗方式亟待探索。维迪西妥单抗已经革新了晚期尿路上皮癌治疗格局,向早期前移推进是必由之路,也是迫切的临床需求所在。
本研究结果提示,接受维迪西妥单抗单药或联合治疗的HR-NMIBC患者,达到CR者有望安全豁免手术,获得高质量长期生存;达到PR、保持SD者后续有望获得完全切除肿瘤的机会。本团队已经启动了相关的前瞻性研究,进一步验证维迪西妥单抗联合PD-1抑制剂对于HR-NMIBC的价值,以期为临床应用提供更多证据支持,优化NMIBC的综合治疗模式。值得一提的是,维迪西妥单抗与PD-1抑制剂在晚期尿路上皮癌治疗中已经显示了显著的协同增效作用,精准靶向的细胞毒药物可诱导免疫原性细胞死亡,提高免疫治疗敏感性,两者相得益彰,在早期尿路上皮癌中也有望大放异彩。本研究严格筛选了来自于HER2 IHC过表达(IHC 2/3+)的HR-NMIBC,鉴于维迪西妥单抗在mUC HER2低表达(IHC 0/1+)通过联合免疫治疗,仍有接近33%左右的有效率,得益于其“旁观者效应”以及联合免疫的协同机制,因此未来HER2低表达的HR-NMIBC患者或许亦有望从中获益。
HR-NMIBC患者的高危因素不尽相同,未来或许需要进一步细分人群、细化治疗方案,比如高级别肿瘤、CIS、T1期肿瘤或需要更强的治疗方案,以抵抗其侵袭性更高的生物学行为。这些都需要更多临床研究深入探索、精准回答。希望以维迪西妥单抗为代表的ADC药物能够为尿路上皮癌围术期治疗、保膀胱治疗等带来更多突破,帮助更多患者走向治愈、拥有高质量的长生存,期待这方面的临床研究设计和进展未来会越来越丰富!
[1]国家卫生健康委员会.膀胱癌诊疗指南(2022年版).
[2]中国临床肿瘤学会(CSCO)尿路上皮癌诊疗指南(2022年版).
[3]Journal of Clinical Oncology 40, no. 16_suppl (June 01, 2022) 4520-4520.
[4]Journal of Clinical Oncology 40, no. 16_suppl (June 01, 2022) 4519-4519.
[5]Journal of Clinical Oncology 40, no. 6_suppl (February 20, 2022) 515-515.
排版编辑:肿瘤资讯-Ivy











 苏公网安备32059002004080号
苏公网安备32059002004080号


