从2013年哌柏西利横空出世获得FDA突破性创新药后,CDK4/6抑制剂如雨后春笋,相继展开大型临床研究。CDK4/6抑制剂联合内分泌的治疗模式,历经大型随机对照研究结果的证实和真实世界研究的验证,扎实而稳健地走到国内外各大指南、专家共识晚期乳腺癌一线治疗推荐的前列。美国真实世界研究结果显示1:2015年至2018年间,将CDK4/6抑制剂联合内分泌治疗作为HR+/HER2-转移性乳腺癌一线治疗方案的比例从22%升高至48.4%。
哌柏西利在HR+/HER2-晚期乳腺癌的治疗中占先机、开新局,而2022年6月5日ASCO公布了PALOMA-2次要研究终点OS的阴性结果,惊讶之余更应重新审视PALOMA-2的临床研究设计、冷静分析导致PALOMA-2 OS阴性可能的原因。
请点击视频,观看精彩解说
大连医科大学附属二院肿瘤内科主任
辽宁省百千万人才百人层次
中国肿瘤临床学会理事
中国临床肿瘤学会(CSCO )乳腺癌专家委员会常委
中国抗癌协会乳腺癌专业委员会委员
辽宁省医学会肿瘤分会副主任委员
辽宁省抗癌协会乳腺癌专业委员会副主任委员
辽宁省抗癌协会肿瘤转移委员会候任主任委员
大连市医学会肿瘤分会候任主任委员
大连医科大学肿瘤学博士在读
研究方向:乳腺癌分子机制研究
参与国家自然科学基金面上项目1项
辽宁省自然科学基金面上项目1项
第一作者发表SCI论文1篇
温故PALOMA-2
PALOMA-2是一项全球多中心、随机双盲、安慰剂对照的III期临床研究,纳入666例绝经后未经晚期系统性治疗的ER阳性HER2阴性晚期乳腺癌患者,2∶1随机分组至PAL+LET的治疗组或PBO+LET的对照组。主要研究终点是由研究者评估的无进展生存期(PFS),次要终点包括总生存期(OS)、客观缓解率、临床获益、患者报告结局及安全性。

PALOMA-2达到改善PFS的主要研究终点和其他次要研究终点2-3:中位随访38个月,PAL+LET组相比对照组,显著改善mPFS(27.6 vs 14.5个月;HR=0.563),且所有亚组患者均获益;在有可测量疾病的患者中,PAL+LET的ORR为55.3%,PBO+LET的ORR为44.4%(odds ratio 1.55[1.05–2.28];P=0.03);PAL+LET长期使用没有累积的毒性;维持了生活质量。

鉴往以知来——PALOMA-2 OS知新
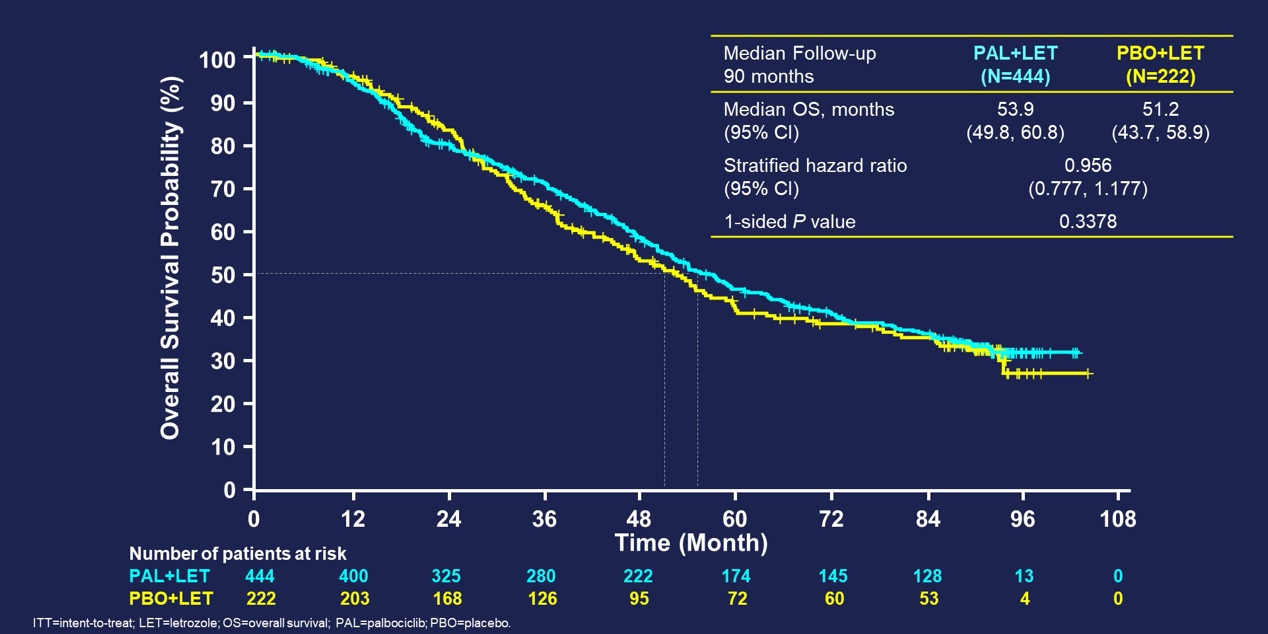
2022年ASCO公布的PALOMA-2总生存结果显示4:中位随访90个月后(数据截止2021年11月15日),总生存事件数为405(占全体60.8%);有相当比例的患者无法进行随访(撤回同意或失访)导致其数据删失:安慰剂组删失患者比例为21%,哌柏西利组为13%。PAL+LET组和PBO+LET组的中位OS分别为53.9个月(95% CI:49.8-60.8)和51.2个月(95% CI: 43.7-58.9)(HR=0.956;95% CI:0.777-1.177;单侧P=0.3378)。PAL+LET组对比PBO+LET组,总生存在数值上显示出一定程度的延长,但未达到统计学差异。
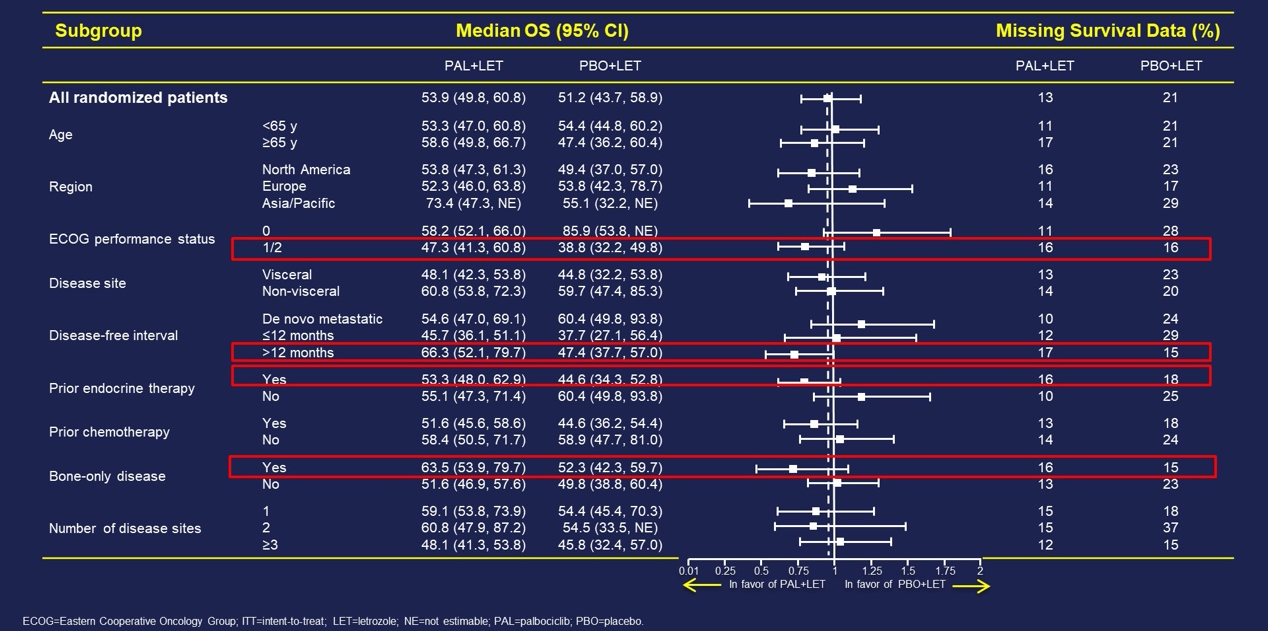
OS亚组分析显示:多数亚组的风险比位于1附近,未显示出联合治疗的总生存获益。而结合删失数据比例来看,在PAL+LET组和PBO+LET组数据缺失比例均衡的亚组(如:ECOG评分1-2、DFI>12个月、辅助治疗阶段曾接受内分泌治疗和单纯骨转移)其风险比值显示出PAL+LET联合治疗较PBO+LET更加获益。
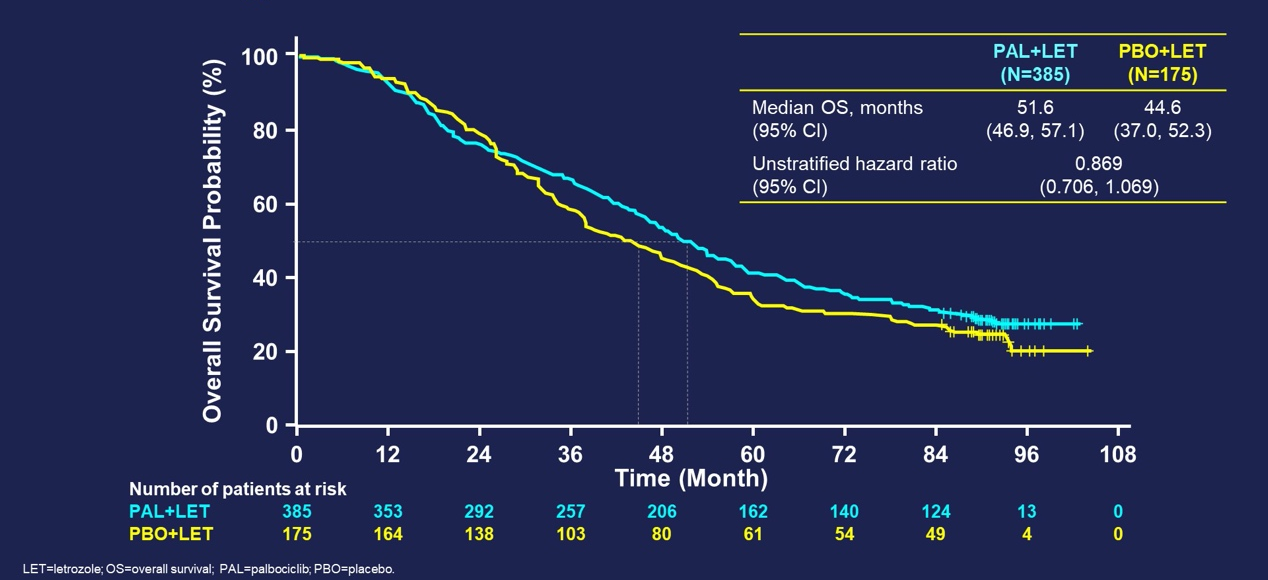
排除无法获得生存数据的事后敏感性分析结果显示:PAL+LET组和PBO+LET组的中位OS(95% CI)分别为51.6个月(46.9-57.1)和44.6个月(37.0-52.3)(HR=0.869;95% CI:0.706-1.069)。
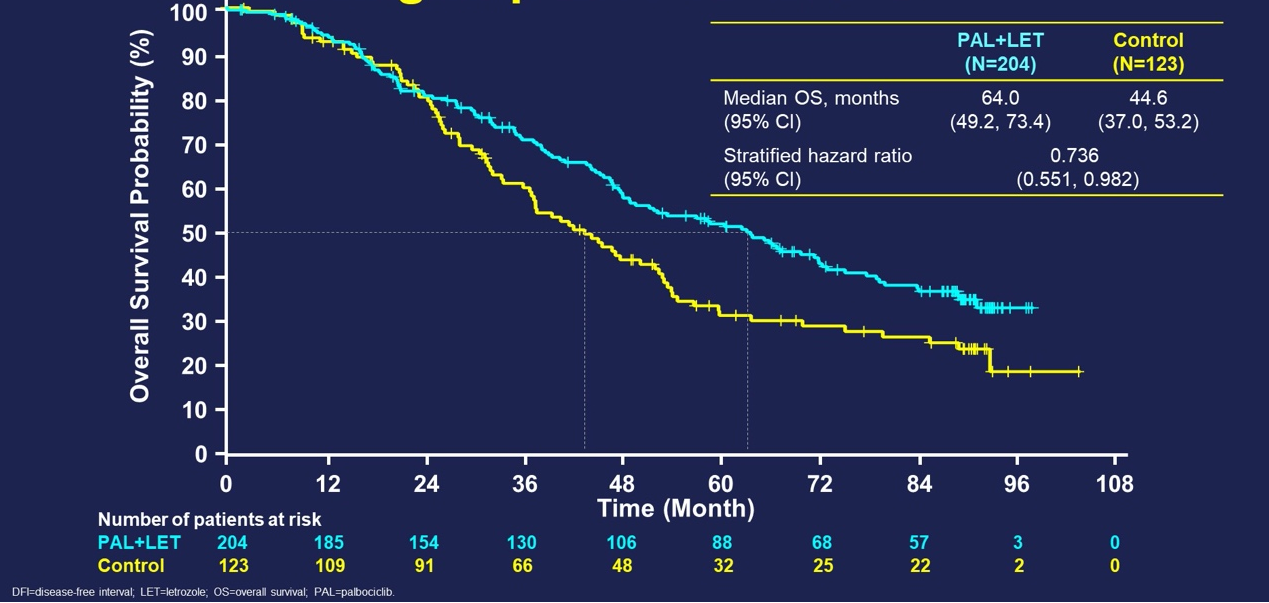
PALOMA-2作为PALOMA-1的III期验证研究,两个研究联合分析结果显示: 在DFI>12个月的PAL+LET组和PBO+LET组失访率相似(分别为17% 、15%),PAL+LET组(179例)的中位OS为64个月(95%CI,49.2-73.4),PBO+LET组(93例)为44.6个月(95%CI,37.7-53.2);HR=0.736(95%CI,0.551-0.982)。
安全性与既往报道的一致,PAL+LET组最常见的不良事件是中性粒细胞减少、感染、白细胞减少、关节痛、疲乏感、恶心和脱发。最常见的3或4级不良事件是中性粒细胞减少,未观察到新的不良事件。
循道以致远——借PALOMA-2 OS更新和大样本P-reality X真实世界数据看哌柏西利生存获益
一、分析PALOMA-2取得阴性结果的原因,包括以下几个方面与大家共同探讨
1、入组耐药患者对OS具有稀释作用
从入组人群特征上看,PALOMA-2研究一线患者包括以下三类:初诊晚期naive(167例,37.6%),DFI>12个月(178例,40.1%),DFI<12个月(99例,22.3%),其中前两类属于内分泌敏感患者,DFI<12个月为继发性耐药患者。MONARCH-3则纳入全部内分泌敏感的患者,MONALESSA-2中继发性耐药的患者仅有4例(占比1.2%),其余均为内分泌敏感。因此,PALOMA-2纳入高比例继发性耐药人群可能对OS的最终结果起到稀释作用,导致阴性结果的产生。
2、生存数据删失率过大导致有效样本量减少与组间不均衡
从研究公布的结果中我们看到,随着随访时间的不断延长,失访及撤回同意等导致数据删失率逐渐增加,哌柏西利组删失患者比例为13%,安慰剂组更是达到了21%,不仅体现在数值大,更重要的是二者不成比例。这将导致可用于生存分析的样本量大大下降,降低统计学效能,并导致两组之间基线数据的不均衡从而对两组的可比性产生怀疑。在数据缺失比例均衡的亚组中,我们可以看到较好的哌柏西利联合来曲唑治疗的获益趋势,而在数据缺失比例失衡的亚组结果均未看到获益。
3、生存曲线交叉违反PH假设,用Cox比例风险模型进行整体HR解读不恰当
无论对于ITT人群,还是去除无法获得生存数据后的人群,Kaplan-Meier生存曲线均呈现交叉,表明数据存在违反PH假设。而满足PH假设是进行Cox比例风险回归分析的前提条件,因此使用Cox比例风险模型进行整体HR解读是不恰当的,采用时依Cox回归模型进行风险比解读可能更为适合,亦可能有不同的研究结论产生。

二、基于真实世界设计的大样本P-reality X研究主要研究终点OS取得了显著获益结果
今年ESMO BC会上公布了迄今为止样本量最大的一项CDK4/6抑制剂联合AI对照AI单药一线治疗晚期HR阳性HER2阴性乳腺癌真实世界研究P-reality X,研究共入组2888例,以总生存为主要终点。P-reality X研究使用美国Flatiron数据库,使用PSM和sIPTW方法平衡患者人口统计学和临床特征。结果显示,在经过sIPTW和PSM校正后哌柏西利联合AI组对比AI治疗组中位总生存有显著获益,分别为49.1个月对比43.2个月(风险比:0.76,p=0.0001)和57.8个月比43.5个月(风险比:0.72,p<0.0001)。

三、那么对于P-reality X真实世界研究与PALOMA-2得出的截然不同的OS获益结果该如何考量,我们从以下几个角度来进行讨论分析
(1)研究类型不同
首先,P-reality X属于真实世界研究,PALOMA-2为RCT研究。相对于RCT研究,真实世界研究的研究对象常采用相对较少的排除条件,研究结果外部真实性相对更好。仅有3%的乳腺癌患者参与RCT,因此真实世界数据更能代表真实诊疗过程中的患者。并且,OS为P-reality X研究的主要研究终点,而仅为PALOMA-2的次要研究终点。Flatiron数据库的OS终点除健康记录外还包括外部数据源(即国家死亡指数、美国社会保障死亡指数、讣告和商业死亡数据),并已得到验证。减少了失访的患者,提高了死亡率数据的完整性。
(2)样本量不同
P-reality X真实世界研究具有样本量优势,P-reality X共纳入2888例患者,而PALOMA-2仅入组666例患者,并且数据删失后仅剩余560例患者用于分析。大样本量将更有利于减少分析中产生的选择偏倚。
(3)均衡性不同
PALOMA-2研究过大且不成比例的数据删失率可能导致了组间不均衡,数据可比性产生怀疑。而P-REALITY X研究来源于Flatiron数据库,生存数据更为完整,并且采用PSM和sIPTW用于解决混杂因素的统计方法(PSM和sIPTW)来平衡患者组间人口学和临床特征,并且PSM结果与sIPTW分析一致,研究结果稳定可信。
小结
因此,PALOMA-2的阴性结果并不能否定哌柏西利在生存上的获益,其失败原因与耐药人群的纳入、数据缺失、统计学分析方法选择密切相关。大样本P-reality X真实世界研究是PALOMA-2 OS的有效补充,其结果更能反映患者临床实际应用过程中的药物疗效,P-reality X结果有力地证明了哌柏西利联合AI对比AI单药治疗显著的总生存获益。
CDK4/6抑制剂时代已来,不但为HR+乳腺癌患者带来生存获益,长期服用也并未增加患者的累积毒性,提高了患者的生活质量。活得更长是基础,活得更好是目标!CDK4/6抑制剂之后的治疗如何合理排布让患者的生存获益更大,仍是临床医生未来需要面对的问题。
道阻且长,行则将至!
1. Adam Brufsky , et al. 2019 SABCS Poster P1-19-26.
2. Rugo HS, et al. Breast Cancer Research and Treatment,2019
3. Finn RS, et al. N Engl J Med. 2016;375:1925-36.
4. Richard S. Finn, Hope S. Rugo, Veronique C Dieras,et al. ASCO 2022 LBA 1003.
仅出于科学教育和信息传递之目的提供相关内容,供医疗卫生专业人士参考,不构成医学建议和产品推广。
GCMA编号:PP-IBR-CHN-0956
到期日期:2024-6-12
排版编辑:肿瘤资讯-小编











 苏公网安备32059002004080号
苏公网安备32059002004080号


