
第54例
在原发性乳腺癌患者中观察到有25%~30%的患者HER2过度表达。曲妥珠单抗是针对细胞核HER2基因调控细胞表达的P185糖蛋白而研制的重组DNA衍生的人源化IgG型单克隆抗体。帕妥珠单抗通过阻滞HER2减缓肿瘤的生长。帕妥珠单抗跟曲妥珠单抗相似,但作用的HER2靶点区域不同。所以这两种不同机制的抗HER2抗体联合在乳腺癌的辅助治疗或者新辅助治疗当中,都是非常有效的。本文通过回顾一个新辅助治疗阶段曲妥珠单抗+帕妥珠单抗双靶联合治疗并获得病理完全缓解的病例,介绍目前有关该类患者的临床治疗思路。

北京大学人民医院乳腺中心 科主任
2006年美国M.D. Anderson肿瘤中心访问学者
2007年美国UMASS肿瘤中心博士后
中国医师协会乳腺疾病专业委员会常委兼秘书长
中国临床肿瘤学会(CSCO)执行委员
中国抗癌协会乳腺癌专业委员会(CBCSG)委员
中华医学会肿瘤分会乳腺学组委员
中国医师协会乳腺疾病培训专家委员会常委
中国老年肿瘤学会乳腺癌专业委员会常委
中华预防医学会乳腺学组委员
《中华乳腺病杂志》编委
《ANNALS OF ONCOLOGY》中文版乳腺专刊编委

北京大学人民医院乳腺中心 主治医师
毕业于北京大学医学部 外科学博士
研究方向:
ctDNA、CTC在乳腺癌诊治中的应用研究
乳腺癌干细胞体外药敏筛选研究
乳光超在乳腺疾病诊断中的应用研究
基本情况
患者女性,48岁。既往史无特殊。月经、婚育史:月经初潮15岁,经期5天,周期28天,未绝经,末次月经2018-10-27,月经规律。适龄结婚,孕1产1,育有1女,配偶体健,子女体健。个人史、家族史均无特殊。
主诉
发现左乳肿物1年半,确诊左乳癌半年,肿物增大2月。
现病史
患者1年半前左乳下方被撞击后自觉可触及肿物,伴触痛,就诊外院,考虑外伤后炎症反应,未予以特殊治疗,肿物逐渐增大;半年前就诊外院,行乳腺穿刺活检,病理结果提示乳腺癌,患者就诊中医诊所,予以中药治疗,起初自觉肿物逐渐缩小,2月前自觉肿物逐渐增大,自行停药治疗,1周前门诊就诊。
体格检查与辅助检查
体格检查:双乳发育正常,乳头等高,左乳下方可见隆起,左乳可触及质硬肿物,大小约7cm×7cm,边界不清,活动度差,伴触痛,左侧腋窝可触及质硬淋巴结,无融合,活动度可。
基线影像检查:乳腺MRI(2018年10月31日):左乳下象限肿块,大小6.8cm×4.8cm×6.7cm,BI-RADS:5,左腋窝多发淋巴结转移。乳腺超声(2018年11月5日):左乳肿物,BI-RADS 6;左乳下方象限可见肿物,左侧腋窝可见皮髓质结构消失淋巴结;右乳未及异常。PET-CT(2018年11月1日):左乳癌,左侧腋窝转移淋巴结可能性大。骨(-)、双肺(-)、肝(-)、脑(-)。
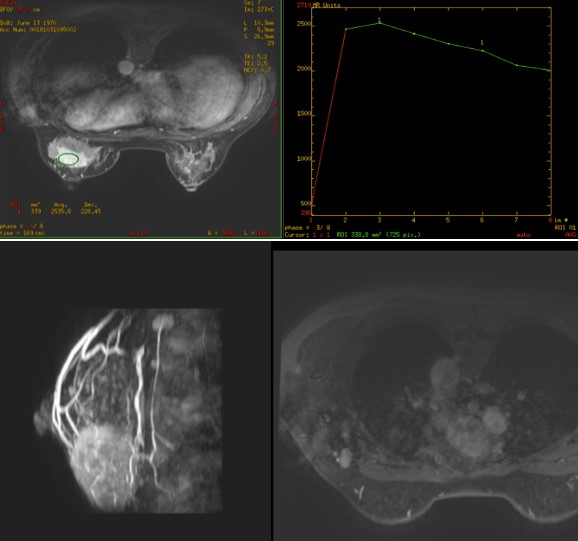
乳腺MRI(2018年10月31日)
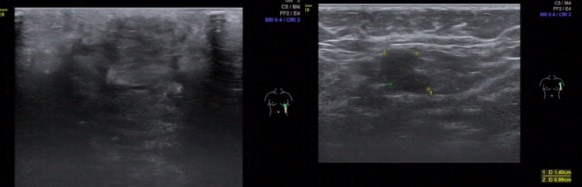
乳腺超声(2018年11月5日)
CNB病理会诊:(左乳腺)穿刺活检组织:可见浸润性癌成分,结合原单位免疫组化染色结果,符合非特殊类型浸润性(导管)癌(Ⅱ级)。免疫组化: ER(90+),PR(100%+),HER2(3+),Ki-67(70%+) 。
诊断
左乳癌并左腋窝淋巴结转移;临床分期:cT4N1M0、cⅢB期;分子分型:HER2阳性HR阳性型。
治疗经过
2018年11月6日—2019年2月18日,予以TCHP方案双靶新辅助治疗6周期,具体剂量:多西他赛 75mg/㎡+卡铂 AUC 5+曲妥珠单抗6mg/kg (首次8mg/kg )+帕妥珠单抗420mg(首次840mg)共计6周期,每3周1次。
新辅助治疗过程中临床评估
肿块明显缩小,皮肤受侵,但无破溃迹象。乳腺超声(2019年3月4日):左乳癌新辅助化疗后未见明确肿物。乳腺钼钯(2019年3月4日):未见明确肿物。乳腺MRI:左乳下象限肿块较前明显缩小,左腋窝多发淋巴结较前减小。疗效评价部分缓解(partial response,PR)。
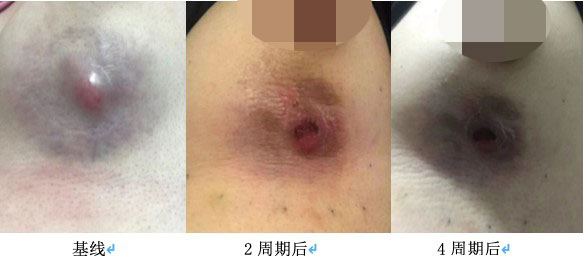
肿块皮肤表现
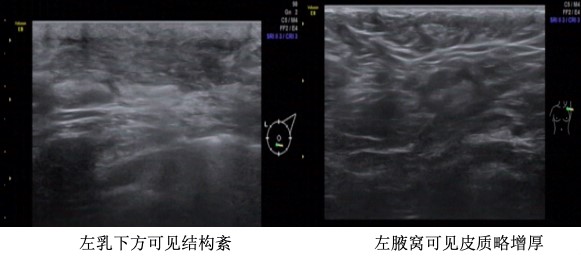
乳腺超声(2019年3月4日)
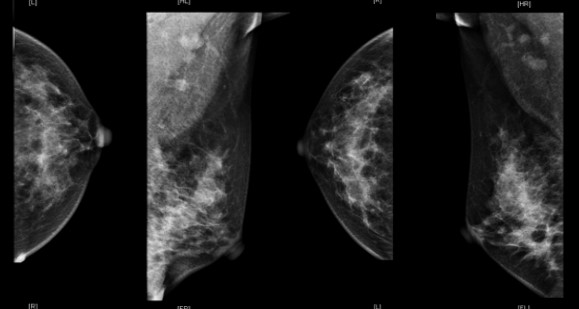
乳腺钼钯(2019年3月4日)
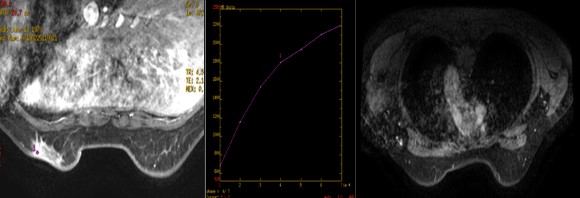
乳腺MRI
手术
排除手术禁忌后于2019年3月5日行左乳改良根治术,术后病理:(左)乳腺改良根治标本:送检乳腺组织广泛取材,乳腺组织中可见广泛水肿变性、炎症及泡沫组织细胞反应,局灶钙化,局灶可见少量高级别导管原位癌成分,未见明确浸润性癌成分,结合临床病史符合乳腺癌化疗后表现,乳头未见癌侵犯;基底切缘未见癌侵犯。腋窝淋巴结未见癌转移(0/18)。(前哨)淋巴结未见癌转移(0/1)。(尖组)淋巴结未见癌转移(0/1)。(肌间组)淋巴结未见癌转移(0/3)。
术后诊断
左乳癌并左腋窝淋巴结转移新辅助化疗后
分期:ypTisN0M0,yp0期
疗效评估:病理完全缓解(pathologic complete response, pCR)
分子分型:HER2阳性HR阳性型
辅助治疗方案
曲妥珠单抗+帕妥珠单抗1年,胸壁+区域淋巴结放疗,他莫昔芬序贯AI共计10年内分泌治疗。
点评专家

山东省肿瘤医院乳腺病中心主任
中国抗癌协会乳腺癌专业委员会副主委
中国临床肿瘤学会乳腺癌专家委员会常委
中华医学会肿瘤学分会乳腺癌学组委员
中国医师协会乳腺外科医师委员会常委
国家卫健委乳腺癌诊疗规范专家组成员
GBCC国际指导专家委员会成员
点评
该病例为初诊局部晚期cT4N1M0、cⅢB期,分子分型为HER2阳性HR阳性型。该病例患者在新辅助治疗阶段使用双靶联合治疗后,术后证实已达到pCR,获益明显,明显改善预后。
1. HER2阳性乳腺癌患者新辅助治疗应及早进行抗HER2治疗
患者分子分型为HER2阳性HR阳性型,根据《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019版指出:满足以下条件之一者可选择术前新辅助药物治疗:(1)肿块较大(>5cm);(2)腋窝淋巴结转移;(3)HER2 阳性 ;(4)三阴性;(5)有保乳意愿,但肿瘤大小与乳房体积比例大难以保乳者。本病例患者乳腺肿物>5cm、HER2阳性且有淋巴结转移,适宜进行新辅助治疗。临床研究证明,HER2阳性患者新辅助治疗,曲妥珠单抗联合化疗与单用化疗相比能够显著提高pCR率,奠定了曲妥珠单抗在HER2阳性乳腺癌新辅助治疗中的标准地位[1]。而曲妥珠单抗联用帕妥珠单抗的双靶向抗HER2治疗也是作为1A级证据进行Ⅱ级推荐。这来源于NeoSphere 研究证实了曲妥珠单抗和帕妥珠单抗与多西他赛联合进一步提高了pCR率[2]。研究结果显示帕妥珠单抗+曲妥珠单抗+多西他赛(P+T+D)组病例pCR率为45.8%,而曲妥珠单抗+多西他赛(T+D)组为29.0% ,(P=0.0141)。TRYPHAENA研究证实[3],A组FEC+H+P×3→T+H+P×3的PCR(ypT0/is)为61.6%,B组FEC×3 →T+H+P×3的PCR为57.3%,而C组的TCH+P×6的PCR为66.2%。其中,分层分析发现激素受体阴性组的PCR阳性率高于激素受体阳性组。在HR+/HER+患者中,A、B、C组的PCR分别为46.5%、48.6%、50%,而在HR-/HER2+患者中,A、B、C组的PCR分别为79.4%、65%、83.8%。由此可知,对于HR+/HER+患者而言,双靶+双化疗药新辅助模式可能获得更高的PCR率,但此结论仍需更进一步的研究以证实。
2. 新辅助治疗后续患者是否仍需强化治疗,应由pCR决定
ESO/ESMO晚期乳腺癌(ABC4)国际共识指南-第4版指出:对于HER2阳性的局部晚期乳腺癌(locally advanced breast cancer ,LABC) (炎症性或非炎症性)患者,无远处转移,经适当的新辅助系统治疗和适当的定位后完全缓解,如果有潜在的治疗意图,则应采用1年的抗HER2治疗的批准辅助疗程。而APHINITY研究则证实[4],帕妥珠单抗联合曲妥珠单抗对比曲妥珠单抗降低了HER2阳性早期乳腺癌患者中19%复发死亡风险(HR=0.81; 95% CI 0.66, 1.00; P= 0.0446) ,分层分析提示淋巴结阳性和HR阴性亚组获益更多。如果新辅助治疗中治疗未达pCR,KATHERINE[5]研究对1,486例HER2阳性早期乳腺癌患者进行新辅助化疗加HER2靶向治疗,包括紫杉烷和曲妥珠单抗,然后进行手术。所有患者在乳房或腋窝淋巴结中都有残留的侵袭性疾病。在手术后12周内,患者随机分配1:1至抗体-药物偶联物T-DM1(每3周3.6mg / kg静脉注射)或曲妥珠单抗(每3周6mg / kg静脉注射),共14个周期。结果表示T-DM1将乳腺癌侵袭性复发风险或死亡的降低了50%,相当于三年无浸润性疾病生存率(iDFS)的绝对改善率提高了11.3个百分点(T-DM1组88.3% vs曲妥珠单抗77%)。由此可知,若患者经新辅助治疗后未达pCR者,可考虑后续强化治疗。本病例中,患者已达pCR,根据实际情况,予以双靶标准治疗1年+辅助放疗+辅助标准内分泌治疗,目前无明显不良反应,未见疾病复发转移,获益明显。
本病例治疗的经验
本病例虽然分子分型为HR+/HER2+型患者,理论上新辅助治疗效果欠佳,但实际应用上在新辅助治疗阶段予以帕妥珠单抗+曲妥珠单抗双靶抗HER2治疗以及多西他赛+卡铂双化疗药物方案强化治疗,效果显著,术后病理提示pCR,临床获益最大化,可见双靶方案强化治疗可作为HR+/HER2+型患者的可选方案。
[1] Buzdar AU, Ibrahim NK, Francis D, et al. Significantly higher pathologic complete remission rate after neoadjuvant therapy with trastuzumab, paclitaxel, and epirubicin chemotherapy: results of a randomized trial in human epidermal growth factor receptor 2-positive operable breast cancer [J]. J Clin Oncol. 2005 Jun 1;23(16):3676-85.
[2] Gianni L,Pienkowski T,Im Yo, et al. 5-year analysis of neoadjuvant pertuzumab and trastuzumab in patients with locally advanced, inflammatory, or early-stage HER2-positive breast cancer (NeoSphere): a multicentre, open-label, phase 2 randomised trial[J] .Lancet Oncol., 2016, 17: 791-800.
[3] Schneeweiss A,Chia S,Hickish T et al. Pertuzumab plus trastuzumab in combination with standard neoadjuvant anthracycline-containing and anthracycline-free chemotherapy regimens in patients with HER2-positive early breast cancer: a randomized phase II cardiac safety study (TRYPHAENA).[J] .Ann. Oncol., 2013, 24: 2278-84.
[4] von Minckwitz G, Procter M, de Azambuja E, et al. APHINITY Steering Committee and Investigators. N Engl J Med. 2017 Jul 13;377(2):122-131.
[5] von Minckwitz G, Huang CS, Mano MS, et al. Trastuzumab Emtansine for Residual Invasive HER2-Positive Breast Cancer.[J]. N Engl J Med. 2019 14;380(7):617-628.












 苏公网安备32059002004080号
苏公网安备32059002004080号


