
第53例
乳腺癌是女性发病第一位的肿瘤,在原发性乳腺癌患者中观察到有25%~30%的患者HER2基因过度表达。而HER2阳性乳腺癌的肿瘤侵袭性更强,预后更差。曲妥珠单抗是抗HER2治疗的标准药物,使用曲妥珠单抗的靶向治疗可以明显改善患者的预后,延长生命并提高生活质量。本文分析一例晚期乳腺癌患者在经历不规范治疗后通过参加临床试验,维持抗HER2治疗,长期获益,总生存近10年的病例,分享HER2阳性乳腺癌抗HER2治疗的重要性。

北京大学肿瘤医院乳腺肿瘤内科
中国女医师协会乳腺疾病研究中心委员
主要研究方向及工作重点为乳腺癌规范化治疗和个体化治疗、肿瘤生物免疫基因治疗及以干细胞为基础的综合治疗
发表专业论文二十余篇,参与编译多部肿瘤专著
手术与辅助治疗
患者女性,既往史:否认高血压、冠心病史,否认糖尿病史。个人史:已婚,23岁结婚,G1P1,月经初潮14岁,49岁闭经。
2010年3月,患者于当地医院行“右乳癌改良根治术”,术后病理:(右)乳浸润性导管癌,组织学分级Ⅲ级,肿瘤大小不详,可见脉管癌栓,腋窝淋巴结转移1/9。免疫组化:ER(-),PR(-),HER2(3+),Ki67(+,10-20%)。术后分期:pTxN1M0。诊断:右乳癌改良根治术后(pTxN0M0,ER-/PR-/HER2阳性型)。
2010年4月—8月,当地医院予以多西他赛+吉西他滨+氟尿嘧啶4周期,序贯多西他赛+环磷酰胺3周期辅助化疗,未行辅助放疗。2011年9月—2012年8月行曲妥珠单抗治疗1年。2010年8月—2013年6月,予以他莫昔芬辅助内分泌治疗。
首次转移与一线治疗
2013年6月,患者因 “右乳癌改良根治术后3年,发现肝转移1周”本院就诊。腹部超声及腹部CT提示:肝脏多发结节,较大约95mm×80mm(图1)。入院后完善PET/CT:肝右后叶见一巨大占位灶,SUVmax 11.3,范围 84mmx75mm,肝S4见两处浓聚结节,SUVmax 6.8,肝S3见摄取轻度增高灶,左9肋高代谢灶,局部骨质密度增高,不除外骨转移。肿瘤标志物:CEA 58.64ng/ml, CA153 81.97U/ml, CA125 27.50 U/ml, CA199 1.41U/ml, AFP 1.93ng/ml。
无病生存期(disease free survival,DFS)为3年3个月。
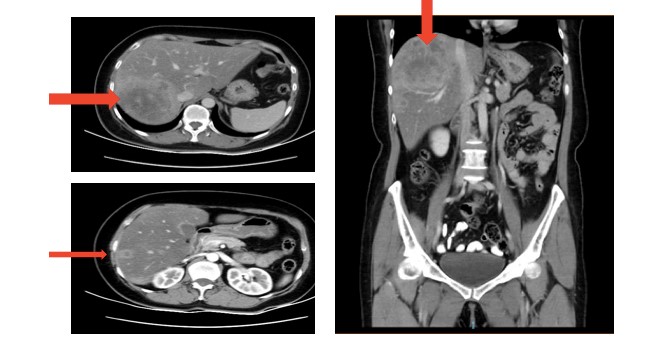
腹部CT(2013年6月)
一线治疗:2013年7月—2015年12月,入组罗氏M028047临床研究:帕妥珠单抗(420mg d1 q21d,首剂 840mg)+曲妥珠单抗(首剂 8mg/kg, 484mg,随后6mg/kg 363mg d1,q21d)+紫杉醇(175mg/m2 270mg d2 q21d)。
疗效评估(图2):3周期SD(缩小25.3%),6周期PR(缩小44.3%),9周期PR(缩小52.7%)。后停用紫杉醇,改为双靶维持治治疗。
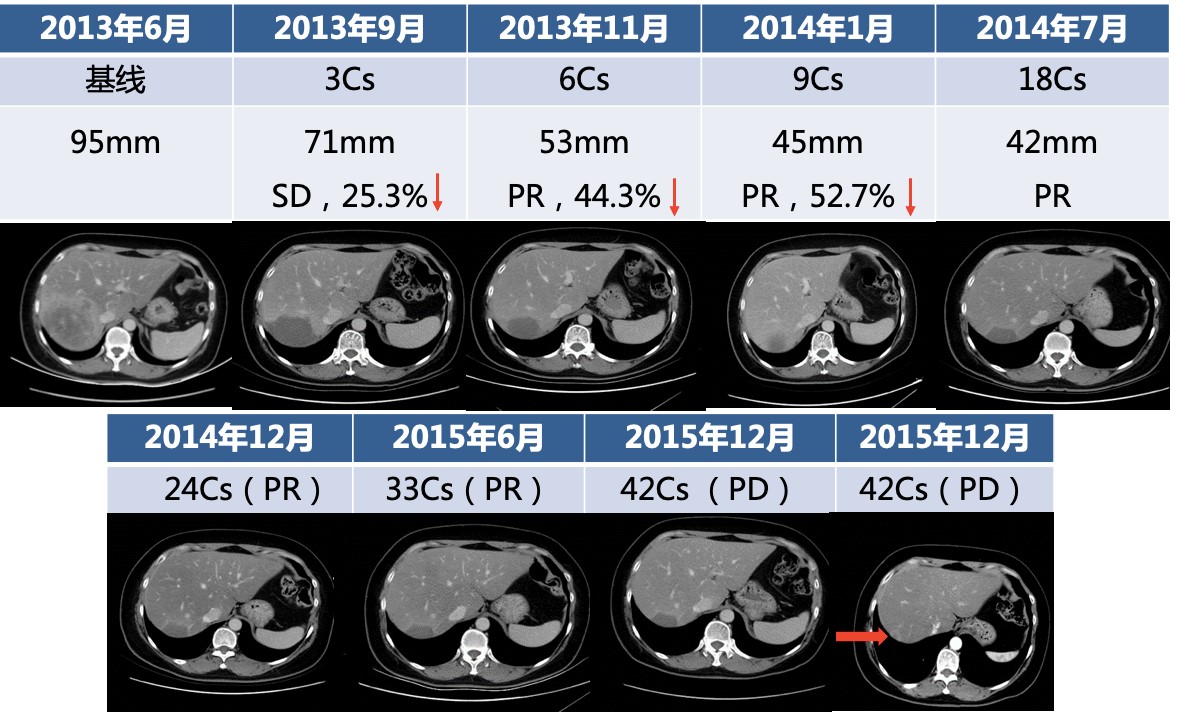
图2 一线治疗定期疗效评价
一线治疗相关不良安全事件分析:
第1周期中性粒细胞Ⅲ度减少,腹泻Ⅱ度(4次/日),手足麻木Ⅰ度
第2、3周期无消化道反应,白细胞Ⅰ度,手足麻木Ⅰ度
第4、5、6周期无骨髓抑制和消化道反应,手足麻木Ⅰ度
第9周期乏力Ⅱ,手足麻木Ⅱ,腹泻Ⅲ,肛周疼痛Ⅱ
第10周期改为双靶向治疗后骨髓抑制0,消化道反应0,手足麻木Ⅰ
EF: 2013年6月:75% (基线),2015年12月,66%(PD出组时)
二次复发转移与二线治疗
2015月12月,发现新发肝转移灶,考虑疾病进展。
一线治疗PFS:2年5个月。
二线治疗及疗效评价:2015年12月—2016年10月,予以EC方案6 周期,疗效评价SD,卡培他滨维持治疗,第2周期因乏力明显减量,4周期复查,疗效评价PD。
三次复发转移与三线治疗
2016年10月,患者再次发现疾病进展。
二线治疗PFS:10个月。
三线治疗及疗效评价:2016年12月,患者入组罗氏M028241临床研究(全球最大的单臂T-DM1 安全性研究,目前已揭盲),予以T-DM1 3.6mg/kg 237.6mg d1 q21d, 4周期评效PR(靶病灶缩小35.6%),8周期PR(缩小54.2%),至今完成41周期治疗,疗效维持PR(图3)。三线治疗相关AE:粒细胞减少I度,转氨酶升高I度,胆红素升高Ⅰ度。
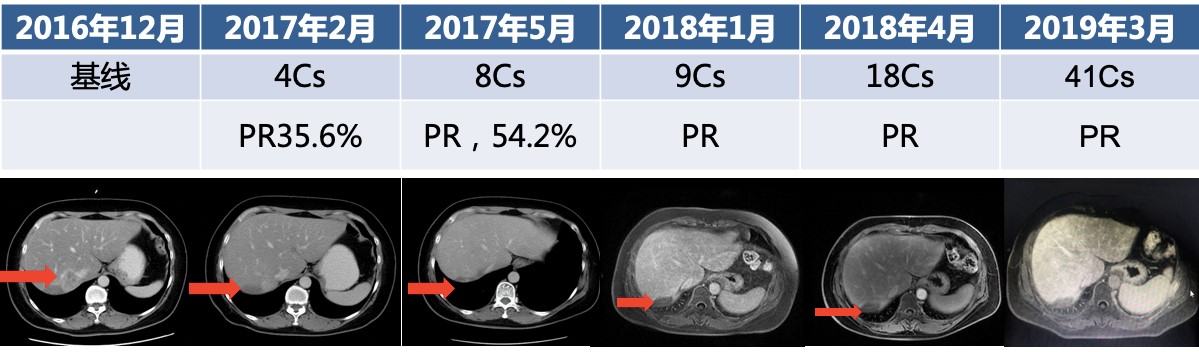
图3 三线治疗定期疗效评价
至今三线治疗PFS:28个月。
至今总生存时间:9年1个月。
点评专家

复旦大学附属肿瘤医院肿瘤内科行政副主任、副主任医师
上海市肿瘤化疗质控中心秘书
中国抗癌协会乳腺癌专业委员会委员
CSCO乳腺癌专家委员会委员
中国研究型医院协会乳腺专业委员会青委会副主任委员
中国研究型医院协会乳腺专业委员会常务委员
CSCO肿瘤支持与康复治疗专家委员会常务委员
CSCO青年专家委员会委员
上海市抗癌协会癌症康复与姑息治疗专业委员会常务委员
上海市抗癌协会青年理事
国家食品药品监督管理总局CDE首批化药临床兼职审评员
JCO中文版(泌尿男生殖系统肿瘤专刊)编委
《中华乳腺病杂志》中青年编委
《Precision Cancer Medicine》青年编委
《中国癌症杂志》青年编委

复旦大学附属肿瘤医院肿瘤内科
点评
患者为中年女性,已绝经。根据手术及术后病理结果,诊断为:右乳浸润性癌术后(pTxN1M0,HER2过表达型)。患者的辅助治疗存在值得商榷之处,术后3年即出现肝内多发转移,但幸运的是晚期一线治疗使用曲妥珠单抗+帕妥珠单抗联合化疗的双靶方案,二线抗HER2治疗使用T-DM1,截至2019年4月OS已达9年1个月,获益明显,且耐受良好。
1、抗HER2 治疗在辅助治疗中的重要地位
根据《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019版、NCCN乳腺癌诊疗指南2019V1版等,对于HR阴性、HER2阳性、同时伴有淋巴结转移的乳腺癌患者,辅助治疗均建议予以紫杉类±蒽环类+抗HER2治疗,后续再进行辅助放疗。抗HER2治疗是HER2阳性乳腺癌治疗成功的关键或者基础,无论是HERA[1]研究、NSABPB-31/NSABP-9831[2]研究,还是BCIRG006[3]研究,均提示术后辅助治疗使用曲妥珠单抗可显著降低复发和病死风险。同时,帕妥珠单抗近期已在国内上市,对于高复发风险患者,可考虑使用双靶联合化疗的辅助治疗。APHINITY[4]研究结果显示,与使用含曲妥珠单抗的方案相比,使用含帕妥珠单抗和曲妥珠单抗的双靶向治疗方案能够降低 19% 的 iDFS 事件(HR=0.81;95%CI 0.66~1.00; P=0.045),其中淋巴结阳性患者和激素受体阴性患者从治疗中获益最多。该患者未行辅助放疗,HR阴性但仍使用内分泌治疗,辅助治疗可以更为规范。同时,该患者术后1年半才行抗HER2靶向治疗,不符合规范治疗,但HERA研究提示辅助治疗延迟使用曲妥珠单抗仍获益,对于辅助化疗已经结束但尚未出现复发转移的患者,五年内仍可以考虑使用曲妥珠单抗,因此该患者后续加上曲妥珠单抗尽管不甚规范但患者预计也是有获益的。
2、一线双靶抗HER2治疗
2013年6月患者腹部CT及PET/CT提示肝转移,DFI为39个月。根据《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019版,对辅助阶段曲妥珠单抗治疗进展后的患者,需要根据疾病复发的时间和治疗情况考虑后进行治疗决策。如果患者在完成以曲妥珠单抗为基础的辅助治疗12 个月内复发或在曲妥珠单抗辅助治疗期间复发,临床医生应该遵循晚期二线抗HER2 的治疗;如果患者12 个月后复发,临床医生应该遵循晚期一线抗HER2 治疗,继续曲妥珠单抗为基础的治疗。该患者在完成曲妥珠单抗治疗的10个月后复发,但由于患者开始曲妥珠单抗的治疗时间晚,因此接受一线抗HER2治疗也是合理的。H0648g[5]和M77001[6]研究已证实在紫杉类基础上联合曲妥珠单抗治疗能够显著提高PFS和OS,确立了曲妥珠单抗联合紫杉类在一线标准治疗的地位。后续的CLEOPATRA[7]研究提示相较于曲妥珠单抗+多西他赛而言,帕妥珠单抗+曲妥珠单抗+多西他赛延长了PFS与OS,因此有条件的患者可予以双靶一线治疗。据此在《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019版中,双靶联合多西他赛方案在HER2阳性晚期乳腺癌抗HER2一线治疗推荐中证据级别为1A。现在帕妥珠单抗亦在中国上市,中国患者也可选择双靶抗HER2治疗,曲妥珠单抗已经进入医保,未来若帕妥珠单抗能够进入医保,将有更多患者从中获益。
目前复发/转移性乳腺癌的治愈很难,需要采取“细水长流,延年益寿”的策略,因此维持治疗也同样重要。根据《中国晚期乳腺癌维持治疗专家共识》[8],接受规范的一线化疗(通常 6~8 个周期)后达到疾病控制的晚期乳腺癌患者,可通过延长药物治疗时间提高PFS。CLEOPATRA 研究表明,帕妥珠单抗联合曲妥珠单抗,在联合化疗结束后继续使用至疾病进展,能显著提高患者的 PFS 与 OS,且并未增加心脏毒性。本病例中,患者使用双靶联合紫杉醇后序双靶维持的方案治疗,最佳疗效PR,PFS长达29个月,获益明显,是充分理解指南与将理论与实际相结合的很好例证。
3、一线抗HER2 治疗进展后,二线仍需注重抗HER2 治疗
一线曲妥珠单抗疾病进展后,推荐二线继续使用抗HER2靶向治疗,因为持续抑制HER2通路能够持续带来生存获益。但患者的二线治疗未使用抗HER2治疗,仅10个月后便再次发现疾病进展,充分印证了临床中抗HER2治疗的重要意义。因此当一线抗HER2治疗进展后临床医师应遵循晚期二线抗HER2治疗。T-DM1[9]是二线抗HER2治疗首选的方案,当T-DM1无法获得时可选择曲妥珠单抗联合另一种化疗药物、拉帕替尼联合卡培他滨、吡咯替尼联合卡培他滨、曲妥珠单抗联合拉帕替尼双靶都是可选方案。T-DM1是一种抗体药物偶联物,该药由细胞毒类药物DM1通过稳定的硫醚连接基团缀合与曲妥珠单抗而成,其目的是锁定HER2并抑制其发出信号,并将化疗药直接释放到HER2阳性的癌细胞内。EMILIA研究[10]确定了T-DM1二线抗HER2治疗的新标准,T-DM1对比拉帕替尼+卡培他滨,PFS分别为9.6个月和6.4个月(P<0.001),OS分别为30.9个月和25.1个月(P<0.001),PFS与OS均有获益。T-DM1目前尚未在国内上市,该患者在三线治疗时幸运地入组T-DM1临床研究,目前已完成41周期的治疗,PFS长达28个月,获益显著。
4、总结
整体而言,该HER2阳性晚期乳腺癌患者在辅助治疗中虽有遗憾,很幸运地在后期治疗中能用上新一代抗HER2靶向药物:如帕妥珠单抗,T-DM1等,最终取得了较为满意的临床获益。因此在临床工作中应充分强调抗HER2治疗的必要性、重要性和长期性。
[1]Gianni Luca,Dafni Urania,Gelber Richard D et al. Treatment with trastuzumab for 1 year after adjuvant chemotherapy in patients with HER2-positive early breast cancer: a 4-year follow-up of a randomised controlled trial.[J] .Lancet Oncol., 2011, 12: 236-44.
[2]Perez Edith A,Jenkins Robert B,Dueck Amylou C et al. C-MYC alterations and association with patient outcome in early-stage HER2-positive breast cancer from the north central cancer treatment group N9831 adjuvant trastuzumab trial.[J] .J. Clin. Oncol., 2011, 29: 651-9.
[3]Slamon Dennis,Eiermann Wolfgang,Robert Nicholas et al. Adjuvant trastuzumab in HER2-positive breast cancer.[J] .N. Engl. J. Med., 2011, 365: 1273-83.
[4]Minckwitz G, Procter M, Azambuja E, et al. APHINITY Steering Committee and Investigators. Adjuvant Pertuzumab and Trastuzumab in Early HER2-Positive Breast Cancer.[J]. N Engl J Med. 2017 Jul 13;377(2):122-131.
[5]Slamon D J,Leyland-Jones B,Shak S et al. Use of chemotherapy plus a monoclonal antibody against HER2 for metastatic breast cancer that overexpresses HER2.[J] .N. Engl. J. Med., 2001, 344: 783-92.
[6]Marty M, Cognetti F, Maraninchi D, et al. Randomized phase II trial of the efficacy and safety of trastuzumab combined with docetaxel in patients with human epidermal growth factor receptor 2-positive metastatic breast cancer administered as first-line treatment: The M77001 study group[J]. J Clin Oncol. 2005;23(19):4265-4274.
[7]Miles D,Im Y-H,Fung A et al. Effect of docetaxel duration on clinical outcomes: exploratory analysis of CLEOPATRA, a phase III randomized controlled trial.[J] .Ann. Oncol., 2017, 28: 2761-2767.
[8]徐兵河,王树森,江泽飞,邵志敏.中国晚期乳腺癌维持治疗专家共识[J].中华普通外科学文献(电子版),2018,12(01):1-5.
[9]Verma Sunil,Miles David,Gianni Luca et al. Trastuzumab emtansine for HER2-positive advanced breast cancer.[J] .N. Engl. J. Med., 2012, 367: 1783-91.











 苏公网安备32059002004080号
苏公网安备32059002004080号


