
第49例
早期乳腺癌患者中30%~40%可发展为晚期乳腺癌(advanced breast cancer,ABC),5年生存率约20%。ABC患者的总体中位生存期为2~3年,不同分子亚型的情况有所不同。对于HER2阳性晚期乳腺癌患者,抗HER2治疗改变了HER2阳性乳腺癌的自然病程,并显著延长了生存时间。本文通过回顾一个具有辅助治疗阶段未使用曲妥珠单抗,复发转移后一线使用曲妥珠单抗+帕妥珠单抗双靶联合治疗并长期获益的病例,介绍目前有关该类患者的临床治疗思路。

浙江省肿瘤医院院长助理、乳腺肿瘤内科主任
中国抗癌协会乳腺癌专业委员会常委
中国临床肿瘤学会乳腺癌专家委员会常委
浙江省抗癌协会乳腺癌专业委员会候任主任委员
浙江省抗癌协会肿瘤内科专业委员会主任委员
浙江省转化医学学会精准医学分会会长

浙江省肿瘤医院
院“1022”人才培养第二层次
浙江省免疫学会青年委员会副主任委员
中国医药教育协会乳腺疾病专业委员会乳腺癌多学科诊疗学组委员
浙江省抗癌协会肿瘤内科专业委员会青年委员
浙江省数理医学肿瘤精准诊治专业委员会委员
浙江省医学会疼痛学分会青年委员会委员
JCO中文版乳腺肿瘤专刊青年编委
浙江省自然科学基金评审专家
基本情况
患者女性,1963年8月27日出生,初诊年龄45岁。2008年9月,因“发现左乳腺肿块1周”至外院就诊。外院体检:肿块约4.6cm,腋窝淋巴结未及明显肿大。左乳肿块穿刺病理示:(左乳腺)浸润性导管癌。IHC示:ER(-)、PR(-)、HER2 (3+)。
外院予以 “TEC”方案治疗4周期,疗效评价为部分缓解(partial response,PR)。于2008年12月27日行左乳腺癌改良根治术。术后病理示:(左乳腺)浸润性导管癌,乳头及基底切缘阴性,左腋下淋巴结20枚均阴性。IHC:ER(-)、PR(-)、 HER2 (3+)、PCNA(+)。
诊断:左乳浸润性导管癌cT2N0M0,ⅡA期,HER2阳性型。
术后继续予以TEC方案辅助治疗2周期,未行抗HER2治疗。
一线治疗
2010年3月,患者复查发现胸骨转移,无病生存期(disease free survival,DFS)约15个月。
胸骨活检病理示: ER(-)、PR(-)、 HER2 (3+)、Ki-67(40%,+)。
未发现肺、肝、脑等远处转移情况。
2010年4月16日,患者诊断为乳腺癌术后,骨转移入组WO20698临床研究,于2010年4月22日使用THP方案(多西他赛+曲妥珠单抗+帕妥珠单抗)9周期后,HP方案(曲妥珠单抗+帕妥珠单抗)维持治疗21周期。2010年4月19日,予以唑来膦酸抗骨转移治疗(图1、图2)。
疗效评价病情稳定(stable disease,SD)。

图1 2010年8月23日 CT检查

图2 2010年8月 ECT检查
不良反应监测:未发现明显心脏毒性(图3)。治疗期间出现双下肢Ⅰ度浮肿,考虑与多西他赛相关。后患者由于自身原因自行退出临床研究,终止治疗,定期随访。
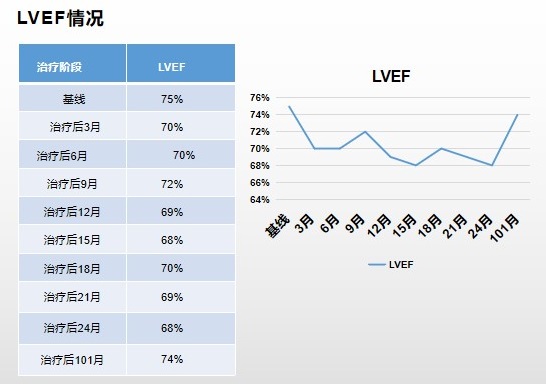
图3 心超LVEF监测情况
复发后二线治疗
2018年8月,患者发现胸骨处隆起明显,并伴有疼痛,NRS评分3分。于2019年9月1日查胸部增强CT,结果示:胸骨、右侧第1、2肋骨骨质破坏,伴软组织影,考虑转移,右侧胸小肌后方结节影,右侧腋窝多发小淋巴结,双肺散在纤维灶,肝脏多发囊肿(图4)。附见,甲状腺右叶低密度影,建议结合其他检查。B超显示:甲状腺右叶结节,BI-RADS 3类。

图4 胸部CT(2018年9月)
临床试验揭盲发现患者为“帕妥珠单抗+曲妥珠单抗+多西他赛”治疗组。
一线PH联合多西他赛解救治疗+PH维持治疗,肿瘤无进展生存期(progression-free survival, PFS)达8年5个月。
2018年9月诊断为乳腺癌术后,骨转移伴软组织肿块,改用NH方案(曲妥珠单抗+长春瑞滨),目前情况均良好。
至今,患者总生存时间10年7个月。
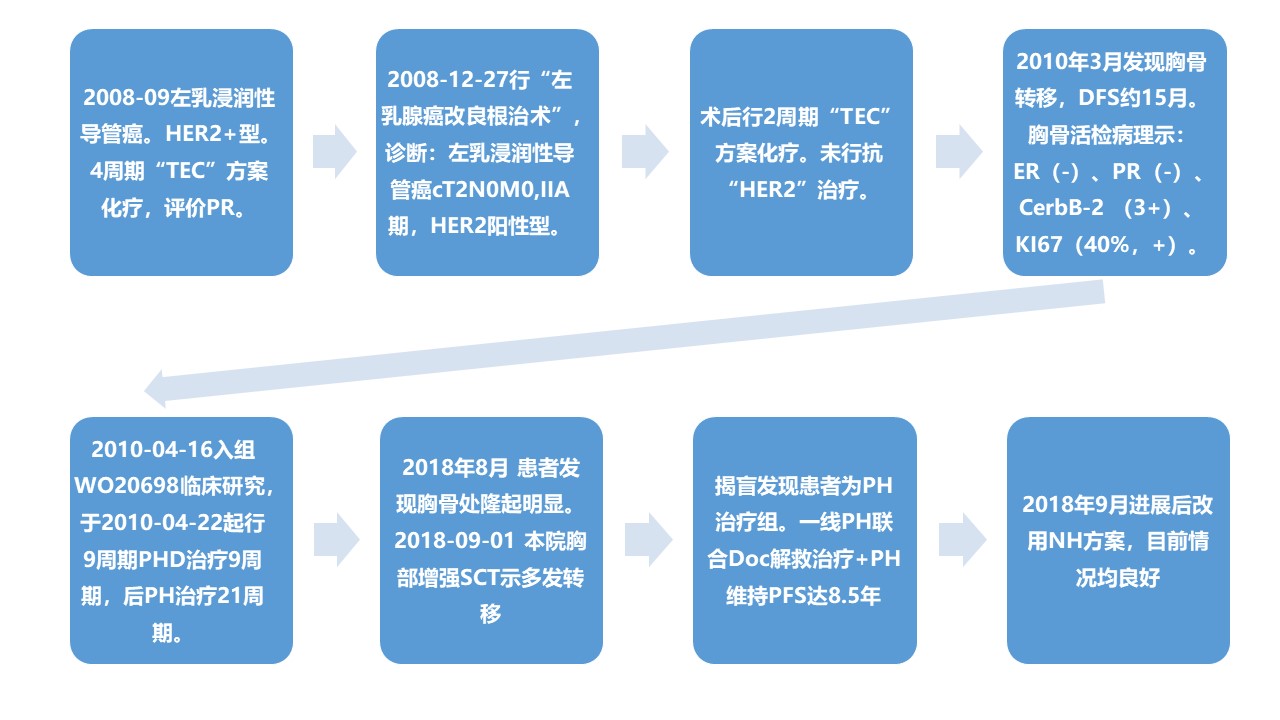
治疗历程图
点评专家

复旦大学附属肿瘤医院肿瘤内科主任 临床试验机构常务副主任 博士研究生导师
ESMO乳腺癌Faculty Member
ABC5 panelist
中国抗癌协会多原发和不明原发肿瘤专委会主委
上海市化疗质控中心主任
中国研究型医院学会乳腺专委会副主委
中国抗癌协会乳腺癌专委会常委兼秘书长
上海抗癌协会癌症康复和姑息治疗专委会主委
国家食品药品监督管理局审评中心审评专家
中国抗癌协会癌症康复和姑息治疗委员会常务委员
国家食品药品监督管理局审评中心审评专家
点评
该病例为初诊cT2N0M0,ⅡA期,分子分型为HER2阳性型。患者在新辅助/辅助治疗阶段未使用抗HER2治疗,但第一次进展后使用曲妥珠单抗+帕妥珠单抗联合化疗这样的双靶方案获益长达8年5个月,二线治疗持续抗HER2治疗目前仍旧获益,且耐受性良好。
1. HER2阳性乳腺癌患者新辅助治疗应及早进行抗HER2治疗
患者分子分型为HER2阳性型,《中国抗癌协会乳腺癌诊治指南与规范(2017年版)》建议对于HER2阳性乳腺癌患者新辅助治疗阶段应该加用抗HER2药物,而HER2阳性乳腺癌患者新辅助获得pCR与长期预后相关性较强。《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019版也指出:临床研究证实,HER2阳性患者新辅助治疗,曲妥珠单抗联合化疗与单用化疗相比能够显著提高病理完全缓解(pCR)率,奠定了曲妥珠单抗在 HER2 阳性乳腺癌新辅助治疗中的标准地位[1]。而曲妥珠单抗+帕妥珠单抗联合化疗这样的双靶方案也是Ⅱ级推荐,1A类证据。推荐来源于NeoSphere 研究[2]证实了曲妥珠单抗和帕妥珠单抗与多西他赛联合进一步提高了pCR率,结果显示帕妥珠单抗+曲妥珠单抗+多西他赛(P+T+D)组病例pCR率为45.8%,而曲妥珠单抗+多西他赛(T+D)组为29.0%(P=0.0141);对于激素受体阴性的患者,在多西他赛联合曲妥珠单抗的基础上加用帕妥珠单抗,可显著提高pCR率,P+T+D组:63.2%,T+D组:36.8%。该患者新辅助治疗阶段未使用抗HER2治疗,可能是DFS时间较短、复发转移较快的可能原因之一。目前帕妥珠单抗已经在国内上市,患者临床可以选择。期待帕妥珠单抗能够进入医保,让更多的患者能够通过医保政策获益。
2.一线治疗双靶合璧,所向披靡
《中国抗癌协会乳腺癌诊治指南与规范(2017年版)》指出,对于HER2阳性乳腺癌晚期一线治疗选择曲妥珠单抗联合的化疗药物和方案有紫杉醇联合或不联合卡铂、多西他赛、长春瑞滨、卡培他滨以及多西他赛+帕妥珠单抗。《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019版亦指出:对于既往未接受过曲妥珠单抗辅助治疗的HER2阳性复发转移乳腺癌,以曲妥珠单抗为基础联合化疗的方案是这部分患者晚期一线治疗标准方案。H0648g[3]和M77001[4]研究证实在紫杉类基础上联合曲妥珠单抗治疗能够显著提高PFS和OS,确立了曲妥珠单抗联合紫杉类在一线标准治疗的地位。CHAT研究[5]证实,对于能够耐受双药化疗的患者,曲妥珠单抗联合多西他赛加卡培他滨,比曲妥珠单抗联合多西他赛效果更好,尤其适用于考虑维持治疗的患者。而曲妥珠单抗联合紫杉醇加卡铂,疗效优于曲妥珠单抗联合紫杉醇。而CLEOPATRA研究[6]则证实,相较于曲妥珠单抗+多西他赛而言,帕妥珠单抗+曲妥珠单抗+多西他赛延长了PFS(18.5个月 vs 12.4个月, P=0.0001)与OS(56.5个月 vs 40.8个月, P=0.0002),因此有条件的患者可予以双靶一线治疗。本病例中,患者使用PHD方案治疗后,评价SD,PFS长达8.5年,治疗获益明显。考虑长PFS原因如下:1.患者复发转移后,仅为胸骨转移,肿瘤负荷小;2.患者分子分型为HER2阳性型,Ki67约40%,多项研究均显示激素受体阴性的患者更能从双靶联合治疗中获益;3.患者为中年女性,耐受力好,可长期接受靶向治疗。
3.二线治疗的选择
《中国抗癌协会乳腺癌诊治指南与规范(2017年版)》和《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019版均指出,曲妥珠单抗治疗进展后,持续抑制HER2通路能够持续带来生存获益。因此一线曲妥珠单抗病情进展后,推荐二线继续使用抗HER2靶向治疗。对于复发转移乳腺癌曲妥珠单抗治疗进展后,需要根据患者既往治疗判断。如果既往治疗有效,因为毒性或经济原因停药,则优先考虑继续使用曲妥珠单抗,换用其他化疗药物[7~8];如果在治疗中进展,才优先考虑更换抗HER2药物。当然HER2阳性乳腺癌二线抗HER2治疗也可以考虑使用T-DM1。该患者一线使用双靶治疗,PFS达到8年5个月,生存获益明显,且长期监测心功能,未发现明显不良反应,后因为个人原因,退出临床试验。因此再次进展仍优先考虑含有曲妥珠单抗的抗HER2方案,并更换化疗药为长春瑞滨。目前仍持续获益。至今总生存时间已经10年7个月。
总结
该患者虽然新辅助/辅助治疗阶段未使用抗HER2治疗,略有遗憾,DFS时间较短,早期出现复发转移,但一线治疗采用了帕妥珠单抗联合曲妥珠单抗+化疗这样的双靶联合化疗的方案获得长期生存获益,总生存时间超过10年,不良反应较轻,效果非常显著,可见对于HER2阳性型患者采用联合靶向治疗优势非常明显,可作为此类患者治疗方案的借鉴。
[1] Buzdar AU, Ibrahim NK, Francis D, et al. Significantly higher pathologic complete remission rate after neoadjuvant therapy with trastuzumab, paclitaxel, and epirubicin chemotherapy: results of a randomized trial in human epidermal growth factor receptor 2-positive operable breast cancer[J]. J Clin Oncol. 2005;23(16):3676-85.
[2] Gianni L, PIENKOWSKI T, Im YH, et al. Efficacy and safety of neoadjuvant pertuzumab and trastuzumab in women with locally advanced, inflammatory, or early HER2-positive breast cancer(NeoSphere):a randomized multicenter, open-label, phase 2 trial [J].Lancet Oncol, 2012,13(1):25-32.
[3] Slamon DJ, Leyland-Jones B, Shark S, et al.Use of chemotherapy plus a monoclonal antibody against HER2 for metastatic breast cancer that overexpresses HER2 [J]. N Engl J Med, 2001,344(11):783-792.
[4] Marty M, Cognetti F, Maraninchi D,et al. Randomized phase Ⅱ trial of the efficacy and safety of trastuzumab combined with docetaxel in patients with human epidermal growth factor receptor 2-positive metastatic breast cancer administered as first-line treatmen: the M77001 study group [J]. J Clin Oncol.2005,23(19):4265-4274.
[5] Wardley AM, Pivot X, Morales-Vasquez F, et al. Randomized phase II trial of first-line trastuzumab plus docetaxel and capecitabine compared with trastuzumab plus docetaxel in HER2-positive metastatic breast cancer. J Clin Oncol. 2010;28(6):976-83.
[6] Swain SM, Kim SB, Cortés J, et al. Pertuzumab, trastuzumab, and docetaxel for HER2-positive metastatic breast cancer (CLEOPATRA study): overall survival results from a randomised, double-blind, placebo-controlled, phase 3 study [J]. Lancet Oncol. 2013;14(6):461-71.
[7] Cameron D,Casey M,Press M,et al. A phase III randomized comparison of lapatinib plus capecitabine versus capecitabine alone in women with advanced breast cancer that has progressed on trastuzumab:updated efficacy and biomarker analyses[J]. Breast Cancer Res Treat,2008,112(3): 533-543.
[8] von Minckwitz G,Du Bois A,Schmidt M,et al. Trastuzumab beyond progression in human epidermal growth factor receptor 2-positive advanced breast cancer:A German Breast Group 26/ Breast International Group 03-05 study[J]. J Clin Oncol,2009,27(12):1999-2006.












 苏公网安备32059002004080号
苏公网安备32059002004080号


