
第43例
乳腺癌是女性发病第一位的肿瘤,目前经过综合治疗后,早期乳腺癌10年生存率有较大的提高,但仍有30%~40%会复发转移。在原发性乳腺癌患者中观察到有25%~30%的患者HER2基因过度表达。而HER2阳性乳腺癌的肿瘤侵袭性更强,预后更差。曲妥珠单抗是抗HER2治疗的标准药物,使用曲妥珠单抗的靶向治疗可以明显改善患者的预后,延长生命并提高生活质量。但是随着患者生命延长,可能出现药物耐药导致疾病进展,此时仍应继续抗HER2治疗,给患者最大获益。本文通过回顾一个自行停用曲妥珠单抗后病情再进展,反复使用曲妥珠单抗获益的病例,介绍目前有关该类患者的临床治疗思路。

江西省肿瘤医院肿瘤综合内科、乳腺内科、癌痛示范化病房
肿瘤与肠道微生物专业委员会会员
基本情况
患者女性,1964年出生。既往体健,适龄婚育,50岁绝经。个人史、家族史无特殊。
首次治疗经过
患者于2013年(49岁)发现左乳肿物, 2014年6月16日行左乳癌改良根治术。术后病理:左乳浸润性导管癌Ⅱ级,6cm×4cm×3cm,基底、乳头、乳头下组织及皮肤切缘阴性,左腋窝淋巴结12/13阳性。免疫组化:ER(-),PR(-),HER2(3+),Ki-67 60%(+,3%)。
▎诊断:左乳浸润性导管癌,pT3N3M0 ⅢC期,分子分型为HR-/HER2+型。
▎辅助治疗:AC×4-T(多西他赛)×4周期(未使用曲妥珠单抗)。不良反应:消化道反应2级,骨髓抑制反应2级。辅助放疗:乳腺辅助放疗50Gy/25次,此后定期复查。
第一次复发
2015年10月15日,患者发现左胸壁红肿伴有皮疹,右乳胀痛(图1),遂进行左胸壁皮疹穿刺细胞学:找见腺癌细胞。右乳穿刺病理及免疫组化:右乳见少许癌。免疫组化:ER(-),PR(-),HER2(2+),Ki-67+,FISH 阳性。2015年11月27日,胸部、上腹部CT平扫未发现内脏转移。诊断:左乳浸润性导管癌术后 Ⅳ期,分子分型HR-/HER2+型;左胸壁复发;右乳转移癌HER2+型。
无病生存期(disease-free survival,DFS)为1年4个月(2014年6月至2015年10月)。
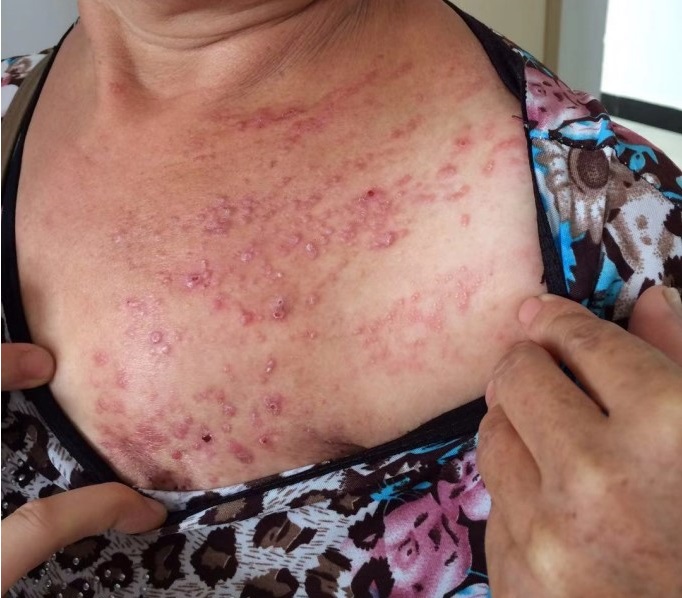
图1 左胸壁复发病灶
▎一线治疗方案
2015年12月至2017年1月,予以HX方案共计6周期,疗效评估为部分缓解(partial response,PR),后续予以HX 12周期,疗效评估接近完全缓解(complete response, CR)。
2017年2月至2017年7月,患者拒绝维持治疗,定期复查,随访。
第二次进展
2017年7月,患者发现右乳肿块再次增大,左胸壁结节再发。
肿瘤无进展生存时间(progression-free survival, PFS)1为20个月。
▎二线治疗
2017年7月至2018年3月,予以NH方案化疗8周期,2、4、6、8周期疗效评价疾病稳定(stable disease, SD)。2018年5月,患者因“心慌、胸闷”不适,自行停用曲妥珠单抗。心脏彩超:二尖瓣、三尖瓣关闭不全,左室舒张功能减退。心电图:室性期前收缩(早搏),不完全性右束支传导阻滞。
2018年5月至2018年9月,予以LX方案(拉帕替尼+卡培他滨)维持治疗,疗效评估为PR。
第三次进展
2018年9月,复查发现右乳肿块、胸壁结节增多增大,肺部新增结节,考虑疾病进展(progressive disease,PD;图2)。
PFS2为14个月。
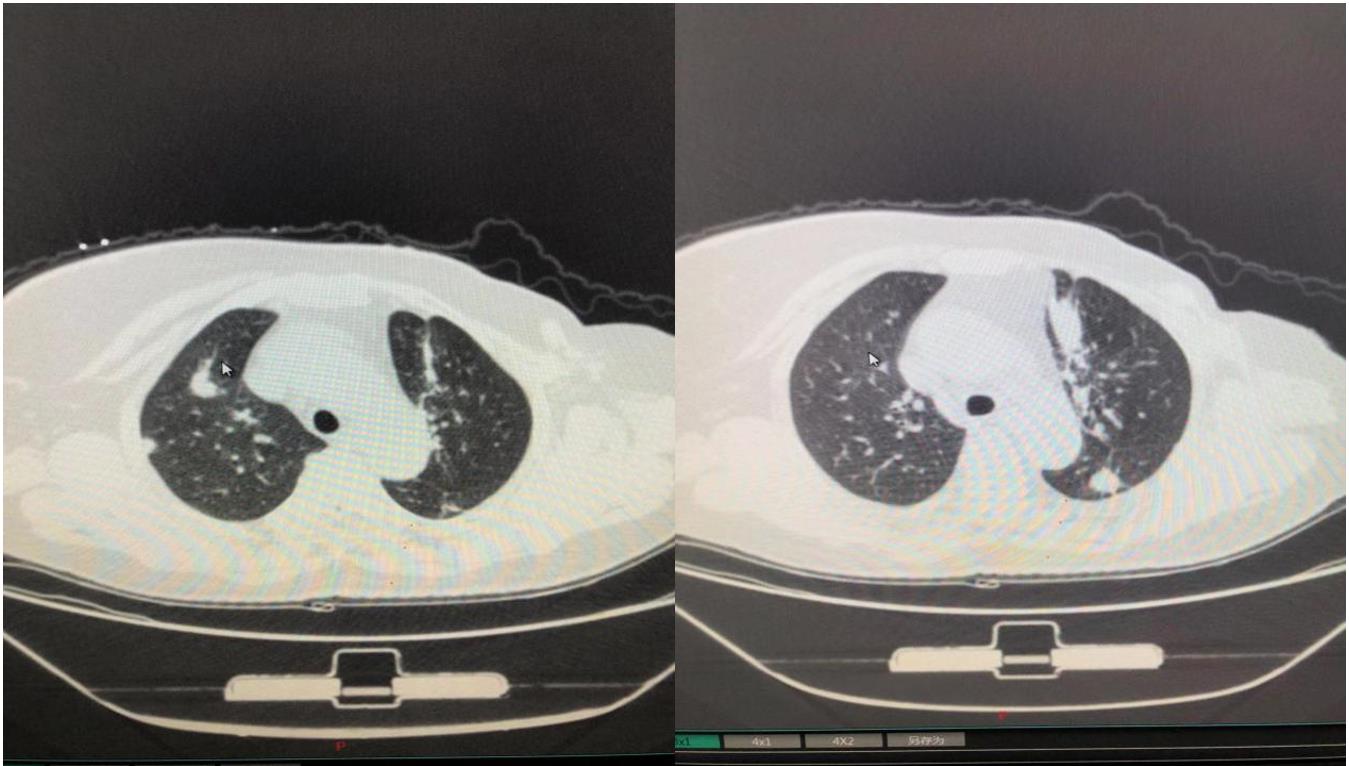
图2 肺部CT提示新增病灶
▎三线治疗
2018年10月开始予以wPH方案治疗,共计8周期,左胸壁皮疹基本消退,右乳肿块缩小。疗效评价PR(图3)。期间监测心脏彩超,2018年10月24日心脏彩超结果示:三尖瓣轻度反流,左室舒张功能减退。2018年11月15日心脏彩超结果示:二尖瓣、三尖瓣轻度关闭不全,左室舒张功能减退。2019年1月3日心脏彩超结果示:左室舒张功能减退。2019年2月25日心脏彩超结果示:二尖瓣、三尖瓣轻度关闭不全,左室舒张功能减退。LVEF波动于58%~65%。持续心脏超声监测未发现严重心脏毒性。
PFS3(至今)为6个月,截至2019年1月,总生存时间(OS)为4年7个月(图4)。
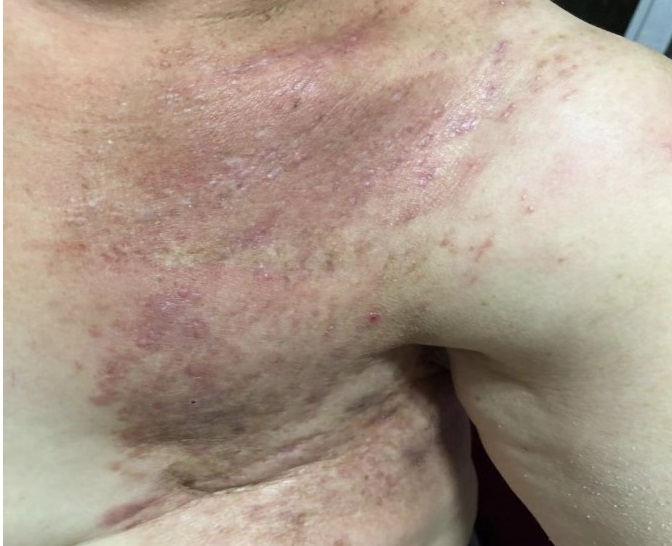
图3 wPH方案2周期治疗后
点评专家

复旦大学附属肿瘤医院肿瘤内科主任
复旦大学附属肿瘤医院药物临床试验机构常务副主任
上海抗癌协会乳腺癌专业委员会副主委
上海市疾病预防控制中心乳腺癌防治专业委员会副主委
中国抗癌协会乳腺癌专业委员会常委兼秘书长
中国抗癌协会癌症康复和姑息治疗委员会常务委员
国家食品药品监督管理总局审评中心审评专家
点评
该病例初诊分期为局部晚期pT3N3M0,ⅢC期,分子分型为HR-/HER2+型。经治疗后多次复发,其间曾改自行停用曲妥珠单抗抗HER2治疗,因疾病进展后再次使用,至今为止OS已达4年7个月,获益明显。截至目前未见再次复发转移。
1.抗HER2治疗是HER2阳性乳腺癌患者治疗成功的关键
患者术后分子分型为HER2阳性型,HERA研究[1]证实曲妥珠单抗用于HER2阳性早期乳腺癌术后辅助治疗,显著提高HER2阳性早期乳腺癌治愈机会,显著降低复发和病死风险,B-31/NSABP-9831、BCIRG 006等均提示对于HER2阳性乳腺癌患者,术后辅助治疗使用曲妥珠单抗可显著降低复发和病死风险。但患者未进行抗HER2治疗,仅给予AC序贯T方案化疗。因此治疗结束1年后出现了复发转移。
2015年出现胸壁及右乳的复发转移,提示分子分型为HER2阳性HR阴性型。根据《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2018 V1版指出:对于既往未接受过曲妥珠单抗辅助治疗的HER2阳性复发转移乳腺癌,以曲妥珠单抗为基础联合化疗的方案是这部分患者晚期一线治疗标准方案。H0648g和M77001研究证实在紫杉类基础上联合曲妥珠单抗治疗能够显著提高PFS和OS,确立了曲妥珠单抗联合紫杉类在一线标准治疗的地位。CLEOPATRA研究则证实,帕妥珠单抗+曲妥珠单抗的PH双靶一线治疗,延长了HER2阳性乳腺癌患者的PFS(18.5个月 vs 12.4个月)。目前帕妥珠单抗已在国内上市,一线治疗也可考虑双靶方案。《HER2阳性乳腺癌临床诊疗专家共识》指出:紫杉类化疗药物治疗失败的HER2阳性乳腺癌,曲妥珠单抗可以联合长春瑞滨[2]、铂类、卡培他滨[3]、吉西他滨[4]等其他化疗药物。研究显示 [3],曲妥珠单抗+卡培他滨联合治疗后中位OS达到 6.9个月。本例患者一线使用HX方案18周期后未进一步维持治疗,PFS达20个月,评价为PR,获益明显。可知,对于HER2阳性乳腺癌而言,抗HER2治疗是获益的关键。
2.一线抗HER2治疗进展后,二线仍需注重抗HER2治疗
曲妥珠单抗治疗进展后,持续抑制HER2通路能够持续带来生存获益。因此一线曲妥珠单抗治疗病情进展后,二线继续使用抗HER2靶向治疗。根据《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2018 V1版指出:如果既往治疗有效,因为毒性或经济原因停药,则优先考虑继续使用曲妥珠单抗,换用其他化疗药。本病例中使用了NH方案,GBG26/BIG03-05随机临床试验[5]显示,卡培他滨组的中位进展时间为5.6个月,卡培他滨+曲妥珠单抗组为8.2个月;卡培他滨组OS率为20.4个月(95% CI,17.8~24.7),卡培他滨组为25.5个月(95% CI,19.0~30.7)。本例患者使用8周期,约9个月后出现心脏毒性反应,病情并未明显进展,可知已明显获益。2018年10月再次出现复发进展后,继续使用曲妥珠单抗抗HER2治疗,仍可获益。由此可知,持续抗HER2是HER2阳性乳腺癌治疗成功的关键。
3.警惕药物的心脏毒性,持续监测是关键
本病例中,使用曲妥珠单抗抗HER2期间曾出现明显心脏毒性反应,心脏彩超:二尖瓣、三尖瓣关闭不全,左室舒张功能减退。心电图:室性期前收缩(早搏),不完全性右束支传导阻滞。心脏毒性是曲妥珠单抗最主要的不良反应。高龄患者、既往心脏病史、胸部放疗史、蒽环类药物使用史都会增加曲妥珠单抗的心脏毒性。因此在首次使用曲妥珠单抗之前,应充分评估患者的心功能,包括病史、体格检查以及通过超声心动图或放射性心血管造影扫描检查测定LVEF值。 治疗期间每3个月,以及治疗结束后进行LVEF复测。对LVEF相对治疗前绝对降低≥16% 或者 LVEF低于正常值范围且相对治疗前绝对降低≥10% 时,应停止曲妥珠单抗治疗。本例患者2018年5月因胸闷不适自行停用曲妥珠单抗,但未知具体下降指标。此后2018年10月再次使用曲妥珠单抗后复查心脏彩超LVEF为60%,已恢复正常,按原则可继续使用曲妥珠单抗。此后多次复查,最低时为58%,较未使用曲妥珠单抗时未降低超过10%,且患者无明显心力衰竭症状,控制良好。
4.本病例治疗的经验及不足
本例患者目前OS为4年7个月,治疗获益明显。治疗经过显示,在持续抗HER2治疗后,患者持续获益,复发至今的生存时间已达3年7个月,目前病情仍未进展。对于HER2阳性患者而言,抗HER2治疗非常必要。
本例患者围手术期的治疗不足,术前未充分评估分期情况,未进行新辅助治疗;术后明确分子分型后未进行抗HER2治疗,若能够尽早抗HER2治疗,可能可以有更长的DFS;患者中途因心脏毒性自行停药,抗HER2持续治疗中断,可能也与患者疾病进展相关。
整体而言,本例患者治疗及时、有效。治疗过程中虽然存在部分不足与遗憾,但最后治疗的获益非常明显,值得临床借鉴。
1.Cameron D , Piccart-Gebhart M J , Gelber R D , et al. 11 years’follow-up of trastuzumab after adjuvant chemotherapy in HER2-positive early breast cancer: final analysis of the HERceptin Adjuvant (HERA) trial[J]. The Lancet, 2017, 389(10075):1195-1205.
2. Papaldo P, Fabi A, Ferretti G, et al. A phase II study on metastatic breast cancer patients treated with weekly vinorelbine with or without trastuzumab according to HER2 expression: changing the natural history of HER2-positive disease[J]. Ann Oncol. ,2006,17(4):630-636.
3. Harder J, Ihorst G, Heinemann V, et al. Multicentre phase II trial of trastuzumab and capecitabine in patients with HER2 overexpressing metastatic pancreatic cancer[J]. Br J Cancer,2012,106(6):1033-1038.
4. Yardley DA, Burris HA, Hanson S, et al. Weekly gemcitabine and trastuzumab in the treatment of patients with HER2-overexpressing metastatic breast cancer[J]. Clin Breast Cancer,2009,9(3):178-183.
5.Tripathy D. Trastuzumab beyond progression in human epidermal growth factor receptor 2–positive advanced breast cancer: a German Breast Group 26/Breast International Group 03-05 Study[J]. Journal of Clinical Oncology, 2009, 20(4):420-422.











 苏公网安备32059002004080号
苏公网安备32059002004080号


