2026年中国临床肿瘤学会(CSCO)指南会于2026年4月24~25日在哈尔滨盛大召开。此次盛会由CSCO与北京市希思科临床肿瘤学研究基金会联袂主办,汇聚了国内肿瘤学领域的知名专家学者,共襄学术盛举。
本届指南会上,复旦大学附属中山医院胡洁教授、解放军总医院汪进良教授以及中国医学科学院肿瘤医院毕楠教授,分别从病理及分子病理、内科和放疗三个部分讲解了2026版《CSCO小细胞肺癌诊疗指南》更新及相关研究进展。本文特整理本次更新核心内容,帮助广大肿瘤医生共同学习。
病理及分子病理
病理学诊断
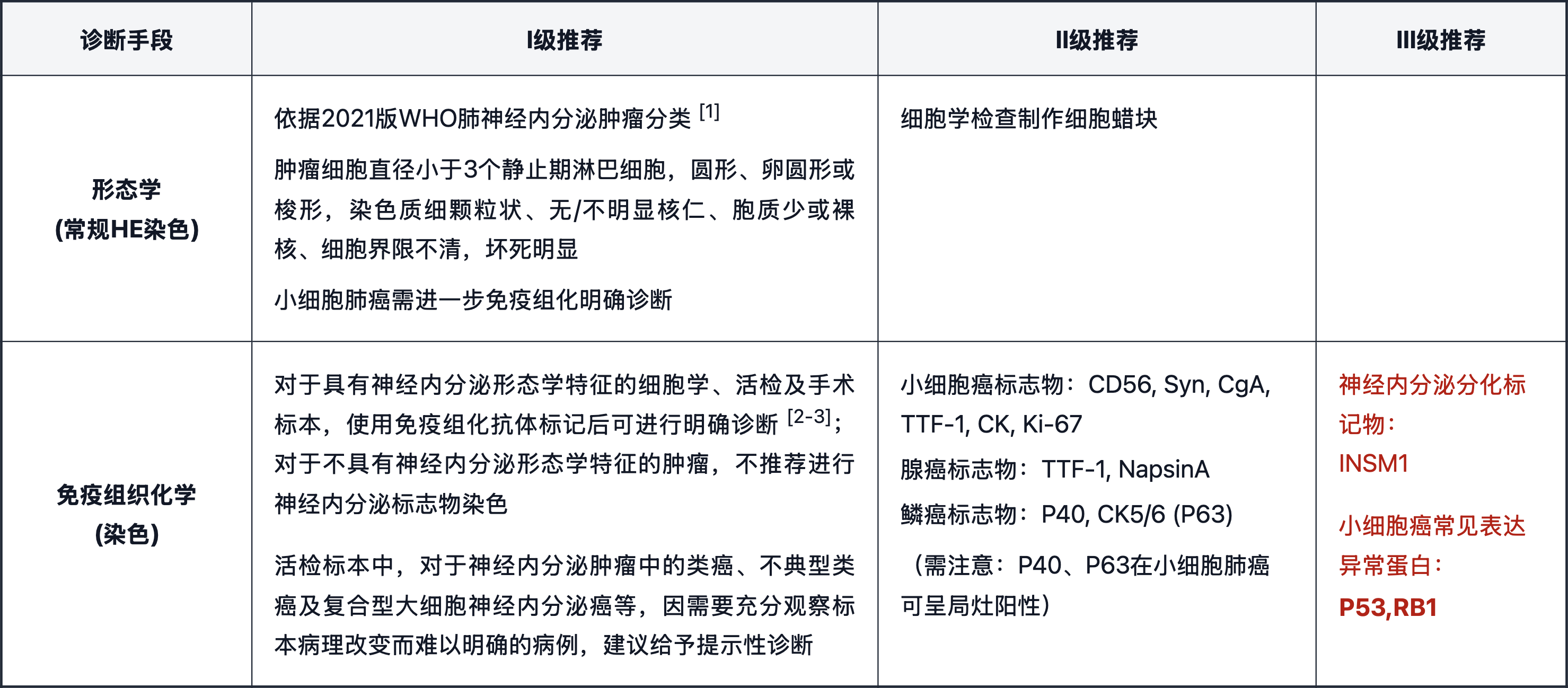
本次病理学诊断更新主要集中在免疫组织化学(IHC)诊断标志物的推荐以及病理诊断报告原则的完善。
1. 免疫组织化学诊断更新
【新增】神经内分泌分化标记物推荐:INSM1。
注:INSM1区分肺高级别神经内分泌癌与其他肺癌亚型的敏感性为86%,特异性为97%,为细胞核染色。
【新增】异常蛋白表达提示:小细胞肺癌常见表达异常蛋白P53和RB1。
注:P53“过度表达型”和“完全缺失型”均为异常表达;RB1表达完全缺失提示RB1失活,采用联合判读可高度提示SCLC诊断。
2. 小细胞肺癌病理诊断报告原则更新
在病理诊断报告中,新版指南对报告原则中的必备信息和可选信息提出了新的关注点,如下表红字所示: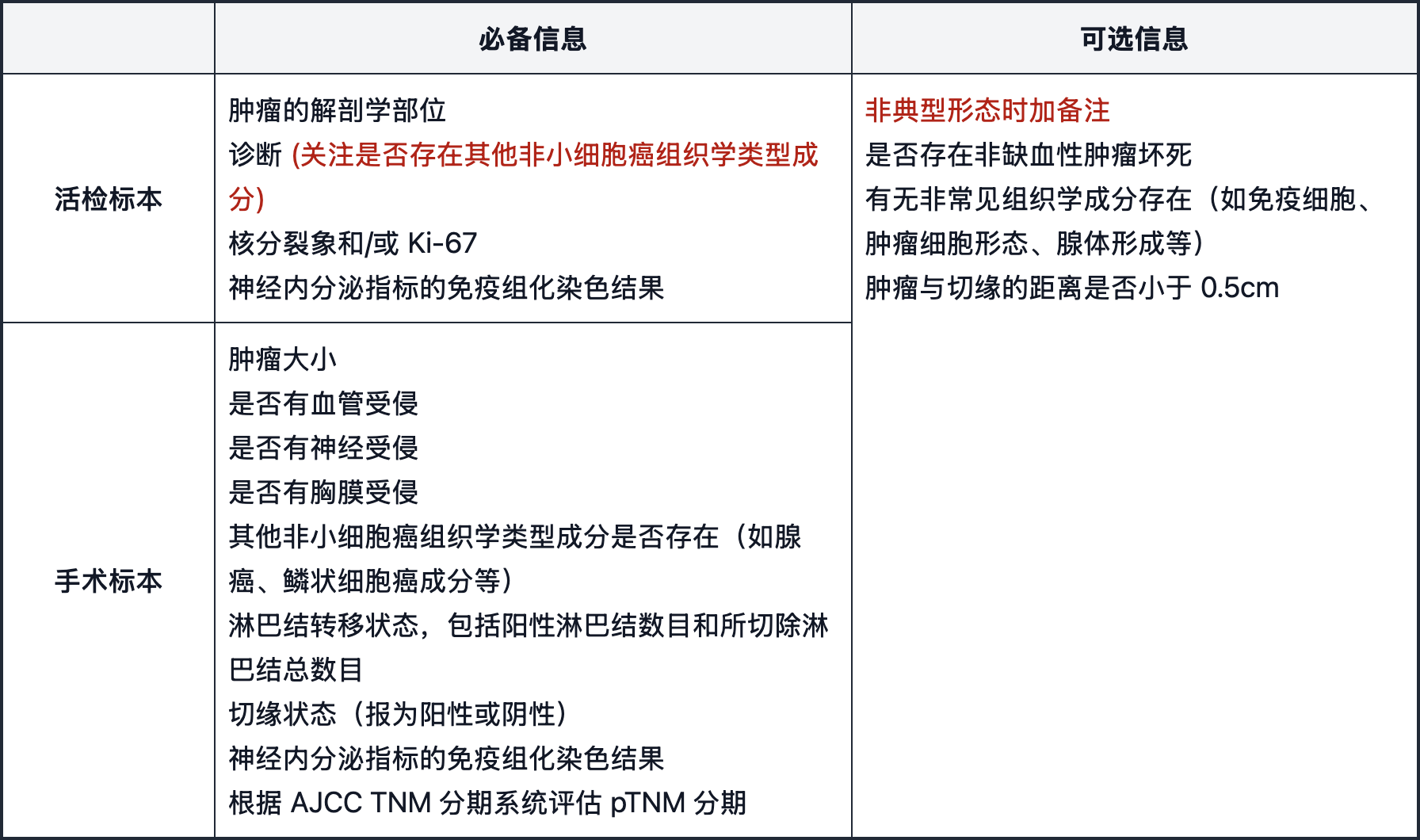
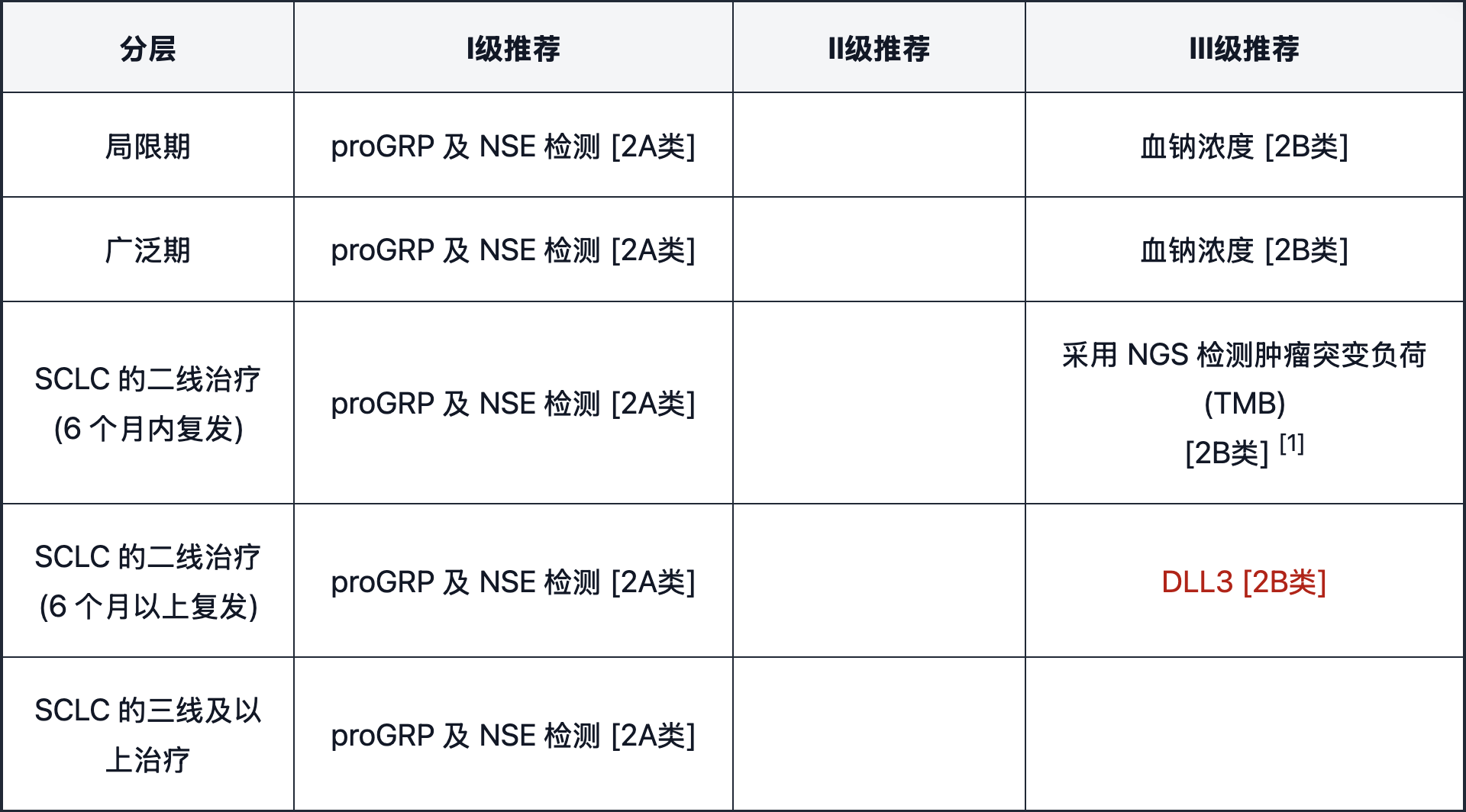
分子标志物
分子标志物部分,新版指南主要针对晚期/复发患者的靶向药物或指导治疗的标志物进行了更新,重点增加了DLL3靶点的推荐。DLL3在85%-96%的SCLC细胞表面高表达,在原发灶与转移灶表达一致性高,是兼具SCLC诊断与治疗价值的理想靶点。
然而,DeLLphi-301研究中,未检测DLL3表达以及DLL3阴性的患者接受DLL3/CD3双特异性T细胞衔接器治疗后,也表现出临床获益。DLL3能否作为可靠疗效预测标志物,尚待检测技术标准化与更大规模前瞻性临床研究的验证。
【注释更新】
分子标志物的【注释】模块中新增了多个探索性治疗靶点和联合分析新证据的描述:
DLL3靶点
SEZ6靶点
B7H3靶点
MHC-I相关特征与免疫治疗
外周血蛋白组学新证据
多组学联合分析新证据
内科
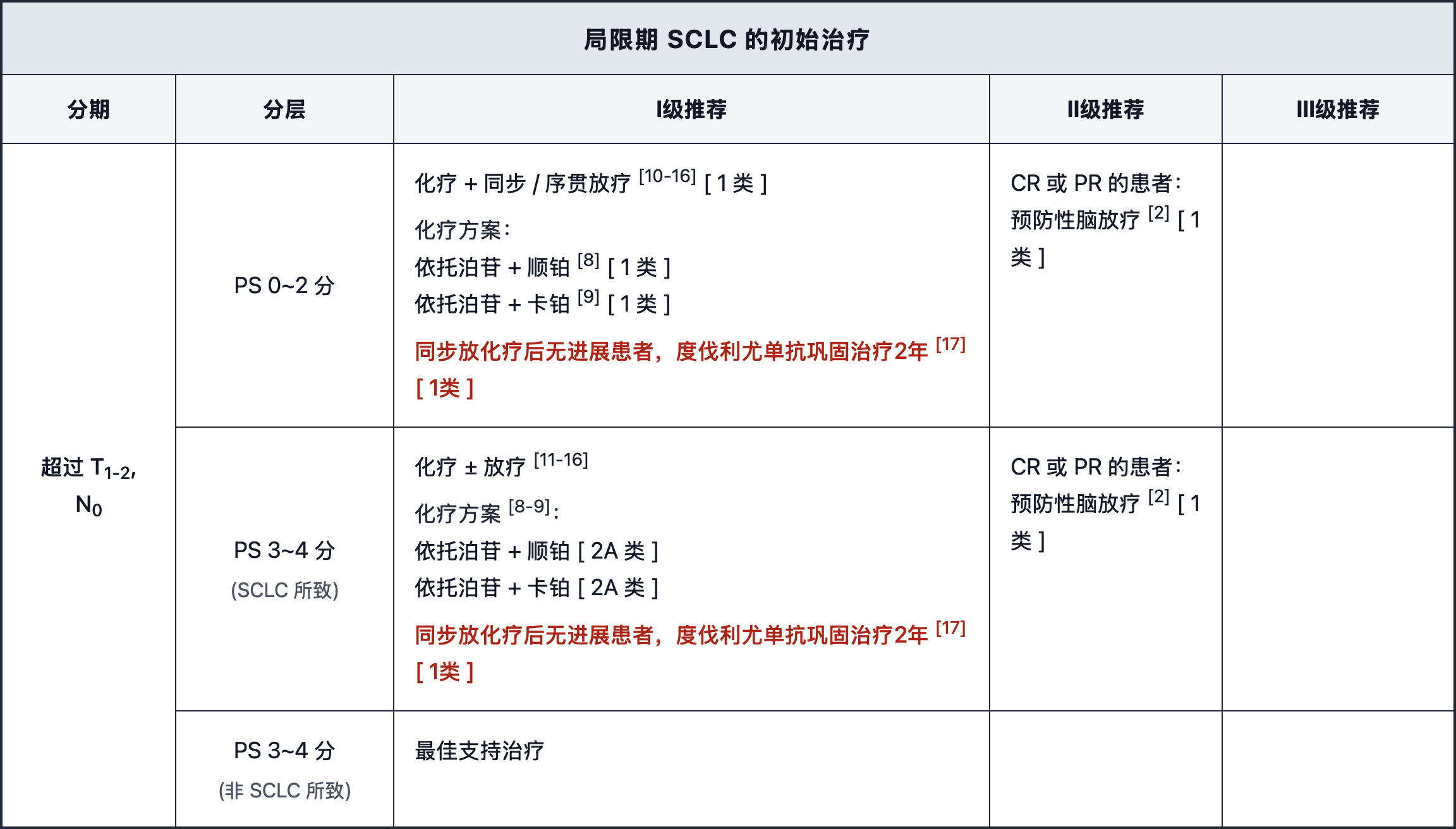
局限期 SCLC 更新要点
对于局限期小细胞肺癌的初始治疗,更新主要集中在超过T1-2, N0分期的患者:
T1-2, N0阶段:无更新。
超过T1-2, N0阶段:对于接受同步放化疗后无进展的患者,将“度伐利尤单抗巩固治疗2年”上调为Ⅰ级推荐(1类证据)。
注:2025年5月,NMPA批准度伐利尤单抗用于在接受铂类药物为基础的放化疗后未出现疾病进展的LS-SCLC成人患者的治疗。
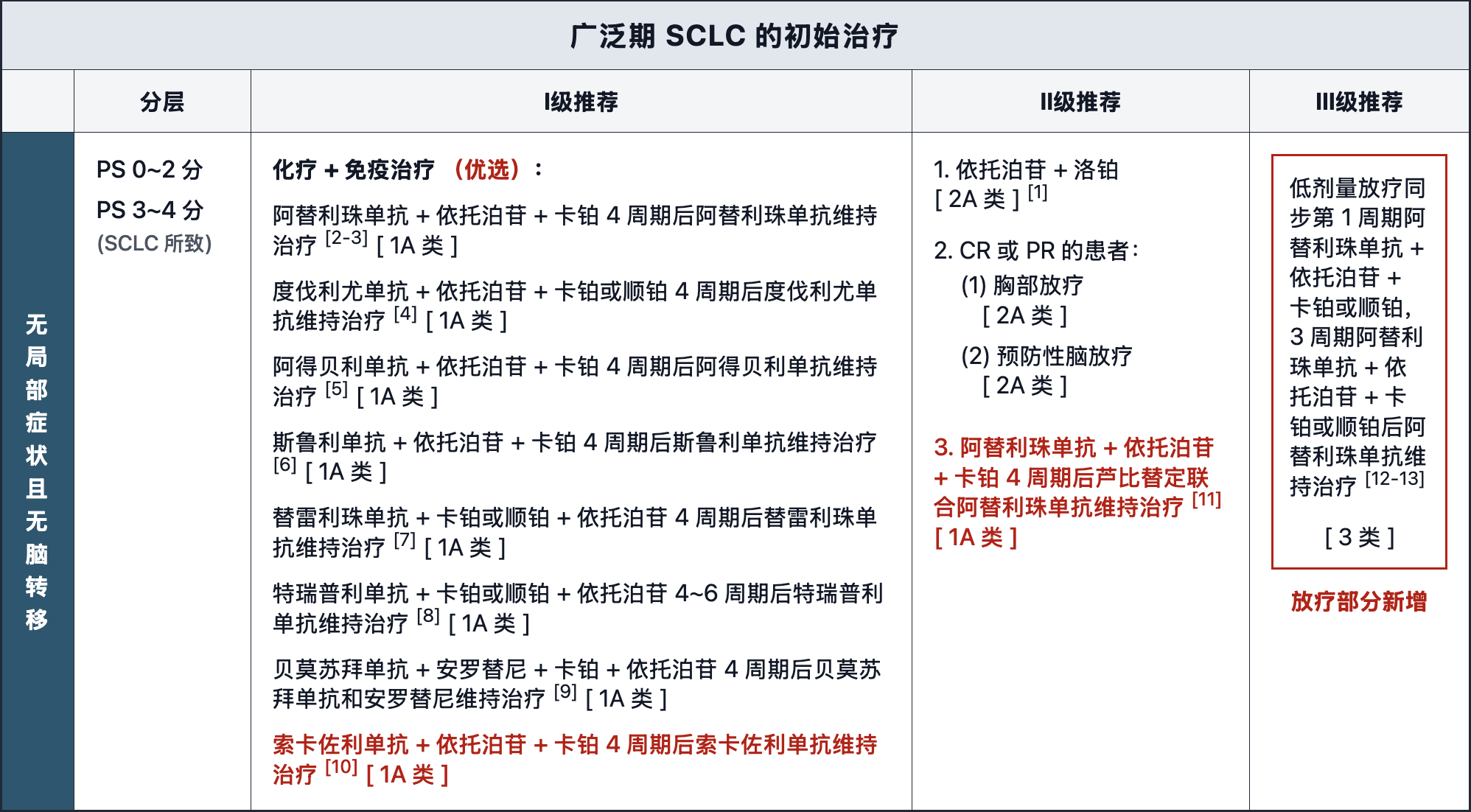
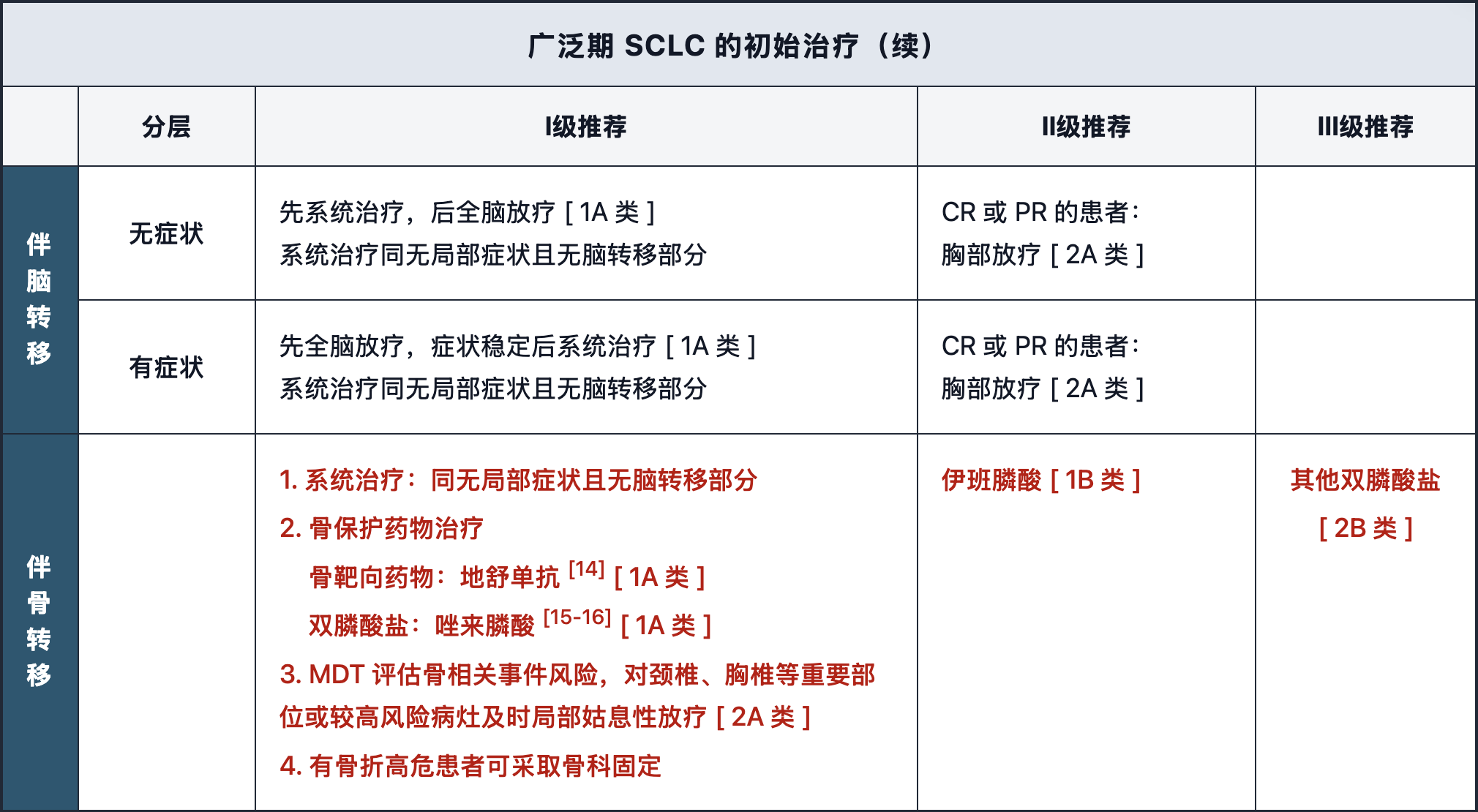
广泛期 SCLC 初治及一线维持治疗更新要点
调整化疗+免疫治疗统一作为“优选”推荐。
新增“索卡佐利单抗+依托泊苷+卡铂4周期后索卡佐利单抗维持治疗”作为Ⅰ级推荐。
新增“阿替利珠单抗+依托泊苷+卡铂4周期后芦比替定联合阿替利珠单抗维持治疗”作为Ⅱ级推荐。
新增“伴骨转移”分层,补充了骨保护药物的临床建议。
注:2025年7月30日,NMPA批准索卡佐利单抗联合卡铂和依托泊苷用于广泛期小细胞肺癌患者的一线治疗。
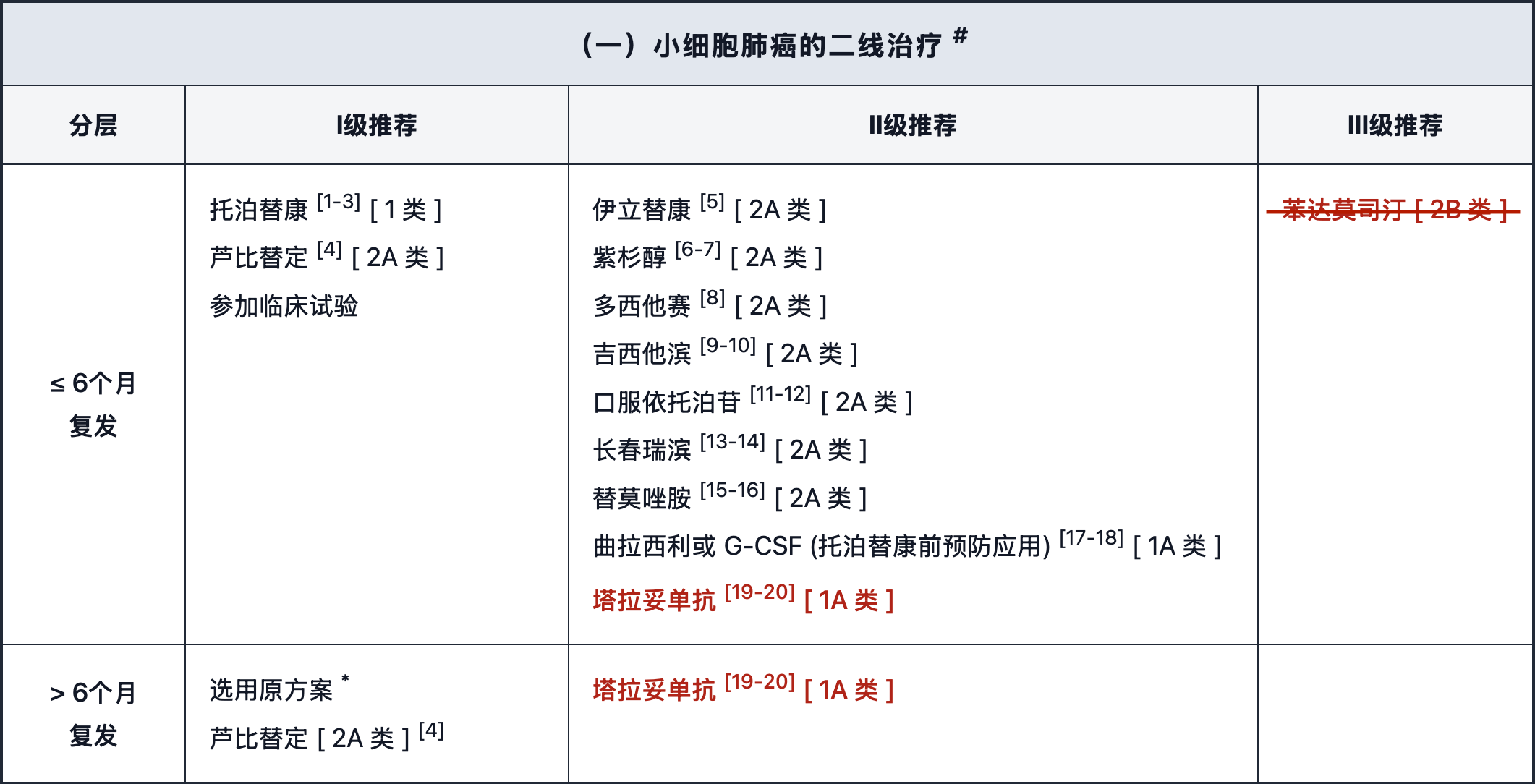
广泛期 SCLC 后线治疗更新要点
删除小细胞肺癌二线治疗Ⅲ级推荐“苯达莫司汀”。
新增“塔拉妥单抗”作为小细胞肺癌二线治疗Ⅱ级推荐(1A类)。
新增“塔拉妥单抗”作为小细胞肺癌三线及以上治疗Ⅱ级推荐(1A类)。
注:塔拉妥单抗是以DLL3和CD3为靶点的T细胞衔接器(TCE),引导T细胞杀伤表达DLL3的肿瘤细胞。塔拉妥单抗是目前首个且唯一获批用于实体瘤治疗的TCE类药物。基于DeLLphi-304研究,2025年11月,FDA完全批准塔拉妥单抗用于≥2L SCLC的治疗。2025年7月,NMPA受理塔拉妥单抗用于2L SCLC治疗适应症申请。
放疗
局限期SCLC放疗更新要点
同前所述,对于超过T1-2, N0阶段,PS评分0-2的患者,将“同步放化疗后未进展者接受度伐利尤单抗巩固治疗2年”从II级推荐上调为I级推荐(1类证据)。
放疗分割模式
【注释更新】
(4) 放疗总剂量和分割方案:目前尚未确定最佳的放疗剂量和分割方案。根据INT0096研究,45Gy/1.5Gy,每天2次/3周方案优于45Gy/1.8Gy,每天1次/5周方案[11-12]。而两项Ⅲ期研究CONVERT研究和RTOG0538研究均未能证明66Gy或70Gy(每天1次)方案优于45Gy(每天2次)方案,但前者的总生存率和毒性均与后者相似[13,30],因此推荐局限期SCLC患者胸部放疗总剂量为45Gy/1.5Gy,每天2次/3周或总剂量为60~70Gy,1.8~2.0Gy,每天1次/(6~8周)[13-14]。回顾性和随机工期研究表明,加速大分割方案总剂量为40~42Gy(每天1次,3周完成)可产生与45Gy/1.5Gy,每天2次相似的结果[31-32]。一项中国Ⅲ期研究显示45Gy/3Gy/15次的大分割放疗方案与高剂量常规分割放疗相比(60Gy/2Gy/30次)生存相似;但大分割放疗组显示出更高的安全性,≥3级急性治疗相关不良事件的发生率显著较低(48.7% vs. 67.7%, P<0.001),≥2级放射性肺炎(radiation pneumonia, RP)发生率也显著降低(7.7% vs. 14.5%, P=0.001)[33]。
免疫巩固治疗
【注释更新】
(4) ADRIATIC研究[17]的成功也引发了关于LS-SCLC研究中免疫治疗介入时机、与免疫治疗联合的最佳胸部放疗分割方式,免疫治疗的不同药物和免疫治疗的时长,PCI在LS-SCLC免疫治疗中的疗效和安全性,选择卡铂还是顺铂能够与LS-SCLC免疫治疗发挥最大协同作用等问题的深入思考。在免疫巩固治疗方面:ASTRUM-LC01 Ⅱ期研究(斯鲁利单抗巩固治疗1年)和GASTO-1052 Ⅱ期研究(特瑞普利单抗巩固治疗6个月)均证实在LS-SCLC同步放化疗后使用免疫巩固治疗显著提高疗效(前者PFS中位数为27.5个月,后者尚未达到)[46-47]。而ACHILES Ⅱ期研究在同步放化疗后使用阿替利珠单抗巩固治疗未观察到生存获益[48]。正在进行的DeLLphi-306、HLX10-020-SCLC302、MK 7339-013/KEYLYNK-013等研究结果值得期待。NRG LU005研究同步放化疗中联合阿替利珠单抗治疗与同步放化疗相比并没有看到生存获益。目前免疫治疗从诱导治疗开始就介入的研究SHR-1316-Ⅲ-302研究、HLX10-020-SCLC302仍然在探索中。一项Ⅱ期研究显示,卡瑞利珠单抗联合化疗诱导后序贯CCRT及免疫巩固治疗,在客观缓解率、无进展生存和总生存方面均优于单纯CCRT[49]。
广泛期SCLC放疗更新要点
广泛期SCLC初始治疗表格放疗部分新增III级推荐:低剂量放疗同步第1周期阿替利珠单抗 + 依托泊苷 + 卡铂或顺铂,3周期阿替利珠单抗 + 依托泊苷 + 卡铂或顺铂后阿替利珠单抗维持治疗(3类)。
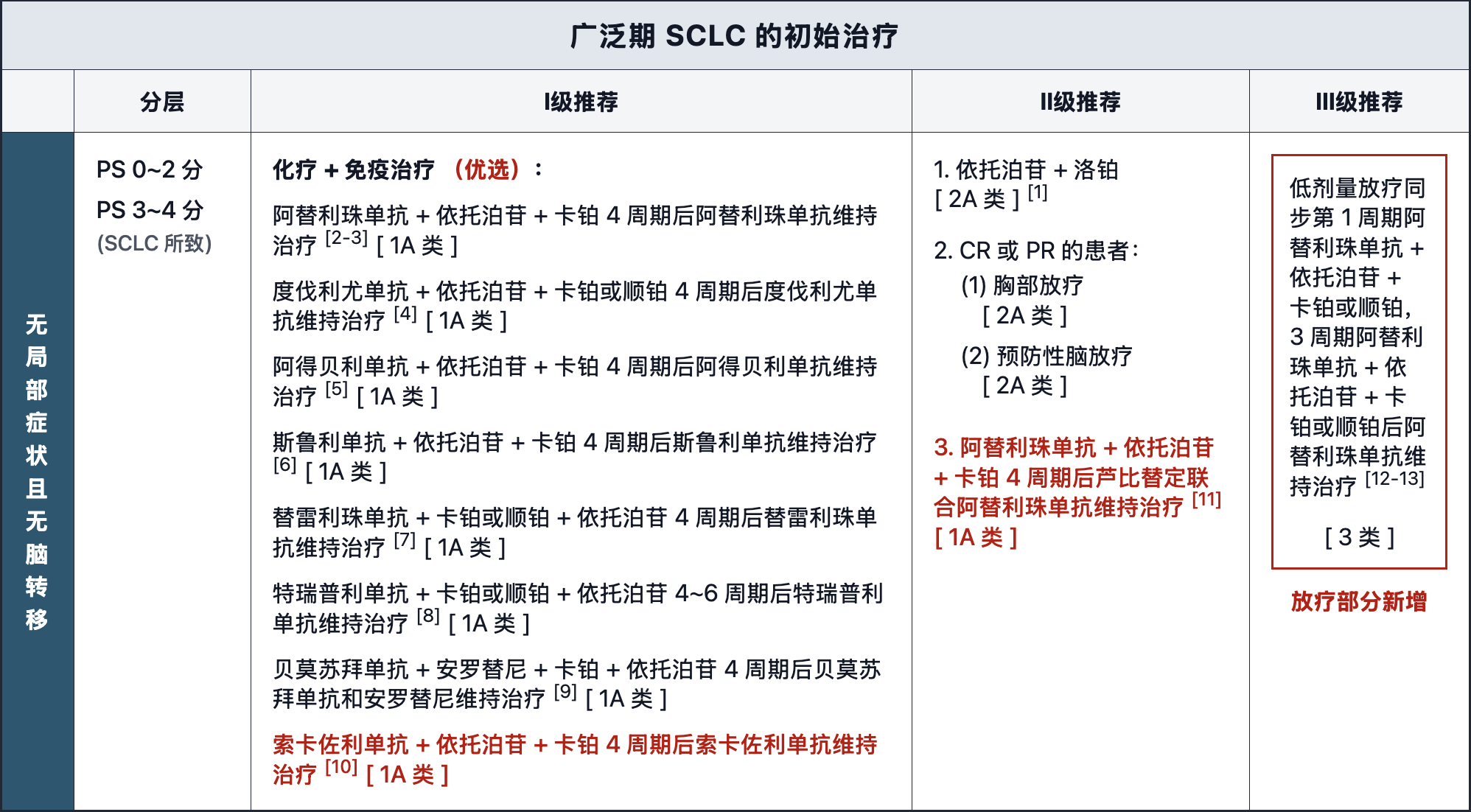
【注释更新】
一项胸部低剂量放疗(low-dose radiotherapy,LDRT)15Gy/5次同步一线阿替利珠单抗+依托泊苷/顺铂或卡铂,并阿替利珠单抗维持治疗的II期试验(MATCH试验)显示出肿瘤免疫微环境的重塑,良好的安全性和可行性,以及近期和中期疗效(ORR为73.3%,PFS中位数为6.9个月),OS中位数为16.9个月。1、3年PFS率分别为27.3%和20.7%,1年和3年OS率分别为69.9%和35.1%。进一步,相似设计的LDRT(15Gy/5次)同步一线联合化疗与免疫治疗的2项前瞻性多中心Ⅱ期临床试验进一步报道结果,安全性和耐受性均良好,联合度伐利尤单抗的PFS中位数和OS分别为8.3个月和23.6月(LEAD试验)[31];联合斯鲁利单抗的PFS中位数为7.3个月,OS中位数尚不成熟(SPUR试验)[32]。
放疗并发症的处理
【注释更新】
在“(一)放射性肺损伤”注释部分修改完善
放射性和免疫性肺损伤共存:对于(序贯或同期)合并使用免疫检查点抑制剂的患者,特别是免疫相关细胞因子明显变化的患者,在诊断放射性肺损伤的情况下,需注意同时合并免疫相关肺损伤(checkpoint inhibitor pneumonitis, CIP)的可能性。这种复合性肺损伤的个案或回顾性报道自2018年以来逐步增多,部分患者糖皮质激素减量时症状反复,可能需使用其他免疫抑制剂。鉴别放射免疫相关性肺炎对于其治疗至关重要。(1)在发病时机上,RILI多在放疗后6个月内出现,尤其在放疗后1~3个月内较为常见,而CIP可能在治疗后2~24个月内的任何时间发生。(2)影像学上,RILI通常局限于放射区域内,表现为渗出、实变和纤维化;CIP的影像学表现则更为多样,可分为5种类型:隐源性组织性肺炎、磨砂玻璃样结节的磨玻璃样混浊、小叶间隔增厚的间质性肺炎、小叶中心结节的超敏反应性肺炎,以及未明确定义的肺炎。临床上,RILI和CIP的鉴别常依据病变位置,RILI多见于照射的高剂量区域,与放疗剂量参数紧密相关,而CIP则多见于高剂量区域之外。(3)在临床实践中,除了明确放射-免疫相关性肺炎的性质,还需与其他可能引起相似症状的疾病进行鉴别诊断。RILI和CIP均为无菌性炎症,与感染性疾病相比,通常不伴有发热和白细胞升高等典型感染症状。感染性肺炎的影像学表现早期为毛玻璃样阴影,细菌性肺炎多局限于肺叶或肺段,而不良反应肺炎则表现为多发毛玻璃样阴影。(4)此外,还需注意与肿瘤进展的鉴别,后者常表现为咳嗽、咯血、胸痛、体重减轻、呼吸困难,肿瘤标志物可能升高,影像学上可见肺癌原发灶增大及新的结节状影、片状影、毛玻璃影等[4]。
在“(四)放射性皮肤损伤” 注释部分修改完善
因此,在进行局部治疗的同时,应积极进行全身治疗[11]。目前在国内外相关指南和共识中,关于生长因子类或生物制剂类药物在放射性皮肤损伤预防与治疗中的应用推荐意见尚不统一。国内的相关指南、共识中,对于EGF、GM-CSF在放射性皮肤损伤/放射性皮炎中的预防或治疗性应用予以弱推荐[12]。
排版编辑:肿瘤资讯-丹忱











 苏公网安备32059002004080号
苏公网安备32059002004080号


