2026年3月,《新英格兰医学杂志》(NEJM)发表了首个针对KRAS G12D突变晚期实体瘤的Ⅰ期临床研究。该研究由美国纪念斯隆-凯特琳癌症中心Wungki Park教授领衔,全球多中心参与,系统评估了首个KRAS G12D靶向蛋白降解剂Setidegrasib(ASP3082)在既往经治的晚期非小细胞肺癌(NSCLC)和胰腺癌(PDAC)患者中的安全性、药代动力学、药效学及抗肿瘤活性。Setidegrasi通过诱导突变蛋白的降解而非传统抑制,为这一长期被视为“不可成药”的KRAS G12D靶点提供了全新治疗策略。该研究首次在人体中证实了靶向蛋白降解技术应用于KRAS G12D突变实体瘤的可行性与临床潜力。

为何在KRAS G12D突变晚期实体瘤中探索蛋白降解策略?
KRAS是实体瘤中最常见的驱动基因突变之一,其中G12D亚型在胰腺癌(PDAC)中发生率高达40%,在非小细胞肺癌(NSCLC)中约为5%。尽管KRAS G12C抑制剂已成功进入临床,但针对G12D突变的小分子抑制剂开发长期面临挑战,主要原因在于G12D突变蛋白的GTP亲和力高、结合口袋浅,传统抑制策略难以奏效。
Setidegrasib采用蛋白降解靶向嵌合体(PROTAC)技术,通过招募E3泛素连接酶诱导KRAS G12D蛋白的泛素化与蛋白酶体降解,从而实现突变蛋白的清除。临床前研究显示,该策略可更持久地抑制下游信号通路,并可能克服传统抑制剂的部分耐药机制。
研究设计与方法
该研究为开放标签、国际多中心、Ⅰ期临床试验,于2022年6月21日至2025年4月24日在5个国家28家中心开展,共入组203例既往接受过治疗的晚期实体瘤患者,其中NSCLC 59例、PDAC 124例、其他实体瘤20例。
入组标准
·经本地或中心检测证实携带KRAS G12D突变的局部晚期不可切除或转移性实体瘤成年患者;
·依据RECIST 1.1版标准存在可测量病灶;
·ECOG体能状态评分0~2分(剂量递增)或0~1分(剂量扩展);
·既往接受过至少一线系统性抗肿瘤治疗,未接受过KRASG12D抑制剂、泛RAS抑制剂或降解剂;
·无症状、已治疗中枢神经系统转移的患者可入组,研究修订后排除基线白蛋白≤3.0g/dl的PDAC患者。
治疗方案
研究分为剂量递增组(123例)和剂量扩展组(80例),患者接受每周1次静脉输注setidegrasib,剂量范围为10~800mg,依据Bayesian连续评估方法确定剂量限制性毒性,最终选定600mg为Ⅱ期推荐剂量。患者持续接受治疗至疾病进展、不可耐受毒性或主动退出。
研究终点
数据截止日期为2025年10月9日(安全性)和2025年11月10日(疗效)。主要终点为安全性(剂量限制性毒性、不良事件)及确定最大耐受剂量与Ⅱ期推荐剂量(RP2D)。次要终点包括客观缓解率(ORR)、缓解持续时间、疾病控制率(DCR)、药代动力学及肿瘤KRAS G12D蛋白降解水平。探索性终点包括无进展生存期(PFS)、总生存期(OS)及药效学标志物。
主要结果:安全性可控,KRAS G12D突变肿瘤展现明确疗效
1. 患者基线特征
在76例接受600 mg剂量治疗的患者中,包括45例NSCLC和31例PDAC。中位年龄:NSCLC组为68岁(36~81岁),PDAC组为65岁(36~79岁)。两组患者既往中位治疗线数均为2线(1~5线)。NSCLC患者中42例(93%)既往接受过铂类化疗联合免疫检查点抑制剂治疗;PDAC患者中26例(84%)既往接受过吉西他滨联合紫杉醇/白蛋白紫杉醇治疗,16例(52%)接受过改良FOLFIRINOX方案治疗。
2. 安全性结果
·600 mg剂量组所有患者均在治疗期间发生不良事件,3级及以上不良事件发生率42%。治疗相关不良事件发生率为93%。
·最常见治疗相关不良事件为输注相关反应(80%)和恶心(30%)。输注相关反应绝大多数为1~2级,主要表现为瘙痒(30%)、皮疹(30%)和荨麻疹(25%),未见3级及以上输注相关反应。输注相关反应最常发生于首次输注时(78%),后续输注中发生率显著下降。
·治疗相关3级及以上不良事件发生率仅9%,包括谷丙转氨酶升高(3%)、中性粒细胞减少(3%)、中性粒细胞计数降低(3%),无治疗相关死亡事件,仅2例患者因不良事件永久停药。
·剂量限制性毒性仅发生于3例患者(2%),整体耐受性良好,未达到最大耐受剂量。
3. 疗效数据:
(1)NSCLC
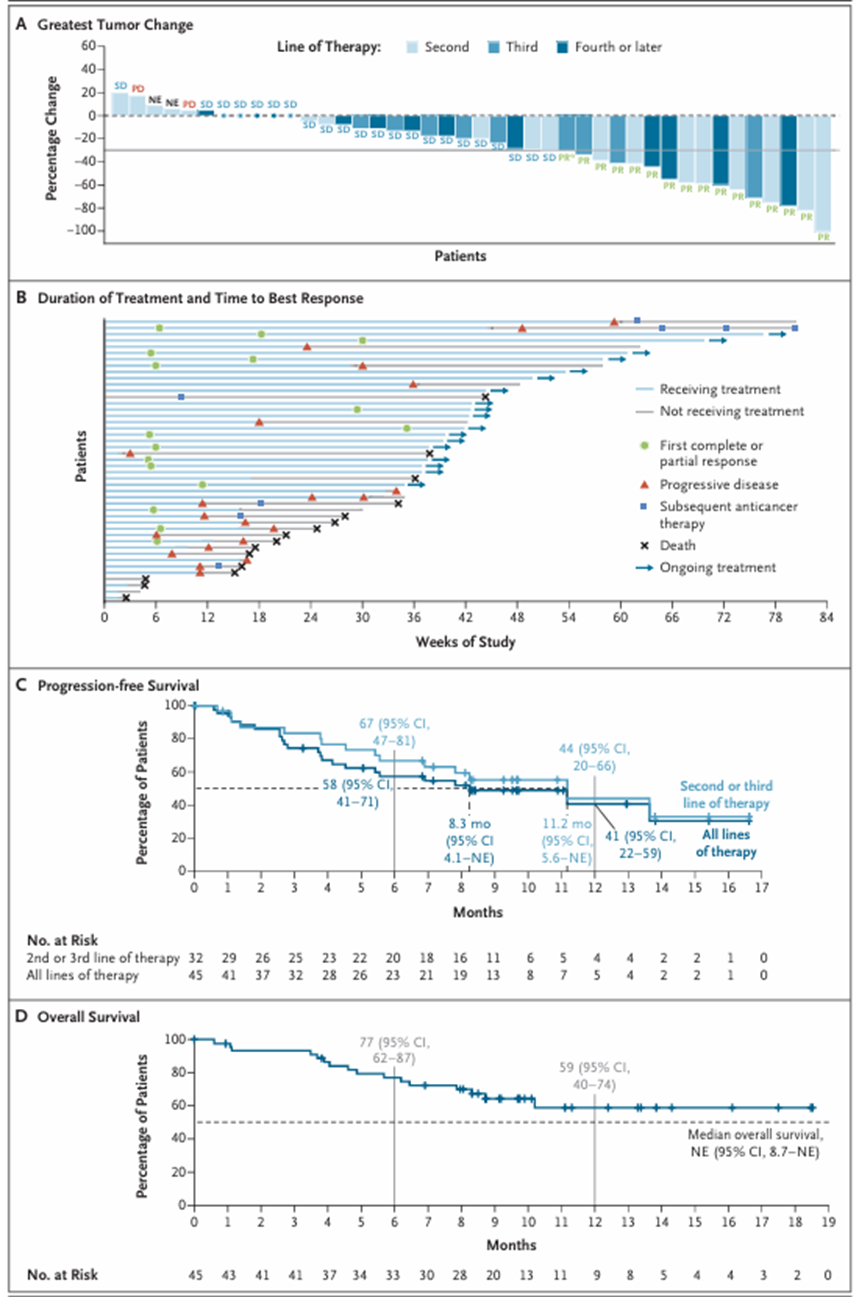
在45例接受600 mg剂量作为二线及以上治疗的NSCLC患者中,中位随访时间为9.7个月。ORR为36%(95% CI:22%~51%),均为部分缓解(其中1例待确认);DCR未明确报告,但瀑布图显示多数患者肿瘤负荷较基线下降;中位PFS为 8.3个月(95% CI:4.1个月~未评估);12个月OS率为59%(95%CI:40~74);在二线或三线治疗的患者亚组中(约占多数),ORR为38%,中位PFS为11.2个月。
研究者指出,这一疗效数据优于目前标准二线治疗方案(多西他赛±雷莫西尤单抗的历史ORR约为9%~23%,中位PFS约为3.0~4.5个月),与同类KRAS G12D抑制剂I期研究结果相当。
(2)PDAC
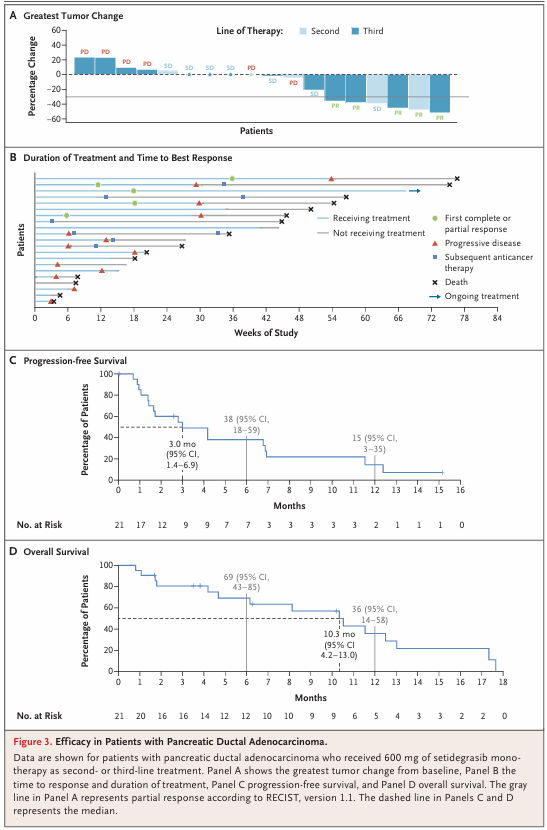
在21例接受600 mg剂量作为二线或三线治疗的转移性PDAC患者中(其中7例二线,14例三线,67%为三线治疗),中位随访时间为15.2个月。ORR为24%(5/21;95%CI,8%~47%),均为部分缓解。中位缓解持续时间为4.2个月;中位PFS为3.0个月(95%CI,1.4~6.9个月),中位OS为10.3个月(95%CI,4.2~13.0个月)。
研究者指出,转移性PDAC二线化疗的历史中位PFS通常不足3个月,中位OS约为6个月,且三线治疗尚无标准方案。该研究中位OS达到10.3个月,提示Setidegrasib在这一难治人群中具有明确的抗肿瘤活性。
4. 亚组与探索性分析
·基线白蛋白>3.0g/dl的PDAC患者可能具有更好的疗效趋势。
·ctDNA清除与肿瘤退缩高度相关,可作为早期疗效预测指标。
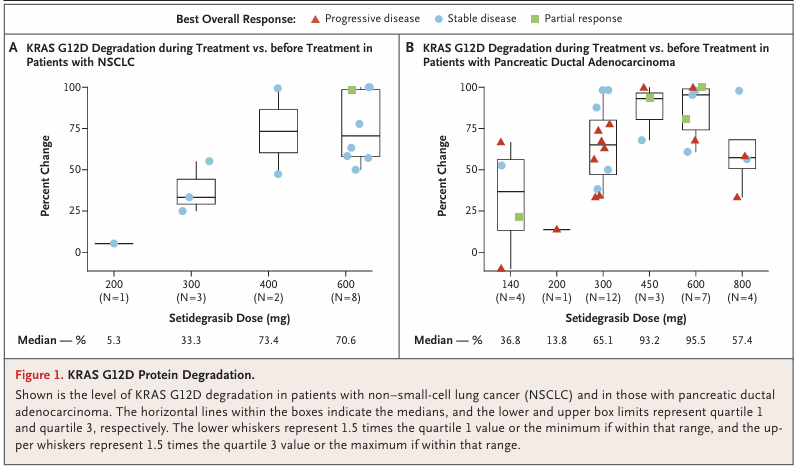
·KRAS G12D蛋白降解程度与临床获益呈正相关,PDAC靶点降解更充分。
转化性分析:蛋白降解机制带来差异化优势
该研究通过配对肿瘤活检与ctDNA动态监测,揭示了Setidegrasib的作用特征:
1. 靶点降解彻底性:PDAC中KRAS G12D降解率高达95.5%,显著高于NSCLC,与临床疗效趋势一致;
2. 分子响应快速性:治疗1周期即可观察到ctDNA突变频率显著下降,早于影像学评估;
3. 耐药机制差异:蛋白降解通过清除靶点蛋白发挥作用,与传统小分子抑制剂的耐药机制不同,为克服耐药提供新方向;
4. 肿瘤微环境影响:不同肿瘤类型的信号依赖与微环境异质性,导致疗效存在差异,需进一步探索生物标志物。
研究意义与临床价值
突破KRAS G12D靶向治疗瓶颈
该研究是全球首个KRAS G12D靶向蛋白降解剂的人体临床试验,首次证实该类药物在晚期实体瘤中的安全性与有效性,填补了KRAS G12D突变靶向治疗的空白。
确立蛋白降解技术临床价值
Setidegrasib通过催化降解致癌蛋白,区别于传统抑制机制,在难以靶向的KRAS突变肿瘤中展现明确活性,证明蛋白降解是实体瘤靶向治疗的可行新方向。
改善难治肿瘤生存获益
对于既往治疗有限的晚期PDAC,Setidegrasib二线/三线治疗中位OS达10.3个月,显著优于传统化疗;NSCLC的ORR与PFS优于标准二线方案,为KRAS G12D突变患者提供高效新选择。
指导后续临床开发
研究确定600mg每周一次为Ⅱ期推荐剂量,安全性可控,支持开展联合治疗探索;ctDNA与蛋白降解水平可作为疗效监测与生物标志物,助力精准治疗。
Park W, Kasi A, Spira AI, et al. Setidegrasib in Advanced Non-Small-Cell Lung Cancer and Pancreatic Cancer. N Engl J Med. 2026;394(14):1409-1420. doi:10.1056/NEJMoa2600752.
排版编辑:肿瘤资讯-ZJN











 苏公网安备32059002004080号
苏公网安备32059002004080号


