NTRK融合会异常激活下游信号通路致癌,尽管在常见实体瘤中发生率极低,但新一代TRK抑制剂已为其带来显著的生存获益。另一方面,NRG1融合导致ERBB通路持续激活,此类患者对传统化疗及免疫治疗极不敏感,而新型双特异性抗体则成功打破了这一治疗僵局。鉴于这两种突变的高度隐蔽性,临床目前强烈推荐使用基于RNA的NGS进行精准筛查。
NTRK融合突变
生物学与功能
NTRK(神经营养因子受体酪氨酸激酶)基因家族包括NTRK1、NTRK2和NTRK3,它们分别编码TRKA、TRKB和TRKC受体。这些受体在人体中发挥着不同的生理作用并对应特定的配体:
TRKA:主要配体为NGF(神经生长因子),参与疼痛和体温调节。
TRKB:主要配体为BDNF和NT-4,涉及运动、记忆、情绪和食欲的调控。
TRKC:主要配体为NT-3,负责本体感觉。
当这些基因发生融合时,会产生异常的融合蛋白,导致下游信号通路(如PLCγ、PI3K、ERK等)的持续激活,从而不受控制地驱动细胞的异常增殖、存活和分化,促进肿瘤发生。
流行病学与临床特征
TRK融合在不同类型癌症中的发生率呈现两极分化的特点。在一些极其罕见的癌症中,如分泌型乳腺癌、唾液腺分泌型癌(MASC)、婴儿纤维肉瘤和先天性中胚层肾瘤,NTRK融合的发生率超过90%。甲状腺癌、Spitz样肿瘤、胃肠道间质瘤和胆管癌中,发生率在5%到25%之间。
而,在诸如NSCLC、乳腺癌、结直肠癌等常见的成人实体瘤中,其发生率极低,普遍不到5%。根据FoundationCORE数据库中超过29.5万例患者的分析,NTRK融合的整体流行率约为0.3%。在超过5.4万例NSCLC患者中,其发生率仅为0.24%。
在NSCLC患者中,NTRK融合通常与其他致癌驱动基因互斥。这类患者的临床特征通常表现为:中位年龄48岁,55%为男性,高达73%为从不吸烟者,且病理类型绝大多数(82%)为腺癌。
诊断与检测策略
针对NTRK融合,目前可用的检测技术主要包括:
免疫组化:具有高敏感性,可检测TRK蛋白表达,非常适合作为初筛工具,但缺点是无法检测出具体的融合伴侣。
DNA测序(DNA seq):敏感性中等,在检测NTRK3融合时容易出现假阴性。此外,检测到的DNA重排在转录水平上不一定能形成功能性融合。
基于RNA的下一代测序:具有极高的敏感性和特异性,能准确检测所有融合基因及其伴侣,是目前最受推荐的方法。
ESMO指南建议:如果患者的肿瘤组织学类型并非高频携带NTRK融合的罕见类型,可首先使用IHC进行筛查;或者在一线检测中直接使用能可靠检测NTRK融合的NGS平台,并强烈建议在可能的情况下优先包含RNA水平的检测。
当前与未来的治疗方案
目前靶向NTRK融合的治疗已经取得显著进展:
第一代TRK抑制剂:Larotrectinib和Entrectinib分别于2018年和2019年获批,均获得FDA和EMA的批准,用于治疗无满意替代方案的NTRK融合阳性实体瘤患者。
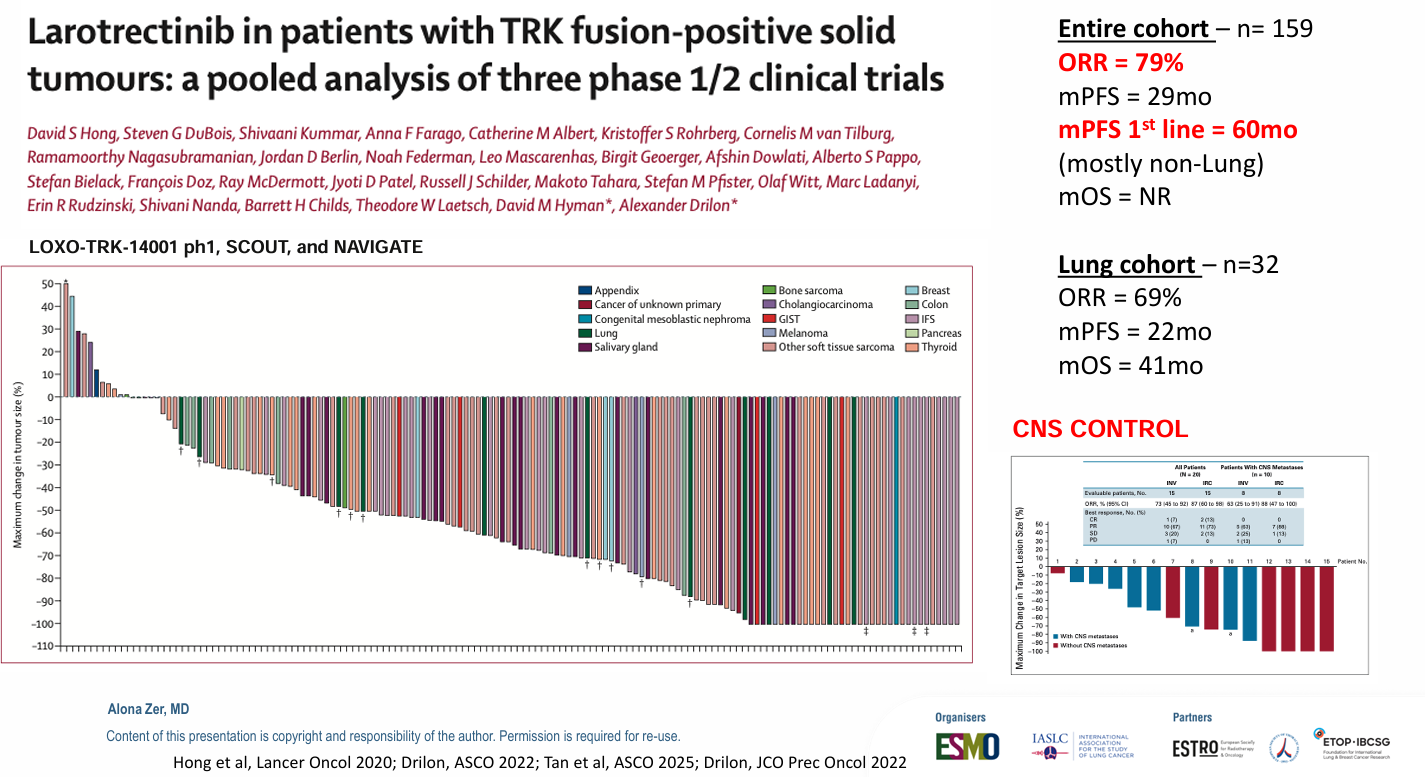
Larotrectinib:在整个患者队列中的ORR达到79%,中位PFS为29个月。在肺癌队列中,ORR为69%,中位PFS为22个月,中位OS达41个月。该药物还显示出卓越的中枢神经系统控制能力。
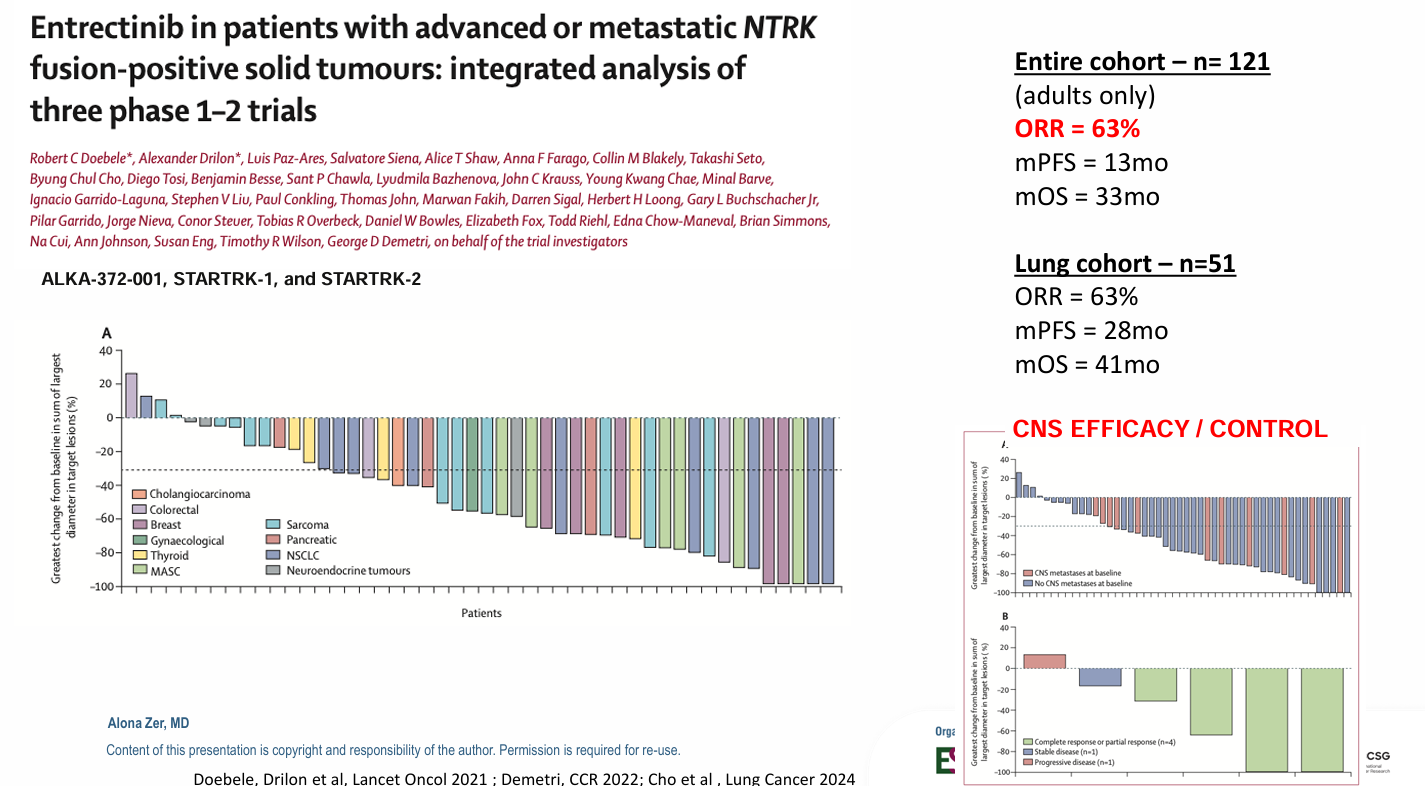
Entrectinib:在整体队列和肺癌队列中的ORR均为63%。肺癌队列的中位PFS长达28个月,中位OS同样为41个月,且在基线有CNS转移的患者中也展现出强大的疗效。
第二代TRK抑制剂:如Repotrectinib(2024年获批),旨在解决第一代药物的耐药问题。针对未接受过TKI治疗的患者,ORR为59%,中位PFS高达30个月。对于已接受过TKI治疗的患者,ORR仍可达48%,中位PFS为7个月。
获得性耐药与免疫治疗的潜力
患者对第一代TKI的获得性耐药机制主要包括在靶突变和脱靶耐药。
在靶突变:包括网守突变(如TRKA F589L)、溶剂前沿突变(如TRKA G595R, TRKC G623R)和xDFG基序突变(如TRKA G667C)。以Repotrectinib为代表的新一代TKI在应对溶剂前沿突变时表现优异(ORR为60%,中位PFS为8.6个月)。
脱靶耐药:包括MET扩增、BRAF V600E突变、KRAS突变等。
在免疫治疗方面,NTRK融合阳性并非免疫治疗的禁忌。根据MSKCC和OAK/POPLAR的数据,接受免疫检查点抑制剂治疗的NTRK突变患者,其OS与野生型患者相当甚至更优(尤其是NTRK3突变者),且PD-L1表达不能作为有效的预测指标。
不良反应管理
TRK抑制剂的不良反应分为两大类:
脱靶不良事件:包括肝酶(ALT/AST)升高、贫血、恶心、腹泻、疲劳和便秘等。
在靶神经系统不良事件:由于NTRK基因对神经系统的生理作用,抑制其功能会导致特异性反应。例如,抑制TRKA会引发感觉或自主神经病变以及痛觉缺失;抑制TRKB会导致食欲亢进、体重异常增加和记忆损伤;抑制TRKC会导致本体感觉缺陷。此外,停药痛和头晕、共济失调也是常见的不良反应。在因AE导致剂量调整方面,Repotrectinib的剂量减少率最高(35%),而Larotrectinib仅为8%。
NRG1融合突变
生物学功能与流行病学
NRG1基因负责编码ERBB受体激酶的配体。NRG1基因融合会导致配体的过度表达或将其强行锚定在细胞膜上,与相邻的HER3受体结合。这会形成一个持续的自分泌环,导致ERBB信号通路(特别是ERBB3与ERBB2的异二聚体)的结构性激活,进而促进肿瘤细胞的增殖与存活。
NRG1融合在所有肿瘤中的整体发生率极低,约为0.2%。在NSCLC中的发生率为0.3%,而在胰腺癌和胆囊癌中约为0.5%。对于NSCLC患者,其临床特征相当典型:94%为腺癌(主要是浸润性黏液腺癌亚型),57%为从不吸烟者,女性占60%。这类肿瘤通常极具侵袭性,容易向肺部(71%)、骨骼(34%)、淋巴结(23%)和脑部(21%)转移。最常见的融合伴侣是CD74(41%)和SLC3A2(20%)。
诊断困境与检测推荐
由于NRG1基因拥有极其庞大的非编码区(超过99%),传统的DNA测序技术在检测NRG1融合时敏感性大打折扣。因此,目前业界强烈推荐使用基于RNA或DNA/RNA混合捕获的NGS技术进行确诊。IHC和FISH不被推荐作为筛查手段。
治疗方案的演进与突破
NRG1融合阳性肿瘤通常具有低TMB和“冷”免疫微环境的特征,这导致传统标准疗法疗效堪忧。含铂双药化疗的ORR仅为13%,单药免疫治疗ORR为20%,而化疗联合免疫治疗的ORR竟然为0%。
目前在针对NRG1的靶向治疗探索中:
泛ERBB抑制剂:如Afatinib,在一些回顾性研究中显示出25%到37%的ORR,但疗效相对有限。
新一代TKI:如Zongertinib,在Beamion Lung-1的1期临床试验中表现不俗,取得43%的ORR和86%的DCR。
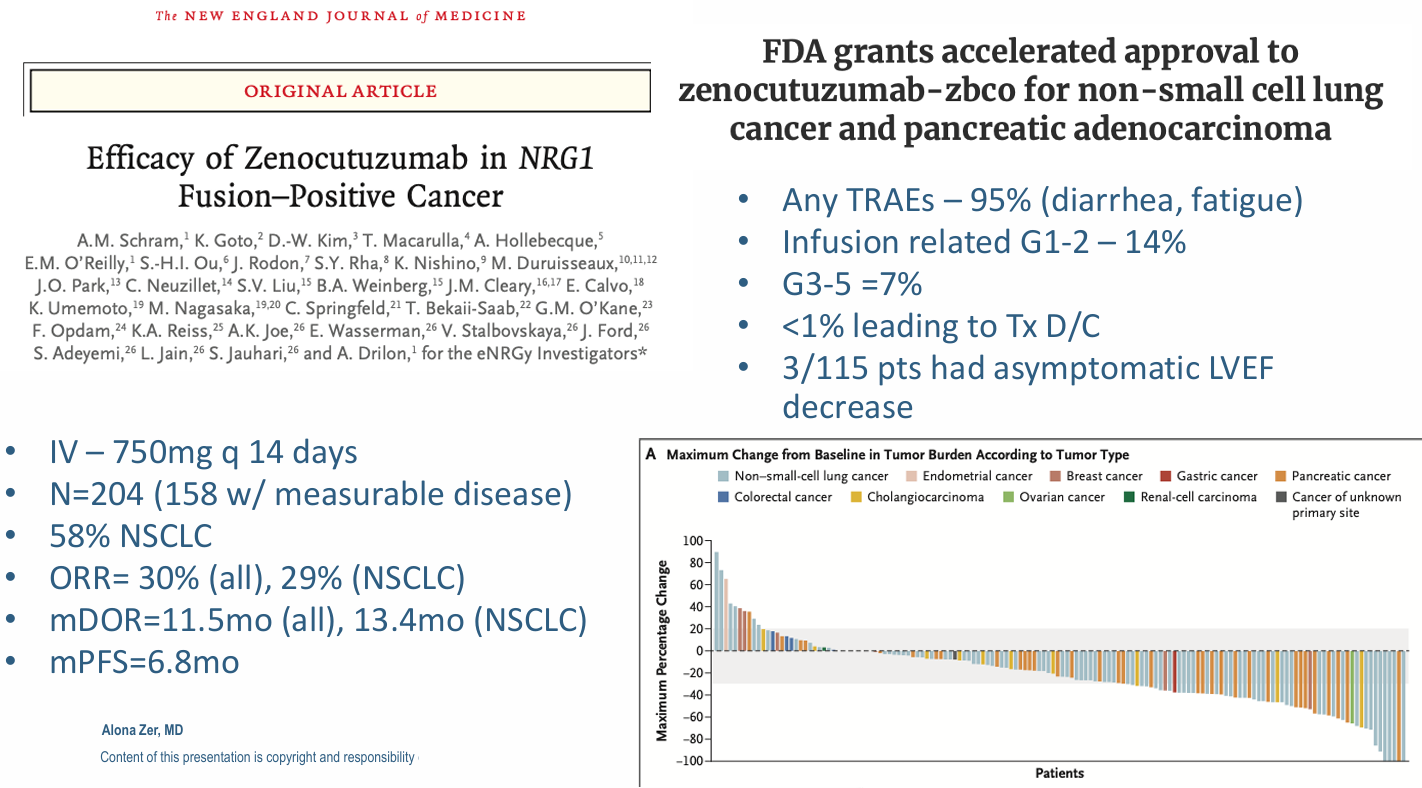
双特异性抗体:Zenocutuzumab是目前最大的突破,近期已获得FDA的加速批准,用于治疗NSCLC和胰腺腺癌。研究数据显示,Zenocutuzumab在整个队列中的ORR为30%(在NSCLC中为29%),中位中位DoR达11.5个月,中位PFS为6.8个月。此外,该药的安全性良好,绝大多数不良事件(如腹泻、疲劳)可通过管理控制,导致停药的比例不到1%。
其他在研疗法还包括Seribantumab(临床2期ORR 36%)、抗HER3单抗HMBD-001以及抗体偶联药物Patritumab deruxtecan等。
排版编辑:肿瘤资讯-Bear











 苏公网安备32059002004080号
苏公网安备32059002004080号


