随着靶向治疗在肿瘤学领域的不断突破,KRAS G12C抑制剂已成为近年来的研究热点。与大量基于体外细胞和动物模型的临床前数据不同,本文将聚焦于来自真实患者的转化医学数据,深入探讨KRAS G12C抑制剂(如Sotorasib和 Adagrasib)的生物标志物以及肿瘤产生获得性耐药的具体机制。
靶向治疗的“逃逸”理论基础
KRAS作为核心的GTP酶“开关”,负责将RTK的信号整合并传递给多种细胞内信号转导通路,特别是MAPK通路和 PI3K/mTOR通路。当使用靶向药物精准打击这一核心节点时,癌细胞为了生存,必然会演化出逃逸机制。从生物学逻辑出发,癌细胞的“突围”策略通常包括以下四种路径:
靶点自身突变:产生对当前靶向药物不敏感的KRAS替代性突变。
旁路或下游激活:通过下游基因突变或平行通路激活,绕过受阻的KRAS节点,继续向细胞核传递生长信号。
释放促存活通路:例如激活NRF2介导的转录程序,提升细胞的抗逆性。
干扰细胞周期:直接改变细胞周期机制的调节,导致癌细胞失控增殖。
问题在于:这些理论上的逃逸机制,在真实接受靶向治疗的患者体内是否真正发生?
原发性耐药的决定因素:从回顾性到前瞻性数据的验证
多中心回顾性研究的启示
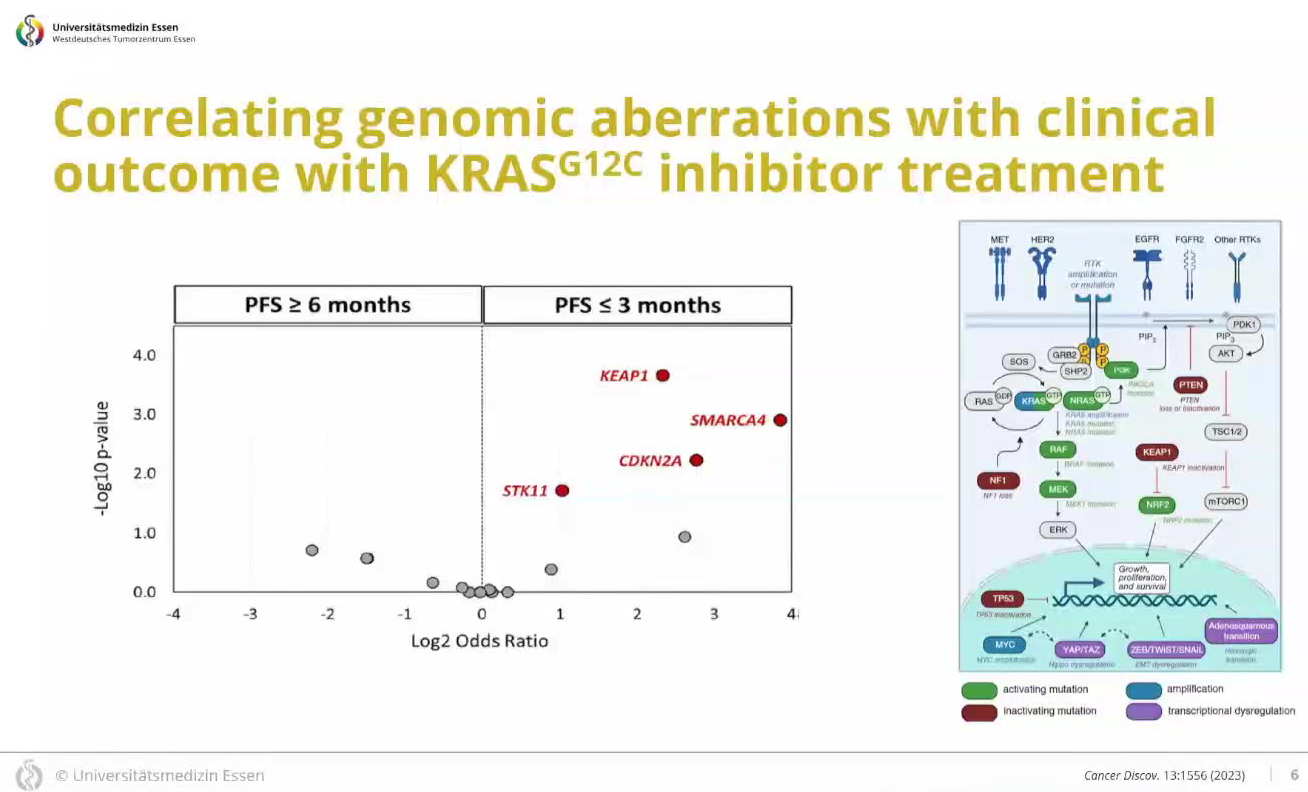
由MD安德森癌症中心协调的一项国际合作研究,汇总约 400例接受Sotorasib或Adagrasib治疗的患者数据。研究人员对这些患者的组织标本或ctDNA进行基因组测序分析。通过将患者按疗效分为“无获益组”(PFS<3个月)和“较好获益组”(PFS≥6个月),研究揭示与不良预后高度相关的基因组信号:
CDKN2A突变:直接影响细胞周期的调控。
KEAP1突变:解除对NRF2依赖性信号传导的负调控,激活细胞促存活程序。
SMARCA4突变:作为BAF复合体的一部分,涉及表观遗传和基因表达的调控。
STK11 (LKB1)突变:作为一种肿瘤抑制因子,其突变会阻断AMPK从而释放其他信号通路。
这项研究证实理论推演的耐药机制在真实世界中的存在。然而,由于该研究是单臂回顾性队列,无法区分这些突变究竟是KRAS抑制剂特有的预测性标志物,还是普遍适用所有疗法的预后不良标志物。
CodeBreak 200前瞻性随机对照试验的突破
为了进一步验证上述假设,包含多西他赛对照组的前瞻性随机试验CodeBreak 200提供绝佳的契机。该试验不仅拥有高度完善的生物标志物数据(组织NGS测序、RNA测序以及纵向ctDNA分析),还得出一系列具有临床指导意义的结论:
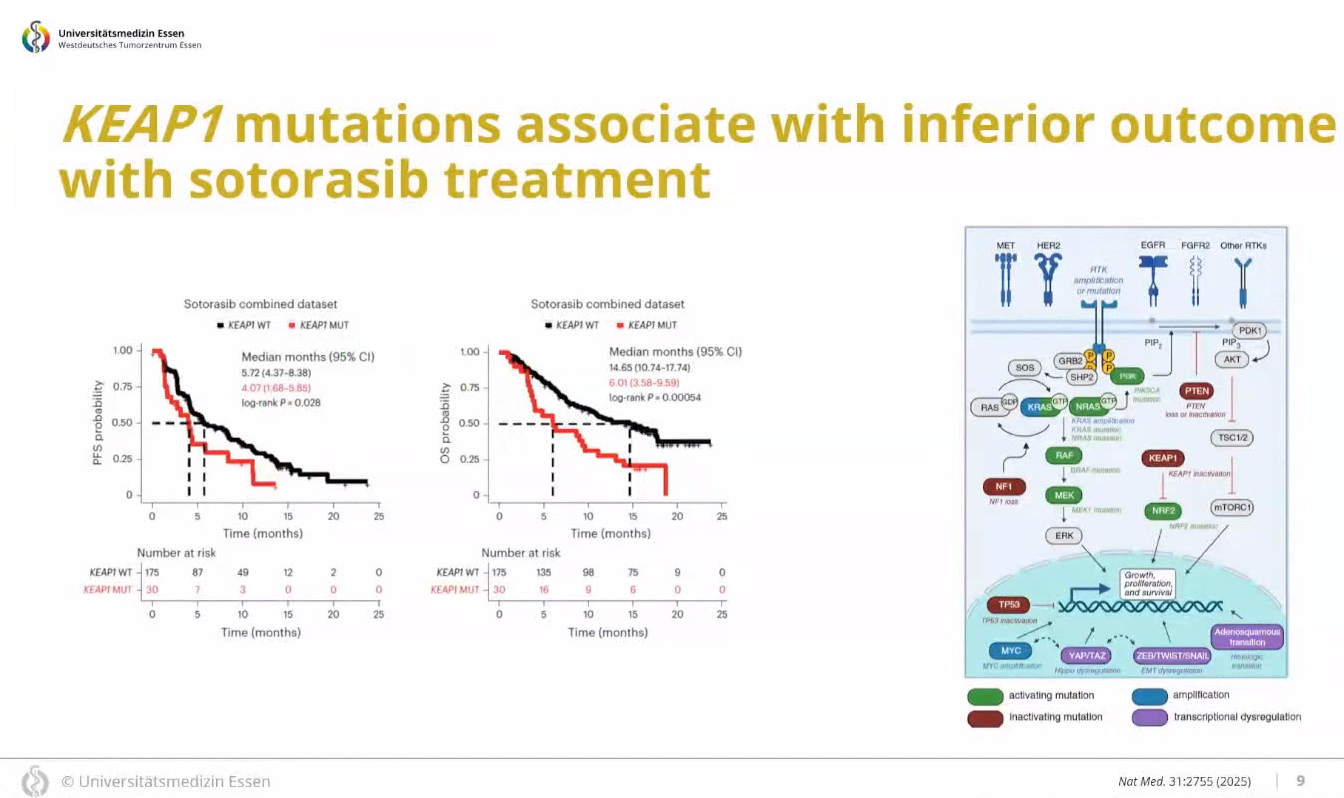
KEAP1突变的确认:无论是单独在CodeBreak 200还是结合CodeBreak 100的庞大数据集中,均证实携带KEAP1突变的患者在使用Sotorasib时,其PFS和OS表现更差。RNA 测序进一步证实,携带KEAP1突变的肿瘤高度激活NRF2 转录程序,这与生存期缩短直接相关。
ATM突变的独特预测价值:这是在回顾性分析中未被捕捉到的新信号。数据表明,ATM野生型肿瘤对Sotorasib的缓解更好;而ATM突变型、KRAS突变的癌症,似乎对传统的细胞毒性化疗更为敏感。从生物学上看这非常合理:ATM 是调节DNA链断裂修复和细胞周期检查点的核心肿瘤抑制因子。当ATM突变导致DNA修复功能受损时,使用引发 DNA损伤的化疗药物往往更为有效。这可能成为未来指导临床用药决策的重要标志物。
转录组学特征与临床实用标志物:TTF-1的价值
除了基因突变,转录组学特征也为肿瘤分类提供新视角。基于早期转基因小鼠模型的转录谱,KRAS突变肺癌可分为三个亚群:
KP亚群:富含TP53突变。
KL亚群:以STK11 (LKB1)突变为特征。
KC亚群:富含CDKN2A突变。
将这套分类系统应用于CodeBreak数据集后发现,KC亚群(占患者总数超20%)在接受KRAS G12C抑制剂治疗时,表现出显著劣势的PFS和OS。然而,高昂且复杂的转录组测序目前并非临床常规手段。为了寻找具有临床可操作性的“替代指标”,研究团队发现KC亚群表现出TTF-1转录因子的低表达。更为关键的是,通过IHC这一病理科常规手段验证,TTF-1蛋白表达的缺失与RNA低表达高度一致。
临床结论:TTF-1低表达能够精准描绘出一小群在 Sotorasib治疗下预后极差的KRAS G12C突变肺癌患者(这些患者中几乎未观察到ORR)。因此,TTF-1低表达、KEAP1突变以及ATM突变,都有潜力成为临床上判定原发性耐药的实用生物标志物。
获得性耐药机制:不仅仅是基因组水平的较量
随着靶向药物的使用,肿瘤发生获得性耐药几乎不可避免。全球多个团队通过对复发患者进行再次活检或液体活检,揭示以下现象:
靶点与旁路突变:部分患者按理论预测,出现非 G12C 的 KRAS 替代突变,或激活平行的信号转导通路(甚至出现基因融合)。这在 Adagrasib 和 Sotorasib 的治疗中均有观察到。
癌种异质性:潜在的基因组耐药机制在不同癌症中分布各异。在肺癌中,约三分之一的患者存在单一耐药突变;在结直肠癌中,超过 50% 的患者携带多重突变;胰腺癌则介于两者之间。
未知的基因组“暗物质”:值得注意的是,在所有癌种中,都存在庞大的患者群体——通过常规聚焦于基因序列改变的测序技术,无法找到任何合理的基因组逃逸机制。
总结与展望
综上所述,来自前瞻性和真实世界的转化数据清晰地表明,KRAS G12C 抑制剂的疗效受到肿瘤特定生物学亚群的严格限制。
在原发性耐药方面,KEAP1 突变、ATM 突变以及低 TTF-1 表达等临床可行标志物,有望在未来指导患者的前期分层。
在获得性耐药方面,肿瘤通过靶点变异或平行通路激活(如 HER2 扩增)进行反击,而基于个体分子图谱的靶向联合策略将是破局的关键。
展望未来,随着新型调控药物(如 Pan-RAS 抑制剂、RAS(ON) 抑制剂等)步入临床,研究这些全新作用机制下的逃逸策略,以及验证它们是否会重演现今 G12C 抑制剂的耐药路径,将成为肿瘤学领域的下一阶段课题。
排版编辑:肿瘤资讯-Bear











 苏公网安备32059002004080号
苏公网安备32059002004080号


