2026年3月,一年一度的欧洲肺癌大会(ELCC)如期举行。作为全球肺癌领域最具影响力的学术盛会之一,ELCC始终致力于分享胸部肿瘤领域最前沿的预防、诊断及治疗进展。本次大会吸引了来自全球各地的临床医生与科学家,共同探讨在精准医疗背景下肺癌治疗模式的演进。来自纪念斯隆凯特琳癌症中心(MSKCC)的Suresh Ramalingam教授受邀在教育专场(Educational Session)发表了题为“Managing locally advanced EGFRm NSCLC: Where does TKI fit?”的专题报告。Ramalingam教授系统阐述了表皮生长因子受体(EGFR)突变局部晚期非小细胞肺癌(NSCLC)的独特生物学行为特征,并结合LAURA等里程碑式研究,深度解析了靶向治疗(TKI)在该人群中的精准定位,为这一临床难治人群的治疗策略提供了高级别循证医学依据。【肿瘤资讯】特将本场教育专场的内容进行梳理,以飨读者。

EGFR突变疾病的独特生物学特征:微转移风险显著升高
Ramalingam教授首先通过对比分析,揭示了EGFR突变局部晚期NSCLC与全人群肺癌在复发模式上的本质差异。在全人群可手术患者(I-IIIA期)的历史队列中,局部区域复发率约为15%,远处转移率约20%,脑转移发生率不足5%;即便是专门针对III期全人群患者的NADIM试验,其脑转移率也仅为5%。然而,在ADAURA试验的对照组(EGFR突变患者)中,远处转移率接近30%,脑转移发生率高达11%。这一对比强烈提示:EGFR突变肺癌的微转移事件在疾病早期即已频繁发生。
对于不可手术切除的局部晚期患者,多项历史队列研究一致显示,EGFR突变患者经放化疗后的远处失败率(distant failure)接近70%,显著高于野生型患者;而局部区域失败率反而相对较低。Ramalingam教授指出,这一现象表明放化疗对原发肿瘤控制良好,但“微转移才是该人群面临的主要挑战”。
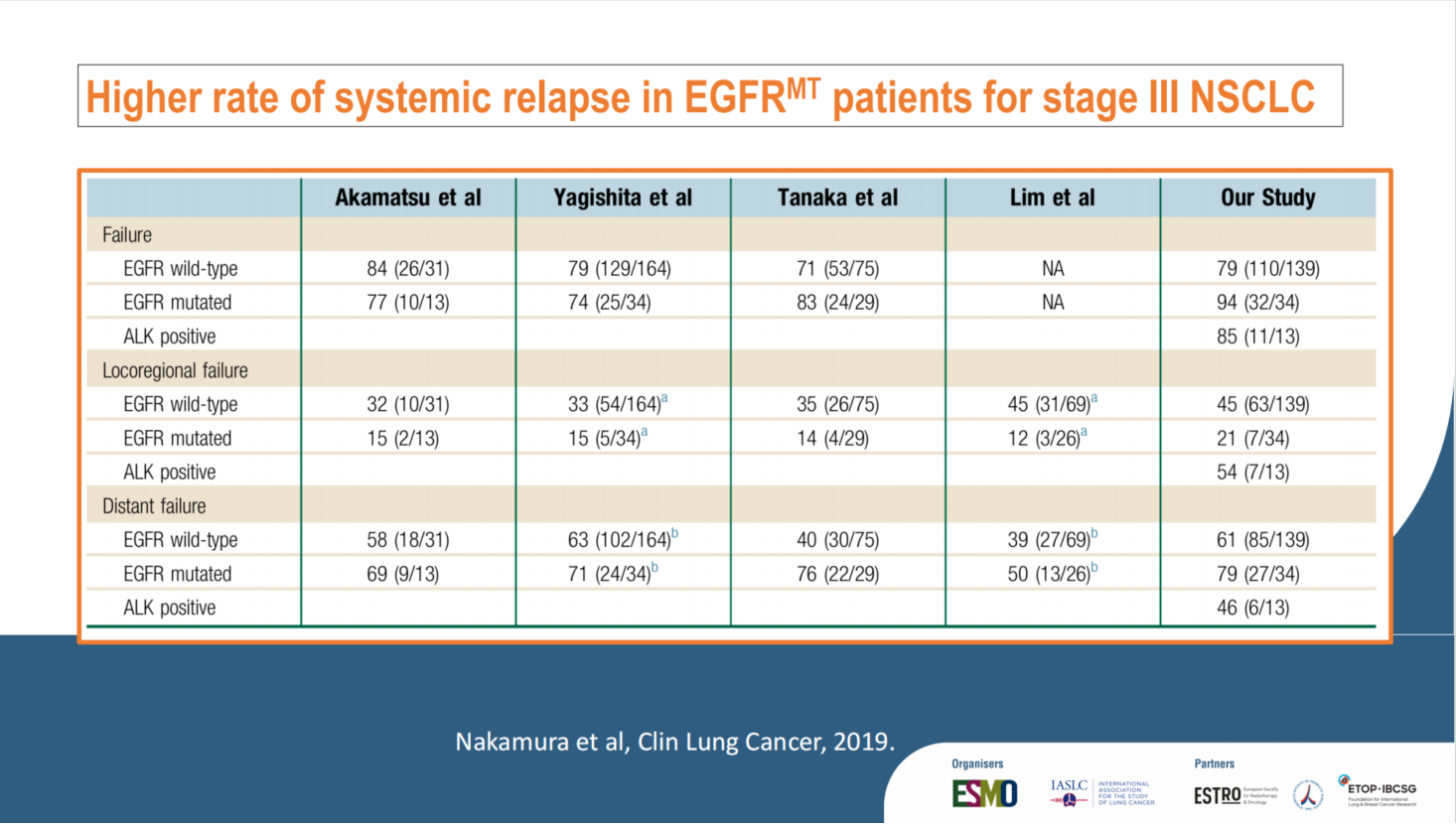
通过对比PACIFIC试验(主要纳入野生型人群)与LAURA试验对照组(仅EGFR突变患者)的数据,EGFR突变人群的脑复发率高达近30%,而PACIFIC对照组仅为11%,进一步证实了该人群独特且更具侵袭性的复发模式。

免疫巩固治疗的局限与LAURA研究的里程碑意义
基于PACIFIC试验中EGFR突变亚组(35例患者)的探索性分析,度伐利尤单抗巩固治疗的生存曲线与安慰剂几乎完全重叠。Ramalingam教授强调,现有证据一致表明,免疫检查点抑制剂无法为EGFR突变NSCLC患者带来持久的临床获益,正是在这一临床困境的催生下,LAURA III期随机对照试验得以开展。
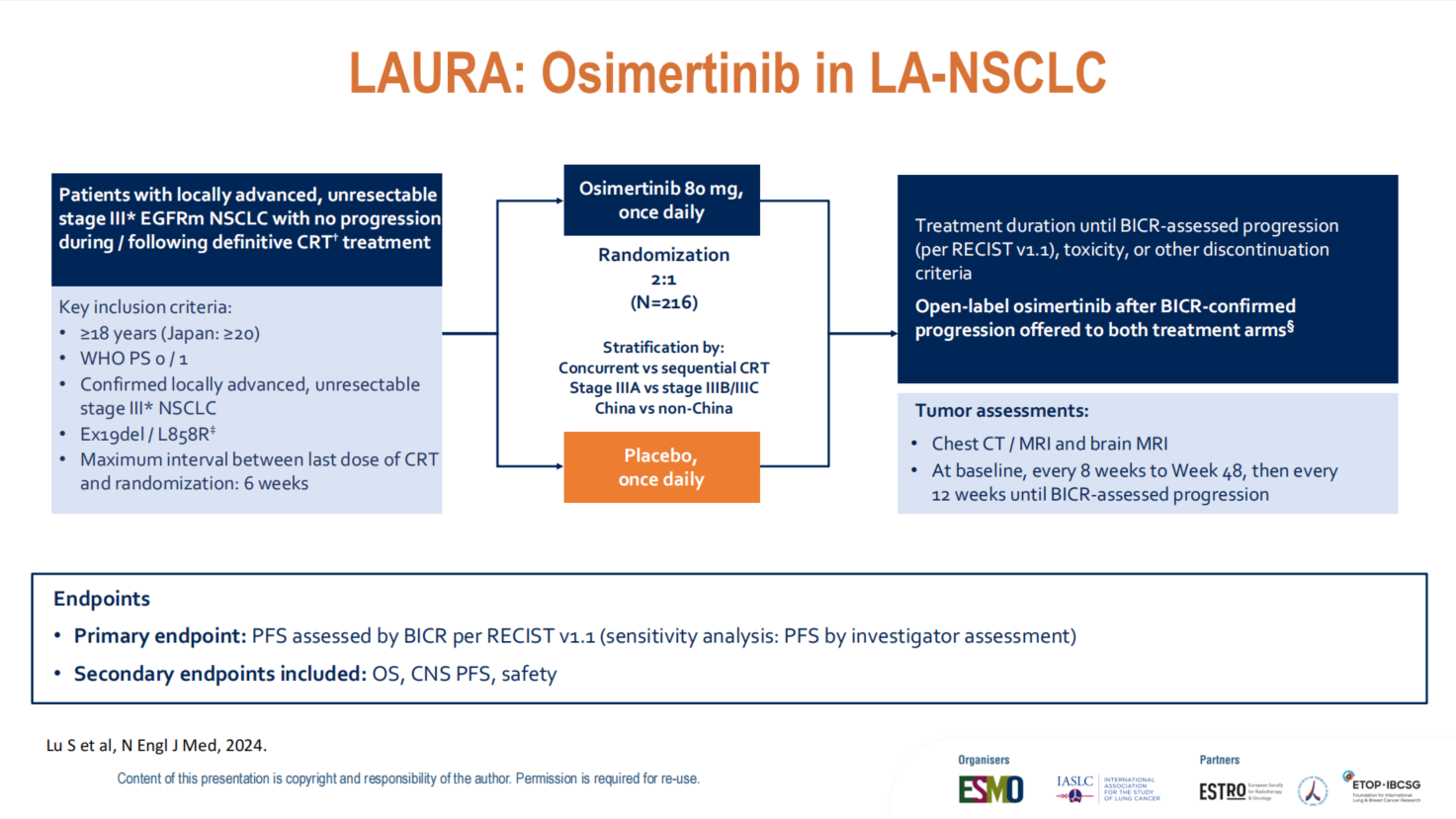
LAURA研究纳入接受根治性放化疗后未进展的不可切除III期(EGFR 19del或L858R突变)患者,按2:1随机分配接受奥希替尼巩固治疗或安慰剂。与ADAURA研究的固定疗程不同,LAURA研究采用持续治疗直至疾病进展的策略,并允许安慰剂组患者在进展后交叉接受奥希替尼治疗。
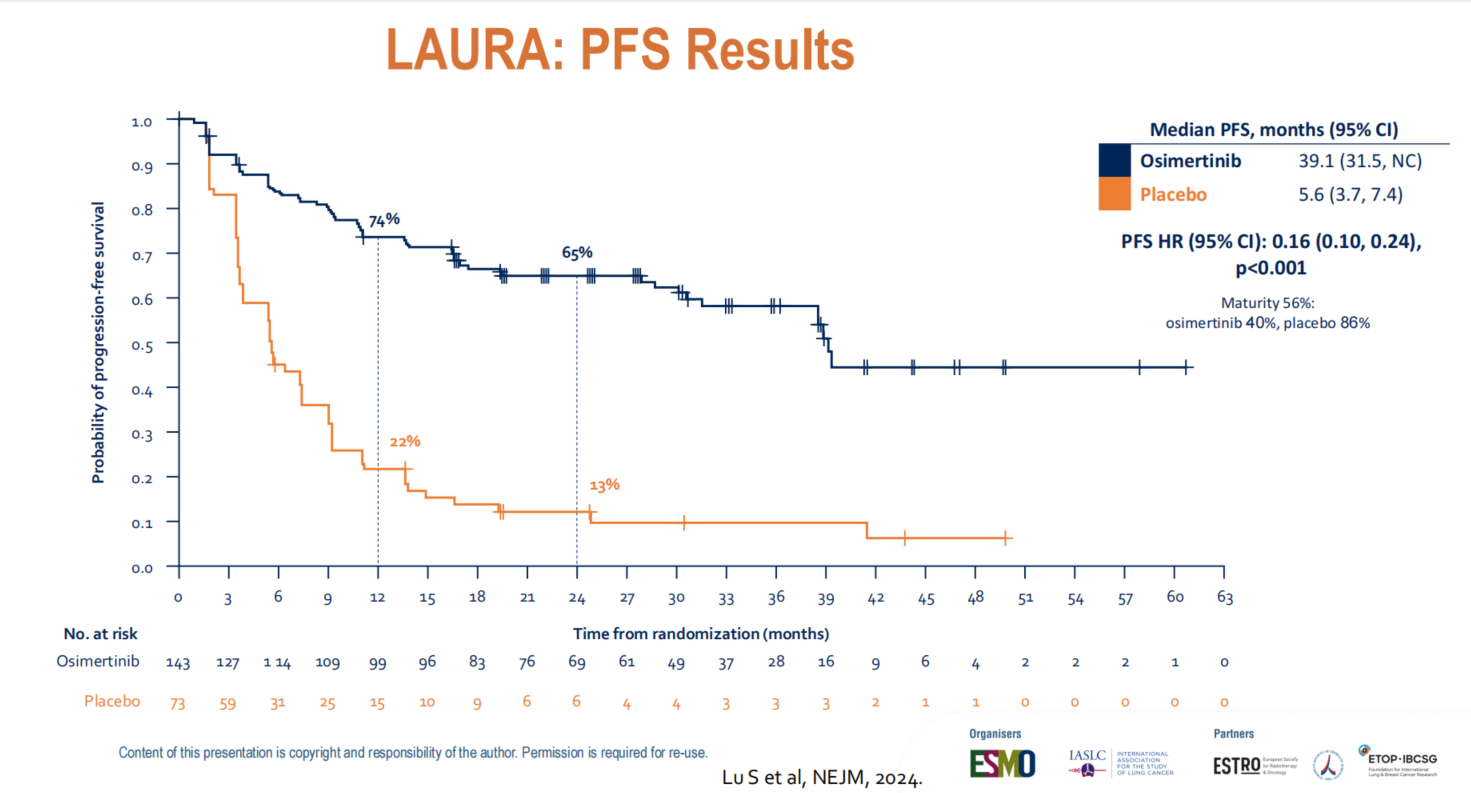
研究结果显示,奥希替尼组的中位无进展生存期(PFS)达到了39.0个月,而安慰剂组仅为5.6个月。Ramalingam教授特别指出,安慰剂组5.6个月的极短中位PFS深刻揭示了EGFR突变局部晚期疾病的侵袭性——即使经过根治性放化疗,疾病仍在短期内快速进展。
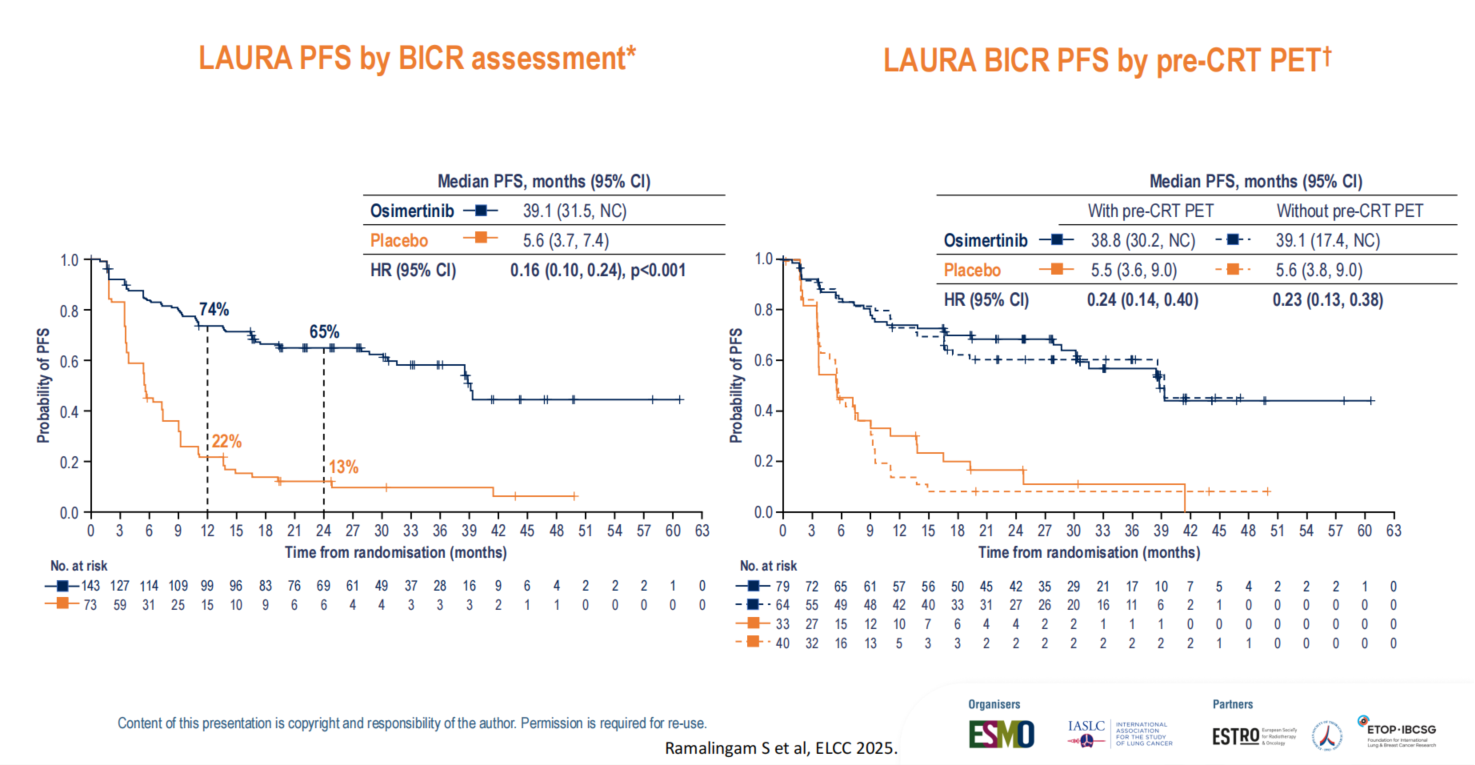
针对研究设计中关于基线分期准确性(是否常规进行PET-CT)的探讨,此次ELCC会议公布的亚组分析显示,在接受过PET-CT精准分期的患者中,奥希替尼带来的PFS获益程度与总体人群高度一致,证实分期方式未对研究结果产生偏倚。
此外,至首次后续治疗时间(TFST,HR=0.13)和第二次无进展生存期(PFS2,HR=0.62)均显示出奥希替尼带来的深远临床获益。总生存期(OS)数据目前成熟度为31%,已显示出有利于奥希替尼的获益趋势(HR 0.67),最终分析计划在成熟度达到60%时进行。
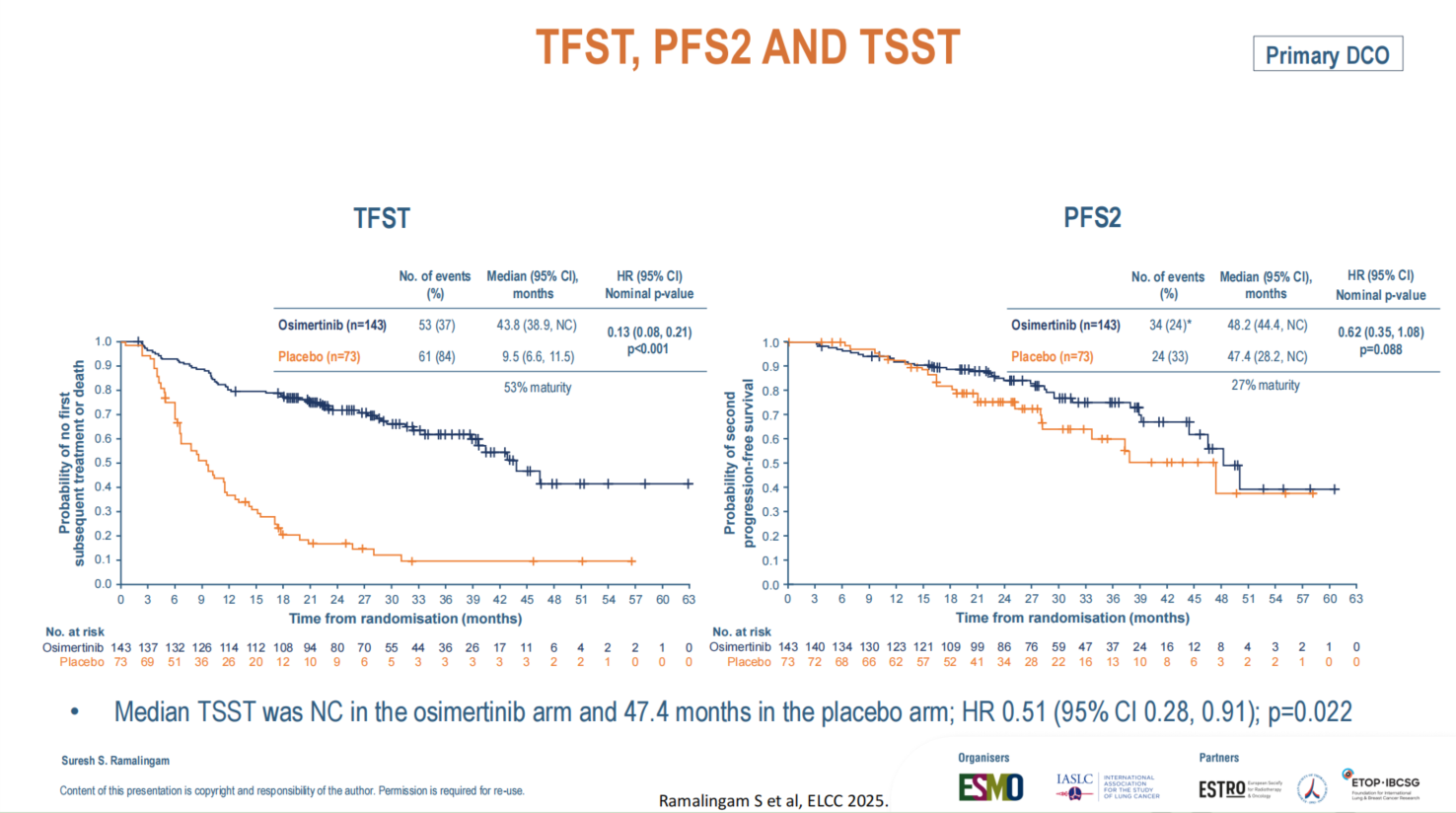
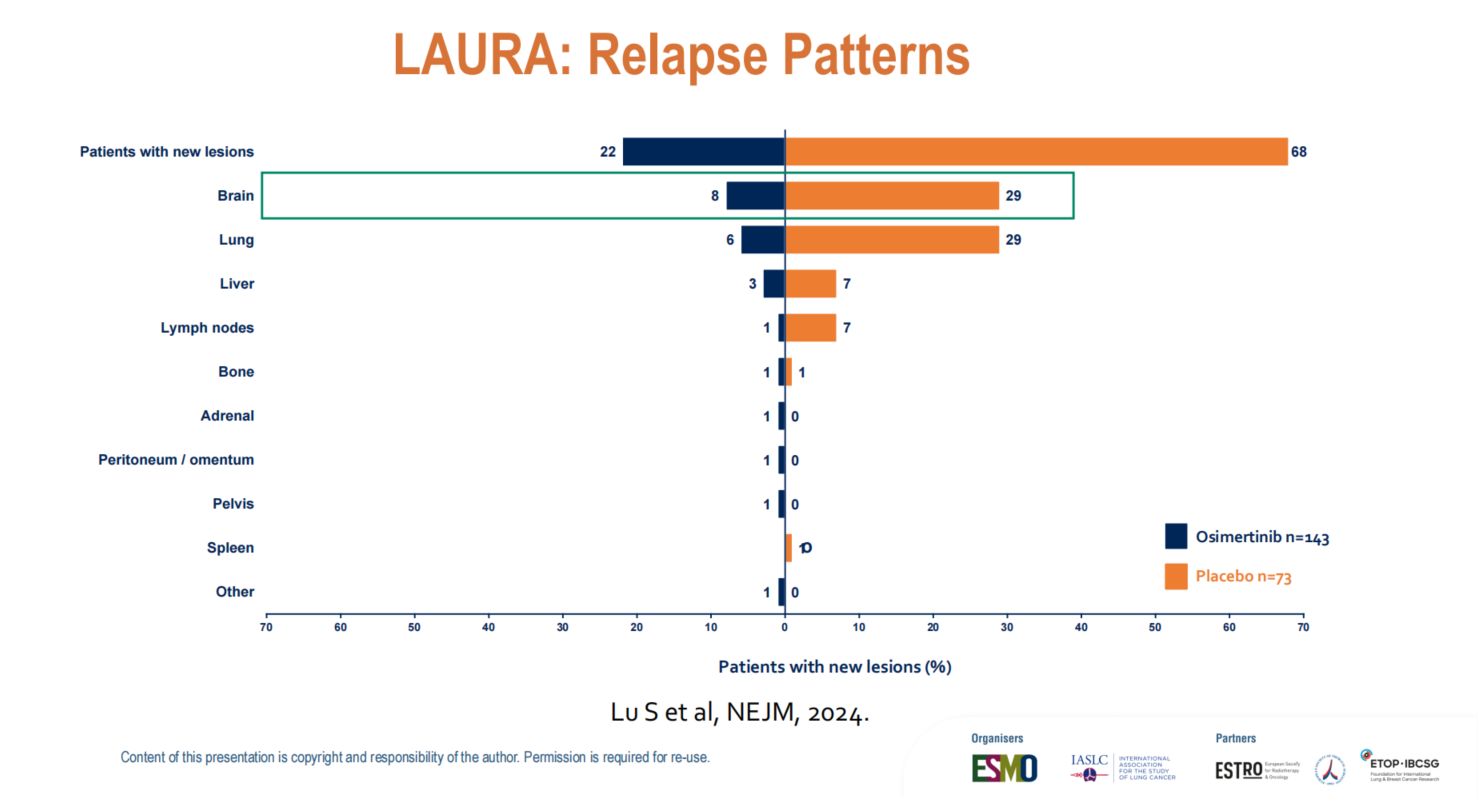
值得注意的是,在安慰剂组发生疾病进展的患者中,约80%交叉接受了奥希替尼或其他三代TKI治疗,如此高比例的有效交叉治疗将如何影响最终的OS,结果令人期待。复发模式分析则显示,安慰剂组脑进展发生率近30%,肺部进展约30%;而奥希替尼组分别大幅降至8%和6%。这充分证实奥希替尼巩固治疗可同时有效预防局部区域复发和脑转移。
安全性方面,放射性肺炎在奥希替尼组发生率为48%(安慰剂组38%),多数为1-2级(3级仅2%);间质性肺病(ILD)在奥希替尼组发生率为8%,整体安全可控。
MRD检测前景广阔但尚未进入临床常规
Ramalingam教授详细介绍了LAURA研究中采用肿瘤知情(tumor-informed)超高灵敏度检测方法进行的分子残留病灶(MRD)探索性分析。在216例患者中,52例完成了完整的MRD分析(奥希替尼组34例,安慰剂组18例)。
研究结果显示,56%的患者在放化疗后、研究入组时即可检测到MRD阳性。在安慰剂组中,基线MRD阳性者的中位PFS仅为5.8个月,而MRD阴性者为11.1个月。并且值得关注的是,安慰剂组100%的患者在放化疗后要么MRD阳性,要么存在残余影像学病灶,意味着几乎所有患者体内都有疾病持续存在的证据,这也解释了安慰剂组患者的预后不佳。在治疗动态变化上,奥希替尼组中有84%的基线MRD阳性患者实现了MRD清除,而安慰剂组的自发清除率为0%。MRD检测到分子复发的时间,比影像学进展(PD)中位提前了5个月,凸显了其预警价值。
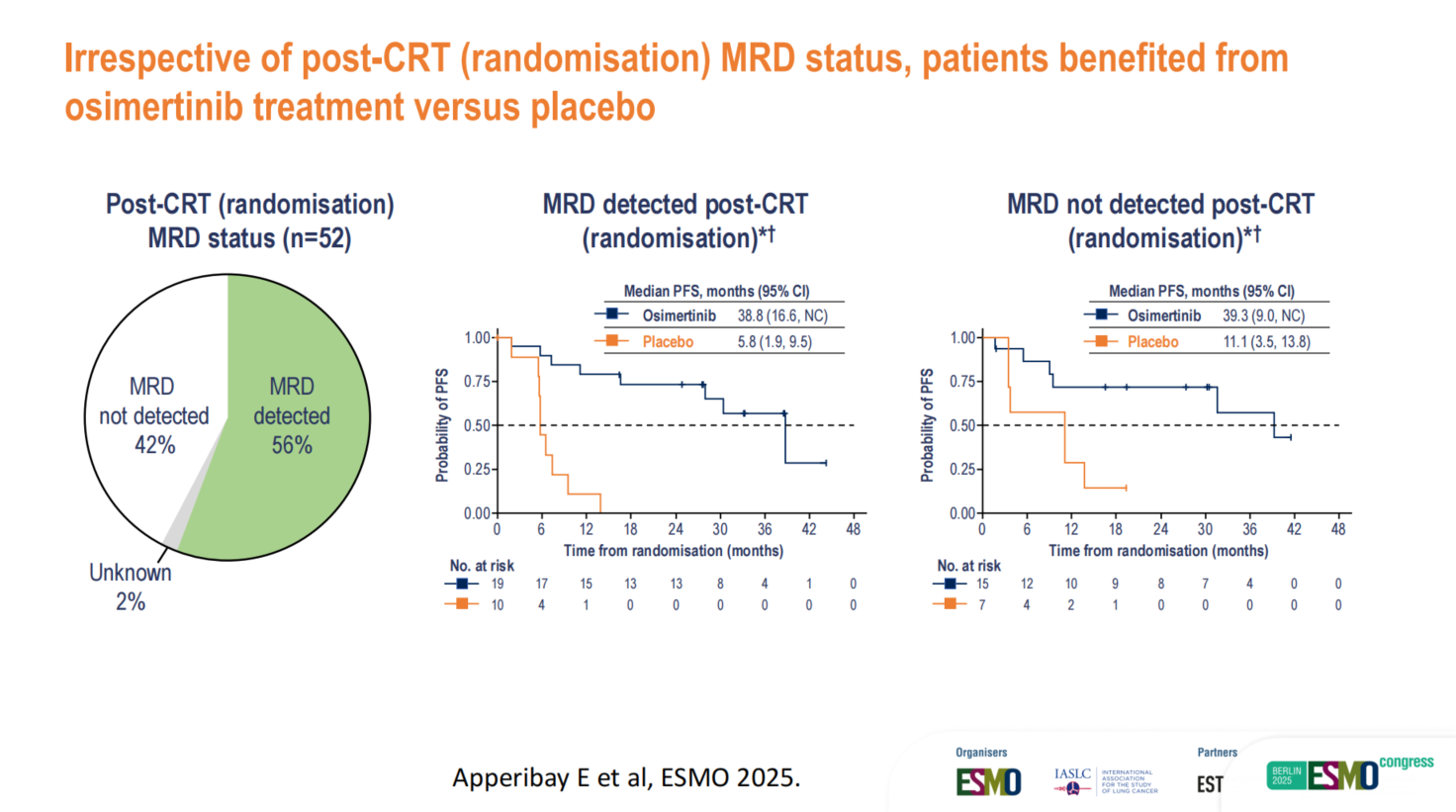
然而,Ramalingam教授发出了极其审慎的提醒:在30例未发生MRD分子进展的患者中,仍有11例出现了影像学进展。“MRD阴性并不等同于绝对安全。” 他强调,基于现有的检测技术,不建议根据MRD状态来决定治疗降级或停药,这一个体化策略目前仍应严格限制在临床研究范畴内。
POLESTAR研究与其他驱动基因探索
来自中国人群的POLESTAR研究为LAURA的结果提供了强有力的验证。该研究采用三代TKI阿美替尼,设计与LAURA高度一致(共纳入147例患者)。结果显示,阿美替尼组中位PFS为30.4个月,而安慰剂组仅3.8个月(POLESTAR研究安慰剂组PFS甚至差于LAURA),疾病进展风险降低80%(HR=0.20),且复发模式的改善也与LAURA高度一致。
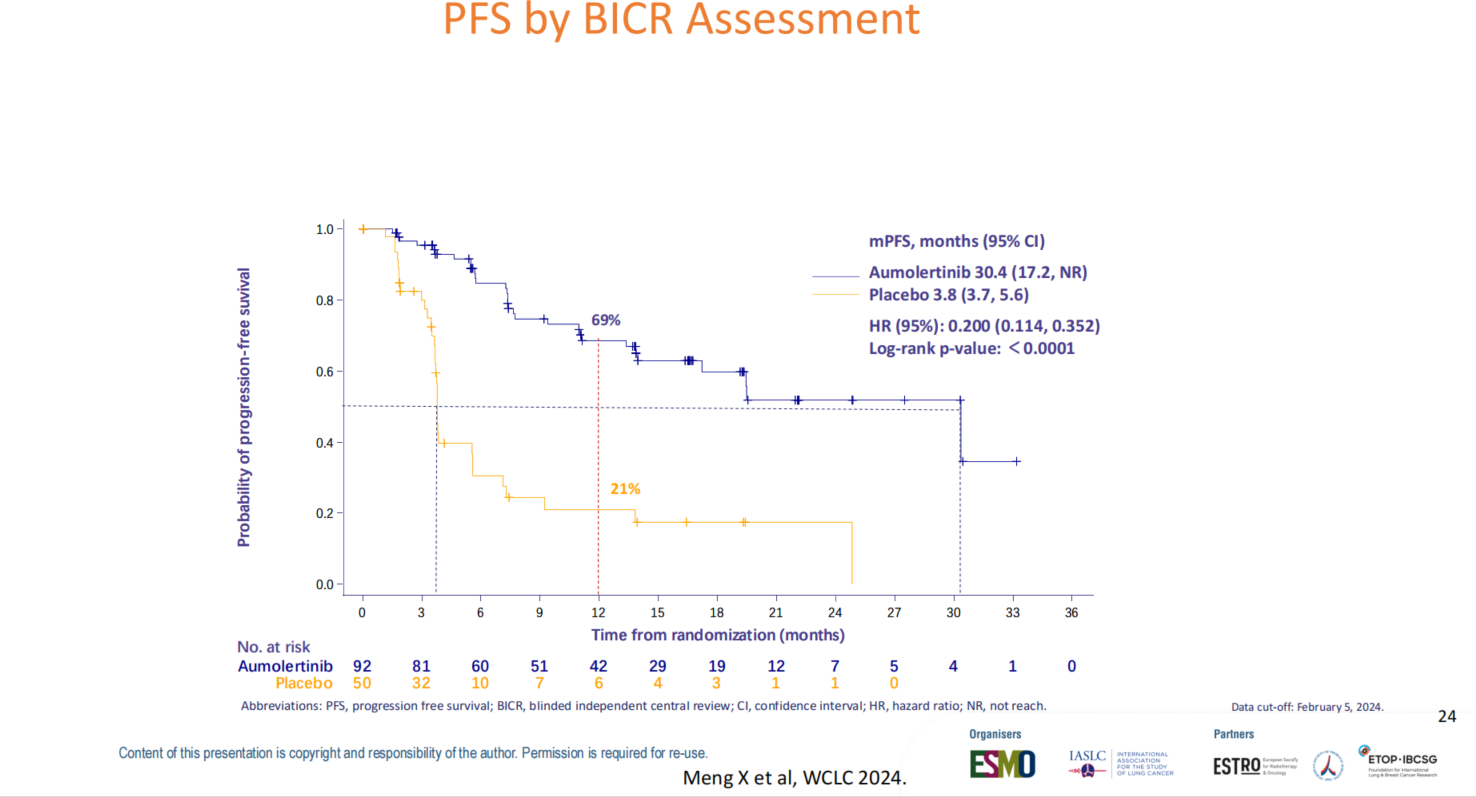
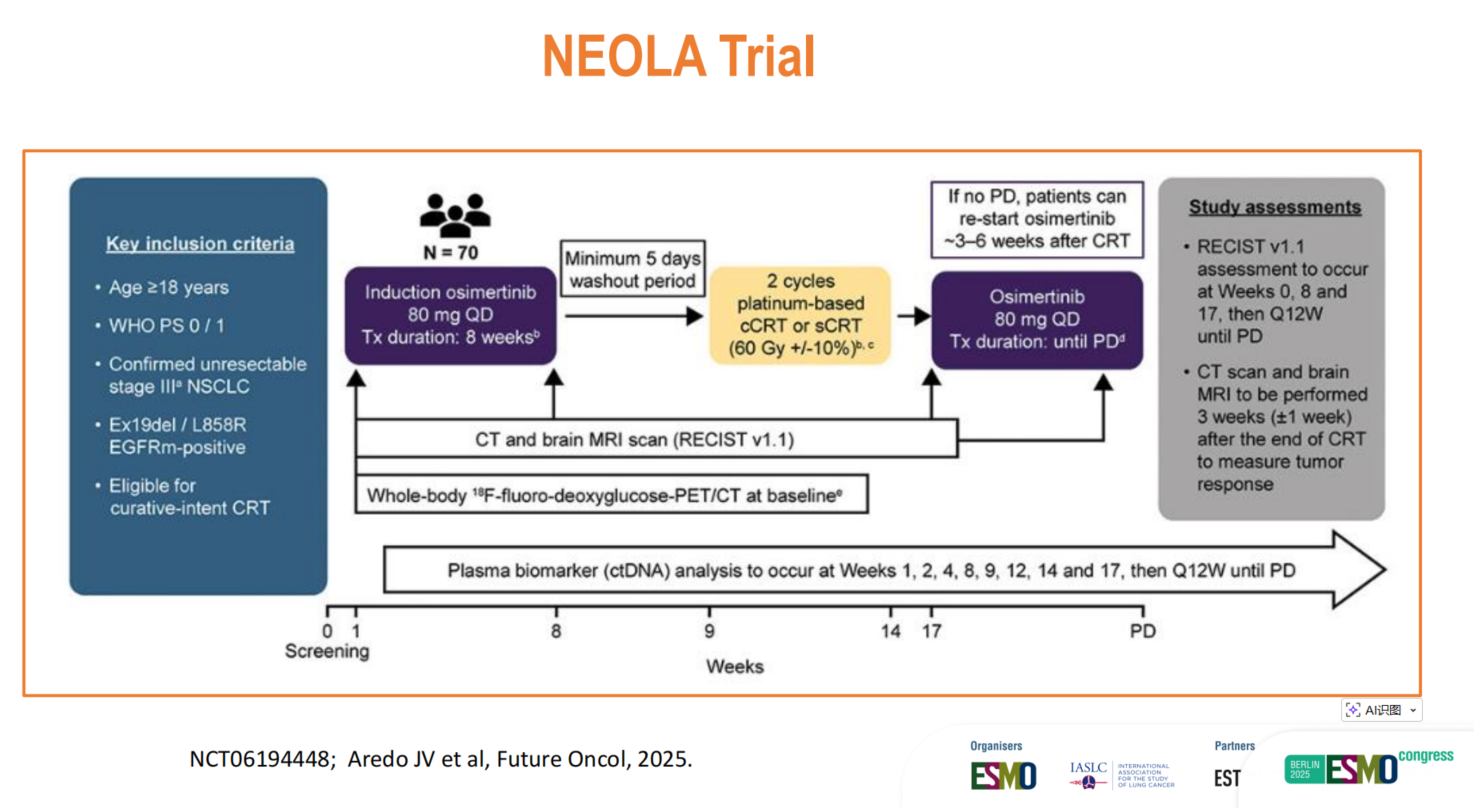
在探索性治疗模式方面,Ramalingam教授分享了多项前沿进展:NEOLA试验(进行中,70例)正在评估“诱导奥希替尼8周→序贯放化疗或同步放化疗→奥希替尼再巩固”的全新模式。
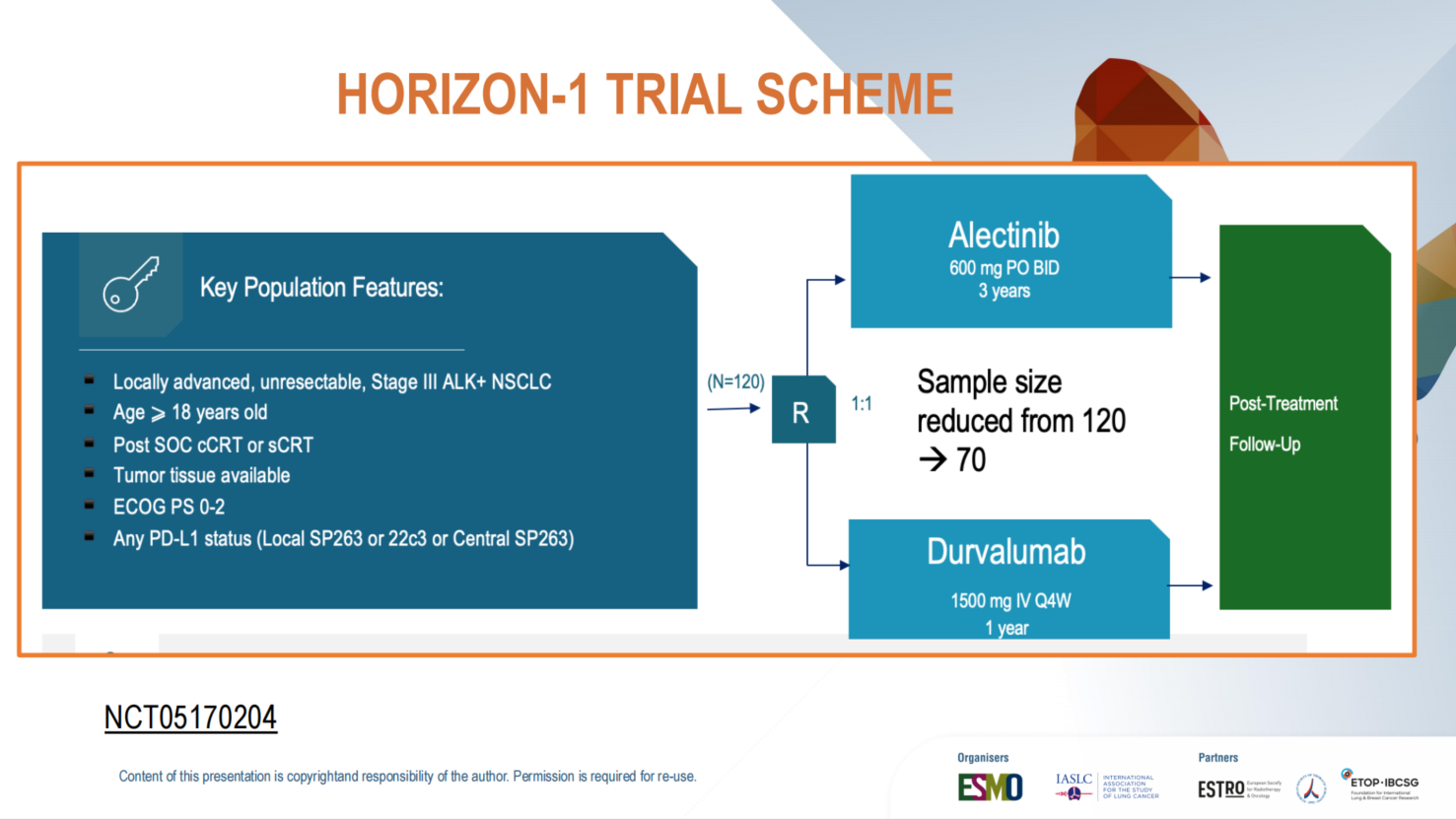
针对ALK阳性患者,多中心回顾性分析显示,放化疗后ALK-TKI巩固治疗较度伐利尤单抗或临床观察预后更优。目前,HORIZON-1试验正在前瞻性比较阿来替尼巩固3年与度伐利尤单抗1年的疗效。
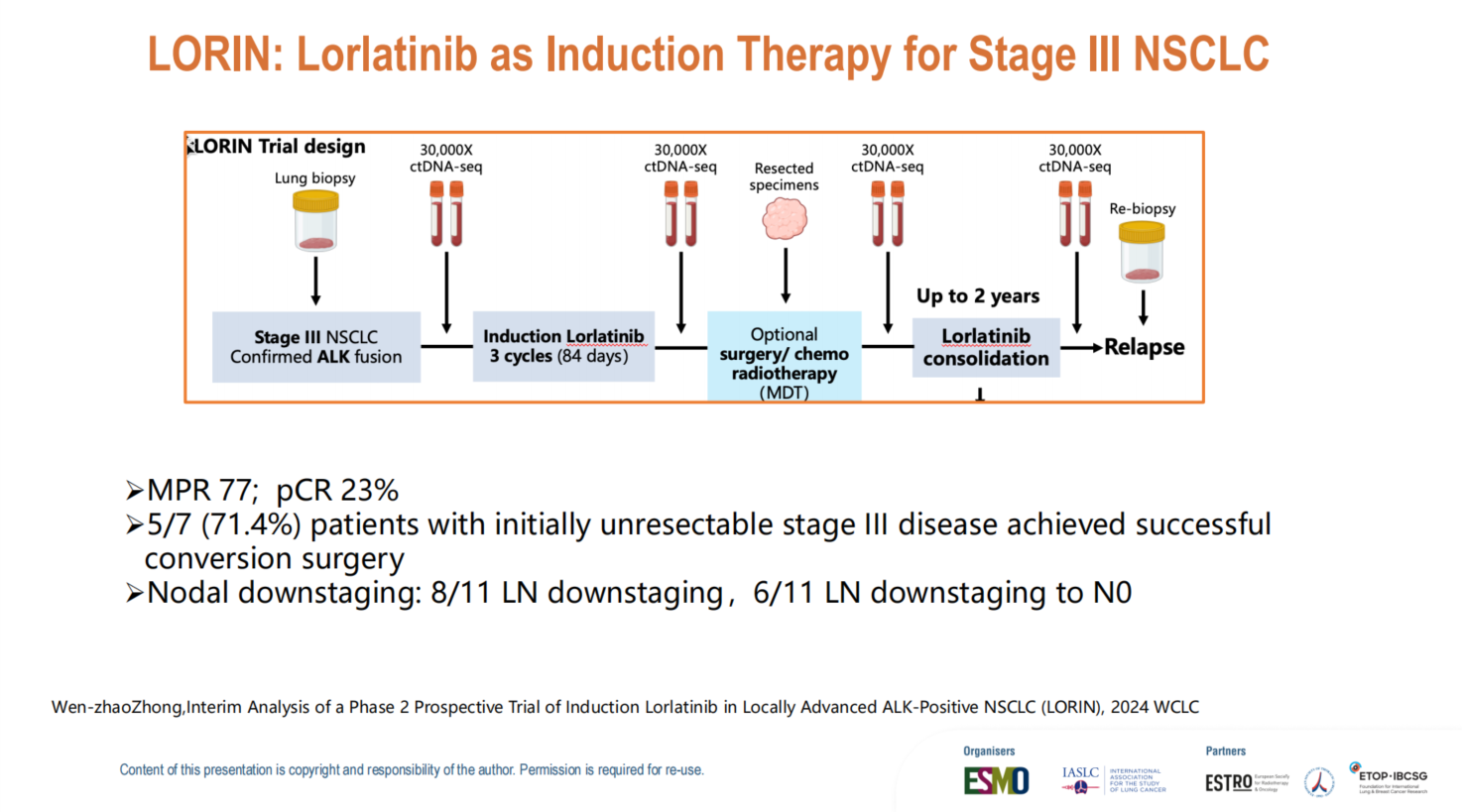
洛拉替尼新辅助治疗(3个月)的初步数据显示,主要病理缓解率(MPR)达77%,病理完全缓解率(pCR)为23%,7例初始不可切除患者中有5例成功实施了手术,展现出巨大的转化治疗潜力。
临床实践建议与未来方向展望
在大会总结环节,Ramalingam教授基于现有循证医学证据,提出了极具指导意义的结论:
EGFR突变的分子特征:脑进展是常见事件,全身系统性微转移是局部晚期EGFR突变患普遍存在的问题。
靶向巩固治疗:针对EGFR突变局部晚期不可切除NSCLC,放化疗后EGFR-TKI巩固治疗可显著改善PFS并显示出OS获益趋势。
TKI角色的重新定义:针对其他驱动基因突变,TKI 的作用尚待进一步研究。
MRD的临床应用:尽管 MRD 评估是一项令人振奋的新型工具,但在其正式进入常规临床应用之前,仍需经历多个环节。因此,在临床试验以外的场景中,我目前不建议使用该项评估手段进行临床决策。
排版编辑:肿瘤资讯-明小丽











 苏公网安备32059002004080号
苏公网安备32059002004080号


