三阴性乳腺癌(TNBC)是乳腺癌分子亚型中侵袭性最强、预后最差的类型,当转移性肿瘤负荷易引发器官功能急剧恶化,即出现内脏危象(VC);其中肝内脏危象(HVC)因常伴随胆红素快速升高,即便接受标准治疗,死亡率仍高达90%。尽管靶向滋养层细胞表面抗原2(Trop-2)的抗体药物偶联物(ADC)戈沙妥珠单抗(SG)在ASCENT研究中已确立其转移性TNBC二线标准治疗的地位,但由于内脏危象患者未被纳入研究中,SG在HVC人群中的临床应用始终缺乏循证依据。【肿瘤资讯】结合1例多线治疗失败后突发HVC的晚期TNBC患者的完整诊疗过程,深入探讨SG在HVC挽救治疗中的疗效与价值,以期为此类极重症患者的临床诊疗提供新思路与参考。

治疗过程
初诊与根治性治疗阶段
2020年8月,一名43岁女性因发现乳腺肿物就诊,该患者无基础疾病史及肿瘤家族史,经穿刺活检确诊为TNBC伴左侧腋窝淋巴结转移。完成8个周期新辅助化疗后,患者于2021年1月接受左乳改良根治术。术后病理提示:乳腺浸润性导管癌,组织学Ⅲ级,肿瘤大小4 cm×2.5 cm×2 cm,可见脉管瘤栓,伴1枚腋窝淋巴结转移。
免疫组化结果:雌激素受体阴性(ER-)、孕激素受体阴性(PR-)、人表皮生长因子受体2阴性(HER2-),Ki-67增殖指数70%。
术后患者接受总剂量50 Gy/25次的辅助放疗,序贯口服卡培他滨强化辅助化疗。该阶段患者综合治疗耐受性良好,未出现显著不良反应。
首次远处转移(肺转移)的一线治疗
根治术后不足1年,患者于2021年9月复查胸部CT发现肺部多发转移灶。针对此次复发,临床团队采用晚期TNBC标准治疗方案——白蛋白结合型紫杉醇化疗。完成6个周期化疗后,影像学随访评估显示肺部转移灶稳定,病情得到初步控制。
脑转移进展与二线联合治疗
2022年5月,患者常规随访行头颅MRI检查,发现脑转移灶。患者接受脑部病灶定向放疗;同时联合程序性死亡受体1(PD-1)抑制剂帕博利珠单抗行免疫治疗,以期通过激活系统性T细胞抗肿瘤免疫反应,实现颅内外病灶的长效控制。
疾病反复进展与多线后线治疗
2023年4月,胸部CT提示肺部转移灶再次增大。因患者主观强烈拒绝继续接受全身静脉化疗,临床团队调整治疗策略,予肺部转移灶定向放疗联合帕博利珠单抗单药维持治疗。
2023年9月,患者颅内病灶出现进展。经充分沟通后,患者勉强同意重启化疗,接受顺铂联合吉西他滨(GP方案)化疗叠加帕博利珠单抗的综合治疗。2个周期后复查显示,肺部及脑部病灶较基线缩小,评估达到部分缓解(PR)。但患者在此期间出现严重化疗相关不良反应,拒绝继续静脉化疗,治疗方案被迫调整为口服卡培他滨联合帕博利珠单抗维持。
2024年1月复查提示脑转移灶消退、肺部病灶稳定,此时患者拒绝继续口服化疗,最终仅予帕博利珠单抗单药维持治疗。
HVC爆发
2024年4月,患者突发明显腹胀。肝脏MRI检查示:肝内见弥漫性多发转移灶;超声引导下肝穿刺活检证实为乳腺来源低分化癌伴坏死,IHC再次确认ER(-)、PR(-)、HER2(-),Ki-67指数60%,且BRCA1/2结果为阴性。实验室检查显示患者总胆红素飙升至40.6 μmol/L(超过正常上限1.5倍),天门冬氨酸氨基转移酶(AST)、丙氨酸氨基转移酶(ALT)、碱性磷酸酶(ALP)、γ-谷氨酰转移酶(GGT)等肝酶指标亦显著升高。该临床表现完全符合欧洲肿瘤内科学会(ESMO)指南中HVC的诊断标准。
戈沙妥珠单抗(SG)挽救治疗
针对多线治疗失败且合并HVC的绝境,结合患者既往接受帕博利珠单抗治疗曾获临床缓解的病史,临床团队启动新型靶向Trop-2的ADC药物戈沙妥珠单抗联合帕博利珠单抗的挽救性治疗方案。
仅完成2个周期治疗后,2024年5月复查影像学显示肝内转移肿瘤负荷显著降低,同时血清糖类抗原125(CA125)、糖类抗原153(CA153)水平明显下降。治疗期间,患者出现尿频、尿急、尿痛伴血肌酐升高,临床高度怀疑为免疫介导性膀胱炎,遂停用帕博利珠单抗,改为SG单药维持治疗。
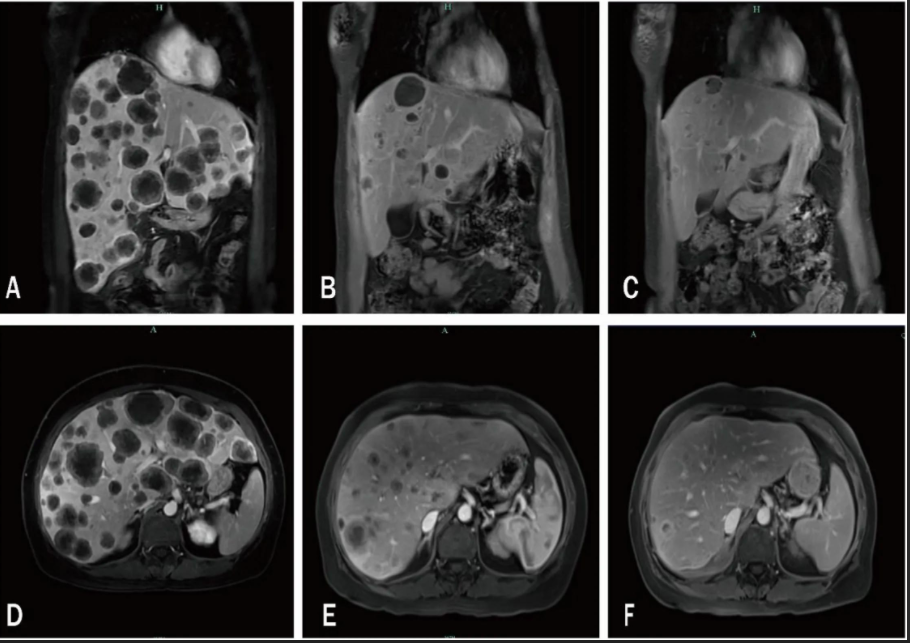
注:A, D:2024年4月9日,显示多处肝内转移;B, E:两次治疗周期后,2024年5月26日显示肿瘤显著退化;C, F:2024年7月31日随访显示肝转移负荷持续减少。
后续随访显示肝脏病灶持续退缩,患者生活质量良好,PFS延长至16.3个月,HVC被成功逆转。然而,因SG为自费药物且费用高昂,患者自行延长给药间隔、减少治疗频率,转而寻求口服中药治疗。
2025年8月CT检查提示肝内病灶再次增大;2025年11月,患者因大量腹水、重度贫血及无尿入院,腹腔穿刺抽出不凝血性液体,提示肝转移瘤破裂出血,最终因循环衰竭离世。
讨论
TNBC因缺乏ER、PR及HER2表达,传统内分泌治疗和抗HER2靶向治疗均无效,预后极差。Trop-2是一种跨膜上皮糖蛋白,80%~90%的TNBC中呈高表达,且与肿瘤增殖加速、生存期缩短直接相关,是当前极具潜力的治疗靶点。SG是由人源化抗Trop-2单克隆抗体、可裂解连接子及高活性拓扑异构酶Ⅰ抑制剂(SN-38)构成的创新型ADC药物,不仅可通过精准内吞作用将高浓度毒性载荷递送至肿瘤细胞内并释放,造成DNA链断裂,还能通过“旁观者效应”杀伤周围Trop-2表达阴性的异质性肿瘤细胞,同时介导抗体依赖性细胞毒性(ADCC)。这种多重杀伤机制,使其在多线耐药、高度异质性的晚期TNBC中仍能发挥强效抗肿瘤活性。
在Ⅲ期注册临床研究ASCENT中,SG已被证实可显著延长既往接受≥2线系统治疗的转移性TNBC患者的PFS和总生存期(OS);尤其在肝转移亚组分析中,SG亦展现出优于标准化疗的生存获益,奠定了其作为TNBC后线标准治疗方案的地位。但需明确的是,由于内脏危象患者病情进展极快、预期生存期极短,包括ASCENT研究在内的各类新药临床试验均将严重内脏受累或合并HVC的患者严格排除。
本病例作为全球首个报道SG治疗TNBC合并HVC疗效的真实世界病例,具有极高的临床突破价值:在患者因肝弥漫性转移导致肝功能急剧恶化、无标准治疗可用的绝境下,SG仅经2个周期治疗便实现肝内病灶快速大幅缩瘤,迅速逆转胆红素异常及脏器衰竭;其16.3个月的PFS,远超既往文献报道的HVC患者3-15个月的中位生存期,直接填补了SG在危重乳腺癌治疗领域的循证医学空白。
最后,本病例的结局令人惋惜,也深刻凸显药物经济学的价值与意义。ADC药物的抗肿瘤效应高度依赖规范的给药剂量和暴露周期,患者因无法承担高昂治疗费用,自行延长用药间隔、降低治疗频率,导致血药浓度无法维持有效杀伤水平,最终诱发肿瘤耐药复发及致命性破裂出血。这一结果警示业界:在推动前沿医学创新的同时,亟需通过大幅价格谈判、完善患者援助项目、优化医保支付路径等综合手段,打破创新药物的可及性壁垒,避免患者因经济原因错失生存机会的悲剧重演。
小结
该病例详细报道了全球首例SG成功逆转TNBC合并HVC的真实诊疗全过程,充分证实SG不仅可用于晚期耐药性TNBC的治疗,即便在患者肝功能因弥漫性转移极度恶化、多线传统治疗无效的内脏危象绝境下,仍具备起效迅速、缩瘤强效、疗效持久的卓越临床潜能,为这部分被常规临床试验排除的高危极重症患者开辟了新的生存希望。未来,亟需针对内脏危象等特殊人群开展更深入的前瞻性临床研究,同时通过全社会多方协同提升药物可及性,以期让更多危重症患者真正从靶向ADC治疗中获得长期高质量生存。
Ye J, Ye J, He H, Jiang Z, Wang Y, Wang L. Efficacy of sacituzumab govitecan in triple-negative breast cancer with hepatic visceral crisis: a case report. Front Oncol. 2026 Feb 27;16:1790357.
排版编辑:肿瘤资讯-slb











 苏公网安备32059002004080号
苏公网安备32059002004080号


