2026年3月,一项针对同源重组缺陷(HRD)转移性胰腺癌的II期临床研究——POLAR试验的结果,在知名医学期刊Nature Medicine(IF 50)正式见刊。该研究由美国纪念斯隆-凯特琳癌症中心发起,在生物标志物分层的转移性胰腺癌患者中,系统评估了帕博利珠单抗联合奥拉帕利作为铂类化疗后维持治疗的疗效与安全性。
胰腺癌是预后极差的恶性肿瘤之一,免疫检查点阻断(ICB)在未经基因组选择的胰腺癌患者中几乎无效。POLAR试验的重要价值在于:在生物标志物精准分层的铂敏感性胰腺癌人群中,系统检验了PARP抑制剂与PD-1阻断联合维持治疗的策略,并同步整合了深度转化性分析,为胰腺癌精准免疫治疗路径的后续研究提供了重要的生物学依据和临床参考。
为何在HRD转移性胰腺癌中探索这一联合策略?
胰腺癌是预后最差的实体瘤之一,预计将成为2030年前癌症相关死亡的第二大原因。尽管多药化疗方案有所进步,总体生存获益依然有限。更关键的是,胰腺癌对免疫检查点阻断几乎普遍耐药,根本原因在于其低免疫原性和高度免疫抑制性的肿瘤微环境。
然而,携带BRCA1、BRCA2或PALB2胚系/体系突变的HRD胰腺癌患者(约占全部胰腺癌的9%以内)是一个特殊亚群:这类肿瘤对铂类化疗高度敏感,奥拉帕利单药维持治疗亦已获美国FDA批准并证明了无进展生存期(PFS)获益(POLO试验)。与此同时,HRD肿瘤特有的基因组不稳定性,包括插入/缺失突变负荷升高、移码突变富集,从理论上赋予其更高的免疫原性,由此提出了一个临床假设:在铂类诱导化疗后的维持窗口期,将PARPi与PD-1阻断联合,能否在HRD胰腺癌中实现更持久的疾病控制?POLAR试验正是对这一假设的前瞻性检验。
POLAR研究设计:精准分层的三队列
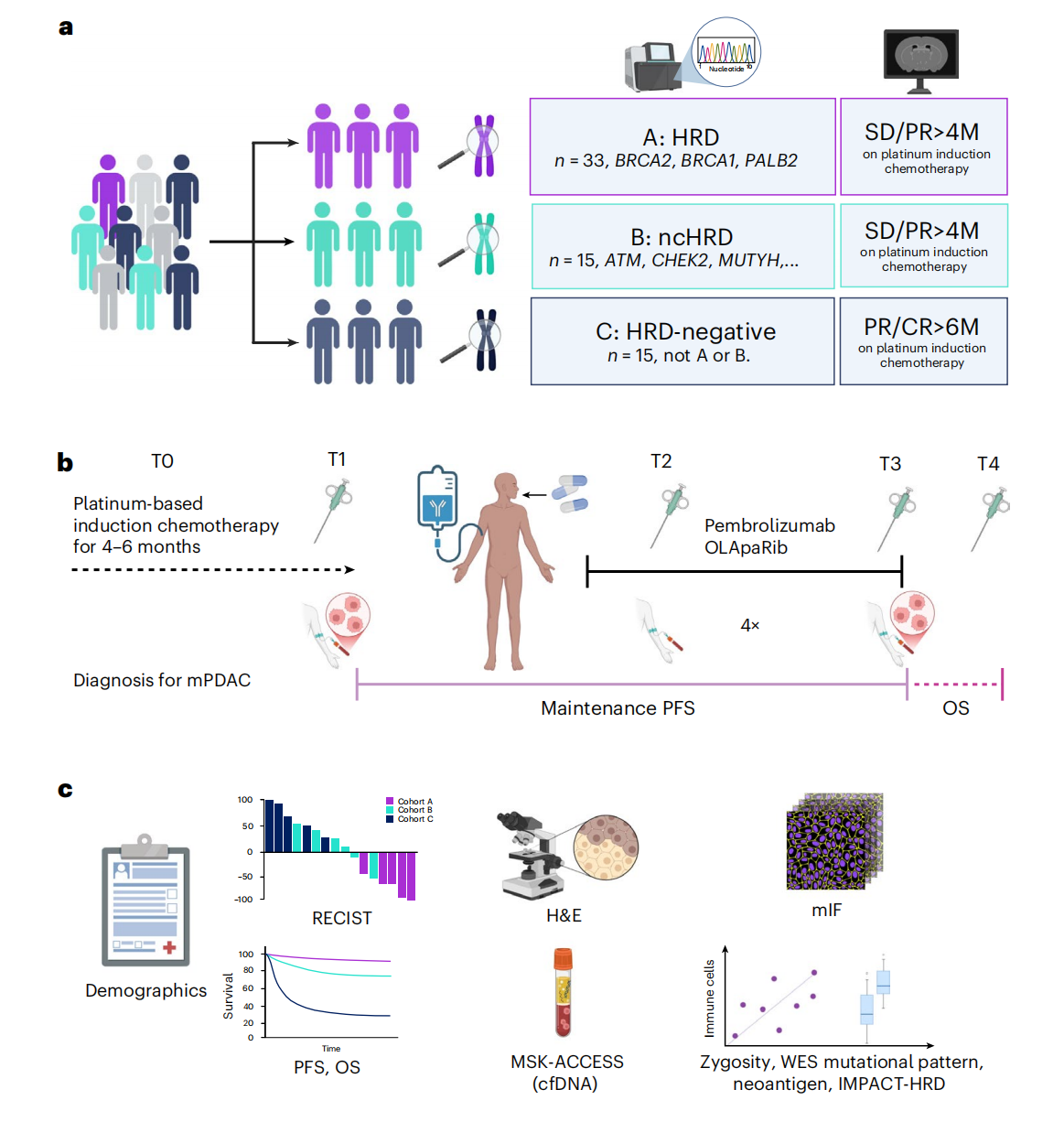
POLAR是一项单中心、非随机化的II期生物标志物篮子研究,于2021年1月至2024年3月共入组63例转移性胰腺癌患者,依据基因组特征和铂类治疗临床反应前瞻性分为三个队列:
队列A(核心HRD,n=33):携带BRCA1、BRCA2或PALB2致病性胚系/体系突变,且铂类治疗超过4个月无进展。其中BRCA2突变最常见(n=18,53%),其次为BRCA1(n=10)和PALB2(n=6)。
队列B(非核心HRD,n=15):携带其他候选HRD基因突变(如ATM、CHEK2、MUTYH等),铂类治疗超过4个月无进展。ATM突变最常见(n=8,53%)。
队列C(HRD野生型铂敏感,n=15):铂类治疗至少6个月(12周期改良FOLFIRINOX)持续有效,但无HRD或非核心HRD基因突变。
所有患者均接受奥拉帕利300 mg每日两次口服联合帕博利珠单抗静脉输注(前6个月每3周一次,此后每6周一次),直至疾病进展或不可耐受的毒性。研究同步收集了基线、治疗中及进展后的肿瘤组织和外周血样本,用于全外显子测序(WES)、循环肿瘤DNA(ctDNA)和多重免疫荧光(mIF)分析。数据截止日期为2025年6月25日。
队列A采用两阶段设计,共同主要终点为:根据RECIST标准,客观缓解率(ORR)≥43%,及6个月PFS率≥77%。
主要结果:HRD队列呈现持久生存获益,但未达预设主要终点
主要终点
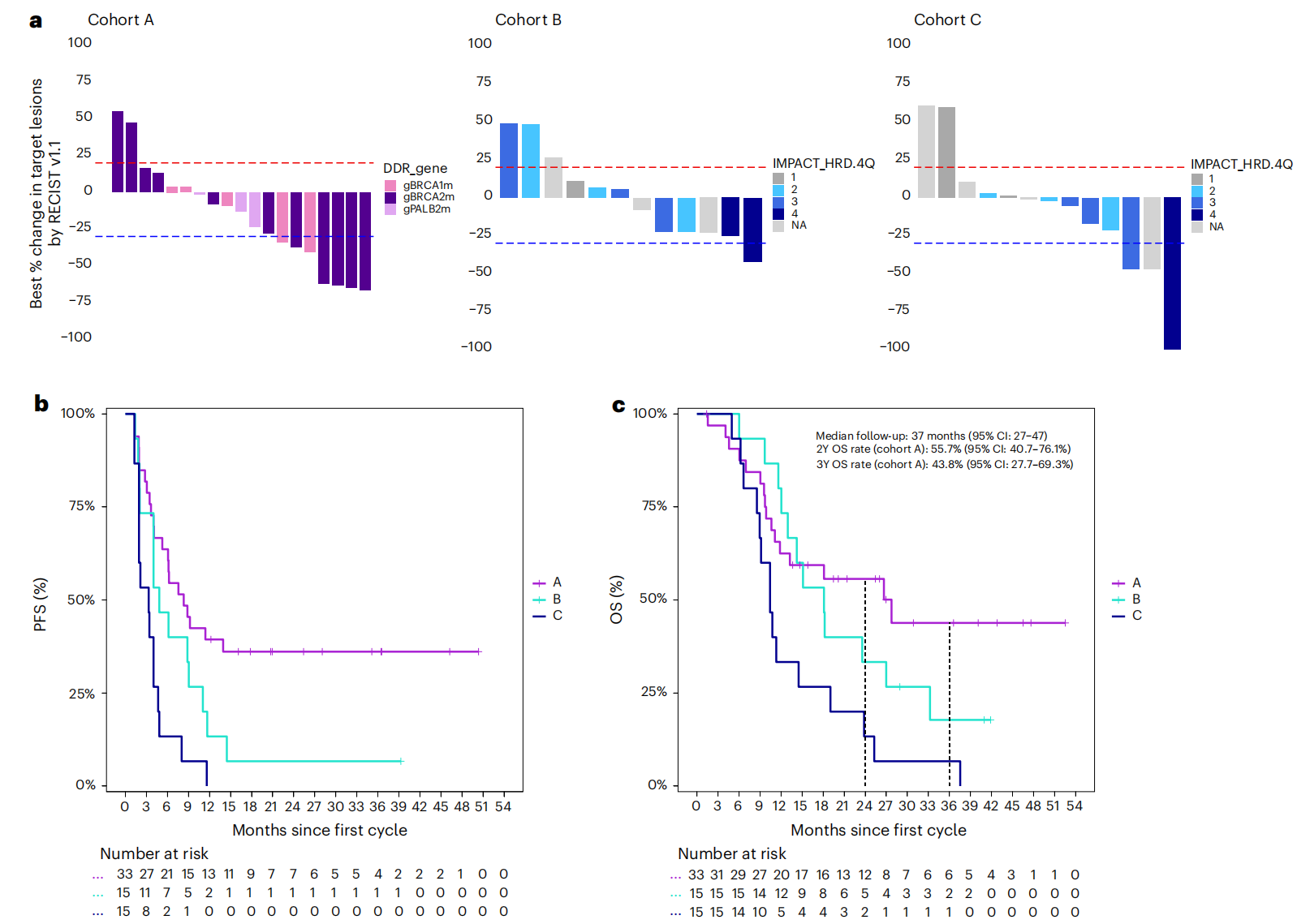
在63例入组患者中,46例(73%)在维持治疗启动时存在可评估病灶(RECIST标准)。队列A中,20例可评估患者的ORR为35%(7/20),6个月PFS率(全队列n=33)为64%。两项共同主要终点均未达到预设标准(ORR≥43%、6个月PFS率≥77%)。
值得关注的是,队列A中有13例(39%)患者在入组时影像学呈不可测量病灶状态。在这13例中,10例在维持治疗期间无进展时间超过4个月(其中2例PFS>6个月,8例PFS>12个月)。若在事后探索性分析中将这部分患者纳入计算,队列A的探索性缓解率升至52%(17/33)。
生存数据(PFS、OS)
队列A的中位随访时间为37个月,主要生存数据如下:中位PFS 8.3个月,中位总生存期(OS)28个月,2年OS率56%,3年OS率44%;队列B的中位PFS为4.8个月,中位OS为18个月;队列C的中位PFS为3.3个月,中位OS为10个月。
疾病控制率(DCR)
队列A的疾病控制率(DCR)为80%(16/20),队列B为75%(9/12),队列C为50%(7/14)。
亚组分析
在队列A内部,BRCA2突变(n=18)和PALB2突变(n=6)患者的中位PFS和OS在数值上相近且长于BRCA1突变患者(n=9):中位PFS分别为9.9个月、12.0个月和6.1个月;中位OS分别为28.0个月、27.0个月和18.0个月;24个月OS率分别为59%、67%和42%。
安全性
治疗的总体耐受性良好,未出现新的安全性信号,无4-5级治疗相关不良事件(TRAE)。奥拉帕利相关3级不良事件主要为贫血(n=10,15%)。帕博利珠单抗相关3级免疫相关不良事件(irAE)发生于4例患者,包括肺炎和结肠炎。
转化性分析:谁在获益,为什么?
POLAR试验整合了系统性转化性分析,揭示了哪些生物学特征与持久临床获益相关。
ctDNA动态与分子残留病灶
研究对30例代表性患者的基线(T1)与治疗6周(T2)血浆进行了MSK-ACCESS液体活检配对分析。基线ctDNA检测显示大多数患者处于分子残留病灶(MRD)状态,平均变异等位基因频率(VAF)低。在5例PFS超过36个月的长期获益患者中,4例在T1和T2两个时间点均呈现不可检测或接近不可检测的ctDNA水平,提示MRD阴性状态可能是持久获益的潜在预测指标。
HRD肿瘤的免疫原性特征
对35例基线肿瘤样本的WES分析显示,队列A(HRD)相比队列C(HRD野生型),总插入/缺失突变负荷(中位数10 vs 2,P<0.01)和移码插入/缺失负荷(中位数8 vs 2,P<0.01)均显著更高。WES来源的肿瘤突变负荷(TMB)在队列A中也显著高于队列C(中位数2.8 vs 1.25,P=0.035)。IMPACT-HRD评分同样在队列A中显著更高(中位数47 vs 24)。
在免疫浸润方面,队列A的基线肿瘤浸润淋巴细胞(TIL)密度(H&E评分中位3.5)显著高于队列C(中位2,P=0.035),且TIL密度较高的患者PFS更长。mIF定量分析进一步显示,队列A的CD3⁺CD8⁺ T细胞浸润显著高于队列C(P<0.05)。
值得注意的是,尽管IMPACT-HRD评分与预测新抗原负荷呈显著正相关(R=0.48,P=0.008),但新抗原负荷与CD8⁺ T细胞浸润之间并无显著相关性(P=0.95)。
研究意义与临床价值
POLAR试验有几点值得临床医生和研究者关注:
关于未达主要终点的解读:研究者在讨论中指出,队列A的预设主要终点门槛(ORR≥43%,6个月PFS率≥77%)在事后看来设定过于严格,对于一项非注册性研究而言具有较强假设性。试验未达主要终点,但在核心HRD人群中观察到的持久缓解和长期生存数据,仍具有明确的临床信号价值。
HRD分型的精准性:研究再次证实,以BRCA1/2和PALB2突变界定的核心HRD是目前胰腺癌中很强的预后和预测生物标志物,铂敏感性作为HRD生物学的临床替代指标,亦在本研究中得到进一步支持。
MRD状态作为疗效监测工具:探索性ctDNA分析提示,分子残留病灶阴性可能是长期获益的潜在预测指标,为未来免疫治疗试验中整合液体活检监测提供了依据。
研究者指出,基于POLAR的发现,针对HRD胰腺癌的随机对照研究(如SWOG S2001,NCT04548752)正在推进,整合DDR状态、新抗原质量和肿瘤微环境重塑的精准免疫治疗策略是下一阶段研究方向。
Park W, O'Connor CA, Chou JF, et al. Pembrolizumab and olaparib in homologous-recombination-deficient metastatic pancreatic cancer: the phase 2 POLAR trial. Nat Med. 2026 Mar 25.
排版编辑:肿瘤资讯-Marie











 苏公网安备32059002004080号
苏公网安备32059002004080号


