近期,国际顶尖医学期刊《新英格兰医学杂志》(NEJM)发表了随机、开放标签、III期ATOMIC研究的结果。该研究由美国梅奥医学中心Frank A. Sinicrope教授牵头,联合全球300多家中心共同完成。研究聚焦根治术后的III期错配修复缺陷(dMMR)结肠癌患者,证实了在标准辅助化疗(mFOLFOX6)基础上联合PD-L1抑制剂(阿替利珠单抗)的辅助治疗方案,相比于单纯mFOLFOX6辅助化疗,能够显著延长无病生存期(DFS),3年DFS率为86.3% vs 76.2%(HR 0.50,P<0.001)。
在同期发表的社论中,美国纪念斯隆-凯特琳癌症中心Deb Schrag教授对ATOMIC的研究价值给予了高度评价,称其为III期结肠癌辅助治疗30年探索历程中的一场胜利,同时也以提出了关于dMMR患者化疗必要性、辅助与新辅助免疫治疗策略以及未来“生物标志物定制化”方案的客观思考。
【肿瘤资讯】特此整合研究核心内容及同期社论精粹,以飨读者。

研究背景与临床需求
结直肠癌(CRC)是全球范围内高发的恶性肿瘤,在Ⅲ期结肠癌患者中,尽管接受了根治性手术切除和术后辅助化疗,仍有约30%的患者最终出现疾病复发。其中,约10%~15%表现为错配修复缺陷(dMMR),从而导致微卫星高度不稳定(MSI-H)。dMMR肿瘤具有独特的生物学特征,一方面对传统的氟尿嘧啶类单药辅助化疗反应较差;另一方面,其高突变负荷及丰富的免疫原性新抗原使其对免疫检查点抑制剂(ICI)表现出高度敏感性。
2004年发布的MOSAIC研究证实,6个月氟尿嘧啶、亚叶酸钙和奥沙利铂(FOLFOX方案)辅助治疗相较6个月氟尿嘧啶和亚叶酸钙治疗,可显著改善Ⅲ期结肠癌患者的无病生存期(DFS),且这一获益同样适用于占比10%的dMMR肿瘤患者。尽管FOLFOX方案在过去20年间已成为临床标准治疗,但仍有约30%的Ⅲ期患者在接受该标准辅助治疗后出现疾病复发。在转移性dMMR结直肠癌中,KEYNOTE-177等研究已证实ICI(如帕博利珠单抗)疗效优于传统化疗。基于此,ATOMIC试验旨在探索在标准mFOLFOX6化疗基础上联合阿替利珠单抗(一种抗PD-L1抗体)是否能进一步改善Ⅲ期dMMR结肠癌患者的预后。
研究设计与方法
ATOMIC试验是一项国际多中心、随机、开放标签的Ⅲ期临床试验,由美国国家癌症研究所(NCI)下属的Alliance研究网络和德国AIO研究组共同完成。研究共纳入712例经根治性切除(R0)、病理确诊为Ⅲ期且经免疫组化确认dMMR状态的结肠癌患者,按1∶1比例随机分配至两组:
试验组(n=355):接受阿替利珠单抗(840mg,每2周一次)联合mFOLFOX6方案治疗6个月,随后继续接受阿替利珠单抗单药维持治疗6个月,总免疫治疗时长为12个月。
对照组(n=357):接受单纯mFOLFOX6方案治疗6个月。
主要终点为DFS,次要终点包括总生存期(OS)和安全性。患者中位年龄为64岁,女性占55.1%,T4和/或N2期(高危)患者占53.9%。两组患者在基线临床病理特征及预设的分层变量方面均保持良好平衡。
疗效结果:DFS显著获益,OS尚待成熟
中位随访40.9个月的数据显示,试验组显示出显著的生存获益:
DFS获益:试验组的3年DFS率为86.3%(95%CI 81.8~89.8),显著高于对照组的76.2%(95%CI 70.9~80.6),HR为0.50(95%CI 0.35~0.73,P<0.001)(图1)。
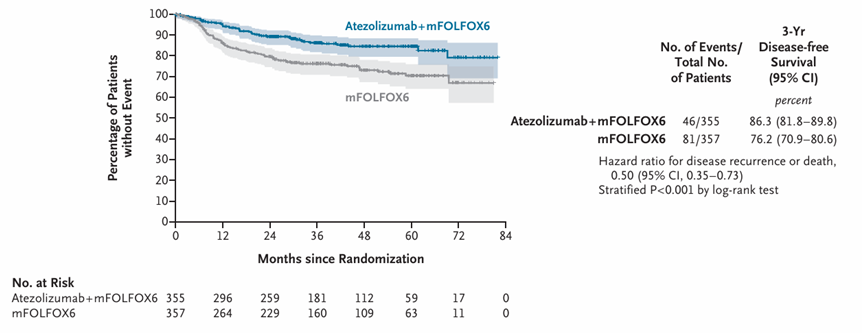
OS:整体生存的中位随访时间为45.8个月时,试验组5年OS率为89.7%,对照组为87.9%(HR 0.90,95%CI 0.55~1.47,P=0.68),尚未显示出统计学差异。同期社论指出,随着随访时间延长,OS差异仍可能不显著,原因在于对照组中复发患者后续接受了免疫治疗(84%的复发患者接受了免疫治疗),可能削弱了早期免疫干预带来的生存优势。
探索性亚组分析
预设的亚组分析显示,接受超过6个周期mFOLFOX6的患者中,联合阿替利珠单抗的DFS获益显著(HR 0.41,95%CI 0.27~0.64),而接受6个周期或更少化疗的患者中,联合治疗未观察到明显获益(HR 0.97,95%CI 0.44~2.11)。
这一发现提示,免疫治疗在辅助阶段的疗效可能与化疗的充分暴露有关,但需谨慎解读,因该分析为探索性,尚不能确立因果关系。
安全性分析:免疫联合化疗毒性可控
3级及以上不良事件在试验组更常见(84.1% vs 71.9%),以非血液学毒性(如疲劳、周围神经病变)和血液学毒性(如中性粒细胞减少)为主。免疫相关不良事件在试验组发生率略高,但3级及以上免疫相关不良事件的发生率在两组间无临床显著差异,整体安全性可控。
社论中特别指出,试验组治疗时长(12个月)长于对照组(6个月),这在一定程度上解释了疲劳等毒性反应的增加,也提示未来在免疫治疗时长上仍有优化空间。
社论评述与临床启示
1. 实践意义显著
社论指出,ATOMIC试验是在大规模、真实世界背景下完成的生物标志物导向的辅助治疗研究,其10.1%的DFS绝对获益差异已经超过了MOSAIC研究确立FOLFOX方案时的获益幅度,充分说明免疫联合化疗在高危分子亚型患者中的价值。
2. 对化疗必要性的反思
在KEYNOTE-177研究之后,免疫单药在转移性dMMR患者中已显示出优于化疗的疗效。社论敏锐提出,在辅助治疗阶段,化疗是否仍是必需?未来的试验应探讨是否可以省略化疗而仅使用ICI,以进一步降低治疗负担。
3. 辅助与新辅助之争
鉴于NICHE-2等研究已显示出新辅助免疫治疗在dMMR结肠癌中极高的病理缓解率(pCR),且新辅助策略可能诱导更广泛的T细胞应答,未来需通过前瞻性研究对比“辅助”与“新辅助”策略在dMMR结肠癌中的优劣。
4. 研究模式的转型
ATOMIC试验的成功标志着基于分子分型的大型辅助治疗试验的成熟,但未来研究需要向平台化、适应性设计转型,整合生物标志物监测与个体化治疗策略,以更高效地回答“哪些患者需要哪些治疗”的问题。
总结
在Ⅲ期dMMR结肠癌患者中,标准mFOLFOX6化疗基础上联合阿替利珠单抗辅助治疗,显著改善了DFS,疾病复发或死亡风险下降50%,且安全性可控。结合社论观点,这一成果为Ⅲ期dMMR结肠癌患者提供了新的标准辅助治疗选择,未来的研究重点将转向优化治疗周期、探索非化疗联合方案以及进一步筛选更细分的获益人群,以实现最大化的临床获益和最小化的治疗毒性。
[1] Sinicrope FA, Ou FS, Arnold D, et al. Atezolizumab plus FOLFOX for Stage III Mismatch Repair-Deficient Colon Cancer. N Engl J Med. 2026;394(12):1155-1166. doi:10.1056/NEJMoa2507874.
[2] Schrag D. ATOMIC Energy - Biomarker-Bespoke Adjuvant Therapy for Colon Cancer. N Engl J Med. 2026;394(12):1227-1228. doi:10.1056/NEJMe2517910.
排版编辑:肿瘤资讯-ZJN











 苏公网安备32059002004080号
苏公网安备32059002004080号


