

胃癌是全球高发的恶性肿瘤,中国占全球胃癌新发病例约1/3~2/5 [1] ,其中 HER2 阴性晚期患者占比超 80% [2] ,长期面临精准治疗手段匮乏的困境。
CLDN18.2 作为胃癌领域继 HER2 之后首个被证实具有明确临床价值的特异性靶点,打破了 HER2 阴性晚期胃癌缺乏有效靶向方案的僵局。《CSCO 胃癌诊疗指南》(2025 版) [3] 中针对“HER2 中低或不表达、CLDN18.2高表达”群体,已将佐妥昔单抗联合FOLFOX/XELOX作为一线重要推荐选项。
值得关注的是,因为CLDN18.2靶点独特的生物学特性,CLDN18.2靶向治疗展现出明显有别于HER2靶向和免疫治疗的获益特征,有些在既往研究中表现出“HER2靶向、免疫疗法不敏感”的人群,反而对CLDN18.2靶向治疗更为敏感,并在临床试验中体现出相较全人群更佳的生存获益。
明确这些CLDN18.2靶向治疗独特的高获益人群,对于临床上更清晰的治疗方案选择有重要意义。
本次我们邀请 中国科学技术大学附一院何义富教授 ,基于 SPOTLIGHT [4] 和 GLOW [5] 两项研究的亚组数据,深度剖析CLDN18.2治疗的高获益人群特征,并揭示其背后的生物学机制。

中国科学技术大学附一院
何义富 教授
消化道肿瘤亚专科主任
医学博士,主任医师,教授,博士生导师
青年领军人才(安徽省卫生厅第五周期学术和技术带头人)
CSCO胃癌专家委员会常委
CSCO食管癌专家委员会常委
CSCO肝癌/胆道肿瘤/临床研究专委会委员
中国抗癌协会肿瘤内科专委会常委
中国抗癌协会食管肿瘤整合康复专委会常委
中国抗癌协会胃癌/肠癌专委会委员
中国抗癌协会靶向治疗/国际医疗交流分会委员
中国抗癌协会支持治疗专业委员会内科学组副组长
中华医学会肿瘤学分会青年委员会委员
安徽省抗癌协会副理事长
安徽省医学会肿瘤内科学分会副主任委员
安徽省医师协会肿瘤分会副主委
安徽省抗癌协会食管癌专业委员会候任主委
安徽省抗癌协会癌症康复与姑息治疗专委会候任主委
安徽省临床肿瘤学会胃肠肿瘤专委会主委
2025国之名医.优秀风范

既往接受过胃切除术
mOS可达24.8个月
在佐妥昔单抗两项III期临床研究GLOW及SPOTLIGHT研究中,有一类明显高获益的人群,就是“既往接受过胃切除术”的患者。
SPOTLIGHT研究中约有30%的患者既往接受过胃切除术治疗 , 这部分患者的的中位无进展生存期(mPFS)超过1年,达到了12.4个月(vs 9.3个月),HR值为0.62(95% CI:0.41~0.94) ,获益优于全人群(10.6个月 vs 8.7个月,HR 0.75)。 而中位总生存期(mOS)达到了惊人的24.8个月(vs 15.7个月),HR值进一步降低达到了0.58(95% CI :0.38~0.87) ,显著优于全人群的获益(18.2个月 vs 15.5个月,HR 0.75)。
在GLOW研究中也展现了同样结果,对于既往接受过胃切除术的患者, mOS达到了18.8个月(vs 12.5个月),HR值为0.63(95% CI:0.41~0.98) ,优于全人群(14.4个月 vs 12.2个月,HR 0.77)。
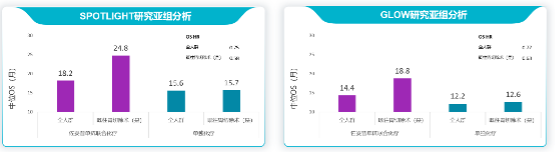
并且,在两项研究中,OS获益的HR值置信区间上限均小于1,提示该亚组可能存在更大获益,其背后的原因可能与药物安全性、耐受性有关。
佐妥昔单抗联合化疗的主要不良反应为恶心、呕吐、食欲下降等消化道反应,这类反应与胃组织的完整性密切相关——未接受胃切除术的患者因胃组织完整,对消化道刺激更为敏感,发生中重度恶心呕吐的风险更高,部分患者可能因无法耐受而中断治疗或降低剂量,影响最终疗效。
而接受过胃切除术的患者,残胃组织体积显著缩小,消化道结构发生改变,对佐妥昔单抗相关的消化道不良反应耐受性明显提升,能够足量、足疗程完成 CLDN18.2 靶向治疗,进而最大化生存获益。
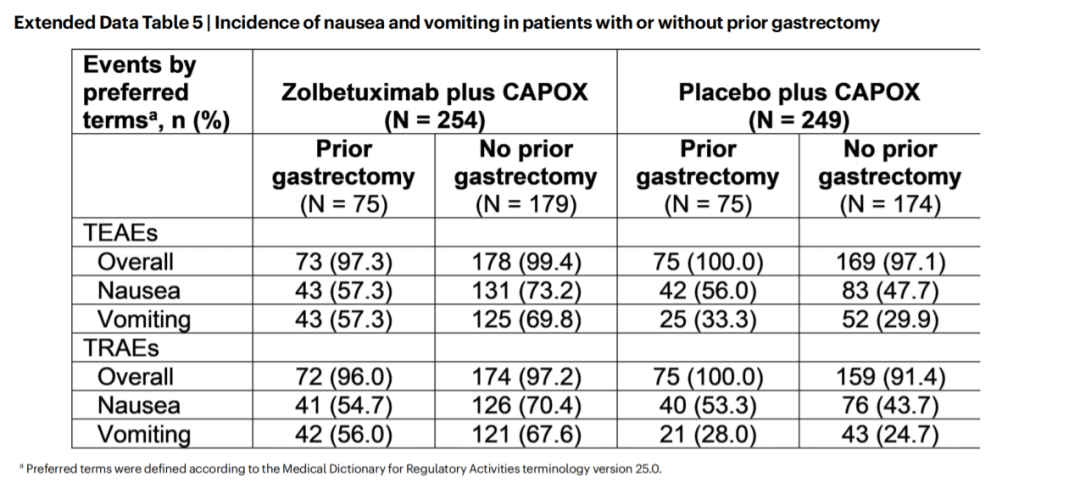
对于未接受过胃切除术的患者,我们要做好消化道不良反应的针对性管理,让其尽可能接受完整疗程,这样也可以获得显著的生存获益提升。在SPOTLIGHT研究中,研究者排除未接受研究治疗、缺乏充分药物暴露或缺乏影像学评估的患者进行重新评估后,发现依从性良好的患者mPFS突破1年,达到12.5个月,mOS更是达到了21.5个月。
而以往的晚期胃癌III期临床研究中,接受过胃切除术的患者则并未展现出类似的由安全性、耐受性带来的疗效优势。
对于HER2靶向治疗而言,ToGA研究 [6] 中曲妥珠单抗治疗组全人群OS结果的HR值为0.74。而以既往胃切除术分层,接受与未接受过胃切除术患者OS的HR值分别为0.81和0.72,二者均未与全人群形成明显的获益差异。
免疫联合化疗亦是如此。CheckMate 649 [7] 、KEYNONTE-859 [8] 、RATIONALE-305 [9] 中,全人群OS的HR值分别为0.79、0.78和0.80,既往接受过胃切除术的患者OS的HR值分别为0.76、0.69和0.78,并未展现出明显的获益差异。
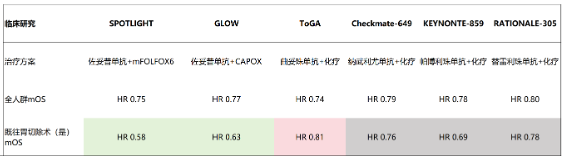
即便是考虑到CPS表达情况,免疫疗法对该类患者依旧无明显的额外获益。在CheckMate 649研究中,纳武利尤单抗联合化疗治疗PD-L1 CPS≥5、既往接受过胃切除术的患者mOS为16.2个月(vs 12.7个月 HR 0.70),与PD-L1 CPS≥5亚组相当,OS绝对值和HR值均弱于SPOTLIGHT、GLOW两项研究的对应亚组。
目前佐妥昔单抗已在CLDN18.2 高表达晚期胃癌全人群中展现出明确的生存获益,而从治疗依从性的角度看,只要通过规范的不良反应管理保障治疗连续性,就能充分释放CLDN18.2 靶向治疗的疗效潜力,让更多患者获得理想的生存获益,这为我们更好的在临床上使用CLDN18.2靶向治疗提供了重要参考。
腹膜转移
CLDN18.2靶向治疗更精准
在佐妥昔单抗两项III期临床研究中,“基线伴腹膜转移” 是极具临床价值的高获益人群。
腹膜转移作为胃癌最常见的远处转移模式之一,约 25%~43% 患者在病程中发生 [10,11] ,因腹膜微环境的免疫抑制特性、肿瘤细胞广泛播散等特点,免疫治疗在胃癌腹膜转移患者中的疗效仍不明确。
既往研究显示,不同PD-1抑制剂在腹膜转移治疗中存在较大的疗效差异。ATTRACTION-4研究显示,纳武利尤单抗联合化疗方案并未给胃癌腹膜转移亚组患者带来总生存期获益 [12] 。
在已公开的关键III期研究分层/亚组披露中,RATIONALE-305提示其OS获益在不同腹膜转移状态下相对一致,但在该亚组患者中,联合治疗组较单纯化疗组的mOS仅延长了0.5个月 [13] 。
今年ESMO Aisa上公布了针对SPOTLIGHT和 GLOW研究“腹膜转移”亚组的事后分析 [14] ,分析显示,对于基线伴腹膜转移的患者,佐妥昔单抗联合化疗展现出生存获益优势,mPFS达10.35个月(vs 8.08个月,HR 0.68),mOS达15.47个月(vs 13.17个月,HR 0.79)。排除肝转移混杂因素后分析,获益优势依然稳定,mPFS达10.38个月(vs 8.08个月,HR 0.67),mOS提升至15.51个月(vs 13.60个月,HR 0.77)。
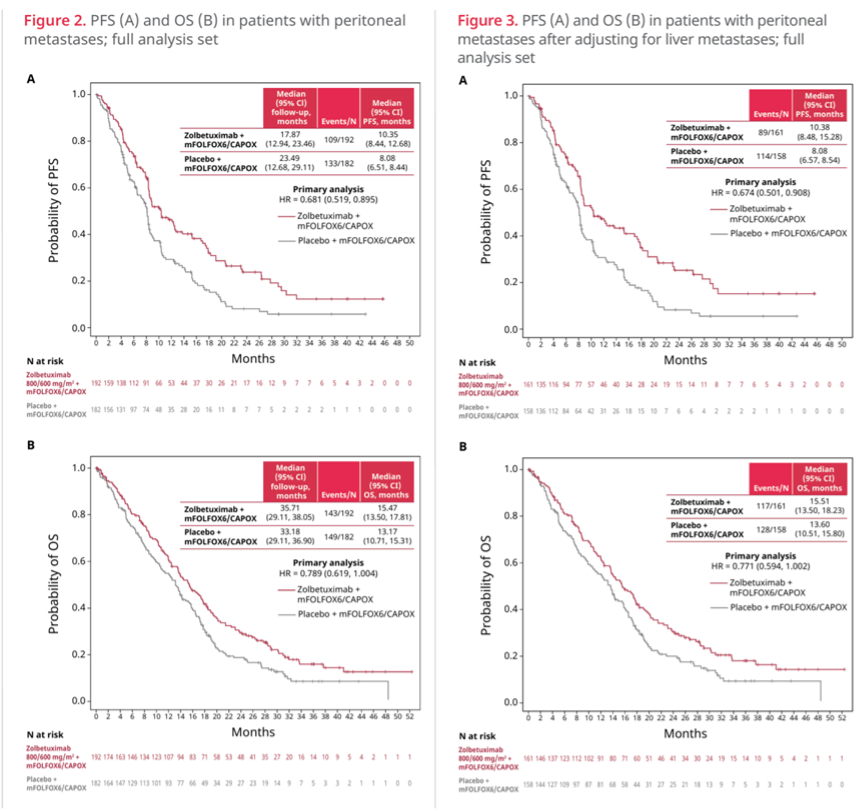
CLDN18.2靶向治疗的良好疗效可能来自CLDN18.2表达在原发灶和转移灶中的良好一致性。临床前研究表明,CLDN18.2不仅在胃癌原发灶中表达,在胃癌的淋巴结及其他远处转移部位中也均有表达,且 原发灶与转移灶的表达保持了良好的一致性 [15] 。
这意味着 CLDN18.2 靶向药物能精准识别并结合腹膜转移灶中的肿瘤细胞,更有效地应对胃癌腹膜转移,突破免疫疗法的治疗局限。
总结
作为新兴的、极具潜力的胃癌治疗靶点,CLDN18.2靶向治疗给晚期胃癌诊疗格局带来了巨大的变化。而在实际的、更为复杂多样的临床工作中,我们经常面对现有循证之外的挑战和困扰。
把握不同治疗方案的治疗特点,对不同人群的预后有更明确的判断,对提高临床决策的准确性和效率有巨大帮助。
目前,CLDN18.2 靶向治疗与免疫疗法的联合策略已在积极探索中,正如 KEYNOTE-811 研究为 HER2 阳性胃癌带来的突破,未来 “靶免化” 三联方案有望进一步突破疗效天花板,成为CLDN18.2高表达、PD-L1阳性胃癌患者的有潜力的治疗方案选择。期待相关研究能尽早获得有力的疗效证据,为临床提供关键的指导。
参考文献
[1] Bray F, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA A Cancer J Clinicians, 2024, 74(3): 229~263
[2] 梁寒,李子禹,张小田,等.胃癌抗HER2治疗中国专家共识(2024年版)[J].中国肿瘤临床,2024,51(23):1189-1205.
[3] 中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)胃癌诊疗指南2025[M]. 北京:人民卫生出版社, 2025. ISBN 978-7-117-37780-5.
[4] Shitara K, et al. Zolbetuximab plus mFOLFOX6 in patients with CLDN18.2-positive, HER2-negative, untreated, locally advanced unresectable or metastatic gastric or gastro-oesophageal junction adenocarcinoma (SPOTLIGHT): a multicentre, randomised, double-blind, phase 3 trial. Lancet. 2023 May 20;401(10389):1655-1668.
[5] Shah MA, et al. Zolbetuximab plus CAPOX in CLDN18.2-positive gastric or gastroesophageal junction adenocarcinoma: the randomized, phase 3 GLOW trial. Nat Med, 2023, 29(8): 2133~2141.
[6] Bang YJ, et al. Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA): a phase 3, open-label, randomised controlled trial. The Lancet, 2010, 376(9742): 687~697.
[7] Janjigian YY, et al. First-line nivolumab plus chemotherapy versus chemotherapy alone for advanced gastric, gastro-oesophageal junction, and oesophageal adenocarcinoma (CheckMate 649): a randomised, open-label, phase 3 trial. The Lancet, 2021, 398(10294): 27~40.
[8] Rha SY, et al. Pembrolizumab plus chemotherapy versus placebo plus chemotherapy for HER2-negative advanced gastric cancer (KEYNOTE-859): a multicentre, randomised, double-blind, phase 3 trial. The Lancet Oncology, 2023, 24(11): 1181~1195.
[9] Qiu MZ, et al. Tislelizumab plus chemotherapy versus placebo plus chemotherapy as first line treatment for advanced gastric or gastro-oesophageal junction adenocarcinoma: RATIONALE-305 randomised, double blind, phase 3 trial. BMJ, 2024, 385: e078876.
[10] de Moraes FCA, et al. Does Malignant Ascites Define Prognosis in Gastric Cancer with Peritoneal Spread? A Systematic Review and Meta-analysis. J Gastrointest Cancer. 2025 Oct 16;56(1):206.
[11] Sirody J, Kaji AH, Hari DM, Chen KT. Patterns of gastric cancer metastasis in the United States. Am J Surg. 2022 Jul;224(1 Pt B):445-448.
[12] Kang YK,et al. Nivolumab plus chemotherapy versus placebo plus chemotherapy in patients with HER2-negative, untreated, unresectable advanced or recurrent gastric or gastro-oesophageal junction cancer (ATTRACTION-4): a randomised, multicentre, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2022 Feb;23(2):234-247.
[13] Miaozhen Qiu et al.Tislelizumab (TIS) + chemotherapy (chemo) vs placebo (PBO) + chemo as first-line (1L) treatment in gastric/gastroesophageal junction adenocarcinoma (GC/GEJC) patients with/without peritoneal or liver metastases: A post hoc analysis of RATIONALE-305 study.. J Clin Oncol 43, 414-414(2025).
[14] Xu RH, et al. Zolbetuximab plus mFOLFOX6/CAPOX as first-line (1L) treatment in patients with claudin 18 isoform 2 positive (CLDN18.2+) metastatic gastric or gastroesophageal junction (mG/GEJ) adenocarcinoma with peritoneal metastases: A post hoc analysis of SPOTLIGHT and GLOW. Annals of Oncology, 2025, 36: S1857.
[15] Rohde C, et al. Comparison of Claudin 18.2 expression in primary tumors and lymph node metastases in Japanese patients with gastric adenocarcinoma. Jpn J Clin Oncol. 2019 Sep 1;49(9):870-876.
审批编号:MAT-CN-VYL-2026-00010
审批时间:2026.1.12
材料有效期:2027.1.12












 苏公网安备32059002004080号
苏公网安备32059002004080号


