

胃癌作为全球高发的恶性肿瘤之一,晚期胃癌治疗长期受限于靶点稀缺与获益人群有限的困境。
特别是由于胃癌的肿瘤异质性原因,在过去的多年时间里,靶向治疗进展缓慢,患者缺乏生存获益。
因此,精准、高效的治疗靶点一直为胃癌临床诊疗的迫切需要。Claudin18.2 靶向治疗的突破性进展,为胃癌精准医疗开启了新维度。
本期FM18.2聚焦临床实践痛点,邀请 苏州大学附属第一医院李伟教授 深入剖析晚期胃癌靶向治疗的历史瓶颈,揭秘 Claudin18.2 靶点特异性优势与临床研究突破,解读其在联合治疗策略中的价值,为胃癌个体化治疗提供前沿思路。

苏州大学附属第一医院
肿瘤科副主任
李伟 教授
医学博士 主任医师
副教授 硕士生导师
• 中国临床肿瘤学会(CSCO)胰腺癌专家委员会委员
• 中国临床肿瘤学会(CSCO)青年专家委员会委员
• 江苏省医学会肿瘤化疗与生物治疗分会青年委员
• 苏州市医学会肿瘤学分会青委副主委
• 苏州市抗癌协会肿瘤营养专业委员会主任委员

晚期胃癌靶向治疗的发展有什么困境?
首先我们来回顾一下胃癌靶向治疗历史。对于胃癌来说,奠定胃癌靶向治疗的最经典的临床研究就是 ToGA 研究 [1] ,这项研究其实已经诞生了十几年了。
ToGA 研究告诉我们,对于 HER2 阳性的胃癌患者来说,我们进行抗 HER2 的靶向治疗,能够给患者带来生存上的获益。可是问题在于, HER2 阳性的胃癌患者在真实世界当中的占比只有 10% 到 20% [2] 左右 ,所以对于胃癌患者来说,能够进行抗 HER2 靶向治疗的患者仍然是少数。
VEGF&VEGFR是在 HER2 之后诞生的胃癌靶向治疗靶点。靶向药物包括雷莫西尤单抗,以及国产的呋喹替尼。
呋喹替尼的 FRUTIGA 研究 [3] 证明,抗血管生成治疗也是能够让胃癌患者从靶向治疗获益的。 抗血管生成靶点 是一个比较“泛”的靶点,虽然说适用的范围很广,但是 目前仍然缺乏带来 OS 获益的证据 。
如果我们把靶向治疗的概念拓宽一点的话,其实在胃癌里面,有助于我们去做精准的人群筛选的靶点,还包括微卫星不稳定、PD-L1 表达等等,但 微卫星不稳定型在胃癌当中的占比只有 5% 左右 [4] 。
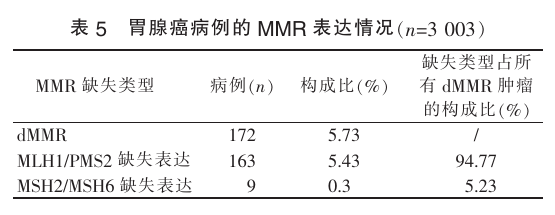
图片来源:马乾宸, 张本炎, 芮炜玮, 王婷, 罗方秀, 王朝夫, 袁菲. 中国3 071例胃癌病理分型分析[J]. 诊断学理论与实践, 2022, 21(05): 560-566.
微卫星不稳定型肠癌患者,通过一线免疫治疗,能够得到非常好的生存获益。但在胃癌当中的免疫治疗证据,目前主要是基于几个 II 期研究的数据,我们使用单免疫或者是双免疫,都能够看到一定的生存获益,但也是因为微卫星不稳定的胃癌患者占比确实非常少,所以能够从这种治疗策略当中获益的人群也是非常有限的。
对于 PD-L1 靶点而言,目前胃癌一线化疗联合免疫治疗的策略,主要获益人群仍是PD-L1高表达的人群,这部分人群在胃癌当中的占比大概只有三分之一左右,所以仍然是获益占比较少的人群。此外,PD-L1 表达, 并非 CPS 评分越高生存获益就一定越明显 。
PD-L1这个靶点其实并不能够十分精准地区分,从免疫治疗当中能够获益的人群。
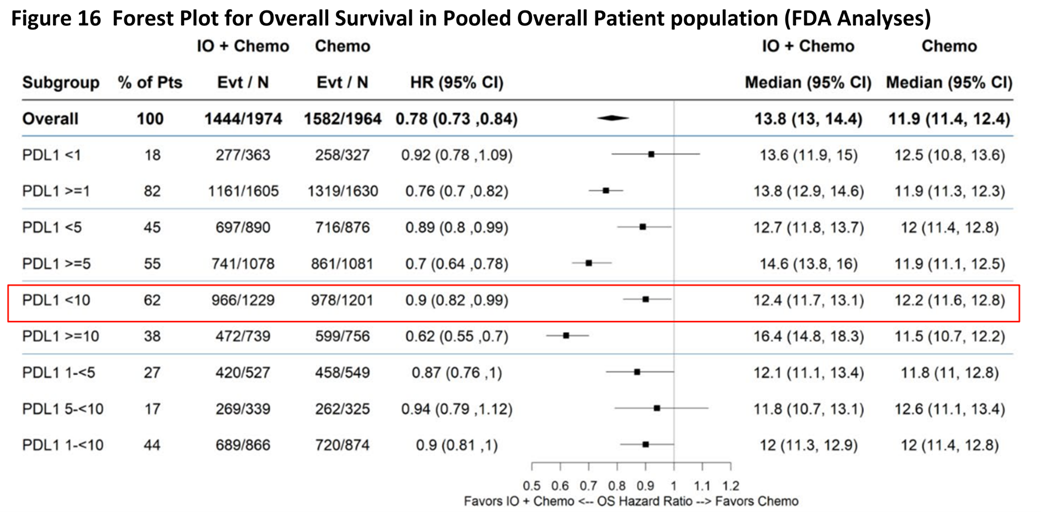
来源:参考文献5
所以对于胃癌患者来说,目前精准靶向治疗的困境在于——真正能够从精准靶向治疗当中获益的患者的占比仍然是非常有限的,所以也急需去探索一些新的有效的治疗靶点。
在靶向治疗纷纷失败的情况下,CLDN18.2 靶向治疗为什么得以成功?
对于包括胃癌在内的消化道肿瘤来说的话,近几年最大的靶向治疗突破,就是 Claudin18.2 靶点上的突破。
目前我们针对这个靶点有抗体,也有 ADC 类药物,甚至还有 CAR-T。目前已经在临床可及的,主要是 Claudin18.2 抗体佐妥昔单抗,更多的 ADC 的药物和 CAR-T 仍在临床研究当中。
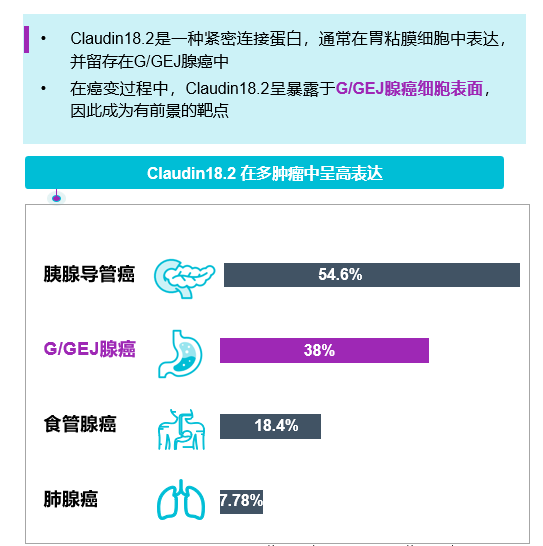
Claudin18.2 这个靶点之所以成功,一个非常重要的原因是——Claudin18.2在肿瘤当中有非常出色的特异性。CLDN18.2在正常组织中的表达严格局限于胃黏膜的紧密连接,埋在超分子复合物中。然而,在恶性转化时,细胞极性的扰动导致CLDN18.2的表位暴露在癌症细胞表面,可被抗体靶向结合 [6] 。
佐妥昔单抗的主要作用机制是通过抗体所介导的 ADCC 和 CDC 效应来杀伤肿瘤细胞。
这样的机制,一方面实现了针对 Claudin18.2 高表达的肿瘤细胞的特异性杀伤作用。
另一方面,我们也看到像包括 HER2、Claudin18.2 这样的靶向治疗,其实跟免疫治疗之间也并不是互斥的,在部分患者当中,用靶向治疗联合免疫治疗可能会产生一定的协同作用。
目前Claudin18.2抗体药物已经看到了非常积极的疗效,意味着将来有可能在现有的治疗的模式上做进一步的突破,让患者的生存有进一步的延长。
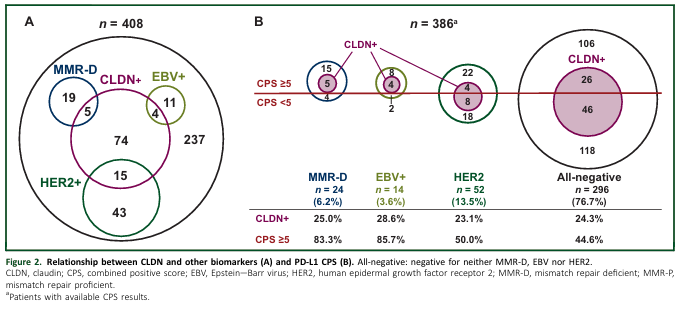
晚期胃癌或胃食管连接部癌中
Claudin18.2表达与其他靶点的重合比例
Kubota, et.al. Shitara, K. (2023). Comprehensive clinical and molecular characterization of claudin 18.2 expression in advanced gastric or gastroesophageal junction cancer. ESMO Open, 8(1), e100762. https://doi.org/10.1016/j.esmoop.2022.100762
当然,Claudin18.2 抗体之所以能够在临床当中成功的应用,关键还在于它的临床研究取得了成功。
我们看到佐妥昔单抗的全球大三期研究,SPOTLIGHT [8] 和 GLOW 研究 [9] 都取得了 OS 的延长。我们知道,对于一个新药的研发来说,是否能够成功上市,最关键的指标还是在于能不能延长 OS。
佐妥昔单抗对于胃癌患者,取得了 3 到 4 个月左右的 OS 延长,也就意味着对于 Claudin18.2 阳性的患者,佐妥昔单抗是能够真正让患者得到生存期延长的新药。
如何理解 Claudin18.2 给临床带来的价值?
目前我们在 Claudin18.2 这个靶点上,现有的基于 SPOTLIGHT 和 GLOW 研究的数据,我们知道化疗联合佐妥昔单抗,对比化疗是有明显的生存的获益的。
但是目前我们在临床当中,晚期胃癌的一线治疗的标准方案,大家更多地会采用化疗联合免疫的策略。如果说我们既可以选用化疗联合佐妥昔单抗,同时也可以选择化疗联合免疫的时候,那这个时候该如何决策呢?
其实我们可以参考一下 HER2 这个靶点的研发历程。从 ToGA 研究开始,明确了化疗联合曲妥珠单抗能够给 HER2 阳性的患者带来明显的生存获益。
但那是一个没有免疫治疗的时代,当时化疗联合靶向取得了明显的生存获益,并且成为了临床上的标准的一线治疗。
但是随着时代的进步,我们有了更多的治疗的手段,我们也看到在 KEYNOTE-811 研究当中,对于 CPS >1 的患者,化疗联合曲妥珠单抗联合帕博利珠单抗,取得了明显的生存的获益。这也就意味着对于 HER2 阳性的患者来说的话,靶向治疗和免疫治疗它并不是一个互斥的治疗手段。
在临床上,应当积极地去探索化疗联合靶向联合免疫的策略,但是我们也需要注意到,在 KEYNOTE-811 研究当中,对于 CPS <1 的患者,采用化疗联合曲妥珠单抗、联合帕博利珠单抗,其实并没有得到明显的生存的获益,反而是有生存受损的趋势。
所以这就意味着对于 PD-L1 低表达且Claudin18.2阳性的人群,靶向治疗相较于免疫治疗会更有优势。
可以优先选用循证医学证据更加充分的化疗联合Claudin18.2靶向治疗的策略。
可否谈一谈对 Claudin18.2 未来的展望?
Claudin18.2 靶点的出现,给我们在未来胃癌治疗的领域带来了无限的遐想。
随着科技的进步,临床上不仅只有抗体类药物,还有 ADC、CAR-T 等更多治疗手段,能够对于一些特异性靶点,进行更有效的有针对性的治疗。
虽然从 ToGA 研究到目前的 KEYNOTE-811 研究,其实已经走过了十多年的历程;但是,Claudin18.2 这个靶点从发现之后,到现在临床研究如火如荼的开展,其实经历的时间是非常短的。
针对Claudin18.2现在拥有了更多的治疗的手段,包括抗体、ADC、CAR-T 等等治疗的手段,在未来可能去跟免疫以及抗血管药物等建立联合治疗方案等。这也就意味着未来可以通过更多的不同药物组合,让更多的患者从Claudin18.2治疗中获益。
晚期胃癌预后疗效不佳的主要原因之一,就是因为胃癌是一个异质性非常强的肿瘤。在 Claudin18.2 这个靶点出现之前,能够进行个体化针对性治疗的患者比例仍然非常少,主要是 HER2 阳性的人群和微卫星不稳定的这部分人群。
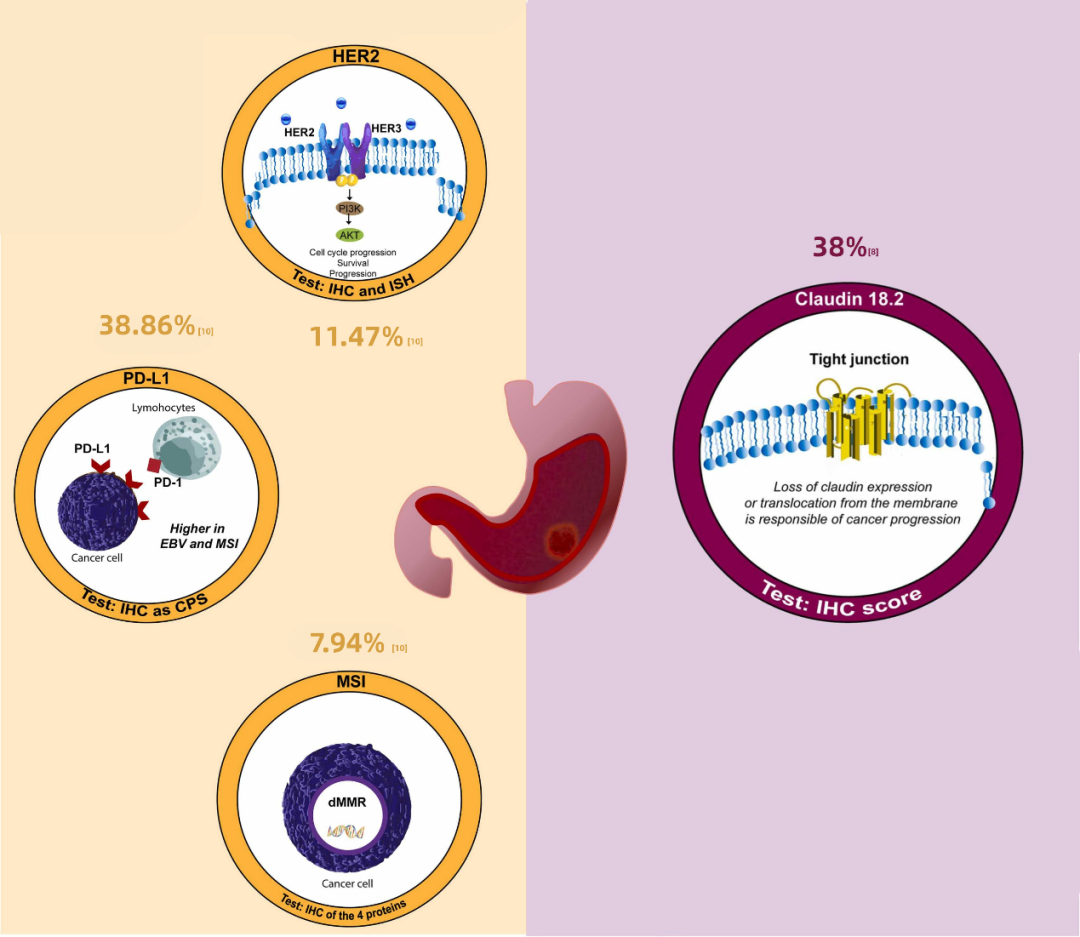
几种胃癌生物标志物在亚洲人群中的阳性率
其他很多靶点其实在胃癌当中都进行过探索,但没有看到非常好的生存获益。对于更多的胃癌患者来说,既往的治疗手段其实是缺乏个体化的。
所以这也就意味着未来通过更加精细化的人群的分层,有助于对患者进行更加精细化的区分,有助于选择更加个性化的治疗方案,有可能在未来。让异质性非常强的胃癌,能够真正实现个体化的精准靶向治疗。
参考资料
[1] Bang YJ, et al. Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA): a phase 3, open-label, randomised controlled trial. Lancet. 2010 Aug 28;376(9742):687-97.
[2] 中国抗癌协会胃癌专业委员会,等. 胃癌抗HER2治疗中国专家共识(2024年版)[J]. 中国肿瘤临床,2024,51(23):1189-1205.
[3] Wang F, et al. Fruquintinib plus paclitaxel versus placebo plus paclitaxel for gastric or gastroesophageal junction adenocarcinoma: the randomized phase 3 FRUTIGA trial. Nat Med. 2024 Aug;30(8):2189-2198.
[4] 马乾宸,等. 中国3071例胃癌病理分型分析[J]. 诊断学理论与实践,2022,21(5):560-566.
[5] FDA简报文件
[6] Sahin U, et al. Claudin-18 splice variant 2 is a pan-cancer target suitable for therapeutic antibody development. Clin Cancer Res. 2008 Dec 1;14(23):7624-34.
[7] Kubota Y, et al. Comprehensive clinical and molecular characterization of claudin 18.2 expression in advanced gastric or gastroesophageal junction cancer. ESMO Open. 2023 Feb;8(1):100762.
[8] Shitara K, et al. Zolbetuximab plus mFOLFOX6 in patients with CLDN18.2-positive, HER2-negative, untreated, locally advanced unresectable or metastatic gastric or gastro-oesophageal junction adenocarcinoma (SPOTLIGHT): a multicentre, randomised, double-blind, phase 3 trial. Lancet. 2023 May 20;401(10389):1655-1668.
[9] Shah MA, et al. Zolbetuximab plus CAPOX in CLDN18.2-positive gastric or gastroesophageal junction adenocarcinoma: the randomized, phase 3 GLOW trial. Nat Med. 2023 Aug;29(8):2133-2141.
[10] Chen Y,et al. The current landscape of gastric cancer and gastroesophageal junction cancer diagnosis and treatment in China: a comprehensive nationwide cohort analysis. J Hematol Oncol. 2025 Apr 15;18(1):42.
审批编号:MAT-CN-VYL-2025-00174
审批时间:2025.6.24
材料有效期:2027.6.24













 苏公网安备32059002004080号
苏公网安备32059002004080号


