不可切除III期非小细胞肺癌(NSCLC)是肺癌治疗领域最具挑战性的阶段之一,约占新诊断NSCLC的三分之一。尽管过去十年免疫治疗革命显著改善了患者预后,但仅约三分之一接受同步放化疗(cCRT)及免疫治疗的患者在5年时仍存活且无进展,疾病复发和远处转移风险持续存在。2025年10月,法国Gustave Roussy研究所Jordi Remon教授团队在肿瘤学顶级综述期刊Nature Reviews Clinical Oncology(IF=82.2)发表了题为“Unresectable stage III non-small-cell lung cancer: state of the art and challenges”权威综述[1],系统梳理了针对不可切除III期NSCLC,从PACIFIC方案确立免疫巩固标准治疗以来该领域的最新进展,深入探讨了双免疫联合、同步放化疗优化、驱动基因阳性患者靶向巩固治疗等前沿策略。聚焦于不可切除III期NSCLC的靶向治疗板块,【肿瘤资讯】特将其精华内容进行整理,以飨读者。
EGFR突变患者的独特挑战:CNS转移风险高与免疫治疗局限性
EGFR激活突变贯穿于NSCLC的各个疾病阶段,在早期与晚期患者中均具有较高的发生率,提示此类突变在肺癌发生早期即已存在。然而,关于EGFR突变状态对放化疗(CRT)后III期患者PFS的影响,既往研究结果尚存争议:部分研究显示PFS无显著差异,而另一些研究则表明EGFR突变患者的PFS劣于野生型患者。但各方研究均达成一项共识:EGFR突变患者面临更高的远处转移风险,尤其是中枢神经系统(CNS)进展风险明显增高。
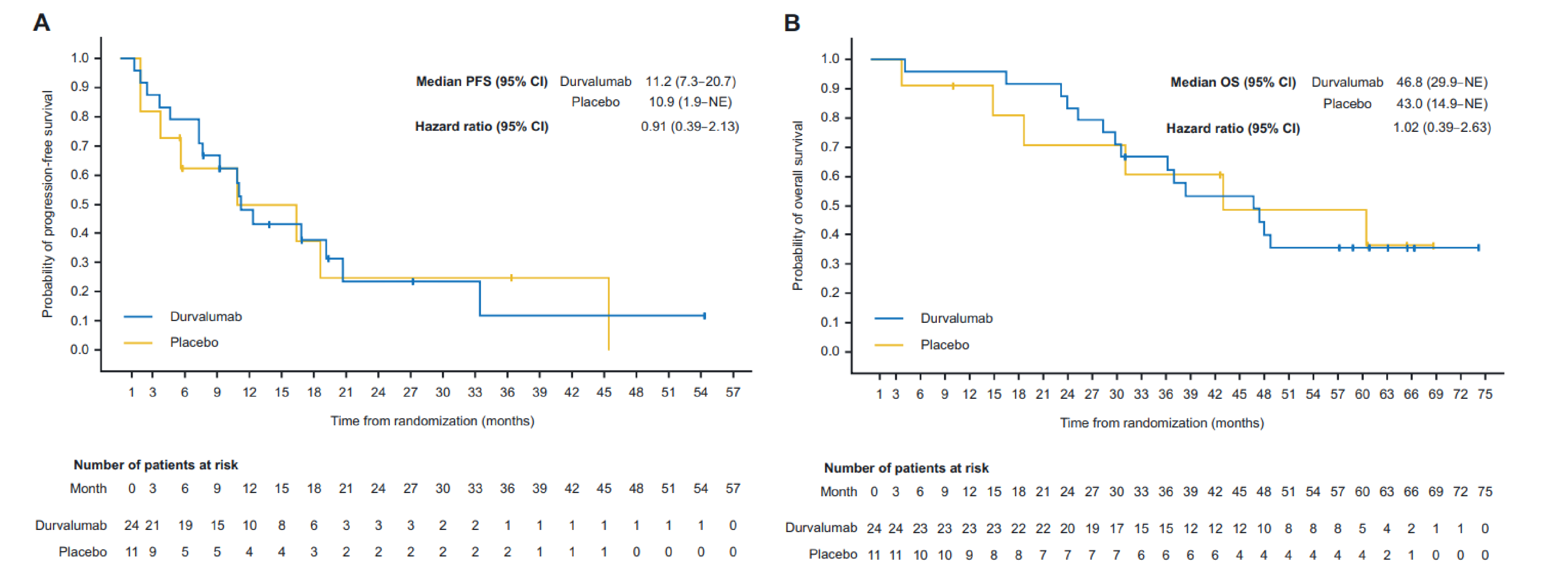
针对EGFR突变患者采用度伐利尤单抗巩固治疗的疗效,后续研究给出了进一步评估。PACIFIC研究的事后分析纳入了35例EGFR突变的不可切除III期NSCLC患者,结果显示,与安慰剂组相比,度伐利尤单抗并未带来显著的PFS获益(中位PFS:11.2个月 vs 10.9个月;HR 0.91,95%CI 0.39–2.13)或总生存期(OS)获益(中位OS:46.8个月 vs 43.0个月;HR 1.02,95%CI 0.39–2.63)(图1)。同样,韩国一项回顾性多中心观察性研究分析了339例CRT后无进展的局部晚期NSCLC患者(含41例EGFR突变和19例ALK阳性),发现EGFR/ALK野生型与突变型患者接受度伐利尤单抗巩固治疗的PFS表现相当(中位PFS:21.4个月 vs 21.0个月;HR 0.76,P=0.74)。此外,另有研究证实,PD-L1≥1%是EGFR突变患者预后不良的独立预测因素。
鉴于上述免疫治疗的局限性,结合第三代EGFR酪氨酸激酶抑制剂(TKI)在早期辅助及晚期治疗中确立的生存优势,特别是其潜在的血脑屏障穿透能力有望降低CNS进展风险,探索第三代EGFR-TKI作为CRT后的巩固治疗已成为该领域极具前景的破局方向。
靶向巩固治疗的里程碑:LAURA与POLESTAR研究重塑治疗范式
两项关键的III期临床研究——LAURA和POLESTAR,分别评估了奥希替尼和阿美替尼在同步或序贯放化疗(cCRT或sCRT)后作为维持治疗,对比安慰剂用于携带常见EGFR敏感突变(外显子19缺失或L858R突变)的不可切除III期NSCLC患者的疗效。两项试验均证实了第三代EGFR-TKI可显著改善PFS:
LAURA研究:奥希替尼组中位PFS高达39.1个月,显著优于安慰剂组的5.6个月(HR 0.16,95%CI 0.10–0.24;P<0.001)(图2)。
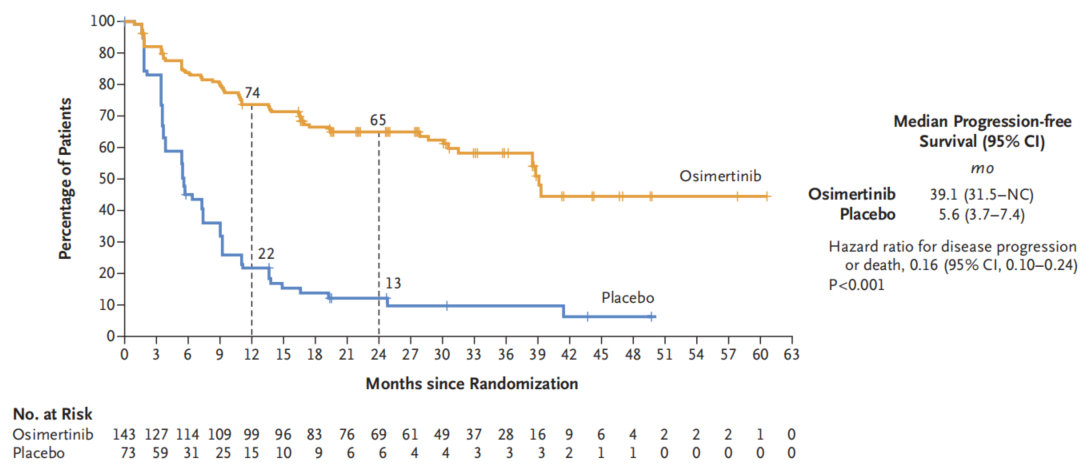
POLESTAR研究:阿美替尼组中位PFS达30.4个月,同样显著优于安慰剂组的3.8个月(HR 0.20,95%CI 0.11–0.35;P<0.0001)。
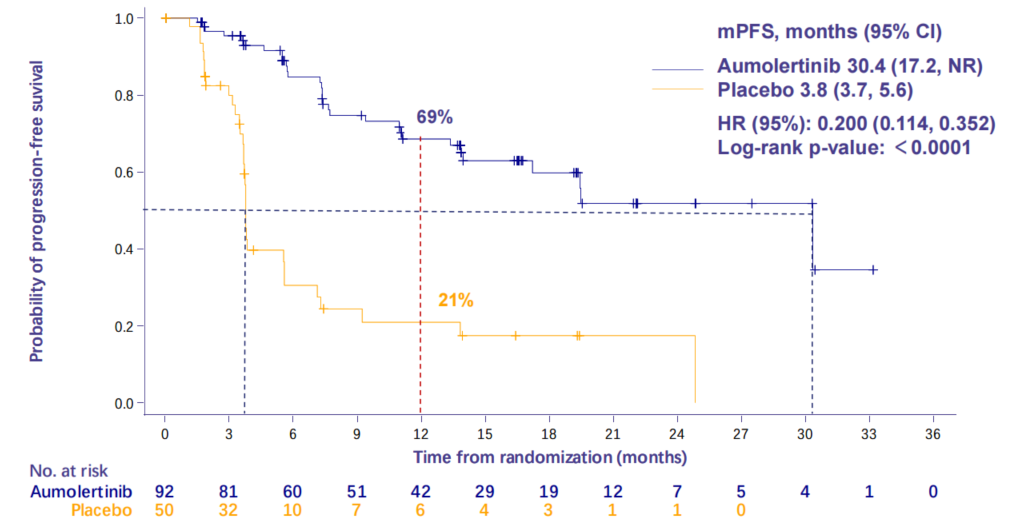
上述PFS的获益也反映了远处转移事件的有效控制,尤其是CNS进展风险的大幅降低。LAURA研究中CNS-PFS的风险比(HR)为0.17(95%CI 0.09–0.32;P<0.01),而POLESTAR研究的HR为0.33(95%CI 0.12–0.92;P<0.0001)。
目前,两项研究的OS数据尚不成熟。在LAURA试验中(OS成熟度31%),尽管奥希替尼组展现出改善趋势(中位OS:58.8个月 vs 54.1个月;HR 0.67,95%CI 0.40–1.14),但由于安慰剂组高达78%的患者在疾病进展后交叉接受了奥希替尼治疗,最终的OS获益可能受到交叉治疗的稀释。
基于这些数据,奥希替尼已获NMPA,FDA和EMA批准用于EGFR突变(Ex19del/L858R)不可切除III期NSCLC的巩固治疗,阿美替尼也在NMPA获批相同适应症。这标志着该领域进入基于生物标志物精准选择靶向巩固治疗的时代。
靶向巩固治疗策略的多元探索:多项II期研究正在进行中
除上述III期试验外,多项II期研究正在积极探索III期不可切NSCLC的靶向治疗的不同介入时机与联合策略:
其他第三代EGFR-TKI的巩固治疗探索
PLATINUM研究(NCT05338619)目前正在评估另一种第三代EGFR-TKI兰泽替尼作为巩固治疗的临床疗效。
诱导联合巩固的双重治疗策略
NEOLA研究(NCT06194448)探索了在接受cCRT或sCRT的患者中,将奥希替尼同时应用于诱导及巩固治疗的双重策略。这一理念在早期的II期ACENT试验中曾使用第一代EGFR-TKI阿法替尼进行过初步尝试(纳入19例EGFR突变可切除或不可切除NSCLC患者)。结果表明,诱导期使用阿法替尼并未阻碍后续多学科综合治疗的顺利实施,且中位生存结局释放出积极信号。然而,该研究也暴露出一定局限:CNS复发率较高(16例复发事件中占6例),且停用TKI后病情进展迅速,这凸显了在真实临床场景中,对于微小残留病灶(MRD)进行早期检测与根除的迫切需求(至少对第一代EGFR-TKI而言如此)。
免疫与靶向的巩固治疗的疗效对比
PACIFIC-4试验(NCT03833154)聚焦于不可切除的I–II期EGFR突变NSCLC患者,旨在对比立体定向消融放疗(SABR)后应用奥希替尼与度伐利尤单抗进行巩固治疗的优劣。
悬而未决的临床命题:干预时机与局部治疗的优先权取舍
尽管LAURA研究和POLESTAR研究的数据成功重塑了临床指南与治疗范式,但仍有数个核心临床问题亟待解答(图4):
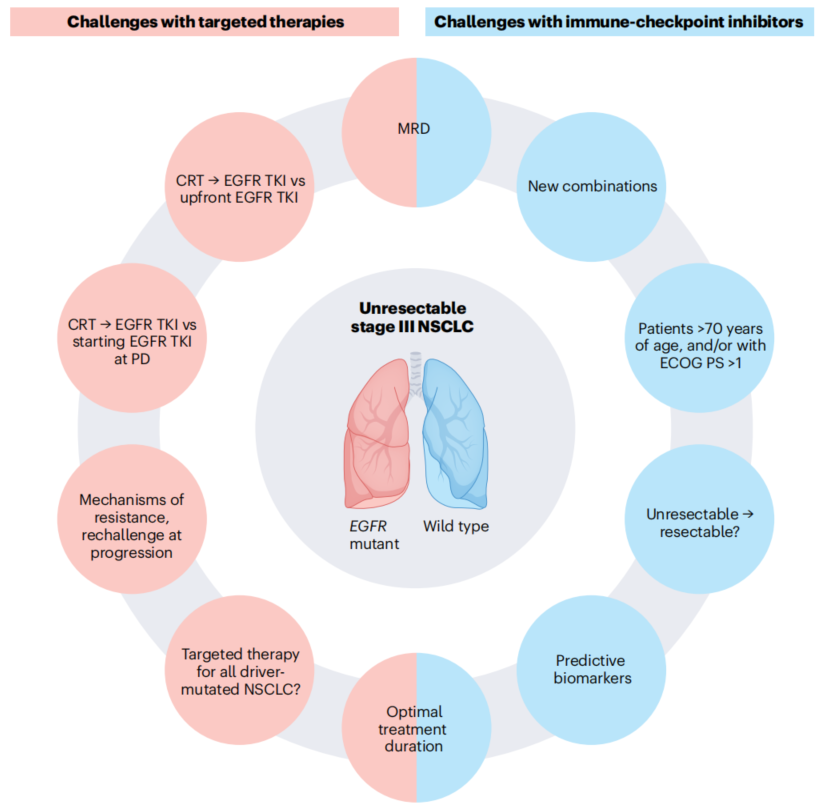
干预时机之争:即刻巩固 vs 进展后延迟干预
LAURA和POLESTAR两项试验目前均尚未证实:与推迟至影像学疾病进展后再启动靶向治疗相比,CRT后即刻使用奥希替尼或阿美替尼能否显著改善OS。因此,当前的核心争议依然存在:EGFR-TKI是应在CRT后立即启用,还是可保留至复发进展时再用?LAURA研究最终的OS随访数据(需充分考量安慰剂组78%的高交叉率)或将为该问题一锤定音。
治疗策略反思:局部放化疗与系统治疗的优先级
值得警惕的是,在LAURA和POLESTAR研究中,疾病的进展模式以局部区域性进展为主。这引发了学界对整体策略的深层探讨:对于此类患者,是否必须将CRT作为一线首选?抑或初始即应采用“EGFR-TKI(±化疗)”的全身系统治疗,而将局部放疗推迟至出现局部进展时进行?这一讨论并非空穴来风,因为上述两项关键试验的安慰剂组中位PFS表现不仅劣于PACIFIC研究的对照组,也不及真实世界队列数据,从而引发了对研究对照组设置的合理性以及入组患者基线分期严谨性的探讨。
在LAURA试验中,仅半数患者在CRT前接受了PET-CT全面评估,且在随机入组前并未强制要求复查影像学,这可能导致部分隐匿性转移的患者被纳入。独立盲法影像学审查(BICR)对脑部MRI的回顾性分析也证实了这一点:奥希替尼组有10%、安慰剂组有7%的患者在基线时实则已存在脑转移。尽管存在上述局限性,但鉴于奥希替尼在颅内病灶控制方面所展现的获益、降低远处转移风险的潜力以及延长PFS的效果,其作为所有此类患者的首选治疗方案仍具有一定的依据。
个体化靶向巩固策略:其他驱动基因阳性的治疗策略
鉴于NSCLC中可靶向驱动基因异常的丰富多样性,探索个体化靶向巩固策略能否通用至其他驱动基因类型至关重要。肿瘤的免疫微环境表型往往因特定的致癌驱动基因而异,这直接决定了巩固治疗策略的制定原则。
对于非吸烟相关突变(如ALK融合),考虑到目前已有具备高水平血脑屏障穿透能力的新一代靶向药物可供临床使用,对于此类患者,采用以ALK-TKI为基础的巩固治疗可能比使用度伐利尤单抗更具疗效优势。这一重要科学问题正在开展的BO42777试验(NCT05170204)中进行评估。
对于吸烟相关突变(如KRAS、BRAF、MET异常等),由于目前获批的针对上述靶点的靶向药物在CNS入脑活性方面相对有限,CRT后序贯度伐利尤单抗巩固治疗目前依然是这部分患者的最优标准选择。
需要强调的是,上述关于非EGFR驱动基因的治疗策略目前多受限于研究的队列规模较小,未来仍亟需大规模前瞻性临床试验数据的进一步确证。
生物标志物指导下的精准降阶梯:MRD指导治疗策略的潜力
然而,在EGFR突变III期NSCLC患者中采用EGFR-TKI巩固治疗同样面临着现实挑战。LAURA试验并未纳入微小残留病灶(MRD)等能够指导巩固治疗进行选择性强化的预后生物标志物,这种干预模式可能导致部分患者接受了不必要的终生全身系统性治疗。如果终生采用EGFR-TKI巩固被确立为最优标准,则亟需进一步探索基于循环肿瘤DNA(ctDNA)的适应性指导策略,以优化治疗的精准度与患者依从性。事实上,基于动态ctDNA状态实施“药物假期”(drug holiday)或采用延长的间歇性给药(on-off treatment)策略,可能有助于扩增或维持对治疗敏感的肿瘤克隆群,同时减少或延缓耐药克隆的涌现,从而延长整体治疗的持续缓解期。未来的临床试验亟需在这一背景下对上述策略展开深入探索。例如,目前正在开展的III期APPROACH研究(NCT04841811),正致力于评估在初始不可切除的EGFR突变III期NSCLC患者中,基于动态MRD监测来指导阿美替尼维持治疗的临床有效性。
不可切除向可切除状态的“转化治疗”探索
鉴于新辅助治疗方案在可切除早期NSCLC中取得的显著临床获益,多项队列和临床试验已相继启动,旨在探索临界可切除(borderline resectable)或不可切除III期NSCLC患者在接受诱导治疗后,其病灶向可切除状态转化的潜力。然而,目前的探索受制于“临界可切除”NSCLC缺乏统一且明确的临床定义。这种界定的模糊性可能导致部分临床试验入组了按常规标准本就属于可切除范畴的患者,从而难以客观、准确地评估真实的降期转化率。
值得注意的是,这种转化策略也正在EGFR突变的不可切除III期NSCLC患者中进行尝试。在一项II期临床试验中,采用阿美替尼进行新辅助诱导,成功使51例患者中的23例(45%)转化为可切除疾病,其中3例(13%)更是达到了病理完全缓解(pCR)。尽管上述结果令人鼓舞,但目前这些数据仍处于产生假设阶段(hypothesis-generating),未来亟需更大规模的前瞻性队列数据予以确证,以明确这种转化策略能否比III期LAURA和POLESTAR试验中所报告的巩固治疗模式带来更优的临床结局。
[1] Remon J, Levy A, Gille R, Martel-Lafay I, Bortolot M, Hendriks LEL, Faivre-Finn C, Leighl N, Reck M, Pérol M. Unresectable stage III non-small-cell lung cancer: state of the art and challenges. Nat Rev Clin Oncol. 2026 Jan;23(1):22-39. doi: 10.1038/s41571-025-01080-4. Epub 2025 Oct 9. PMID: 41068447.
排版编辑:肿瘤资讯-明小丽











 苏公网安备32059002004080号
苏公网安备32059002004080号


