不可切除III期非小细胞肺癌(NSCLC)是肺癌治疗领域最具挑战性的阶段之一,约占新诊断NSCLC的三分之一。尽管过去十年免疫治疗革命显著改善了患者预后,但仅约三分之一接受同步放化疗(cCRT)及免疫治疗的患者在5年时仍存活且无进展,疾病复发和远处转移风险持续存在。2025年10月,法国Gustave Roussy研究所Jordi Remon教授团队在肿瘤学顶级综述期刊Nature Reviews Clinical Oncology(IF=82.2)发表了题为“Unresectable stage III non-small-cell lung cancer: state of the art and challenges”权威综述[1],系统梳理了针对不可切除III期NSCLC,从PACIFIC方案确立免疫巩固标准治疗以来该领域的最新进展,深入探讨了双免疫联合、同步放化疗优化、驱动基因阳性患者靶向巩固治疗等前沿策略。【肿瘤资讯】特将其中精华内容进行整理,以飨读者。
不可切除III期NSCLC治疗模式汇总
本文开篇,作者首先汇总了针对不可切除III期NSCLC,当前正在进行或已完成的关键临床试验中的治疗方案(图1)。随后,作者针对这类患者的众多治疗模式进行了详细解读。

从单纯放化疗到免疫巩固时代
对于体能状态良好(ECOG PS 0-1)的不可切除III期NSCLC患者,cCRT在过去二十年间一直是标准治疗基石,相比序贯放化疗(sCRT)可显著改善总生存期(OS),5年OS率约为30%,中位OS为25-28.7个月。然而,长期以来各种尝试(包括采用诱导化疗或巩固化疗;在未进行肿瘤筛选的患者中加用单克隆抗体或EGFR-TKIs;评估第三代化疗药物;以及提高放射剂量等)均未能进一步突破生存瓶颈。
2018年,PACIFIC试验的公布彻底改变了这一格局。在III期PACIFIC试验中,713例cCRT后无进展的不可切除III期NSCLC患者被随机分配接受度伐利尤单抗或安慰剂,结果显示度伐利尤单抗显著降低了疾病进展和死亡风险,5年OS为42.9% vs 33.4%(图2)。尽管大多数亚组从度伐利尤单抗中获益,但一项非计划的事后分析显示,在PD-L1 TC≤1%或EGFR突变的患者中未检测到OS的显著改善。在度伐利尤单抗组和安慰剂组中,由于AEs停用药物的患者分别有15.4%和9.8%,AE主要是由于肺炎、放射性肺炎或肺炎,且未损害患者报告的结局。
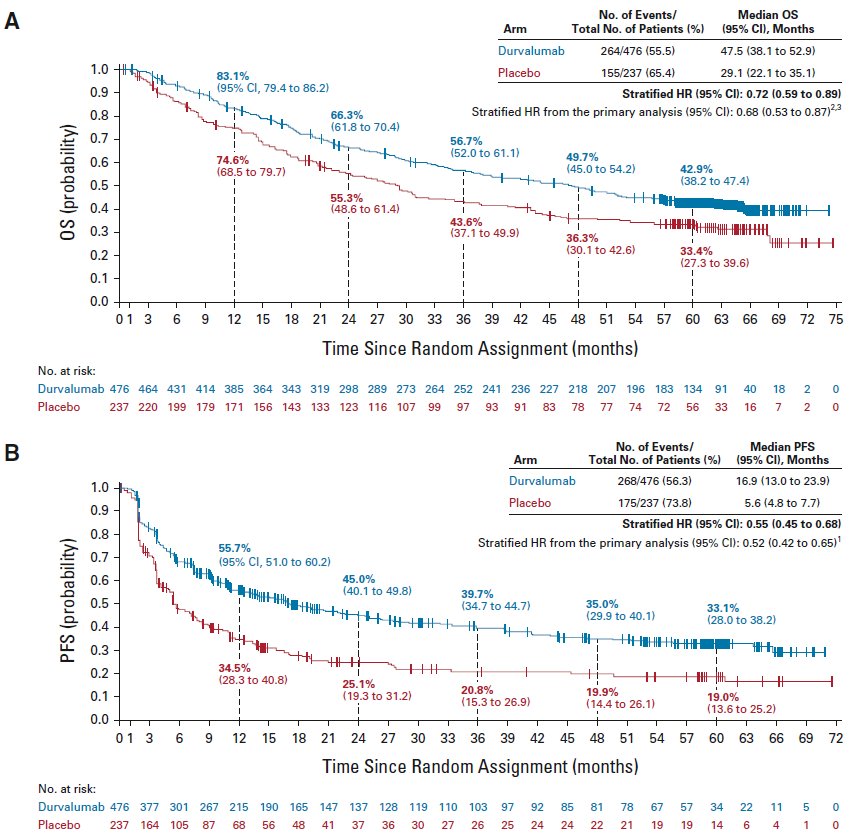
基于PACIFIC的结果,度伐利尤单抗作为cCRT后巩固治疗在2018年成为欧洲PD-L1 TC≥1%患者和美国无论PD-L1表达如何的III期NSCLC患者的标准治疗。2019年,我国也批准度伐利尤单抗上市,用于cCRT后未出现疾病进展的不可切除的Ⅲ期NSCLC患者的治疗。
序贯放化疗后的免疫巩固治疗
PACIFIC试验仅纳入完成cCRT的患者,导致sCRT后免疫巩固治疗的证据缺失。在这一背景下,多项研究相继填补了这一空白:PACIFIC-6单臂II期试验显示,sCRT后度伐利尤单抗巩固治疗的中位PFS为13.1个月,中位OS为39.0个月,2年OS率达67.2%,安全性与PACIFIC相当;PACIFIC-5 III期试验进一步证实,无论cCRT或sCRT后,与安慰剂组相比,度伐利尤单抗巩固治疗均能显著改善中位PFS(14.0个月 vs 6.5个月;HR 0.75,95%CI 0.58–0.99;P=0.038),且PD-L1 TC≥1%患者获益更显著。尽管度伐利尤单抗组患者有更优的OS趋势,但这一改善无统计学意义(mOS 38.3个月 vs 32.5个月,HR 0.87,95%CI 0.66–1.17;P=0.37)。3-4级AE发生率在度伐利尤单抗和安慰剂组相当(26.9% vs 23.9%),任何级别肺炎或放射性肺炎发生率也相似(39.5% vs 40.3%)。
在中国人群中,GEMSTONE-301 III期试验证实了PD-L1抑制剂舒格利单抗对比安慰剂在cCRT或sCRT后的巩固治疗价值,中位PFS达10.5个月(对照组6.4个月;HR 0.65),3年OS率为55.0%(对照组29.5%),且OS获益在序贯放化疗亚组中同样显著。接受舒格利单抗的患者中≥3级TRAEs发生率为11.4%,安慰剂组为5.6%。
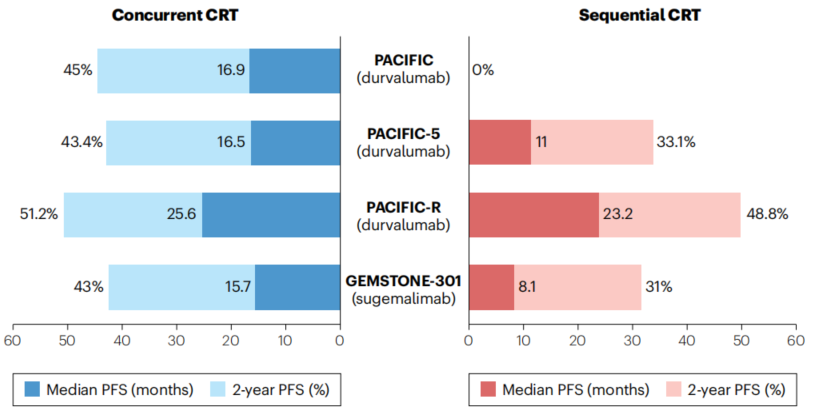
这些研究共同支持:无论采用何种放化疗模式,PD-L1抑制剂巩固治疗均是不可切除III期NSCLC的标准策略。
双免疫联合巩固策略
鉴于仅三分之一接受PACIFIC方案的患者在5年时仍存活且无疾病进展,多项研究探索了强化巩固治疗策略。II期BTCRC Lung 16-081研究结果显示,cCRT后无进展患者接受纳武利尤单抗+伊匹木单抗 vs 纳武利尤单抗单药巩固治疗的中位PFS相似(25.4个月 vs 24.5个月),但双ICI策略增加了与纳武利尤单抗单药相比的免疫相关AEs(irAEs)发生率(84% vs 65%)。II期COAST试验显示,与度伐利尤单抗巩固治疗相比,度伐利尤单抗联合抗CD73抗体oleclumab或抗NKG2A抗体monalizumab可进一步提高客观缓解率(35%和40.3% vs 23.9%)并延长中位PFS(21.1个月和19.8个月 vs 7.3个月),相关III期试验(PACIFIC-9)正在进行中。III期SKYSCRAPER-01试验评估了抗TIGIT抗体tiragolumab联合PD-L1单抗阿替利珠单抗vs 阿替利珠单抗单药在同一治疗背景下的疗效和安全性,但该研究未达到任一主要终点(PFS和OS),尽管在联合组中两个结局均有数值改善。
同步ICIs+CRT
在不可切除III期NSCLC患者中同步给予ICIs与cCRT的方法已获得相当大的关注,主要由临床前证据驱动,表明这些药物与放疗之间存在协同作用。然而,多项III期试验结果令人失望:PACIFIC-2试验显示,相较于安慰剂组,cCRT同步度伐利尤单抗随后度伐利尤单抗巩固治疗并未显著改善中位PFS(13.8 vs 9.4个月;HR 0.85;P=0.2)或中位OS(36.4 vs 29.5个月;HR 1.03;P=0.8);CheckMate 73L试验证实,纳武利尤单抗+cCRT后纳武利尤单抗+伊匹木单抗对比cCRT后度伐利尤单抗同样未改善中位PFS(16.7 vs 15.6个月;HR 0.95;P=0.65);EA5181试验再次验证,度伐利尤单抗同步cCRT后度伐利尤单抗巩固治疗 vs cCRT后标准度伐利尤单抗巩固治疗,中位PFS(15.5 vs 16.4个月;HR 1.05;P=0.65)和中位OS(41.5 vs 39.4个月;HR 1.03;P=0.83)均无差异。
ICIs或ICIs+化疗诱导策略
借鉴可切除NSCLC中新辅助免疫化疗的成功经验,多项II期试验在不可切除III期NSCLC患者中探索了诱导ICIs(±化疗)后续放化疗的模式。AFT-16试验显示,诱导阿替利珠单抗后cCRT再进行化疗+阿替利珠单抗巩固,从cCRT结束时计算的2年PFS率达66.3%,超越PACIFIC中45%的2年PFS率。II期APOLO试验探索了阿替利珠单抗+化疗诱导后cCRT和阿替利珠单抗巩固治疗,研究结果显示中位PFS 20.8个月,cCRT结束后18个月PFS为55.1%。II期PACIFIC-BRAZIL试验评估了诱导度伐利尤单抗+化疗后同步度伐利尤单抗+cCRT和度伐利尤单抗巩固治疗,研究结果显示12个月PFS 68.1%,巩固治疗开始时12个月PFS 为66.4%。
对于不耐受化疗的患者,SPRINT试验探索了纯免疫诱导(帕博利珠单抗)后风险适应性放疗(48-55Gy/20次)+帕博利珠单抗巩固的无化疗方案,研究显示出一定的前景,中位PFS 达到26个月。DEDALUS试验则针对不能耐受标准cCRT的患者,采用诱导度伐利尤单抗+化疗后减量大分割放疗+度伐利尤单抗和随后度伐利尤单抗维持治疗,初步显示安全可行。
驱动基因阳性患者的靶向巩固治疗
对于EGFR突变不可切除III期NSCLC,PACIFIC试验事后分析显示度伐利尤单抗未带来PFS(中位PFS 11.2 vs 10.9个月;HR 0.91)或OS获益(中位46.8个月 vs 43.0个月;HR 1.02)。2024年,LAURA和POLESTAR两项III期试验改变了这一领域格局:LAURA试验显示,cCRT/sCRT后奥希替尼巩固治疗可显著延长PFS(中位39.1个月 vs 5.6个月;HR 0.16,95%CI 0.10–0.24;P<0.001),CNS进展风险降低83%(HR 0.17);POLESTAR试验中阿美替尼同样显示显著PFS获益(中位30.4 vs 3.8个月;HR 0.20,95%CI 0.11–0.35;P<0.0001)。两项试验的OS数据目前尚不成熟。基于这些数据,奥希替尼已获NMPA,FDA和EMA批准用于EGFR突变(Ex19del/L858R)不可切除III期NSCLC的巩固治疗,阿美替尼也在NMPA获批相同适应症。这标志着该领域进入基于生物标志物精准选择靶向巩固治疗的时代。
对于ALK融合阳性患者,ALK-TKI巩固治疗的BO42777试验正在进行中;而对于KRAS、BRAF或MET等吸烟相关突变,度伐利尤单抗仍然是CRT后最佳巩固治疗。
结语
不可切除III期NSCLC的治疗已进入精准医学时代。PACIFIC试验确立了cCRT后免疫巩固治疗的新标准,彰显了ICI在不可切除局部晚期NSCLC中的核心价值。为进一步优化ICI联合放疗的策略,目前的研究主要沿三条路径展开:其一,强化巩固治疗,通过提升CRT后免疫治疗的强度以降低全身复发风险并拮抗CRT诱导的免疫抑制,相关III期试验正在验证其能否带来额外获益;其二,同步联合治疗,即将ICI与CRT同步应用,然而现有证据表明该方法不仅未显示出生存获益,反而因毒性叠加而受阻,凸显了优化放疗与免疫治疗协同效应的复杂性;其三,诱导治疗策略,借鉴可切除NSCLC新辅助治疗的理论框架,在CRT前给予化疗联合ICI,尽管早期研究证实了其可行性,但仍需大规模对照研究以明确其临床价值并在不可切除人群中确立疗效。此外,LAURA与POLESTAR试验已证实,对于通常难以从ICI中获益的EGFR突变亚组,第三代EGFR-TKI作为巩固治疗可显著改善预后,进一步丰富了精准治疗的内涵。
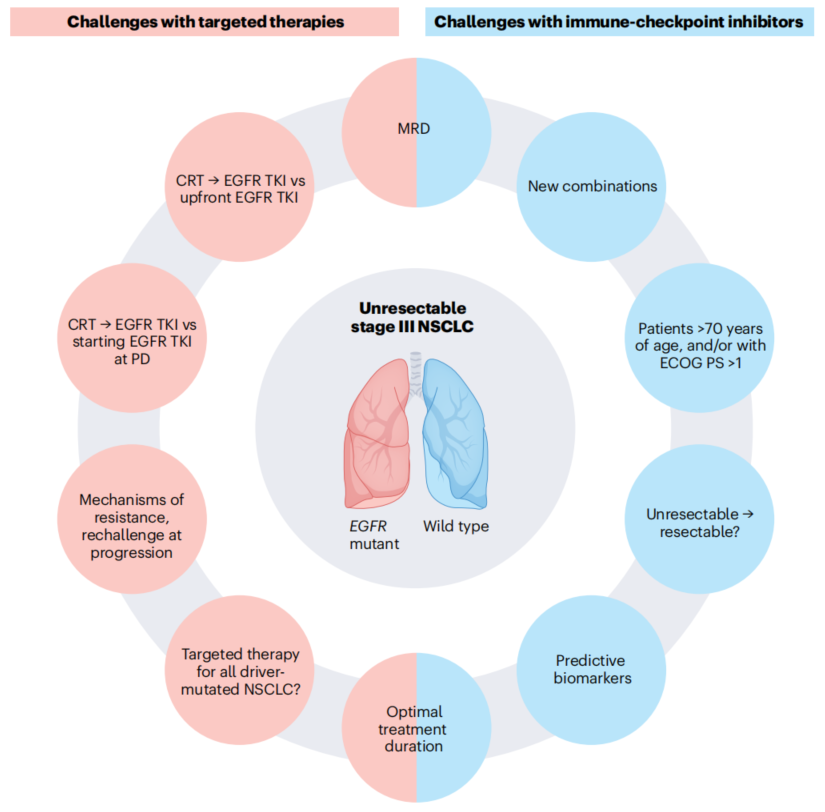
尽管取得上述进展,不可切除III期NSCLC的管理仍面临诸多挑战(图4)。未来的关键方向包括:常规应用ctDNA监测微小残留病灶(MRD)以个体化调整巩固治疗强度;针对CRT不耐受患者(如高龄或体能状态不佳者)优化低强度治疗方案,满足其特殊的临床需求与脆弱性;探索PD-L1表达及其他致癌驱动基因变异之外的新型生物标志物,以实现更精细的治疗分层;同时,通过改进放疗技术(如免疫保护性照射、质子治疗等)最大化其与ICI的协同效应并控制毒性。此外,对于接受ICI巩固治疗后出现局部或转移性复发的患者,亟需建立标准化的后续治疗策略(包括再挑战治疗与局部消融的合理整合);而如何通过系统治疗将不可切除病灶转化为可切除状态,仍是值得深入探索的重要领域。
[1] Remon J, Levy A, Gille R, Martel-Lafay I, Bortolot M, Hendriks LEL, Faivre-Finn C, Leighl N, Reck M, Pérol M. Unresectable stage III non-small-cell lung cancer: state of the art and challenges. Nat Rev Clin Oncol. 2026 Jan;23(1):22-39. doi: 10.1038/s41571-025-01080-4. Epub 2025 Oct 9. PMID: 41068447.
排版编辑:肿瘤资讯-明小丽












 苏公网安备32059002004080号
苏公网安备32059002004080号


