日本国立癌症中心医院胃肠道肿瘤内科的Ken Kato教授以“亚洲胃肠道恶性肿瘤:流行病学、生物学与协作临床研究活动”为题发表重要演讲。该演讲系统阐述了亚洲与西方国家在胃肠道肿瘤领域存在的显著差异,详细介绍了由日本国立癌症中心于2020年发起的ATLAS(Asian Clinical Trials Network for Cancers)国际临床研究网络的建设进展,并重点展示了即将启动的PLATANUS研究和OMESQ项目等前沿研究计划。在全球胃肠道肿瘤治疗格局不断演变的背景下,这一演讲为理解亚洲区域特异性治疗需求、推动跨国研究协作提供了重要视角。
亚洲与西方胃肠道肿瘤存在多维度差异
亚洲与西方国家在胃肠道肿瘤领域存在诸多根本性差异,这些差异直接影响临床研究设计和治疗策略制定。从危险因素来看,幽门螺杆菌感染在亚洲胃癌发病中扮演着关键角色;从组织学和生物学特征而言,食管癌、胃癌和结直肠癌在东西方人群中呈现出不同的病理类型分布;亚洲食管癌以鳞状细胞癌为主,而西方则以腺癌占多数。此外,东亚地区已建立了相对完善的食管癌和胃癌筛查体系,这与西方国家形成鲜明对比。在发病率和死亡率方面,2022年全球癌症数据显示,亚洲地区食管癌、胃癌和胆道肿瘤的负担远高于西方国家。基于上述差异,亚洲与西方在食管癌和胃癌的治疗策略上形成了各自独特的路径。
ATLAS网络:构建亚洲国际癌症临床研究平台
为应对上述挑战并推动亚洲胃肠道肿瘤研究的持续发展,日本国立癌症中心于2020年9月正式启动ATLAS项目。该项目是一个政府支持的多国协作网络,旨在建立覆盖亚洲的国际癌症临床研究平台。ATLAS将日本的研究协作拓展至新加坡、泰国、马来西亚、越南、菲律宾和印度尼西亚等国家,实现了针对不同癌症类型的快速试验启动能力。该项目在9个合作机构强化试验基础设施建设,并开展包括早期药物开发和转化研究在内的多元化国际研究。ATLAS同时提供培训和电子学习资源,致力于培养区域专业人才,最终目标是将亚洲打造成全球癌症临床研究的领军者。
从组织架构来看,ATLAS设立了由日本Kan Yonemori博士担任主席、新加坡Darren Lim Wan Teck博士担任候任主席的理事会,总部设于日本国立癌症中心医院。覆盖马来西亚、菲律宾、泰国、越南、中国台湾、韩国、新加坡和日本等国家和地区的主要癌症中心,已建立起类似于欧洲EORTC和日本JCOG的亚洲临床研究协作组织架构。目前,ATLAS已启动多项临床研究,包括针对罕见癌症的MASTER KEY Asia平台研究、涵盖六种癌症类型的A-TRAIN液体活检研究,以及PATHWAY、HARMONY、CHOICE等多个在研或筹备中的项目。
局部晚期胃癌和胃食管交界部腺癌围手术期治疗策略的东西方分歧
Ken Kato教授详细阐述了局部晚期胃癌和胃食管交界部腺癌围手术期治疗领域东西方策略的演变历程。亚洲传统策略采用“先手术后辅助治疗”的路径,日本ACTS-GC研究确立了D2根治术后S-1单药辅助化疗1年的标准地位,韩国和中国CLASSIC研究则验证了CapeOX辅助化疗6个月的疗效,日本JACCRO-GC07研究进一步证实对于III期患者,S-1联合多西他赛的双药辅助方案优于S-1单药。
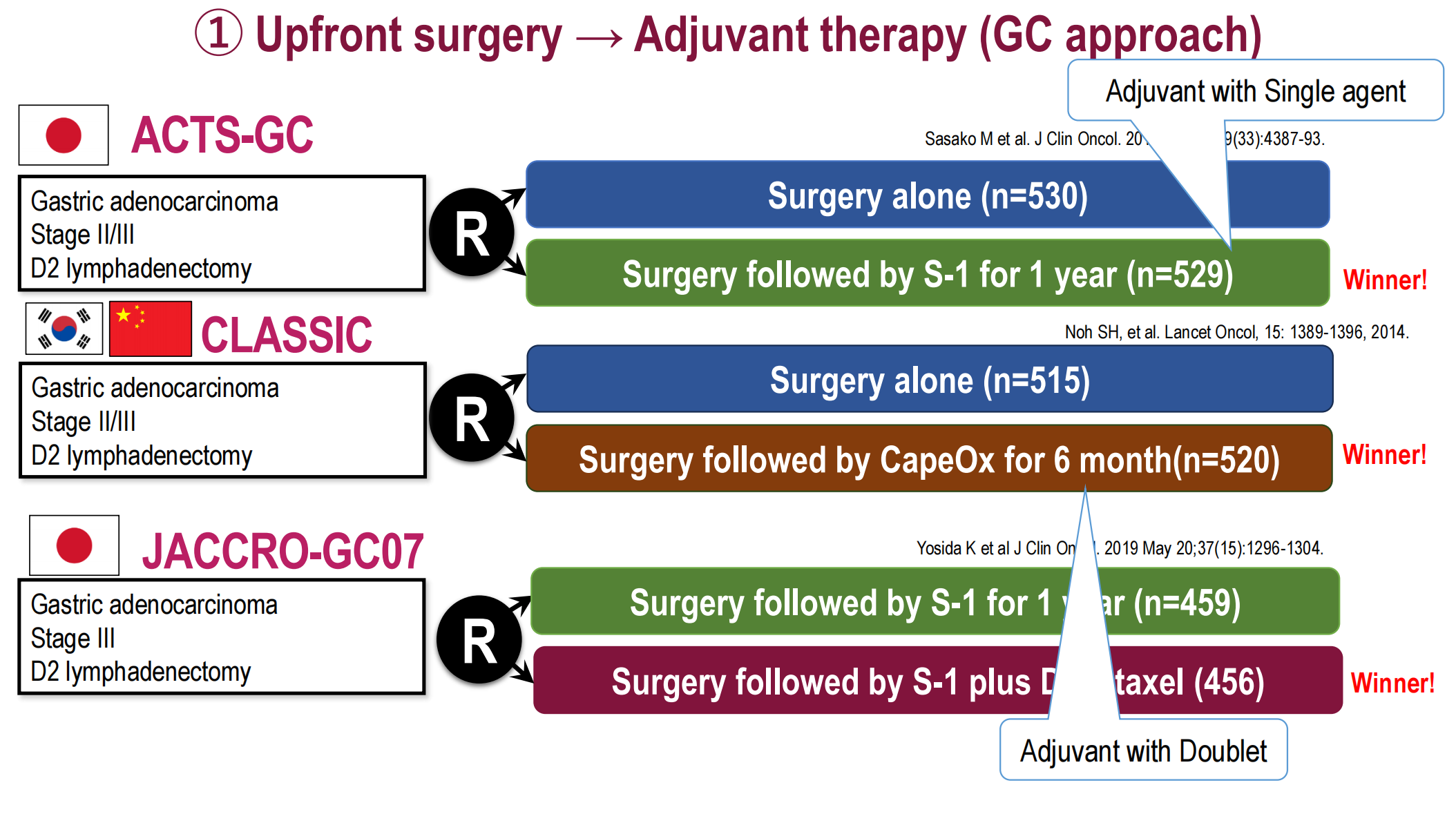
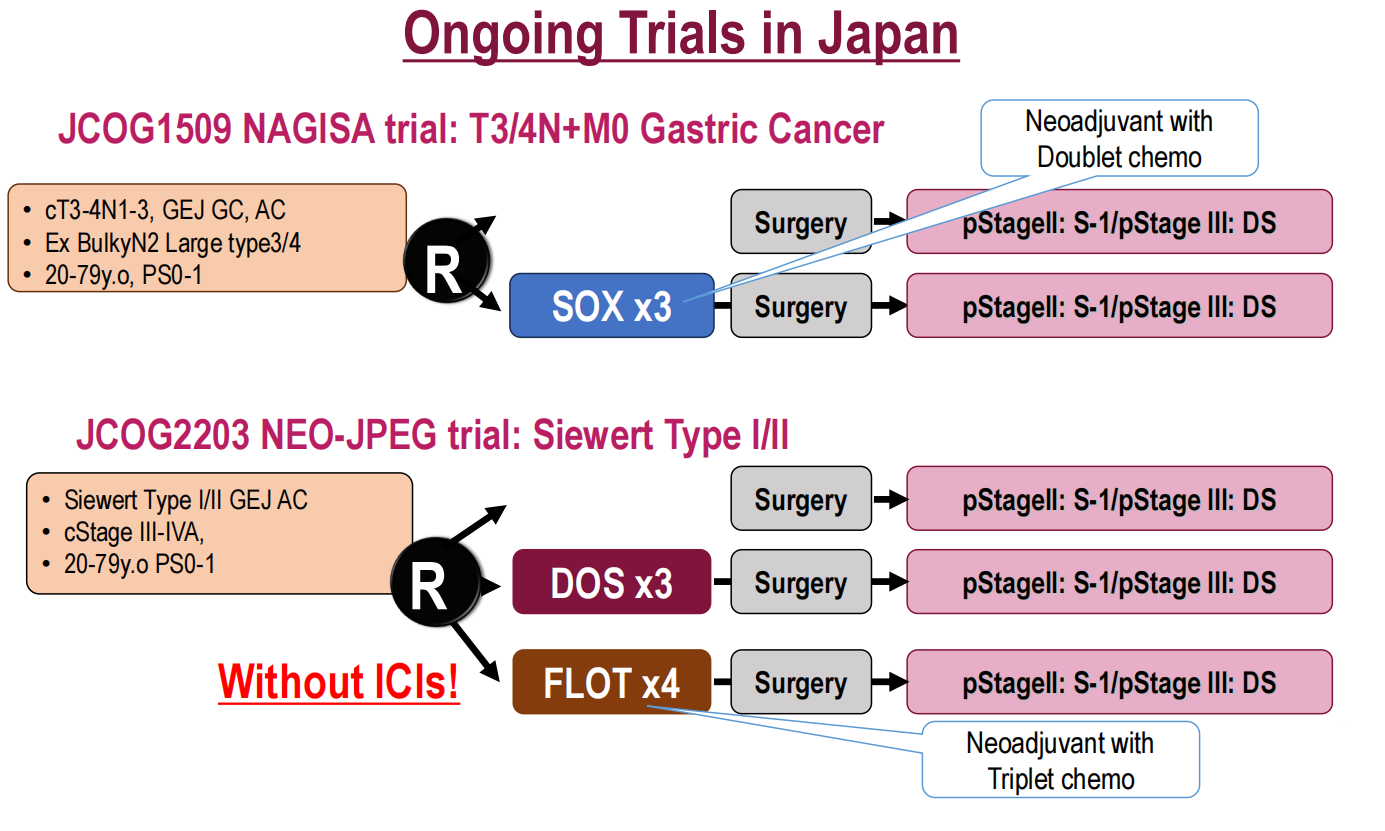
与此同时,日本正在进行的JCOG1509 NAGISA研究探索新辅助SOX方案对T3/4N+M0胃癌的价值,JCOG2203 NEO-JPEG研究则针对Siewert I/II型胃食管交界部腺癌比较新辅助DOS三药方案、FLOT方案与单纯手术的疗效,值得注意的是该研究未纳入免疫检查点抑制剂。
从辅助免疫治疗角度审视,一项针对亚洲患者(日本、韩国、中国)的III期随机对照研究评估了pIII期胃癌或胃食管交界部癌患者术后辅助化疗联合或不联合免疫单药的疗效。结果显示,辅助化疗联合免疫检查点抑制剂未能延长无复发生存期(HR=0.90,P=0.4363),3年无复发生存率在联合组为68.4%,对照组为65.3%。这一结果提示在亚洲胃癌患者中,单纯将免疫治疗叠加于辅助化疗方案的策略可能需要重新审视。
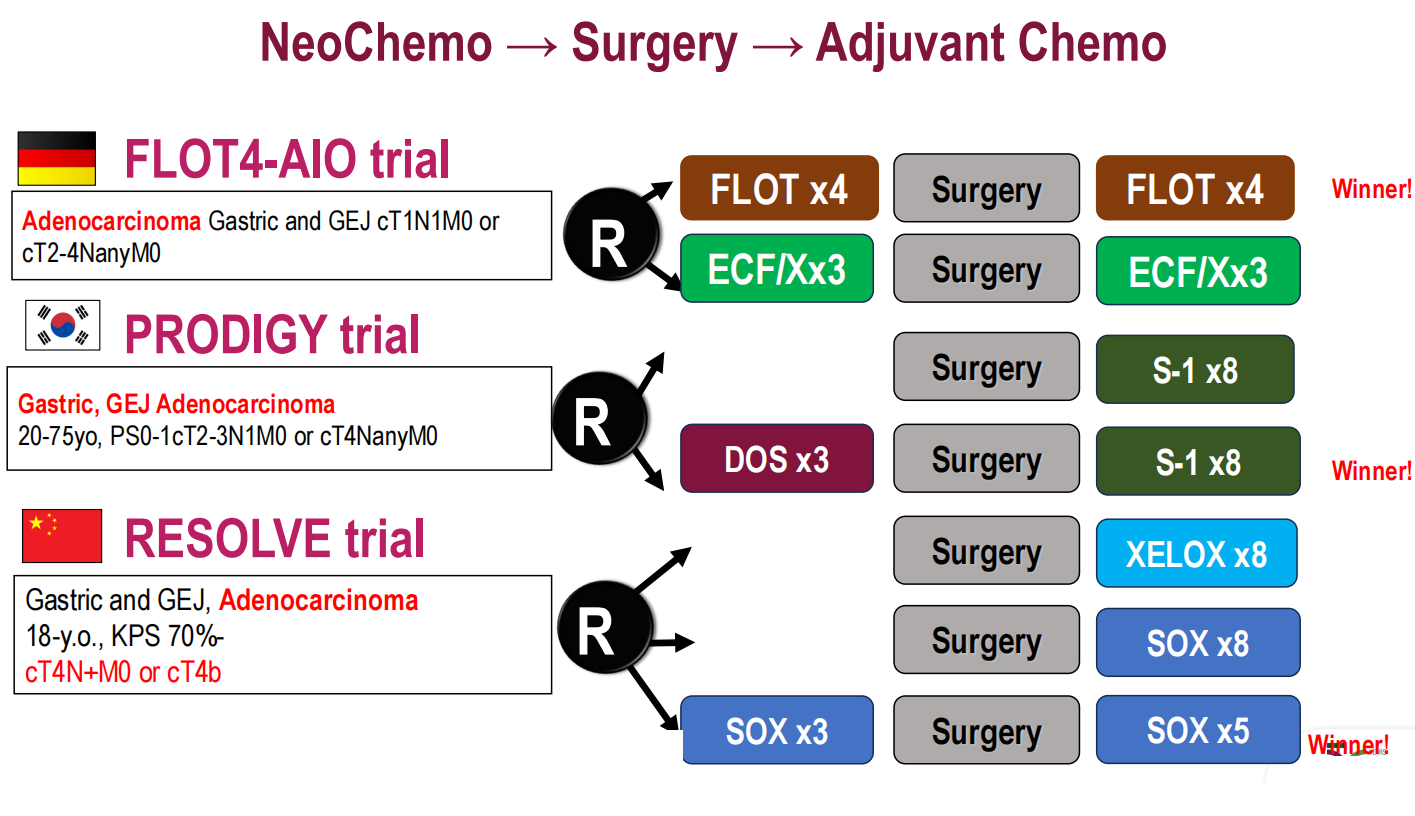
西方策略则遵循了不同的演进路径。荷兰CROSS研究确立了新辅助放化疗联合手术治疗食管癌的地位,该研究中腺癌占75%、鳞癌占25%。在此基础上,CheckMate-577研究证实对于新辅助放化疗后未达病理完全缓解的食管癌和胃食管交界部腺癌患者,术后辅助纳武利尤单抗免疫治疗可显著改善无病生存期。德国FLOT4-AIO研究则确立了围手术期FLOT方案(5-FU、亚叶酸钙、奥沙利铂、多西他赛)治疗胃癌和胃食管交界部腺癌的标准地位,韩国PRODIGY研究和中国RESOLVE研究分别从亚洲视角验证了新辅助化疗+手术联合辅助化疗模式的可行性。
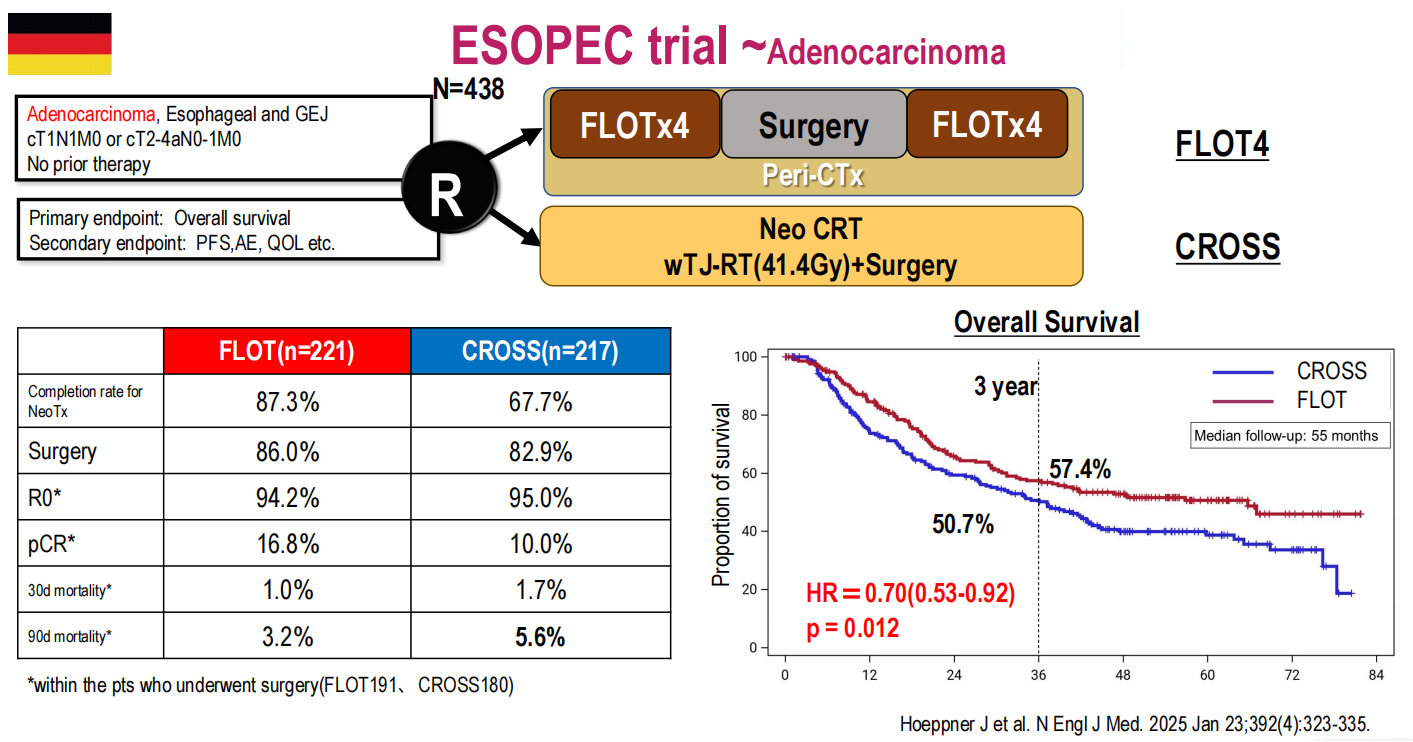
2025年1月发表于《新英格兰医学杂志》的ESOPEC研究进一步强化了西方围手术期化疗策略的证据基础。该研究纳入438例食管和胃食管交界部腺癌患者,随机比较围手术期FLOT方案与新辅助CROSS放化疗方案。结果显示,FLOT组新辅助治疗完成率(87.3% vs 67.7%)、病理完全缓解率(16.8% vs 10.0%)均优于CROSS组,更重要的是FLOT组3年总生存率显著提高(57.4% vs 50.7%,HR=0.70,P=0.012)。
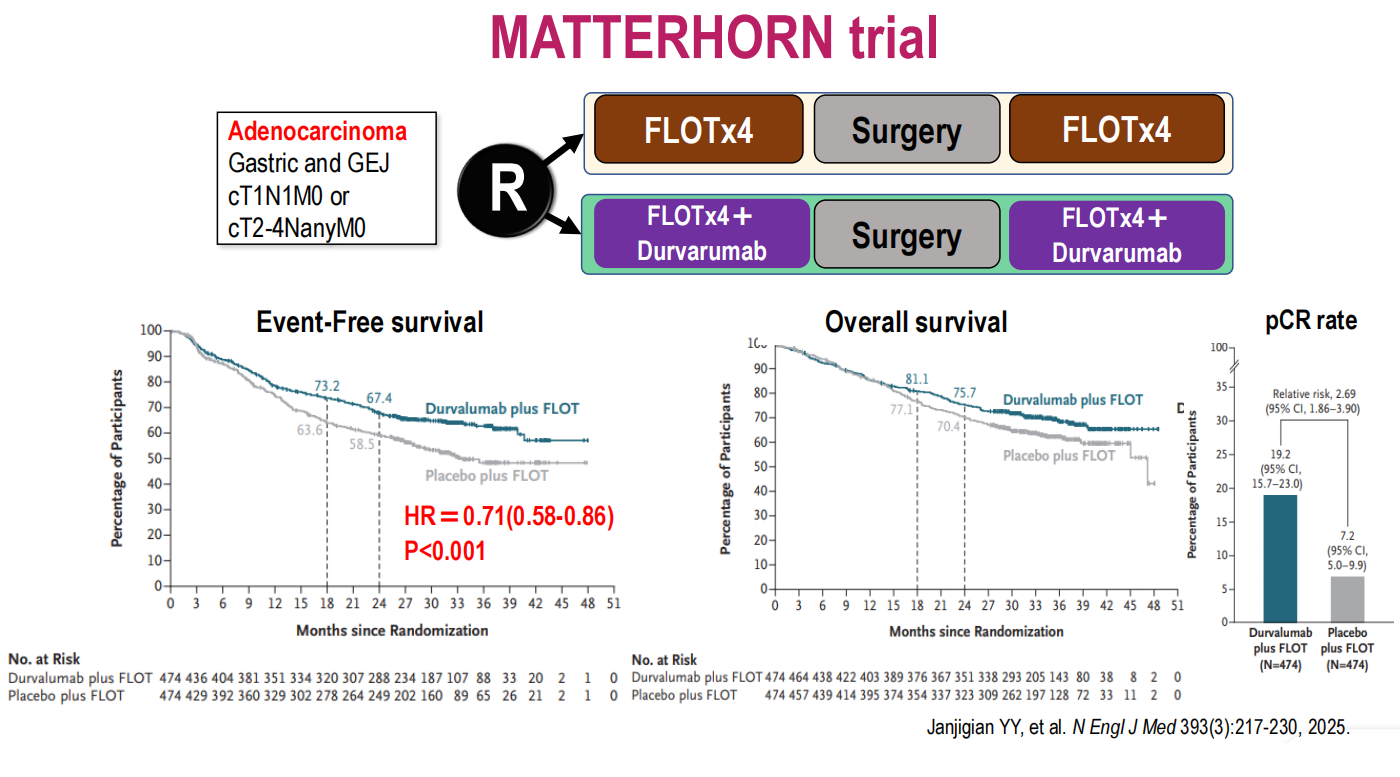
具有里程碑意义的MATTERHORN研究于2025年发表,该研究在围手术期FLOT方案基础上联合了免疫检查点抑制剂度伐利尤单抗。结果显示,度伐利尤单抗联合FLOT组的无事件生存期显著优于单纯FLOT组(HR=0.71,P<0.001),病理完全缓解率亦显著提高(19.2% vs 7.2%,相对风险2.69)。这一结果标志着围手术期化疗联合免疫治疗策略在胃癌和胃食管交界部腺癌中的成功。Ken Kato教授强调,MATTERHORN研究的成功证明了免疫检查点抑制剂与术前化疗联合的有效性,但目前亟须开展研究以弥合亚洲和西方两种治疗策略之间的证据鸿沟。
PLATANUS研究:探索亚洲胃癌围手术期免疫联合化疗新策略
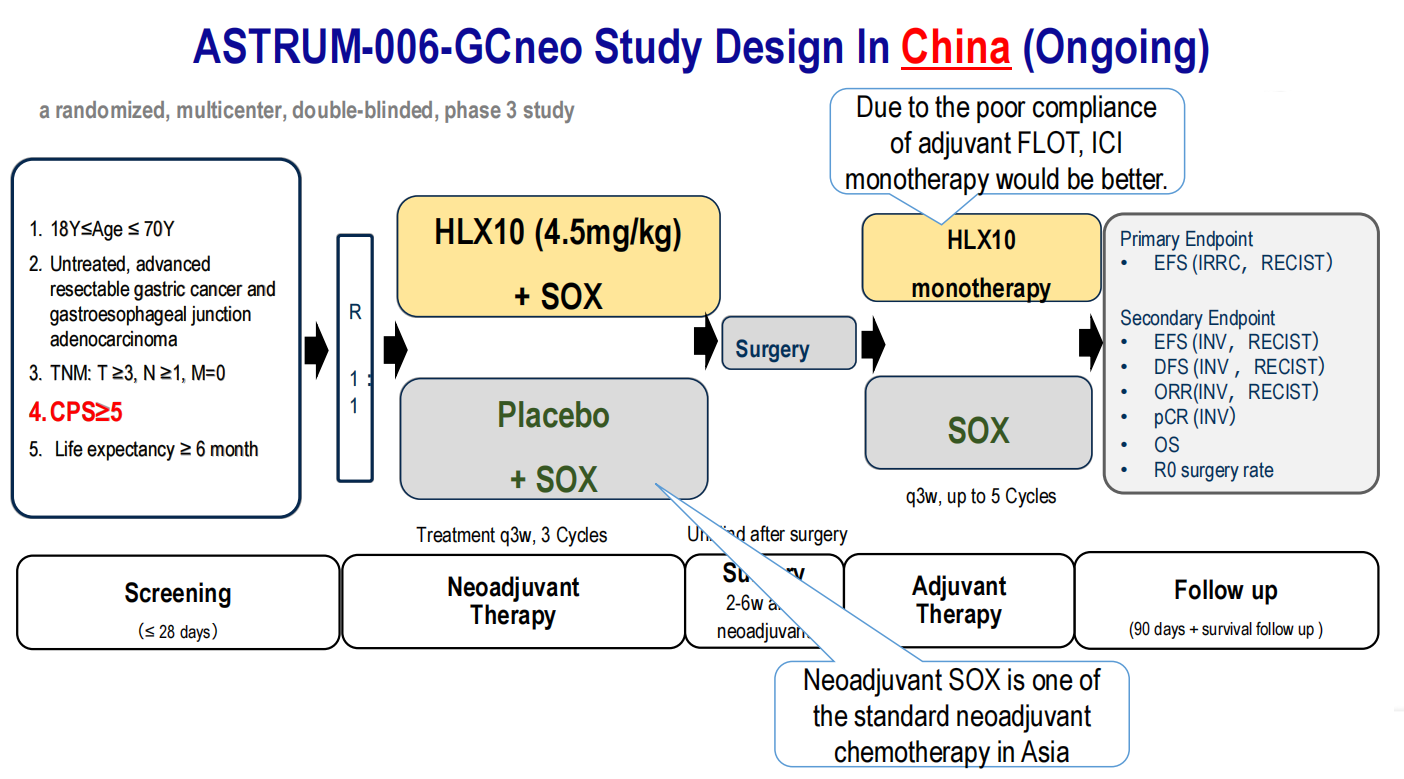
基于上述背景,Ken Kato教授介绍了即将启动的PLATANUS研究。该研究是一项随机、双盲的II期临床研究,旨在作为中国正在进行的ASTRUM-006-GCneo研究的桥接研究。ASTRUM-006-GCneo研究采用HLX10(一种PD-1抑制剂)联合SOX方案进行新辅助治疗,术后根据病理分期给予HLX10单药治疗或SOX辅助化疗,研究纳入PD-L1 CPS≥5的患者,体现了亚洲特色——新辅助SOX方案作为标准新辅助化疗,以及考虑到辅助FLOT依从性较差而采用免疫单药辅助的设计理念。
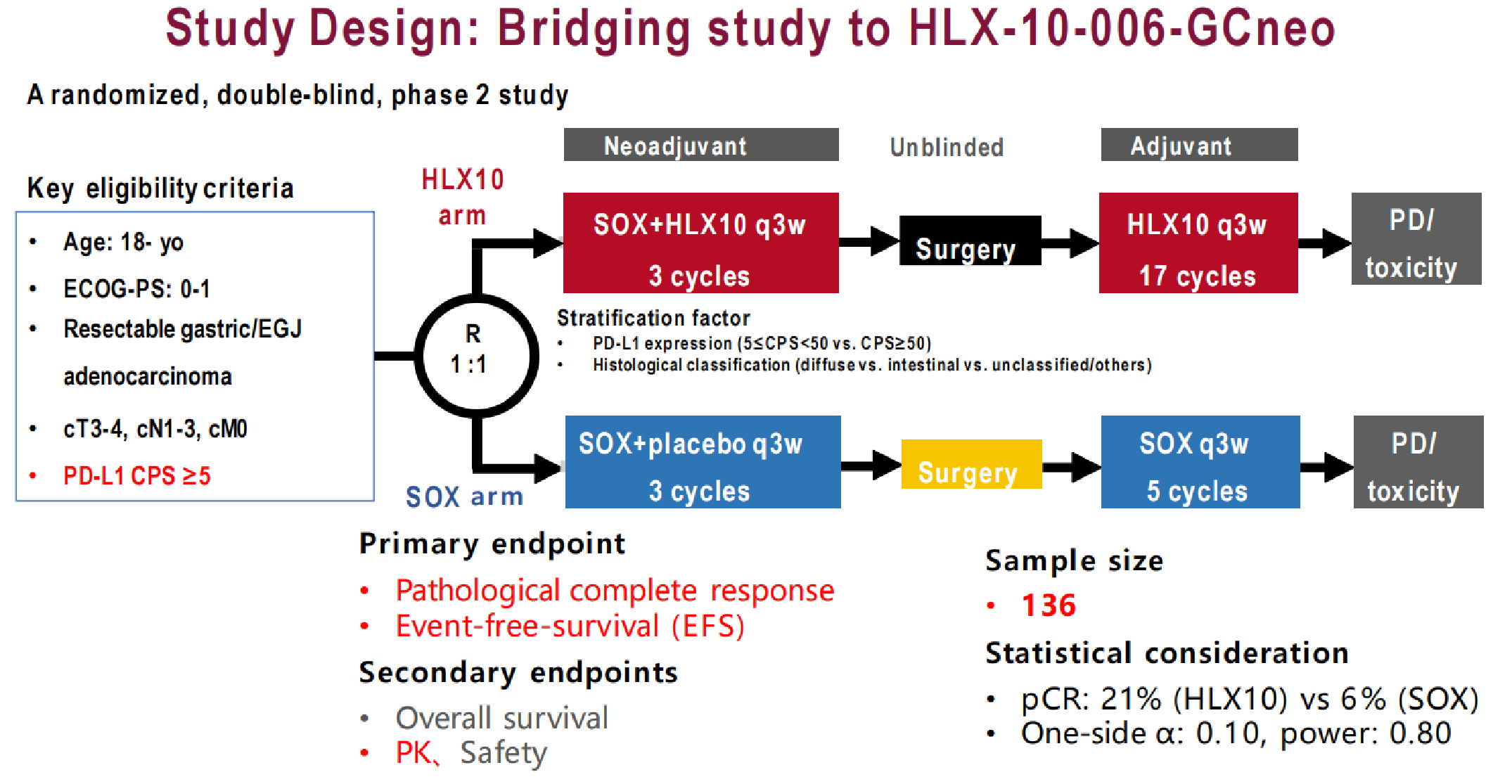
PLATANUS研究计划在日本和韩国开展,纳入可切除的cT3-4、cN1-3、cM0期胃癌或胃食管交界部腺癌患者,要求PD-L1 CPS≥5。患者将1:1随机分配至SOX联合HLX10组或SOX联合安慰剂组接受3个周期新辅助治疗,术后揭盲,HLX10组继续接受HLX10单药治疗17个周期,对照组接受SOX辅助化疗5个周期。主要研究终点为病理完全缓解率和无事件生存期,计划纳入136例患者。统计假设中,HLX10组病理完全缓解率预期为21%,对照组为6%,单侧α=0.10,检验效能0.80。该研究计划于2026年夏季启动,预计2027年12月完成入组,2031年完成分析。
OMESQ项目:建立亚洲食管鳞癌寡转移共识与临床研究框架
Ken Kato教授最后介绍了针对食管鳞癌寡转移状态的OMESQ(OligoMetastatic Esophageal SQuamous cell carcinoma)项目。该项目的背景源于欧洲已开展的OMEC(OligoMetastatic Esophagogastric Cancer)协作组工作,后者获得了ESMO、ESSO、IGCA、EORTC、ESTRO等多个学术组织的认可支持,但主要聚焦于腺癌。考虑到食管鳞癌在亚洲的高发特性,OMESQ项目旨在通过德尔菲(Delphi)共识研究,确定食管鳞癌寡转移的定义和治疗策略。
该项目面临的关键问题包括:寡转移的定义标准(远处转移器官数量、转移病灶数量、病灶大小、转移部位、是否合并原发灶和区域淋巴结转移及其计数方式)、再分期诊断方法(CT、PET、MRI等)、系统治疗方案(方案选择、治疗时长、疗效评估)以及局部治疗选择(手术、立体定向放疗、常规放疗等)。OMESQ项目已完成系统综述(OMESQ-1)、病例讨论(OMESQ-2,分别在日本、亚洲其他国家和欧洲进行)、回顾性数据分析(OMESQ-3),目前正在进行德尔菲共识阶段(OMESQ-4)。2025年5月13日,OMESQ-Asia共识会议在日本国立癌症中心医院召开,来自亚洲多个国家和地区的专家参与了讨论。
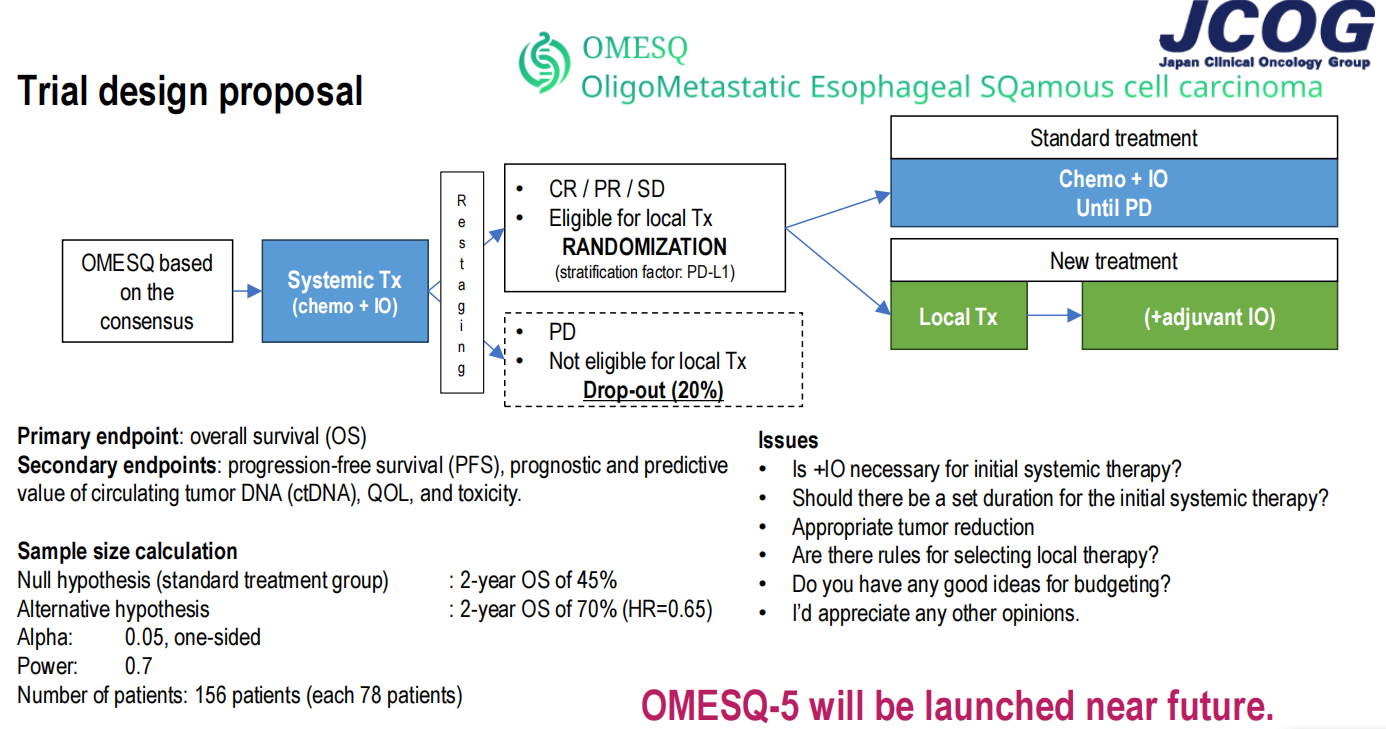
基于共识结果,OMESQ-5研究正在设计中。初步设计方案为:符合共识定义的食管鳞癌寡转移患者首先接受系统治疗(化疗联合免疫治疗),经再分期评估后,达到疾病控制(CR/PR/SD)且适合局部治疗的患者进行1:1随机分组,分别接受继续系统治疗(化疗联合免疫治疗)直至疾病进展(标准治疗组)或局部治疗联合辅助免疫治疗(试验组)。主要研究终点为总生存期,次要终点包括无进展生存期、ctDNA的预后和预测价值、生活质量和毒性。样本量计算基于标准治疗组2年总生存率45%、试验组70%(HR=0.65)的假设,单侧α=0.05,检验效能0.7,需入组156例患者。OMESQ-5不久将启动。
排版编辑:肿瘤资讯-Marie











 苏公网安备32059002004080号
苏公网安备32059002004080号


