
陈凛

徐泽宽

梁寒
 周岩冰
周岩冰
引用本文: 中国抗癌协会胃癌专业委员会机器人手术临床研究协作组. 胃癌患者新辅助治疗围手术期加速康复外科管理热点问题专家共识(2026版)[J]. 中华胃肠外科杂志, 2026, 29(3): 243-257. DOI: 10.3760/cma.j.cn441530-20260209-00079.
作者:中国抗癌协会胃癌专业委员会机器人手术临床研究协作组
通信作者:陈凛,北京大学国际医院,北京 102206,Email:chenlinbj@vip.sina.com;梁寒,天津医科大学肿瘤医院,天津 300060,Email:tjlianghan@126.com;徐泽宽,江苏省人民医院,南京 210029,Email:xuzekuan@njmu.edu.cn;周岩冰,青岛大学附属医院,青岛 266000,Email:zhouyanbing@qduhospital.cn
摘要
加速康复外科( ERAS )理念已被广泛应用于胃癌手术的围手术期管理中,但接受新辅助治疗的胃癌患者存在特殊的病理生理特点,易出现抗肿瘤治疗相关不良反应,更易发生或加重营养相关合并症和心肺功能受损等问题,需结合患者具体情况细化完善 ERAS 的具体条款,而临床医师在对新辅助治疗后的胃癌患者 ERAS 实施方面缺乏指导性共识。为此,中国抗癌协会胃癌专业委员会机器人手术临床研究协作组牵头国内相关领域的专家,经过检索国内外研究成果,借鉴国外经验并结合国内实际情况,经过反复讨论并经专家认可后制定了《胃癌患者新辅助治疗围手术期加速康复外科管理热点问题专家共识( 2026 版)》。本共识针对新辅助治疗(包括化疗、免疫治疗、放疗及靶向治疗)后胃癌患者围手术期 ERAS 管理的热点问题,基于最新的循证医学证据,从病理生理学基础、术前预康复、术中管理及术后康复等多个维度,提出了 21 项核心问题的推荐意见,涵盖新辅助治疗对患者营养状态、功能能力、器官功能的影响机制以及组织水肿与纤维化对手术难度和吻合口愈合的挑战与对策,旨在为临床工作者提供规范化、个体化的围手术期管理指导,以降低术后并发症,改善患者预后,提升生活质量。
我国胃癌以进展期为主,约占全部病例的 80% ,手术联合辅助治疗效果有限,根治性胃切除术是局部进展期胃癌的主要治疗手段 [1] 。新辅助治疗( neoadjuvant therapy , NAT )可明确肿瘤对治疗方案的敏感性,降低肿瘤分期,提高 R 0 切除率,还能控制肿瘤的微转移和减少复发转移风险,进而改善患者预后 [2] 。目前, NAT 已成为局部进展期胃癌的重要治疗策略。
近年来,加速康复外科( enhanced recovery after surgery , ERAS )理念已被广泛应用于围手术期管理并取得显著成效。研究证实,腹腔镜胃切除术围手术期应用 ERAS 安全可行,可缩短住院时间、降低术后并发症发生率、缩短术后辅助治疗启动时间等,且有助于改善患者预后,尤其适用于进展期胃癌病例 [3-5] 。研究进一步证实, ERAS 方案同样适用于接受 NAT 的胃癌患者 [6] 。但接受 NAT 的胃癌患者存在特殊病理生理特点,易出现抗肿瘤治疗相关不良反应,更易发生或加重营养相关合并症和心肺功能受损等问题,需结合患者具体情况细化完善 ERAS 条款 [7] 。同时,该类患者诊疗周期涵盖确诊、 NAT 、术前体能恢复至可耐受手术的水平,建议推行 “肿瘤预康复”全程管理,通过无缝覆盖的预康复措施提升患者功能状态,为手术创造有利条件 [8] 。
目前,临床医师在对 NAT 后的胃癌患者实施 ERAS 方面缺乏指导性共识。为此,由中国抗癌协会胃癌专业委员会机器人手术临床研究协作组牵头,组织包括胃肠外科、麻醉科及临床营养科等国内资深专家组成核心工作组,经过系统检索 PubMed 、 Embase 、 CNKI 等数据库截至 2025 年 10 月的相关文献,借鉴国外经验并结合国内实际情况,收集证据,严格遵循国际规范,从病理生理学基础、术前预康复、术中管理以及术后康复等多个维度展开,完成本共识的撰写工作。并于 2025 年 11 月组织线下专家审议会,于 2026 年 1 月开展 Delphi 法无记名投票;针对存在分歧的内容进行修订后,开展了第二轮投票,仅赞同率超过 80% 的推荐意见被视为达成共识;最终,由总负责人及撰稿人结合各方意见进行修改,并经专家认可后定稿。本共识适用于胃肠外科、肿瘤内科、麻醉科、临床营养科、康复科的医师以及护理团队,旨在为这一特殊群体的 ERAS 临床应用提供切实可行的操作指导,助力多学科协作并提供优质的医疗服务。
共识采用 GRADE 证据质量和推荐强度分级系统(表 1 ) [9] 。已在国际实践指南注册与透明化平台注册( PREPARE - 2025CN1769 )。

热点问题 1 :不同 NAT 模式(化疗、免疫、靶向及放疗)对患者生理功能的特异性影响是什么?
推荐意见:不同 NAT 方案对患者生理功能、营养代谢状态、功能能力的特异性影响各异,制定 ERAS 方案前,需系统评估其对患者多方面的潜在影响,再个体化调整 ERAS 路径。(证据质量等级:高;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
1. 化疗:是胃癌 NAT 的传统方式,可杀伤癌细胞,但对正常细胞存在毒性,易引发营养状况恶化、骨髓造血功能抑制、肝肾功能损伤等问题,我国 RESOLVE 研究已详细报道围手术期一线 SOX 化疗方案(替吉奥 + 奥沙利铂)的不良事件 [10] 。
2. 免疫治疗:其通过激活自身免疫系统攻击癌细胞,对生理功能影响较小,但可能引发免疫相关心肺损伤或内分泌紊乱等特异性不良反应 [11-12] 。
3. 靶向治疗:其在精准抑制肿瘤的同时,存在特定的不良反应。例如,雷莫西尤单抗与紫杉醇联合使用时,容易导致高血压或出血等情况;曲妥珠单抗联合化疗可能引发心脏毒性。对这些不良反应的管理,需要多学科协作以及进行个体化监测 [13-14] 。
4. 放疗:利用高能射线抑制并杀灭癌细胞,通常与全身治疗联合使用。其影响主要集中在照射区域,容易导致胃肠道黏膜损伤,并出现恶心或腹泻等症状 [15] 。
综上所述,胃癌的 NAT 模式对患者的生理功能存在各自的特异性影响。在临床实践中,需依据患者的具体状况,全面考量治疗的获益与风险,制定个性化的治疗方案。
热点问题 2 :如何量化评估 NAT 后患者的功能能力及重要器官功能?
推荐意见:结合心脏超声、肺功能检查、 6 min 步行试验 ( six-minute walk test,6MWT )、心肺运 动试验等功能检测项目,以及血常规、肝肾功能、内分泌功能等实验室检查结果,再辅以欧洲癌症研究与治疗组织生活质量核心量表( EORTC QLQ-C30)和胃癌特异性生活质量量表(QLQ-STO22)等主观评估量表,从多维度对患者的功能能力与重要器官功能进行评估。(证据质量等级:中;推荐强度:强推荐;专家组赞同率:100%)
推荐说明
对胃癌患者在 NAT 后的功能能力进行量化评估,是优化治疗方案、改善预后情况的关键所在。目前,已有多种成熟的量化方法,且每种方法都具备各自的应用优势。
1.6MWT :能够以无创的方式评估患者的运动耐力和心肺适能,其应用标准可参考美国胸科学会指南 [16] ;
2.EORTC QLQ - C30 和 QLQ - STO22 量表:能全面评估身心及社会功能,其有效性已通过临床验证 [17] ;
3. 器官功能评分:美国东部肿瘤协作组( Eastern Cooperative Oncology Group , ECOG )卡氏功能状态评分( Karnofsky Performance Status , KPS )可精准评估体能状态 [18] ; Caprini 评分用于静脉血栓栓塞症风险分层 [19] ;心肺运动试验可多指标评估心肺功能,其临床应用建议可参考 2016 年专家共识,临床可按需选用 [20] 。同时,需结合实验室及影像学检查进行综合评估。借助血常规、肝肾功能检验,排查化疗相关不良反应;通过完善心脏超声和胸部 CT ,评估心肺功能。针对新辅助免疫治疗的患者,还需检测甲状腺功能和皮质醇水平,以评估是否存在免疫相关内分泌功能障碍 [21] 。
热点问题 3 : NAT 如何影响患者的营养状态?其特殊性有哪些?
推荐意见: NAT相关营养并发症具有特殊性,需多维度动态评估营养状态。治疗前用营养风险筛查2002(Nutritional Risk Screening 2002,NRS 2002),≥3分者继以患者主观整体评估(Patient-Generated Subjective Global Assessment,PG-SGA )工具进行评估,推荐全球营养不良领导倡议诊断标准( Global Leadership Initiative on Malnutrition,GLIM)作出相应诊断。(证据质量等级:中;推荐强度:弱推荐;专家组赞同率:97.56% )
推荐说明
NAT 对胃癌患者营养状态的影响具有显著特殊性,主要体现在:抗肿瘤治疗不良反应引发营养摄入减少,且症状可能随治疗加剧;治疗期间患者肌肉量和脂肪量显著下降 [22-24] ;血清白蛋白等营养指标发生改变 [24] ;营养不良易致治疗中断或剂量降低,影响治疗效果,良好营养状态则助力完成治疗 [22] ;影响存在个体化差异,高龄或虚弱患者更易感,不同化疗方案的影响也不同。
所有胃癌 NAT 患者治疗前需行营养风险筛查,推荐用 NRS2002 ,该评分 ≥3 分者术后并发症风险更高,女性患者尤甚 [25-26] 。有营养风险者需进一步评估诊断, PG - SGA 适合胃癌患者营养评估 [27] 。 GLIM 是全球通用营养不良诊断工具,可预测患者功能状态、肿瘤相关症状及生活质量等 [28-29] ;其在中国患者中的有效性亦获验证 [30] 。
热点问题 4 : NAT 是否会对胃癌患者的凝血机制及围手术期出血风险产生影响?
推荐意见:围手术期应常规监测血常规、凝血功能以及 D- 二聚体,对于使用抗血管生成药物或者存在出血倾向的患者,需提高监测频率。为降低术中及术后的出血风险,建议这类患者术前停药至少 2~4 周,且应遵循术中出血分级标准进行质量控制。(证据质量等级:中;推荐强度:弱推荐;专家组赞同率: 97.56% )
推荐说明
1. 化疗:是胃癌 NAT 的常见方式,其中铂类、氟尿嘧啶类等药物可通过多种途径影响患者的凝血功能。一方面,药物对骨髓造血功能具有抑制作用,会致使血小板数量减少以及聚集功能异常,显著提升出血风险;另一方面,部分化疗方案还会损伤血管内皮细胞并异常激活凝血系统,或者通过释放促炎因子诱发高凝状态,进而增加静脉血栓栓塞的风险。临床上常呈现出血倾向与血栓形成并存的矛盾现象 [31-32] 。
2. 免疫治疗:如程序性死亡受体 1 抑制剂( programmed death - 1 inhibitor , PD - 1 )所引发的凝血障碍以及免疫性血小板减少( immune thrombocytopenia , ITP ),其核心机制为免疫活化介导的促凝状态、抗体介导的血小板破坏以及生成抑制。需结合临床表现、凝血功能以及血小板计数等检查来明确诊断,并排除其他病因。应按照分级原则进行处理,且需要多学科协作并密切监测 [33-35] 。
3. 靶向治疗:如雷莫西尤单抗或阿帕替尼等抗血管生成药物,通过抑制血管内皮生长因子 / 血管内皮生长因子受体( vascular endothelial growth factor , VEGF/VEGF receptor , VEGFR )信号通路,干扰血管内皮细胞的修复与再生,致使血管脆性增大,完整性受损,显著增加了黏膜出血或消化道出血等风险;同时,这类药物可能影响内皮细胞促凝与抗凝因子的平衡,进而诱发动脉及静脉血栓 [13] 。曲妥珠单抗等抗人类表皮生长因子受体 2 ( human epidermal growth factor receptor 2 , HER2 )药物对凝血系统的直接影响较小,出血风险较低。然而,当与化疗联合使用时,可能会叠加骨髓抑制效应,从而增加出血风险,并且需要关注其潜在的心脏毒性对凝血微环境所产生的影响。
4. 放疗:其对凝血功能的影响,主要是由于对照射野血管造成直接损伤。在急性期,会引发放射性血管炎,致使内皮细胞水肿坏死,进而增加局部渗血情况;从远期来看,会导致血管纤维化和管腔狭窄,从而增加术中出血风险以及手术操作的难度 [36] 。若采用微创手术,建议参考 Jia 等 [37] 开展的 RCT 研究中所制定的术中出血分级标准,规范手术操作流程,严格执行术中质量控制,以确保手术操作的标准化和安全性,降低术中出血相关不良事件的发生率。
热点问题 5 : NAT 对术后组织愈合的潜在影响是什么?
推荐意见: NAT 中的化疗、放疗、靶向及免疫药物可通过 “直接抑制修复细胞功能”与“间接破坏愈合微环境”双重机制影响组织愈合。(证据质量:低;推荐强度:弱推荐;专家组赞同率: 97.56% )
推荐说明
NAT 对胃癌患者术后出血和组织愈合存在直接与间接双重不良影响。
1. 直接影响:化疗通过阻滞细胞周期、抑制血管生成和阻碍上皮迁移,减少胶原合成、延迟血管重塑和延长上皮化时间 [38-39] ;放疗引发慢性辐射损伤,造成成纤维细胞耗竭、微血管密度骤降,形成缺血性愈合障碍 [40-42] ;靶向药物中,布鲁顿酪氨酸激酶抑制剂( Bruton ′ s tyrosine kinase inhibitor , BTK 抑制剂)降低血小板聚集率增加出血风险, VEGF 抑制剂易致吻合口漏发生率大幅上升 [43-44] ;免疫治疗则阻断巨噬细胞转化,延长炎性期、延迟肉芽形成,增加伤口并发症风险 [45] 。
2. 间接影响:体现在 NAT 后多数患者出现组织水肿与纤维化,加重局部缺血和增加吻合口漏风险 [46] ;同时破坏营养 - 免疫轴,导致白蛋白降低、骨髓抑制,糖皮质激素治疗免疫相关不良事件( immune - related adverse event , irAE )还会进一步抑制组织愈合 [46-47] 。
热点问题 6 :如何实现胃癌 NAT 与术前预康复的同步化与整合管理?
推荐意见:胃癌 NAT 应当在多学科团队诊疗模式下制定个体化方案,明确分期并规范开展治疗。同时,应同步启动预康复工作,整合临床营养、心理、康复以及药学等多学科力量共同参与。此外,要加强对患者及其家属的宣教工作,鼓励他们主动参与预康复及全程管理。(证据质量等级:高;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
1.NAT 的实施:胃癌 NAT 的围手术期全程化管理应当贯穿诊断、 NAT 、术前评估、手术以及术后康复等各个阶段。建议在治疗的关键节点(例如 NAT 前后)采用多学科团队( multidisciplinary team , MDT )诊疗模式,动态调整治疗与康复策略 [48] 。 MDT 至少涵盖胃肠外科、肿瘤科、影像科、病理科、临床营养科、心理科以及康复科的医生。 NAT 方案需依据影像、分期、病理类型以及患者的具体情况共同制定,治疗期间要根据疗效和不良反应进行动态调整。
2. 预康复:预康复团队需包含临床营养科、康复科和心理科医师,结合营养、体能、心理状态及治疗不良反应制定个体化方案。多项研究及荟萃分析显示,术前预康复可缩短虚弱患者住院时间、减少严重并发症,建议纳入常规围手术期管理 [49-51] 。 Sun 等 [52] 的多中心 RCT 研究发现,对于虚弱的老年胃癌患者,术前接受为期 2 周的家庭监督式多模式预康复,可改善其术前功能能力,并有效减少术后并发症的发生。对于有高血压、糖尿病或冠心病等合并症患者,需相关专科医师参与调整用药,评估风险。临床药师需全程参与用药指导及不良反应管理 [53] 。患者及家属应积极参与预康复全过程,配合完成营养记录、运动监督及心理疏导。
3.NAT 与预康复的实施: NAT 的核心目标是为根治性手术创造最佳条件,但治疗可能导致脏器功能下降及营养受损。因此,预康复应与 NAT 同步启动,实现 “治疗开始即康复开始”,尽可能降低术前治疗对患者的打击。
热点问题 7 :如何为接受 NAT 的胃癌患者制定个体化预康复方案?
推荐意见:接受 NAT 的胃癌患者预康复需以 “多学科评估 - 个体化干预 - 动态监测 ”为核心,在 MDT 支持下,针对营养、功能和心理三维度制定方案,预康复同步 NAT 启动实施,以降低治疗相关损伤,优化术后恢复。(证据质量等级:高;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
1. 预康复实施的责任分工:先通过客观量表及各项检查检验,全面评估胃癌患者的营养状态、功能能力及重要器官功能,在确定 NAT 方案后,即刻启动 MDT ,完成预康复方案的制定。由胃肠外科医师统筹整体规划,肿瘤科医师负责治疗与康复的协同推进,临床营养师专责营养状态管理,康复科医师指导功能锻炼,心理科医师开展心理状态干预,护理团队则承担全程执行与监督工作。
2. 预康复方案的制定:预康复方案严格遵循多模式实施原则,包含四大核心内容:( 1 )营养优化:对 NRS2002 评分 ≥3 分的高风险患者,实施营养治疗,能量目标优先经间接测热法测量,或按 104.6~125.5 kJ · kg -1 · d -1 ( 25~30 kcal · kg -1 · d -1 )计算,蛋白质为 1.2~1.5 g · kg -1 · d -1 ,必要时予口服营养补充或空肠营养管肠内营养 [54-55] 。( 2 )功能锻炼:推荐术前完成至少 2~4 周中等强度有氧运动与抗阻训练,提升运动耐力;老年、虚弱等特殊患者由家属严密监护,从低强度有氧运动逐步进阶 [56-59] 。( 3 )心理干预:通过虚拟现实技术( virtual reality , VR )或音乐疗法,缓解患者焦虑抑郁情绪,推行家庭监督式预康复,结合智能手机 APP 实现远程监测与指导 [60-62] 。( 4 )合并症管理:严控糖尿病患者空腹血糖 <8 mmol/L 、高血压患者血压 <140/90 mmHg ,优化冠心病患者术前心肌供血,避免运动诱发心血管不良事件 [63-64] 。
热点问题 8 : NAT 期间如何进行营养状态动态监测与干预?
推荐意见:使用 NRS2002 进行 NAT 前营养风险筛查,定期评估患者身体成分变化。对高风险患者( NRS≥3 分)实施阶梯式营养干预。中高风险患者推荐使用免疫营养制剂。(证据质量等级:中;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
一项 RCT 研究显示,新辅助化疗期间,超过半数患者出现肌肉与脂肪组织丢失;其中皮下脂肪丢失 >12.5% 、内脏脂肪丢失 >15% 或肌肉指数丢失 >4.7% 与无进展生存期( progression - free survival , PFS )和总生存期( overall survival , OS )显著相关( P <0.005 ), NAT 期间,应每 2~4 周行综合营养评估(含常规指标与影像学身体成分分析) [65] 。一项 Meta 分析证实,低预后营养指南( prognostic nutritional index , PNI )与较差的 OS 显著相关( HR=1.344 ),且 PNI 联合 NRS 2002 可提升并发症预测准确性[曲线下面积( area under the curve , AUC ) =0.657 ] [66] 。通过 CT 在第三腰椎层面动态评估身体成分变化,可为预后预测及个体化营养干预提供关键依据。
前瞻性 RCT 研究显示,高蛋白口服营养补充( oral nutritional supplements , ONS )组患者 8 周后微型营养评估( mini nutritional assessment , MNA )评分显著改善( P <0.001 ),营养不良风险降至 4.3% ,对照组为 17.4% ( P =0.003 ),且能量和蛋白质摄入 ONS 组显著高于对照组( P <0.05 );特别是营养不良患者,术前使用含精氨酸、 ω - 3 脂肪酸和核苷酸等免疫营养剂,可有效降低术后感染性并发症发生率( OR : 0.49~0.52 )并缩短住院时间 [67] 。荟萃分析表明,其效果在与常规饮食对比时最为显著,且具有成本效益,目前证据支持优先术前应用,建议对肿瘤患者实施分层营养监测 [68] 。基础监测(每次治疗前)包括 NRS 2002 评分、体质量变化及体力状态评估,建议进行 CT 身体成分分析[第 3 腰椎层面的骨骼肌指数( skeletal muscle index , SMI )和脂肪面积]。干预启动标准为: NRS2002≥3 分、体质量下降 >5% 、 CT 显示机体成分显著丢失或经口摄入不足( <60% 需求 >5 d )。所有患者应先接受膳食指导与症状管理,若无效,则序贯启用 ONS 及肠内营养( enteral nutrition , EN ) [69] 。
热点问题 9 :如何评估与改善患者的心理状态及认知功能?
推荐意见: 在 NAT前、治疗期间及围手术期,对患者进行心理状态动态评估。对存在心理困扰的患者,强烈推荐实施结构化心理干预项目,包括认知行为治疗 (失眠一线疗法: cognitive behavioral therapy for insomnia , CBT-I )联合叙事疗法 / 韧性训练,并整合营养支持治疗。(证据质量等级:高;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
胃癌患者围手术期心理负担显著。一项针对 403 例术后幸存者的研究,识别出 3 种创伤后成长轨迹,决策树模型提示焦虑、应对方式和心理弹性是其关键预测因子 [70] 。推荐使用医院焦虑抑郁量表( Hospital Anxiety and Depression Scale , HADS )、匹兹堡睡眠质量指数( Pittsburgh Sleep Quality Index , PSQI )、心理弹性量表(康纳 - 戴维森量表, Connor - Davidson Resilience Scale , CD - RISC )及 EORTC QLQ - C30 等工具常规评估情绪、睡眠、心理弹性和生活质量 [71-73] 。针对认知功能,建议对老年患者进行术前基线评估,术后常规监测谵妄,并关注长期认知变化。干预上推荐整合心理治疗与精神药理学,认知行为疗法( Cognitive Behavioral Therapy , CBT )是核心方法。一项包括 310 例患者的 RCT 证实,为期 12 周的结构化行为干预(含叙事疗法与 CBT - I )可有效改善患者情绪、睡眠与生活质量 [72] 。
热点问题 10 :术前是否需要以及如何实施器官功能储备评估?
推荐意见: NAT后,胃癌患者术前应常规实施心肺功能评估(推荐6WMT及心肺运动试验(cardiopulmonary exercise test,CPET),AT<11 ml·kg -1 ·min -1 提示高危)。(证据质量等级:中;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
手术安全的核心环节在于充分而精确的术前评估。除常规检查外,推荐使用 CPET 或 6MWT 等客观工具来量化患者的心肺功能储备。峰值摄氧量( peak oxygen uptake , VO2 peak )和无氧阈值( anaerobic yhreshold , AT )是预测围手术期结局的可靠指标。
一项纳入 200 例患者的前瞻性研究显示, AT<9.5 ml · kg -1 · min -1 是预测重大心血管并发症最敏感的指标(敏感度 93% ,特异度 68% ),而 AT<11 ml · kg -1 · min -1 则与任何心血管并发症显著相关( OR=6.33 ) [74] 。对于接受 NAT 的患者,治疗本身可能导致心肺功能显著下降(如氧摄取量在 AT 时平均降低 1.25 ml · kg -1 · min -1 ,峰值降低 3.02 ml · kg -1 · min -1 ),其基线功能与 1 年死亡率独立相关( HR=0.72 ) [75] 。在一般人群中,心肺功能与健康结局存在剂量 - 反应效应,即便是低强度活动带来的小幅改善,也与心血管事件减少相关 [76] 。此外,最大摄氧量水平低,是术后发生呼吸衰竭的危险因素 [77] ;而较高的摄氧量与更好的术后结局密切相关 [78] 。
热点问题 11 : NAT 后手术时机应如何选择?
推荐意见: NAT 后手术时机通常为 4~6 周。(证据质量等级:高;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
MAGIC 和 RESOLVE 研究于新辅助化疗后 3~6 周实施手术 [10,79] ; FLOT4 研究为新辅助化疗后 4 周手术 [80] 。关于新辅助免疫治疗至手术时间的间隔, KERNOTE - 585 研究为 3~6 周 [12] ; MATTERHORN 研究为 4~8 周 [11] 。因此建议,最佳手术时机为 NAT 完成后 4~6 周,具体应由 MDT 评估患者具体情况后个体化决策,如肿瘤治疗反应、营养状态、功能能力、重要器官功能和药物不良反应等;如出现相关手术禁忌,应积极进行干预,保证手术最佳时间窗口;必要时可适当延长,以保证手术安全及术后恢复,但尽量不超过 6 周 [81-82] 。
热点问题 12 : NAT 导致的组织水肿与纤维化对手术技术有何具体挑战?术中应如何应对?
推荐意见: NAT 后组织水肿与纤维化会显著增加手术难度,不仅易导致副损伤,还会增加发生吻合口漏的风险。建议术前充分拟订预案,术中在高清或 3D 腹腔镜或机器人辅助下精细操作,采用锐钝结合的轻柔分离技术,并依据组织条件,选择合适的器械与吻合方式。若分离极端困难,应及时终止手术。(证据质量等级:低;推荐强度:弱推荐;专家组赞同率: 100% )
推荐说明
1.NAT 对组织的影响: NAT 后的组织水肿,可导致解剖层次模糊,标志难辨,延长手术时间并增加出血风险。而 NAT 后的组织纤维化会引起组织粘连,使得淋巴结清扫困难,并可能导致清扫不彻底;同时,会使组织愈合能力下降,增加术后吻合口漏或感染等并发症风险 [83-85] 。
2.NAT 后的手术对策:针对 NAT 后的组织水肿与纤维化这些手术操作难点,推荐高清或 3D 腹腔镜、或机器人辅助手术,建议采取以下策略:( 1 )手术从正常组织区域开始,向病变区域推进,以明确解剖平面;( 2 )在解剖不清时,避免盲目使用能量器械,以防误入错误间隙;( 3 )术中应仔细辨认并充分凝闭血管及淋巴管样结构,预防术后出血或淋巴漏;( 4 )可辅助使用吲哚菁绿荧光成像来帮助识别淋巴结边界,但其效果在淋巴管癌栓患者中可能受限 [85] 。此外,术中适时使用吸引器协助显露和清理,以及加强术者与助手间的默契协作与张力控制,对于应对此类复杂情况也至关重要 [86] 。
热点问题 13 :如何优化 NAT 患者的麻醉管理?
推荐意见:推荐术前 2~4 周完成麻醉门诊评估,应侧重 NAT 相关的心、肺、肾等毒性反应及器官功能储备,建议通过 CPET 等进行客观量化。推荐采用全身麻醉联合区域阻滞的多模式麻醉方案策略,并实施目标导向液体治疗与肺保护性通气策略,以优化围手术期管理,保障患者安全并促进术后康复。(证据质量等级:低;推荐强度:弱推荐;专家组赞同率: 100% )
推荐说明
1. 麻醉前评估:系统性的麻醉前评估与管理,是降低围手术期风险、保障手术安全与促进术后康复的关键环节。麻醉评估的核心内容应在 NAT 全部结束后、择期手术前完成。首先,需全面回顾治疗史,明确具体的化疗、靶向或免疫治疗方案以及末次治疗时间,并详细评估治疗相关不良反应,特别需要关注心脏毒性(如心功能下降、心律失常)、肺毒性(如间质性肺炎)、肾损伤、骨髓抑制及外周神经病变等 [87] ;其次,必须对器官功能与储备进行客观评估,推荐通过 CPET 或无创心功能检查量化心肺储备 [88] ;同时,常规评估肝肾功能、凝血状态及营养指标;最后,完成常规的气道与一般状况评估。建议在术前 2~4 周完成。
若患者在治疗期间已出现显著的心、肺或其他系统毒性,则应提前启动麻醉前评估,以便有足够时间(建议至少 2~4 周)进行多学科会诊与器官功能优化,例如纠正贫血、改善营养状态或调整心功能治疗方案。
2. 麻醉管理:在麻醉管理策略上,应采取个体化方案。麻醉方式以全身麻醉为基础,若凝血功能及神经学状况允许,可联合区域阻滞技术(如胸段硬膜外阻滞或腹横肌平面阻滞),以实现多模式镇痛并减少阿片类药物用量 [89] 。术中管理需精细化,推荐采用目标导向液体治疗策略以维持血流动力学稳定,实施肺保护性通气策略,并严格维持正常体温。同时,需警惕麻醉药物与既往抗肿瘤药物之间潜在的相互作用。术后管理则强调延续多模式镇痛,加强监测以发现可能迟发的免疫相关性等不良反应,并与外科、临床营养科紧密协作,共同推动 ERAS 路径的实施。
热点问题 14 : NAT 后腹腔镜或机器人微创手术的应用价值与注意事项?
推荐意见:对于经验丰富的胃外科中心,可积极开展 NAT 后腹腔镜或机器人微创手术,以提高手术质量及患者安全性,应积极审视 “及时中转”的原则。(证据质量等级:低;推荐强度:弱推荐;专家组赞同率: 97.56% )
推荐说明
对于经验丰富的医疗中心,在 NAT 后开展腹腔镜或机器人辅助胃癌根治术是安全可行的,并符合 ERAS 的理念。微创手术的视野放大和操作精准性,有助于应对治疗后的组织水肿、粘连和纤维化等挑战,不应被视为 “禁忌证”。建议在具备成熟经验的中心积极开展此类手术,并系统收集临床数据,同时推进多中心、前瞻性随机对照研究,以提升循证医学证据级别。
手术应由已度过学习曲线的高年资医师执行。术前可借助影像学(如 CT 三维重建)评估组织纤维化与血管走行。术中如遇严重纤维化、解剖层次不清或出血控制困难,应及时中转开腹。在操作中,应预判组织质地的变化,贯彻 “锐性解剖、层次优先”原则,尤其注意幽门下、脾门和胰腺上缘等高危区域的精细处理,避免盲目操作。当前,人工智能在术中实时识别关键解剖结构与血管方面展现出潜力,有助于减少副损伤、提高手术安全性。未来,结合智能辅助技术与规范的手术策略,有望进一步提升 NAT 后胃癌微创手术的安全性与疗效。
热点 问题 15:NAT后消化道重建方式的选择有无特殊性?
推荐意见: 消化道重建方式的选择,需在考虑肿瘤位置与切除范围基础上,重点关注组织条件,以确保吻合口无张力和血供良好。建议对吻合口进行加固处理,以降低相关并发症风险。(证据质量等级:低;推荐强度:强推荐;专家组赞同率: 100%)
推荐说明
1. 胃癌 NAT 后组织发生的 “损伤 - 炎性改变 - 纤维化 ”级联反应:化疗导致肿瘤坏死,释放高迁移率族蛋白 B1 ( high mobility group box 1 , HMGB1 )等损伤相关分子模式( damage - associated molecular pattern , DAMP ),经 Toll 样受体 4/ 核因子 κB 信号通路( TLR4/NF - κB signaling pathway , TLR4/NF - κB )激活巨噬细胞,分泌肿瘤坏死因子 - α ( tumor necrosis factor - α , TNF - α )和白介素 - 1β ( interleukin - 1β , IL - 1β ),破坏血管内皮连接,引起血浆外渗和组织水肿 [90] 。同时,转化生长因子 - β1 ( transforming growth factor - β1 , TGF - β1 )、血小板衍生生长因子( platelet - derived growth factor , PDGF )等因子通过 Smad 等信号通路激活肌成纤维细胞,促进胶原和 α - 平滑肌肌动蛋白( α - smooth muscle actin , α - SMA )高表达,导致细胞外基质沉积、组织增厚、层次消失及血管脆性增加 [91] 。
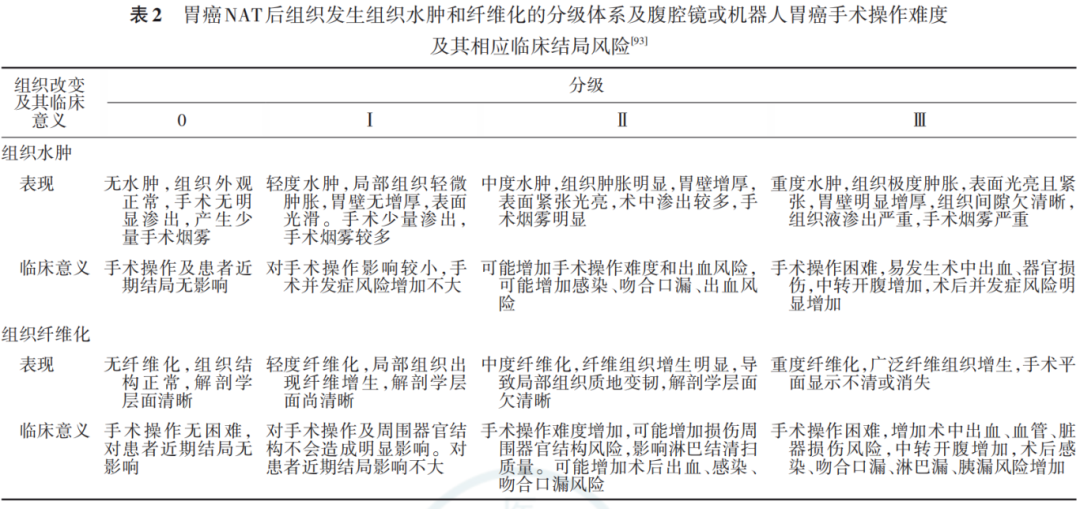
2. 术中吻合方式的选择:应根据组织水肿和纤维化程度,灵活选择适宜的吻合方式,并力求操作简化,以降低吻合相关并发症风险。术中可使用吲哚菁绿( indocyanine green , ICG )荧光显像技术辅助评估吻合口血供情况 [92] 。对于十二指肠残端、胃肠吻合口等关键部位,建议酌情进行浆肌层加固或包埋处理。表 2 显示了不同级别的组织水肿与纤维化,对应不同的手术操作难度,并提示相应的临床结局风险,应作为术式选择和操作决策的重要参考依据。
热点问题 16 :如何优化 NAT 后胃癌患者的术后镇痛策略?
推荐意见:采用以非甾体抗炎药( non- steroidal anti-inflammatory drug,NSAID)和对乙酰氨基酚为基础、联合区域阻滞麻醉或筋膜平面阻滞的多模式镇痛方案,最大限度地减少阿片类药物应用。(证据质量等级:中;推荐强度:强推荐;专家组赞同率:100%)
推荐说明
术后应实施以 NSAID 和对乙酰氨基酚为基础、联合区域阻滞或筋膜平面阻滞的多模式镇痛方案,以最大限度减少阿片类药物使用 [94-95] 。需警惕新辅助化疗药物(如奥沙利铂)相关神经毒性可能与术后神经病理性疼痛叠加,必要时可使用加巴喷丁、普瑞巴林或度洛西汀等药物进行干预 [96] 。
有效镇痛,是 ERAS 的核心环节。其不仅有助于患者早期下床活动、缓解紧张焦虑,还能降低心血管并发症风险,并促进正常呼吸与咳嗽,从而减少肺不张及肺部感染的发生。同时,减少阿片类药物的使用,有利于胃肠功能恢复与早期经口进食 [97-100] 。研究显示,在腹腔镜胃癌根治术的老年患者中,硬膜外麻醉与镇痛可能带来更好的止痛效果、更快的胃肠动力恢复以及更短的住院时间 [101] 。
热点问题 17 : NAT 后患者术后早期进食的安全性与实施路径?
推荐意见:在无吻合口漏高风险因素(如吻合张力高、血运欠佳和术前梗阻)、术中评估吻合确切的情况下,建议术后 24 h 内开始经口清流质饮食,并在 2~3 d 内过渡至半流质饮食。(证据质量等级:中;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
手术后应尽早恢复经口饮水与进食(清流质)。早期摄入营养,有助于促进肠道运动、维护黏膜屏障、减少菌群易位,并可降低感染风险和缩短住院时间。研究证实,术后第 1 天进食,不会增加并发症或死亡的风险,反而有利于肠道功能恢复 [102] 。 Meta 分析显示,胃手术后早期进食,同样具有缩短住院时间的优势 [103] 。对于接受新辅助放疗、组织愈合可能延迟的患者,可酌情调整进食进度,但不宜晚于术后 48 h 。若进食期间出现恶心、呕吐,应积极予以止吐处理,而非停止进食。回顾性研究亦表明, NAT 胃癌患者围手术期实施 ERAS 路径(含早期进食)能促进胃肠功能恢复,且不增加吻合口漏等并发症风险 [6] 。
热点问题 18 :如何制定针对性的术后早期活动方案并保障其落实?
推荐意见:推荐采用四阶段渐进式早期活动方案,督促患者术后早期活动。(证据质量等级:强;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
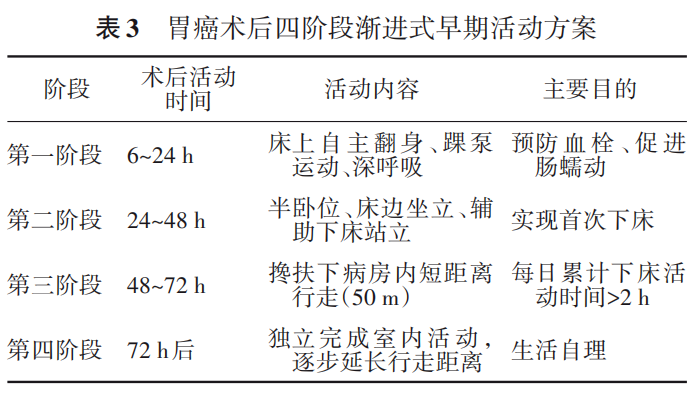
术后早期活动可以预防下肢静脉血栓,预防肺部感染,促进胃肠功能恢复,激活心肺功能,提供情绪激励 [104-107] 。推荐采用四阶段渐进式早期活动方案(表 3 ),并由专职护士监督执行。术后早期活动应严格防滑防摔,建议患者穿平底防滑鞋(袜),在病区走廊内配备扶手,需要搀扶的患者由陪护搀扶;在离床运动时要注意输液、引流等管路的管理,防止脱管。
热点问题 19 :术后如何继续进行营养支持与监测?
推荐意见:术后应尽早启动 EN 或肠外营养( parenteral nutrition , PN )支持治疗,根据能量与蛋白质需要,并动态调整。通过监测体质量、胃肠功能、伤口愈合等临床指标及血清蛋白和生化等实验室数据,全面进行营养状态的评估。需定期再评估营养风险,并通过 MDT 持续优化营养方案,以促进患者康复。(证据质量等级:中;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
1. 术后的营养管理:应继续遵循 ERAS 的营养管理路径,力争在术后 24 h 内恢复经口清流质饮食或启动 EN [108] 。对于术前已存在营养不良(如 NRS2002 评分 ≥3 分),或术后 1 周经口摄入量仍低于目标能量需要量 60% 的患者,应首先提供个体化的膳食指导及症状管理(如控制恶心、呕吐等),必要时启动规范的营养支持治疗 [109] 。
2. 营养支持应遵循阶梯原则:首选 ONS ,若经口摄入不足,则考虑管饲 EN ;当 EN 不能满足需求或出现不耐受时,应及时启用 PN [110] 。术后营养支持需特别重视蛋白质的足量供给。蛋白质摄入不足将导致瘦体质量丢失,进而延缓功能恢复、降低生活质量,并增加术后衰弱及并发症风险 [111] 。因此,营养方案应以维持、甚至提高骨骼肌质量为重要目标。
3. 出院前后的营养管理:应对患者在出院前进行系统的营养再评估,并制定个体化的家庭营养计划。胃术后早期饮食宜遵循少食多餐、细嚼慢咽、均衡搭配的原则;若经口饮食长期无法达标,应鼓励患者持续使用 ONS 。建议建立结构化随访机制,例如术后初期每 2~4 周通过门诊或远程方式进行营养指标监测与指导;病情稳定后,可每 3~6 个月进行一次全面的营养状况再评估,以确保康复效果的持续性 [110] 。
热点问题 20 : NAT 的不良反应可能在术后持续存在,需密切监测。
推荐意见: NAT 的不良反应具有延迟性,可影响血液、消化、心血管及免疫等多系统。术后需警惕其延后效应,通过监测相关实验室指标与临床症状,并结合 MDT ,实现早期识别与处理,以保障患者康复安全。(证据质量等级:中;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
多项临床研究提示, NAT 的相关不良反应持续时间可能较长 [112] ;且手术应激可能加重如中性粒细胞减少等不良事件 [113] 。术后应常规监测血常规至出院后 1~2 周,警惕化疗相关骨髓抑制及继发感染。对 Ⅲ 度及以上骨髓抑制(绝对中性粒细胞计数 <1.0×10 9 /L ),应及时给予粒细胞集落刺激因子( granulocyte colony - stimulating factor , G - CSF )治疗并调整抗感染方案,同时注意肝肾功能监测,避免应用肝肾毒性药物。
随着免疫治疗(如 KEYNOTE - 585 和 MATTERHORN 等研究)在 NAT 中的广泛应用,需高度重视免疫相关性毒性(如甲状腺炎、心肌炎、肺炎)的迟发与持续管理。除术前评估外,术后应至少每 3 个月复查甲状腺功能、心脏彩超及肺部 CT ;若出现相关症状,应及时增加检查频率,以实现早期干预、避免严重后果 [11-12, 114-116] 。
热点问题 21 : NAT 联合 ERAS 模式下,出院标准应如何界定?
推荐意见: NAT 联合 ERAS 模式下的出院标准需从多维度综合考量,确保患者出院时的身体功能、营养状态和心理认知等各方面均达到满足院外康复的基本要求,同时排除严重并发症风险,并具备良好的家庭护理条件,以实现安全、有效的康复过渡。(证据质量等级:中;推荐强度:强推荐;专家组赞同率: 100% )
推荐说明
出院决策应基于整体康复状态判断,不宜将 “肛门排气”等作为唯一标准,以避免不必要的住院时间延长。出院应满足以下核心条件:( 1 )生命体征平稳;( 2 )可耐受经口进食或 EN 制剂;( 3 )疼痛控制良好,视觉模拟评分法( visual analogue scale , VAS ) <3 分、且仅需口服镇痛药维持;( 4 )伤口愈合佳,无感染;( 5 )活动能力恢复至术前水平;( 6 )患者与家属掌握居家护理要点。
出院前,建议完善血常规和肝肾功能等检查,评估有无感染、低蛋白及肝肾功能异常;必要时可行上消化道造影评估吻合口。此外,需关注心理状态,采用抑郁自评量表 “患者健康问卷 - 9 项 ”( patient health questionnaire - 9 , PHQ - 9 )及广泛性焦虑障碍 7 项量表( generalized anxiety disorder - 7 , GAD - 7 )进行评估 [117-118] 。随着可穿戴设备与人工智能应用的发展,也可借助相关技术动态监测患者的血压、血糖和活动量等指标,为出院评估提供客观依据,实现更安全和更个性化的康复过渡。
总结与展望 本共识系统梳理了 NAT 后胃癌患者围手术期 ERAS 管理的 21 个热点问题,核心观点在于,对于接受 NAT 的胃癌患者,围手术期管理必须认识到其病理生理变化的特殊性,并采取多学科、个体化、全程化的 ERAS 策略。目前,关于免疫治疗与 ERAS 的交互影响以及预康复最佳模式等领域仍需更多高质量研究。未来,随着精准医疗和数字疗法的深入应用,胃癌围手术期管理将迈向更精准、更高效的新阶段。
《胃癌患者新辅助治疗围手术期加速康复外科管理热点问题专家共识( 2026 版)》编审组成员名单
专家组组长: 陈凛(北京大学国际医院)、梁寒(天津医科大学肿瘤医院)、所剑(吉林大学第一医院)、徐泽宽(江苏省人民医院)、余佩武(陆军军医大学西南医院)、周岩冰(青岛大学附属医院)
专家组成员 (按姓氏拼音排序) : 陈凛(北京大学国际医院)、丁印鲁(山东大学第二医院)、董千铜(温州医科大学附属第一医院)、冯旭(浙江大学医学院附属邵逸夫医院)、高翔宇(北京大学肿瘤医院)、葛思堂(蚌埠医学院第一附属医院)、郭洪海(河北医科大学第四医院)、郭云童(山西医科大学第一医院)、韩方海(广东省第二人民医院)、蒿汉坤(复旦大学附属华山医院)、贺娟(青岛大学附属医院)、狐鸣(甘肃省人民医院)、黄昌明(福建医科大学附属协和医院)、贾宝庆(解放军总医院)、江志伟(江苏省中医院)、靖昌庆(山东第一医科大学附属省立医院)、孔令信(青岛大学附属医院)、李乐平(山东第一医科大学附属省立医院)、李涛(新疆维吾尔自治区人民医院)、李政焰(陆军军医大学西南医院)、梁寒(天津医科大学肿瘤医院)、林季(温州医科大学附属第一医院)、林建贤(福建医科大学附属协和医院)、刘淦(青岛大学附属医院)、刘光世(新疆维吾尔自治区人民医院)、刘瑞廷(陕西省人民医院)、陆俊(复旦大学附属肿瘤医院)、马云涛(甘肃省人民医院)、牟一平(浙江省人民医院)、牛兆建(青岛大学附属医院)、曲建军(潍坊市人民医院)、覃新干(广西医科大学附属第一医院)、任虎(中国医学科学院肿瘤医院)、任双义(大连医科大学附属第二医院)、沈晓菲(南京鼓楼医院)、石彦(陆军军医大学西南医院)、舒垠(新疆医科大学附属肿瘤医院)、宋武(中山大学附属第一医院)、所剑(吉林大学第一医院)、田锋(山东第一医科大学附属省立医院)、田园(河北医科大学第四医院)、田玉龙(青岛大学附属医院)、汪学非(复旦大学附属中山医院)、汪勇(浙江大学医学院附属邵逸夫医院)、王林俊(江苏省人民医院)、王权(吉林大学第一医院)、魏猛(山东大学齐鲁医院)、徐泽宽(江苏省人民医院)、薛飞(陕西省人民医院)、易波(重庆大学附属肿瘤医院)、于文滨(山东大学齐鲁医院)、余佩武(陆军军医大学西南医院)、张东峰(青岛大学)、张健(浙江大学医学院附属第一医院)、张珂诚(解放军总医院)、张文斌(新疆医科大学附属肿瘤医院)、张子臻(上海交通大学医学院附属仁济医院)、赵利鹏(青岛大学附属医院)、赵群(河北医科大学第四医院)、赵银泉(吉林大学第一医院)、周岩冰(青岛大学附属医院)、周宇石(北京大学人民医院)
执笔组成员: 田玉龙(青岛大学附属医院)、刘淦(青岛大学附属医院)、周宇石(北京大学人民医院)、沈晓菲(南京鼓楼医院)、张珂诚(解放军总医院)、任虎(中国医学科学院肿瘤医院)、狐鸣(甘肃省人民医院)、郭洪海(河北医科大学第四医院)、舒垠(新疆医科大学附属肿瘤医院) 、 张东峰(青岛大学)
秘书: 田玉龙(青岛大学附属医院)
利益冲突 所有参与本共识制定的专家均声明不存在利益冲突
滑动阅读参考文献
排版编辑:肿瘤资讯-as











 苏公网安备32059002004080号
苏公网安备32059002004080号


