免疫检查点抑制剂(ICB)彻底改变了肿瘤治疗格局,但免疫原发/继发性耐药与严重的免疫相关不良反应仍困扰临床,使得相当一部分患者无法从ICB治疗中持久获益。脾脏作为最大的次级淋巴器官,在肿瘤进展中成为免疫抑制性髓系细胞的主要储存库,其PD1/PDL1通路异常激活加剧局部免疫抑制。如何精准靶向脾脏免疫微环境,同时规避系统性毒性,成为突破ICB耐药的关键方向。
2026年2月,西湖大学与浙江大学团队在肿瘤学顶级期刊Nature Cancer上联合发表了一项具有里程碑意义的Ⅰ期临床研究(NCT06026605)。该研究在全球首次报告了针对晚期癌症患者进行的红细胞-抗PD-1抗体偶联物(αPD1-Ery)的临床数据。αPD1-Ery如同特洛伊木马,将PD-1抗体精准运送至人体最大的外周免疫器官——脾脏。在既往抗PD-1/PD-L1治疗耐药的晚期实体瘤患者中,该疗法不仅未发生任何>3级治疗相关不良反应,更取得了客观缓解率(ORR)42.9%、疾病控制率(DCR)78.6%的极佳疗效,有望为免疫耐药患者撕开一道破局的缺口。

为什么是红细胞?为什么靶向脾脏?
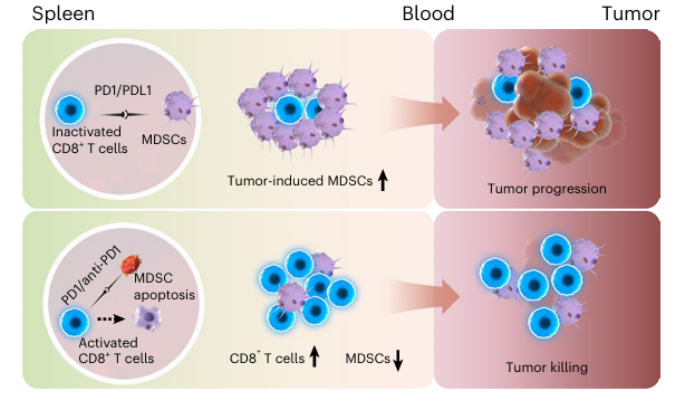
临床上,传统的抗PD-1抗体通过全身静脉给药,导致药物在全身广泛分布。这不仅引发了脱靶效应和潜在致命的免疫相关不良反应,且药物在脾脏等关键免疫器官内的滞留时间短、浓度低,难以充分激活外周免疫池。随着肿瘤进展,脾脏会发生髓外造血,成为髓源性抑制细胞(MDSC)的核心蓄水池。这些MDSC不仅抑制脾脏T细胞激活,还会源源不断地向肿瘤微环境(TME)中输送,促进肿瘤进展和免疫治疗耐药。
红细胞占脾脏细胞的70%以上,其独特的生物学特性(无细胞核、高生物相容性、大表面积体积比),使其成为理想的细胞药物递送载体。研究团队巧妙利用了抗PD-1抗体,通过化学交联剂共价偶联至自体红细胞膜蛋白上,构建了红细胞-抗PD-1抗体偶联物(αPD1-Ery),且这个过程几乎不损伤红细胞的结构与功能。
与游离抗体直接进入全身循环不同,αPD1-Ery完美利用了“红细胞在体内自然衰老或受损后,会被脾脏的单核吞噬系统清除”这一生理机制,实现了PD-1抗体在脾脏(人体最大的外周免疫器官)的特异性、高浓度富集。
临床前研究核心发现与机制
在多种对ICB耐药的同源小鼠模型(如KP肺癌、pB3乳腺癌)中,研究团队对αPD1-Ery的作用机制进行了严谨的表征:
· 重塑脾脏免疫景观:αPD1-Ery在脾脏的富集,有效诱导了效应T细胞的大量扩增。
· 清除抑制性细胞:αPD1-Ery大幅减少了脾脏内的免疫抑制性髓系细胞(特别是MDSC)。
· TME反向重编程:脾脏中被激活的免疫反应产生了系统性级联效应,成功重编程远端肿瘤的微环境,在传统抗PD1治疗耐药的肿瘤模型中展现出显著的抑制肿瘤生长作用。
I期临床试验数据:
“低剂量、高响应、安全性”
基于坚实的临床前数据,研究者开展了首次人体(First-in-Human)、开放标签、多中心的I期临床试验(NCT06026605),评估aPD1-hEry(人源版本)单药治疗在既往抗PD-1/PD-L1治疗耐药的晚期实体瘤患者中的安全性与初步疗效。试验共入组14例患者,病种横跨食管癌、直肠癌、胰腺癌、肝癌及广泛期小细胞肺癌等11个瘤种。患者被均分至两个剂量队列(2×10¹¹或3×10¹¹个偶联细胞/次)。
·安全性与耐受性(主要终点):无剂量限制性毒性(DLT),无3级及以上治疗相关不良事件(AE)。重复给药未导致严重免疫相关毒性,未诱发抗药抗体(ADA)生成或严重溶血反应。这表明通过红细胞靶向脾脏的策略大幅降低了传统抗体的全身脱靶毒性。
·疗效数据(次要终点):客观缓解率(ORR)达到42.9%(6/14),包含1例完全缓解(CR)和5例部分缓解(PR)。疾病控制率(DCR)高达78.6%(11/14)。中位无进展生存期(mPFS)为5.5个月;中位总生存期(mOS)尚未达到。
·典型获益病例:
(1)一例73岁纵隔淋巴结转移的食管癌(ESCA)患者(P3)在治疗后实现CR,影像学及活检均证实病灶消失,且停药后6个月仍维持CR;另一例ESCA伴肋骨转移患者PR持续超15个月。
(2)一例直肠癌(READ)肺转移患者与一例广泛期小细胞肺癌(ES-SCLC)患者,均实现了长达1年以上的PR。
·药效动力学特征(揭示疗效的底层逻辑):临床患者的外周血检测结果与临床前模型高度一致,接受αPD1-Ery治疗的患者(尤其是响应者),其外周血中的PMN-MDSC在首剂治疗72小时内即发生急剧下降(减少28%~70%),同时效应CD8+T细胞(CD45RA+CCR7-)快速且持续扩增。这一外周血细胞动态变化高度印证了脾脏靶向改造的成功。
研究创新:超越传统抗体的“降维打击”
1. 平台技术的革新:开创了利用红细胞作为载体,靶向脾脏免疫微环境的先河,为未来将其他免疫调节剂(如激动剂抗体、细胞因子)精准投递至脾脏提供了思路。
2. 作用机制的升维:不同于传统抗体直接在TME中发挥作用,aPD1-Ery是通过在“免疫总部”脾脏进行系统性的免疫重塑,从而间接地解决全身性的免疫抑制问题。
3. 克服耐药的新路径:证实了靶向MDSC是逆转ICB耐药的关键。aPD1-Ery通过激活脾脏T细胞杀伤MDSC,从而清除了全身最大的MDSC“储备库”,这是其区别于传统疗法的核心机制。
讨论与深思:对临床实践的启示
治疗靶场的战略转移:从“TME”到“脾脏”
以往试图直接“加热”局部冷肿瘤往往事倍功半。本研究证实,脾脏才是抑制性MDSC的“兵工厂”。αPD1-Ery通过精准打击脾脏,直接切断肿瘤免疫抑制的“补给线”,实现了从系统源头重塑局部微环境的降维打击。
极低剂量实现破局:打破ICB耐药与毒性的双重枷锁
传统的PD-1抗体单次剂量高达200mg,而αPD1-Ery每次输注的细胞数仅为2~3×10¹¹个,其携带的抗体总剂量仅为微乎其微的6-10 mg(常规剂量的1/20),即能在耐药人群中斩获42.9%的ORR,且零重度免疫相关不良事件(irAE)。这提示ICB耐药的本质可能并非“靶点失效”,而是“空间分布错误”,为未来联合用药(如双免、靶向、化疗)预留了极广阔的安全窗口。
外周血MDSC有望成为新的“疗效风向标”
研究首次在人体证实靶向脾脏激活可系统性清除耐药驱动因素MDSC。其在治疗后外周血中的快速下降,展现出作为早期、动态预测免疫疗效精准标志物的巨大潜力。
结语
从实验室的偶联技术,到小鼠模型的机制破译,再到Ⅰ期临床试验中的耐药期晚期癌症患者,αPD1-Ery展现出了作为下一代免疫疗法(Next-generation Immunotherapy)的非凡潜力。尽管目前的临床样本较小,但其巧妙的药物递送逻辑和优异的初步疗效,值得给予高度关注。期待更大规模的Ⅱ/Ⅲ期研究进一步证实其临床地位,为深陷耐药困境的晚期肿瘤患者带来新的破局之策。
Nie X, Liu Y, Yao X, et al. Erythrocyte–anti-PD1 conjugates in persons with advanced solid tumors resistant to anti-PD1/PDL1: preclinical characterization and results of a phase 1 trial. Nature Cancer. 2026. DOI: 10.1038/s43018-026-01125-2.
排版编辑:肿瘤资讯-ZJN











 苏公网安备32059002004080号
苏公网安备32059002004080号


