慢性淋巴细胞白血病(CLL)是一种常见的成人血液系统恶性肿瘤。近年来,随着靶向药物的广泛应用,CLL的治疗模式发生了深刻变革。Bruton酪氨酸激酶抑制剂(BTKi)和BCL2抑制剂(BCL2i)已成为一线治疗的核心药物。目前,临床实践中存在两种主要治疗策略:一是基于BTKi的持续治疗,直至疾病进展或出现不可耐受毒性;二是基于BCL2i联合CD20单抗或BTKi的有限期治疗。尽管这两种策略均已显示出显著的临床效益,但此前尚无前瞻性随机研究直接比较二者的疗效与安全性。近期,The New England Journal of Medicine 杂志发表了由德国CLL研究组牵头的CLL17 Ⅲ期随机临床试验结果,首次前瞻性比较了有限期维奈克拉联合方案与持续伊布替尼治疗初治CLL的疗效与安全性,为临床决策提供了高级别循证医学证据。本文将结合该研究核心结果,剖析其对CLL治疗实践的重要影响。

CLL17是一项国际多中心、研究者发起的Ⅲ期随机试验,旨在评估有限期治疗是否非劣效于伊布替尼持续治疗。研究共纳入909例初治CLL患者,随机分为三组:
维奈克拉 + 奥妥珠单抗(VO组):固定疗程治疗(共12个月);
维奈克拉 + 伊布替尼(VI组):固定疗程治疗(共12个月);
伊布替尼单药(I组):持续治疗直至疾病进展或毒性不可耐受;
研究主要终点为研究者评估的无进展生存期(PFS),非劣效界值为风险比1.608(对应3年PFS差异不超过8%)。次要终点包括微小残留病灶(MRD)状态、总缓解率(ORR)、总生存期(OS)及安全性。
疗效结果:有限期治疗非劣于持续治疗,缓解深度更优
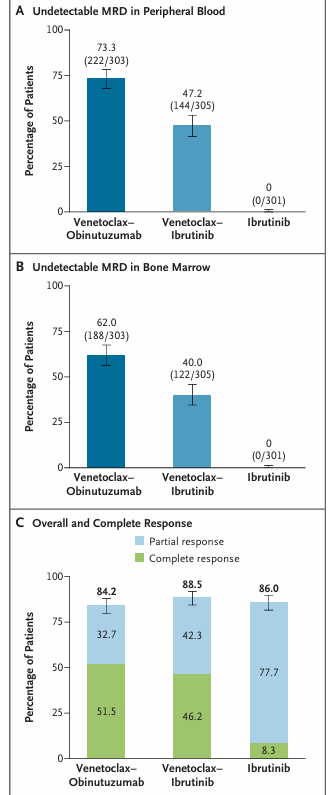
三组3年PFS率无显著差异,且两个有限期治疗组均达到非劣效性标准。维奈克拉 + 奥妥珠单抗组3年PFS率为81.1%(HR=0.87),维奈克拉 + 伊布替尼组为79.4%(HR=0.84),伊布替尼单药组为81.0%。
亚组分析显示,体能状态不佳患者中,维奈克拉 + 奥妥珠单抗组3年PFS率(79.6%)显著优于伊布替尼单药组(70.4%);IGHV未突变患者中,有限期治疗组与伊布替尼单药组PFS相当(75.8%~78.9% vs 79.7%);del(17p)/TP53 突变患者中,维奈克拉 + 伊布替尼组3年PFS率为69.0%,伊布替尼单药组为79.4%,因样本量较小未达统计学差异。
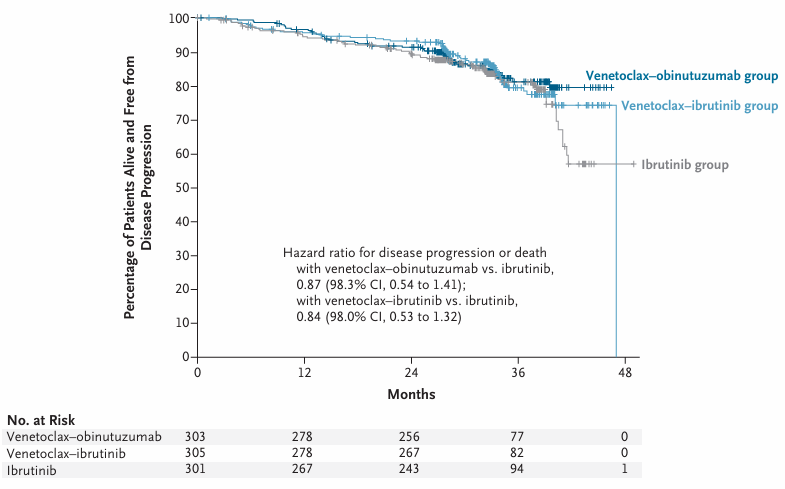
在MRD阴性率方面,有限期治疗组展现出显著优势,而伊布替尼单药组未出现MRD阴性患者。外周血MRD阴性率方面,维奈克拉 + 奥妥珠单抗组为73.3%,维奈克拉 + 伊布替尼组为47.2%;骨髓MRD阴性率分别为62.0%和40.0%,均显著高于伊布替尼单药组(0%)。
在缓解率方面,完全缓解(CR)率差异显著,维奈克拉 + 奥妥珠单抗组为51.5%,维奈克拉 + 伊布替尼组为46.2%,而伊布替尼单药组仅为8.3%;三组的ORR相近,分别为84.2%、88.5%和86.0%。
三组3年OS率均保持较高水平,维奈克拉 + 奥妥珠单抗组为91.5%,维奈克拉 + 伊布替尼组为96.0%,伊布替尼单药组为95.7%,组间无统计学差异。
安全性结果:不同方案毒性特征各异,风险可控
常见不良事件:三组主要不良反应均为感染、胃肠道疾病和血细胞减少,但发生率存在差异。严重感染(3级及以上)以维奈克拉 + 奥妥珠单抗组发生率最高(29.8%),致命感染12例,多与新冠病毒感染、肺炎相关;维奈克拉 + 伊布替尼组(22.1%)和伊布替尼单药组(21.1%)相对较低。
心脏相关不良事件:伊布替尼单药组风险最高,心脏疾病发生率为34.6%,其中房颤发生率为5.9/1000患者-月,高血压发生率为8.9/1000患者-月;维奈克拉 + 奥妥珠单抗组心脏事件发生率最低(13.9%),房颤发生率仅1.1/1000患者-月。
肿瘤溶解综合征(TLS):总体发生率低于5%,维奈克拉 + 奥妥珠单抗组共12例(3例临床病例,9例实验室确诊),多与奥妥珠单抗首次输注相关;维奈克拉 + 伊布替尼组4例,伊布替尼单药组1例,经标准预防措施(维奈克拉剂量递增、肿瘤减负荷)后均得到有效控制。
治疗中断率:伊布替尼单药组早期治疗中断率最高(33.2%),可能与长期用药的累积毒性相关;维奈克拉 + 奥妥珠单抗组为14.6%,维奈克拉 + 伊布替尼组为22.1%。
研究结论
CLL17研究的中期分析结果表明,对于初治CLL患者,为期12个月的固定疗程治疗(无论是维奈克拉 + 奥妥珠单抗还是维奈克拉 + 伊布替尼方案)在PFS方面非劣效于持续伊布替尼单药治疗。同时,固定疗程方案能够诱导更高比例的MRD阴性,并且为患者提供了明确的治疗结束点和无治疗间歇期,在改善长期生活质量、降低累积毒性及治疗成本方面具有潜在优势。该研究为临床实践提供了将固定疗程靶向联合治疗作为大多数初治CLL患者一线选择的高级别证据。
小编解读
CLL17试验作为首个直接对比CLL有限期靶向治疗与持续靶向治疗的Ⅲ期临床试验,其结果具有里程碑式的临床意义,为初治CLL患者的治疗策略选择提供了关键循证依据,同时也引发了对CLL个体化治疗的深入思考。
长期以来,BTKi持续治疗因显著改善CLL患者预后,成为初治患者的重要治疗选择,但持续用药带来的累积毒性、治疗负担及患者依从性问题一直困扰临床。CLL17试验证实,以BCL2i为基础的有限期联合治疗在PFS上非劣于伊布替尼持续治疗,且能实现更深层次的疾病缓解(更高MRD阴性率和CR率),这标志着有限期治疗已成为初治CLL患者的重要治疗选项。
MRD阴性作为CLL深度缓解的关键指标,与长期预后密切相关。CLL17试验中有限期治疗组高达40%~73%的MRD阴性率,意味着部分患者可能通过有限期治疗实现长期无治疗生存,这不仅降低了长期用药的毒性风险,还显著提升了患者的生活质量,为CLL“治愈导向”的治疗目标提供了新的可能。尤其对于体能状态不佳的患者,维奈克拉 + 奥妥珠单抗组展现出更优的PFS,提示有限期方案更适合合并基础疾病、耐受能力较弱的人群,这一结果对临床实践具有重要的指导价值。
值得关注的是,CLL17试验所验证的有限期治疗理念,在新一代BCL2抑制剂的研究中得到了进一步强化。新一代BCL2抑制剂索托克拉通过分子结构优化,对BCL2的结合力较第一代BCL2i高14倍,BCL-2/BCL-xL选择性提升6倍,脱靶效应更低,且半衰期仅约5小时,可显著减少药物蓄积风险。在2025年ASH年会上公布的研究数据显示,索托克拉联合泽布替尼的双药方案,在初治CLL患者中实现了100%的ORR,uMRD4率高达94%,且在高危人群中同样表现优异,这一结果进一步印证了有限期治疗在深度缓解方面的潜力,也为CLL治疗提供了更优的药物选择。
未来研究方向应聚焦于:一是探索MRD导向的个体化治疗策略,明确是否可根据MRD状态调整治疗周期或方案,进一步优化疗效与安全性,这一方向已在索托克拉的相关研究中得到初步探索并显示出良好前景;二是开展下一代BTKi与新一代BCL2i联合的有限期治疗研究,进一步降低不良反应风险,提升深度缓解率;三是针对del(17p)/TP53突变等高危人群,开发更有效的有限期治疗方案,改善其预后。目前,索托克拉的多项3期研究已在全球开展,包括头对头对比现有标准治疗方案的临床试验,有望为CLL治疗提供更高级别的循证医学证据。
总体而言,CLL17试验证实,以维奈克拉为基础的有限期联合治疗在初治CLL患者中疗效非劣于伊布替尼持续治疗,且具有更深的缓解深度和独特的毒性特征。这一结果丰富了CLL的治疗选择,推动了CLL个体化治疗的发展。而索托克拉等新一代靶向药物的出现,进一步优化了有限期治疗的疗效与安全性,为CLL患者带来了“深度缓解 + 精准停药”的新治疗范式。
Al-Sawaf O, Stumpf J, Zhang C, et al. Fixed-duration versus continuous treatment for chronic lymphocytic leukemia[J]. New England Journal of Medicine, 2025.
排版编辑:肿瘤资讯-Sally











 苏公网安备32059002004080号
苏公网安备32059002004080号


