在乳腺癌远处转移谱系中,骨转移始终占据极其重要的位置。它不仅是晚期乳腺癌最常见的转移部位之一,也往往意味着疾病进入长期管理、难以治愈的新阶段。近期,Cell Death Discovery发表的一篇综述,围绕循环肿瘤细胞(CTCs)在乳腺癌骨转移中的作用进行了较为系统的梳理。文章指出,CTCs并不只是转移过程中的“被动产物”或简单液体活检指标,而是深度参与骨转移发生、休眠、再激活与定植全过程的功能性参与者;与此同时,随着检测和分子表征技术不断进步,CTCs也正在成为乳腺癌骨转移风险评估、疗效监测和疾病演进追踪的重要候选工具。

骨转移为何始终是乳腺癌管理中的关键难题
在晚期乳腺癌患者中,约75%会发生骨转移,近70%的乳腺癌相关死亡与骨病灶有关。骨转移不仅可引发骨痛、病理性骨折、脊髓压迫及恶性高钙血症等骨相关事件,还会显著降低患者生活质量,并常常伴随系统治疗耐药增加。作者进一步指出,骨转移并不只是疾病进展的“终点”,还可能作为“次级土壤”,进一步促进更具侵袭性的肿瘤细胞继续播散。
也正因如此,单纯依赖影像学或症状变化来判断骨转移的发生和演进,往往是不够的。综述认为,现有治疗虽可通过内分泌治疗、化疗、HER2靶向、CDK4/6抑制剂以及骨靶向药物改善结局,但整体仍以控制和延缓为主,尚难真正逆转骨转移的生物学进程。这也为能够通过外周血动态捕捉肿瘤演变的CTCs,提供了明确的临床研究空间。
CTCs不只是“脱落细胞”,而是具有高度可塑性的转移种子
文章在生物学部分提出一个很重要的观点:CTCs之所以值得关注,不仅因为它们“能被检测到”,更因为它们本身代表了肿瘤最具迁移和适应能力的一部分细胞群。综述指出,CTCs可来源于原发灶或既有转移灶,进入外周血后可单个存在,也可形成细胞簇。与普通血细胞相比,CTCs通常体积更大,直径多在15–25 μm之间,且具有更高的运动性、变形性以及不同的膜电学特征,这些差异既与其转移能力有关,也构成了CTC富集与分离的重要技术基础。
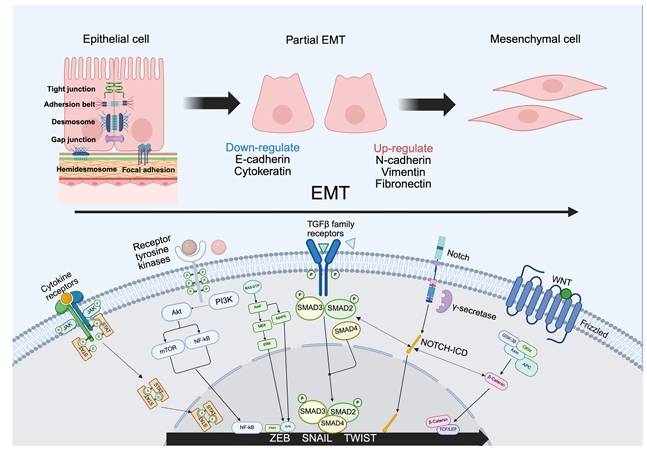
更关键的是,CTCs具有显著的表型可塑性。综述指出,乳腺癌来源CTCs可发生分子分型转换,并在治疗压力下出现受体表达改变。与此同时,上皮-间质转化(EMT)被认为是CTCs获得侵袭与迁移能力的重要机制。EMT并不是简单的“上皮变间质”二元转换,许多CTCs更可能处于上皮-间质混合状态,这类细胞往往更具干性、更易发生转移,也更容易逃逸传统依赖表面标志物的检测。
除单个CTCs外,CTC簇同样值得重视。CTC簇在抗剪切应力、黏附血管内皮以及远处定植方面均优于单个CTC,哪怕仅由2至3个细胞构成的小簇,也可能表现出显著更强的转移效率。其更高的转移潜能,与簇内细胞紧密连接以及其与血小板、成纤维细胞和免疫细胞的协同作用密切相关。
在机制层面,这篇综述对乳腺癌骨转移的形成过程做了较完整梳理。作者认为,CTC介导的骨转移并非随机事件,而是符合“种子与土壤”理论的多步骤动态过程。首先,CTCs之所以偏向骨组织,与CXCR4/CXCL12趋化轴密切相关。乳腺癌来源CTCs常高表达CXCR4,而骨微环境中的间充质基质细胞和周细胞则富集CXCL12,两者相互作用可为CTCs提供明确的骨髓归巢信号;骨组织本身的低氧状态还可通过HIF-1α进一步增强这一趋化过程。
进入骨髓后,CTCs首先需要完成血管外渗并在骨龛位“落脚”。文章指出,骨髓存在血管周围龛位和骨内膜龛位两类关键微环境。CTCs与血管内皮接触后,可借助整合素、GpIIb/IIIa及P-selectin等分子黏附并穿越血管壁,进入骨髓微环境,随后成为播散性肿瘤细胞(DTCs)。值得注意的是,这一过程的效率实际上非常低,最终只有约0.2%的CTCs能够成功在远处器官完成定植。其后,在CXCR4、骨连接素以及骨来源TGF-β1、CCL2等信号引导下,DTCs逐渐深入骨龛位,并依赖OPN、BSP、CD44、胶原I和VCAM-1等分子完成锚定。
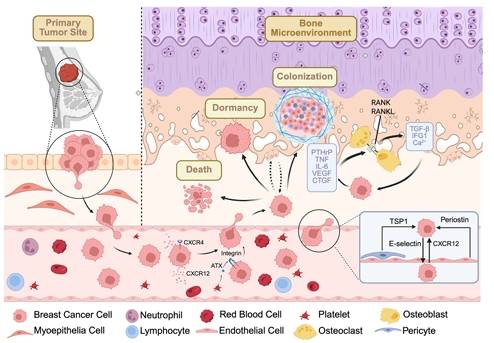
休眠与再激活:乳腺癌骨转移“晚发”的生物学解释
乳腺癌骨转移一个典型特点,是其可在原发灶治疗后多年甚至更久才被发现。综述指出,这与DTCs在骨髓中的长期休眠密切相关。进入骨髓后,DTCs可在成骨细胞富集的龛位中维持静息状态。文中提到,DTCs表面的E-cadherin与成骨细胞表面的N-cadherin可形成异源黏附连接,并通过mTOR通路介导肿瘤—龛位通信;此外,IL-6、BMP、Wnt、TGF-β以及内皮来源TSP-1等,也参与维持肿瘤细胞的长期静息。
但这种休眠并非永久稳定。文章指出,骨重塑与炎症状态可打破这一平衡。VCAM-1可招募α4β1阳性的破骨细胞前体,促使破骨细胞介导龛位重塑,从而削弱维持休眠的信号,推动DTCs重新进入增殖状态,最终形成微转移灶。换言之,休眠并不是“结束”,而更像是骨转移生物学中一个可被重新激活的潜伏阶段。
在骨转移进一步扩展阶段,综述重点提到经典的骨破坏“恶性循环”。乳腺癌细胞可通过旁分泌PTHrP诱导成骨细胞表达RANKL,后者与破骨细胞前体上的RANK结合后,促进破骨细胞分化及骨吸收。随着骨基质被降解,原本储存在骨中的TGF-β等因子被释放,又反过来刺激肿瘤细胞分泌更多PTHrP,形成自我强化的正反馈,最终导致持续性骨破坏和肿瘤扩增。除PTHrP–RANKL轴外,整合素、Notch和RON等通路也可能参与这一过程。
这也意味着,骨转移并不只是肿瘤在骨内“生长”这么简单,而是肿瘤细胞与骨微环境共同塑造出的一个持续放大的病理生态系统。
现有研究总体支持CTC监测在乳腺癌中的可行性及预后相关性,但针对骨转移这一特定场景,证据仍明显不足。多项临床试验曾尝试用CTC计数评估地舒单抗或唑来膦酸在骨转移患者中的治疗反应,但截至目前,多数研究尚无明确结局数据公布;同时,这些研究大多只关注CTC数量变化,而未深入分析CTC表型转变或CTC簇的生物学意义。作者明确指出,现有多数研究并非专为骨相关终点设计。
尽管如此,CTCs在骨转移监测中的潜力仍然清晰可见。综述指出,升高的CTC负荷与更高的转移风险相关,在部分研究中也与骨受累存在关联。以CellSearch系统为例,≥5个CTCs/7.5 mL血液这一阈值已被广泛用于风险分层,并在多项前瞻性研究中显示出一定预测价值。更值得关注的是,CTC水平的动态变化在某些情况下可能先于影像学进展出现,因此理论上具有提示隐匿性骨转移的潜力,但其敏感性和特异性仍需前瞻性验证。
此外,CTC表型本身也可能具有临床指导意义。高CXCR4表达提示更强骨髓归巢能力;BSP、OPN、RUNX2等“骨拟态”标志物有助于增强肿瘤细胞在骨微环境中的黏附、生存和耐药;而受体状态变化则可能提示治疗适应性改变,例如HR阳性CTCs失去激素受体表达常与内分泌治疗不良预后相关,HER2阴性患者出现HER2阳性CTCs则可能提示部分患者存在抗HER2治疗获益机会。
未来的关键,不只是“检测到”,而是“真正能指导决策”
在展望部分,作者强调,CTC研究下一阶段的核心,不应停留在提高检出率,而应推动其从研究工具走向真正可用的临床工具。文章提出,未来应在两类人群中系统开展骨特异性CTC动态研究:其一是接受辅助治疗的高危早期乳腺癌患者,用于识别隐匿性骨播散;其二是接受序贯影像和系统治疗的转移性乳腺癌患者,用于动态判断骨微环境中的治疗反应和疾病演进。若能将CTC分析与骨靶向影像、分子分型及多组学评估结合,才更有可能建立真正有临床意义的精准监测框架。
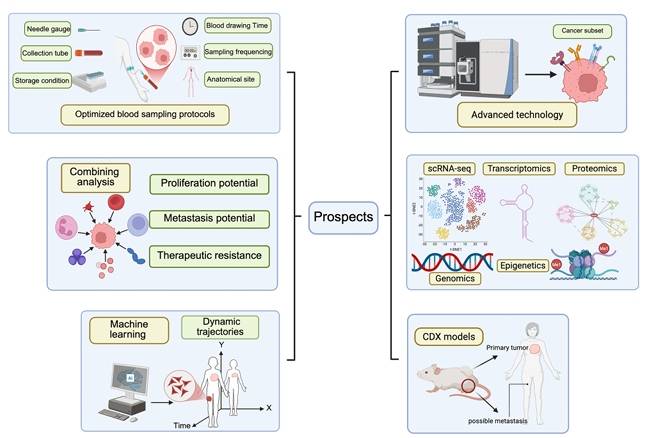
在技术层面,综述也总结了当前主要限制。CellSearch虽标准化程度高,但依赖EpCAM,难以充分捕获EMT样CTCs;而微流控和基于物理性质的富集方法虽可提高对异质性CTCs的捕获能力,却常面临成本高、复杂度高或标准化不足等问题。作者明确指出,目前并不存在一个适用于所有临床场景的“最优平台”,平台选择仍应服务于具体研究目的。
文章还提出,未来方向应包括:开发不依赖表面标志物的富集策略以减少漏检;优化采血时间、频率、采血部位及保存条件;引入机器学习和人工智能以减少判读差异;以及更精细地定义具有高度侵袭性和器官嗜性的CTC亚群。与此同时,单独分析CTCs仍无法完整代表患者全貌,将CTCs与其他循环细胞、蛋白标志物、炎症指标乃至多组学信息整合,可能才是更有前景的方向。
小结
整体来看,这篇综述的价值,并不在于给出某一个直接改变临床实践的新结论,而在于为乳腺癌骨转移中的CTC研究提供了一个相对完整的框架。它提醒我们,CTCs既是骨转移发生发展的参与者,也是观察疾病演进的重要窗口。它们通过归巢、休眠、再激活和定植等多个环节深度嵌入骨转移生物学,同时又因可通过外周血重复采样而具备动态监测优势。只是从“有研究价值”走向“可指导决策”,CTCs仍需要更高质量的前瞻性证据、更统一的检测标准,以及与影像和多维生物标志物的更深度整合。
Ma L, Wang Y, Qiu S, Shi M, Tang W, Hu H, Li C, Lu H, Wang X. Circulating tumor cells in breast cancer bone metastasis: mechanisms, clinical relevance, and future directions. Cell Death Discov. 2025 Dec 10;12(1):48. doi: 10.1038/s41420-025-02910-1. PMID: 41372129; PMCID: PMC12830773.
排版编辑:肿瘤资讯-Kelly











 苏公网安备32059002004080号
苏公网安备32059002004080号


