B细胞急性淋巴细胞白血病(B-ALL)是一种高度侵袭性的血液系统恶性肿瘤。异基因造血干细胞移植(allo-HSCT)是目前唯一可能治愈该疾病的核心手段,然而移植后复发仍是临床面临的重要挑战。此类患者预后较差,中位生存期不足6个月,5年生存率仅约10%,且目前缺乏标准化的有效治疗方案,临床需求亟待满足。
CD19 CAR-T细胞疗法的出现为复发/难治性(R/R)B-ALL带来了治疗变革,其在移植后复发患者中也显示出初步疗效。然而,自体与异基因来源的CD19 CAR-T细胞在长期疗效、安全性方面的比较,以及相关的预后影响因素,目前尚不明确。近期,浙江大学医学院附属第一医院黄河、胡永仙、魏国庆教授作为共同通讯作者,在Cytotherapy发表了一项多中心回顾性研究[1],系统探讨了自体与异基因CD19 CAR-T细胞疗法在allo-HSCT后复发B-ALL患者中的长期疗效与安全性,并明确了相关临床预后因素,为该类患者的临床治疗提供了重要的循证医学证据。【肿瘤资讯】特此整理研究核心内容,以飨读者。

研究设计:多中心回顾性研究探索CAR-T细胞疗法的长期价值
该研究为一项多中心回顾性研究,纳入2016年9月至2021年12月期间,来自国内4个中心的55例allo-HSCT后复发的CD19阳性B-ALL患者。所有患者均接受CD19 CAR-T细胞治疗。
研究的纳入标准包括allo-HSCT后复发的B-ALL患者,骨髓原始细胞比例≥5%,且白血病细胞CD19阳性;排除合并严重移植物抗宿主病(GVHD)、无法控制的感染、器官功能障碍等CAR-T细胞治疗禁忌证者。根据CAR-T细胞来源,患者分为自体CAR-T细胞组(7例)和异基因CAR-T细胞组(48例,主要为移植供者来源)。输注前,多数患者接受氟达拉滨联合环磷酰胺(FC)方案进行淋巴清除预处理,中位CAR-T细胞输注剂量为1.5×10⁶/kg。
研究主要评估完全缓解(CR)率、微小残留病(MRD)阴性率,长期生存终点包括总生存期(OS)、无白血病生存期(LFS)。同时分析累积复发率(CIR)、非复发死亡率(NRM)及安全性指标,包括细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)、急/慢性GVHD等,并探索影响患者生存及不良反应的临床危险因素。
基线特征:高危移植后复发B-ALL人群
研究纳入的55例患者中,男性29例(52.7%),女性26例(47.3%),中位年龄29岁(范围:4~66岁)。其中23.6%的患者携带复杂核型、IKZF1缺失、TP53突变等高危细胞遗传学/分子学异常。
移植类型以单倍体相合allo-HSCT为主(56.4%),同胞全合和无关全合分别占34.5%和9.1%;80.0%的患者在移植前达到骨髓CR,且所有患者移植后均曾实现CR。29.1%的患者在移植后6个月内出现早期复发,14.5%合并髓外复发,29.1%和18.2%的患者分别在移植后发生急性GVHD(aGVHD)和慢性GVHD(cGVHD)。
接受CAR-T细胞治疗前,患者骨髓原始细胞比例中位数为26.9%(范围:0~99.0%),从allo-HSCT到CAR-T细胞输注的中位间隔为10.5个月(范围:2.3~72.2个月),整体为临床预后较差的高危移植后复发B-ALL人群。
疗效结果:高缓解率带来长期生存获益,自体与异基因CAR-T细胞疗效相当
高缓解率实现疾病深度控制,移植前缓解状态影响CAR-T细胞疗效
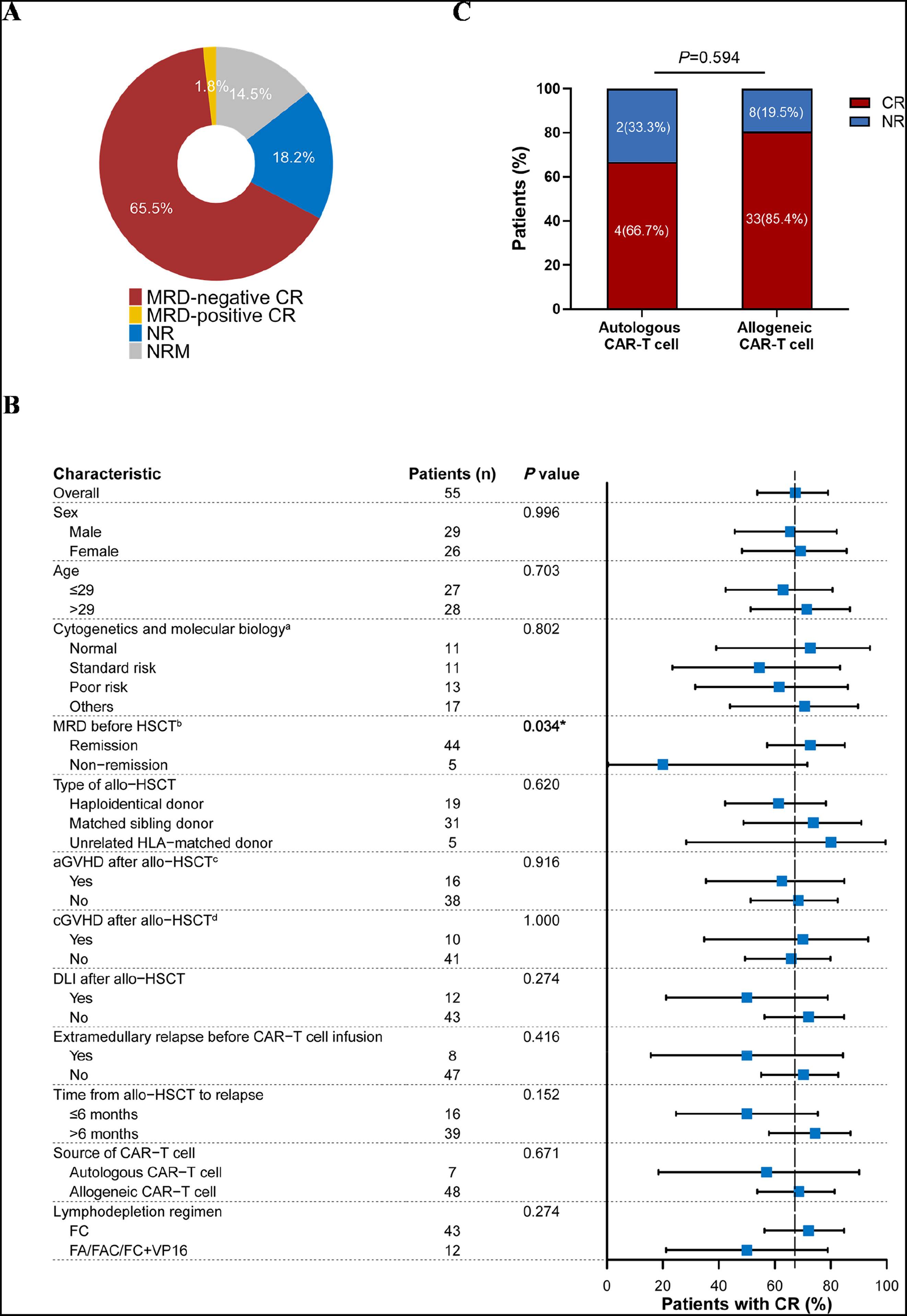
55例患者中,47例完成CAR-T细胞输注后28天疗效评估,最终37例(67.3%)达到CR,36例(65.5%)实现MRD阴性CR,显著优于传统强化疗和供者淋巴细胞输注(DLI)的缓解效果(图1 A)。仅10例(18.2%)患者未缓解(NR),其中1例接受二次CAR-T细胞治疗,9例未接受后续治疗,最终8例死于疾病进展,2例死于感染(图1 B)。
亚组分析显示,移植前达到骨髓缓解的患者,接受CAR-T细胞治疗后获得CR的概率显著更高(P=0.034),提示移植前疾病控制状态是CAR-T细胞疗效的重要影响因素。自体CAR-T细胞组与异基因CAR-T细胞组的CR率无显著差异(P=0.594),表明两种来源的CAR-T细胞在诱导缓解方面效果相当(图1 C)。
3年OS率达36.2%,非CR状态为独立不良预后因素
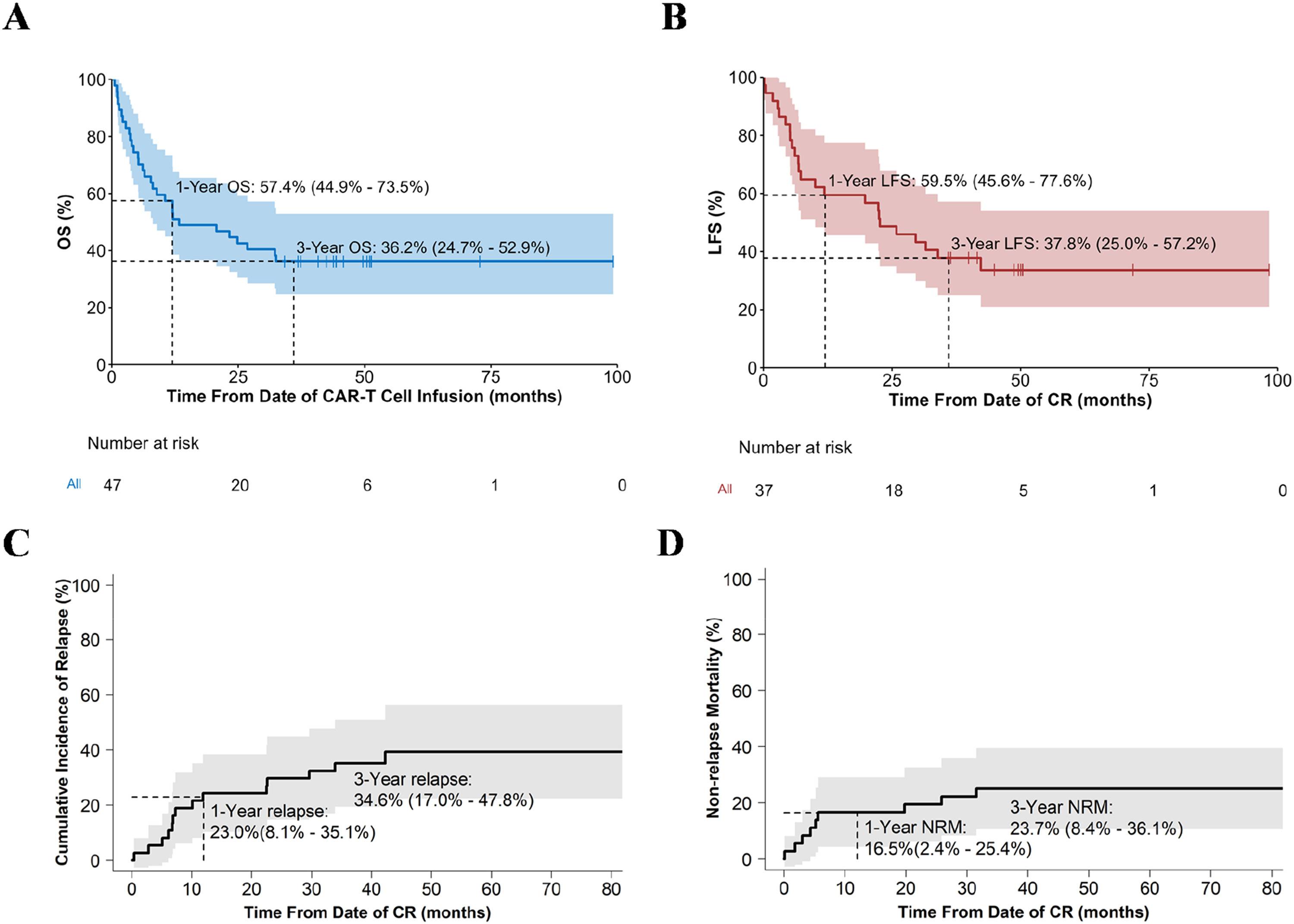
研究中位随访时间为32.3个月,整体患者的中位OS为13.3个月,3年OS率达36.2%,显著优于DLI和二次移植等传统治疗手段(图2 A)。在37例达到CR的患者中,中位LFS为22.6个月,3年LFS率为37.8%,证实CD19 CAR-T细胞疗法能为移植后复发B-ALL患者带来显著的长期生存获益(图2 B)。
多因素Cox回归分析显示,CAR-T细胞治疗后未达到CR是患者OS较差的独立危险因素(P<0.001,HR=13.4);而患者年龄、性别、细胞遗传学风险、移植类型、CAR-T细胞来源等因素与OS无显著关联。此外,CAR-T细胞治疗后发生aGVHD的患者,其LFS显著更差(P=0.049),是影响无病生存的重要因素。
截至随访终点,47.4%的患者死于疾病进展,28.9%死于晚期非复发死亡,其中26.3%为感染所致,3年NRM为23.7%。仅3例MRD阴性CR患者接受了二次allo-HSCT,但预后均不佳,提示CAR-T细胞治疗后亟需更有效的巩固治疗策略以降低复发风险(图2 C, D)。
自体与异基因CAR-T细胞治疗的长期生存结果无差异,各有临床优劣势
研究对比了自体与异基因CAR-T细胞疗法的长期疗效,结果显示两组患者的LFS、OS均无显著差异(P均>0.05),证实两种疗法在移植后复发B-ALL患者中的长期获益相当。但二者存在明显临床特点差异:自体CAR-T细胞具有免疫相容性优势,CRS和GVHD发生率更低,患者无需使用免疫抑制剂,免疫重建更快,治疗相关并发症较少;而异基因CAR-T细胞(供者来源)则表现出更强的活化和扩增效率,抗白血病效应更显著,但治疗相关死亡率较高,其移植物抗白血病(GVL)效应被较高的NRM所抵消,最终导致两组生存预后无显著差异。
安全性结果:不良反应以CRS和aGVHD为主,单倍体移植及短间隔输注增加aGVHD风险
CRS为最常见不良反应,ICANS发生率较低
所有患者中,74.5%发生任意级别CRS,其中16.4%为3~4级重度CRS,4例(7.3%)死于4级CRS,CRS中位起病时间为输注后2天(范围:0~27天)。ICANS发生率较低,仅5.4%的患者发生任意级别ICANS,其中3.6%为4级,1例(1.8%)死于ICANS合并CRS。自体与异基因CAR-T细胞组的CRS、ICANS发生率均无显著差异(P均>1.000)。
aGVHD发生率较高,相关危险因素明确
27.3%的患者在CAR-T细胞治疗后发生任意级别aGVHD,10.9%为3~4级重度aGVHD,累及皮肤、胃肠道、肝脏等部位,aGVHD中位起病时间为输注后15天(范围:5~127天),1例(1.8%)死于4级aGVHD。20.0%的患者发生cGVHD,其中仅3.6%为中重度cGVHD,整体耐受性较好。
多因素Fine-Gray回归分析明确了CAR-T细胞治疗后aGVHD的独立危险因素:既往接受单倍体相合allo-HSCT(P=0.035,HR=5.5)、allo-HSCT至CAR-T细胞输注间隔时间较短(≤6个月,P=0.005,HR=0.2),而CAR-T细胞来源与aGVHD发生率无显著关联(P=0.240)。单倍体移植的HLA抗原错配及短间隔输注后免疫耐受状态不稳定,是导致aGVHD风险升高的核心原因。
总结
该研究是一项多中心回顾性研究,系统报道了CD19 CAR-T细胞疗法在allo-HSCT后复发B-ALL患者中的3年长期疗效与安全性数据。研究证实该疗法能为这一高危人群带来显著的缓解率和长期生存获益,3年OS率达36.2%,且自体与异基因CD19 CAR-T细胞疗法疗效相当,二者各有临床特点。同时,研究明确了CAR-T细胞治疗后非CR状态是患者生存的独立不良预后因素,单倍体相合移植和短间隔输注是CAR-T细胞治疗后aGVHD发生的独立危险因素,为临床治疗决策和不良反应管理提供了重要依据。
该研究是中国学者在移植后复发B-ALL治疗领域的重要探索,填补了自体与异基因CD19 CAR-T细胞疗法长期疗效对比的研究空白,为该类高危患者的临床治疗提供了具有重要参考价值的中国数据。
对于allo-HSCT后复发的B-ALL患者,CD19 CAR-T细胞疗法以67.3%的高CR率和36.2%的3年OS率,成为该人群的优选治疗方案,疗效显著优于传统强化疗和DLI,为患者争取了更多的后续治疗机会。而自体与异基因CAR-T细胞疗效相当、各有特点的研究结果,为临床个体化选择CAR-T细胞来源提供了重要参考:对于移植后免疫重建较好、无明显高危因素的患者,可优先选择自体CAR-T细胞疗法以降低治疗相关并发症;对于骨髓原始细胞比例高、疾病进展迅速的患者,供者来源的异基因CAR-T细胞疗法可能更为适合,但其aGVHD风险需重点防控。
研究同时指出,CAR-T细胞治疗后疾病进展仍是患者死亡的首要原因,且二次allo-HSCT的巩固治疗效果不佳,提示未来需探索CAR-T细胞治疗与靶向治疗、免疫治疗、新型移植技术的联合策略,以进一步降低复发风险。此外,针对单倍体移植和短间隔输注的aGVHD高危人群,制定个体化的预防和干预方案,是提升CAR-T细胞治疗安全性的关键方向。
该研究充分体现了中国血液科医生在CAR-T细胞治疗领域的临床研究实力,为移植后复发血液肿瘤的治疗提供了新的思路,也为后续开展更大规模的前瞻性随机对照研究奠定了基础,有望推动CD19 CAR-T细胞疗法成为allo-HSCT后复发B-ALL患者的标准化治疗方案,为更多高危患者带来长期生存希望。
[1] Fu S, Yu Y, Zhang M, et al. Long-Term Follow-Up of CD19 CAR-T Cell Therapy in Acute Lymphoblastic Leukemia Patients Relapsed After Allo-HSCT[J]. Cytotherapy, 2026. https://doi.org/10.1016/j.jcyt.2026.102074.
排版编辑:Grady











 苏公网安备32059002004080号
苏公网安备32059002004080号


