在上消化道肿瘤领域,尽管PD-1/PD-L1抑制剂已打开局面,但真正能实现持久获益的患者仍是少数,临床获益探索步履未停。TIGIT——这个被誉为“下一个 PD-1”的希望之星,能否点燃消化道“冷”肿瘤的免疫火种,重构上消化道肿瘤免疫格局?
机制:破冰免疫冷肿瘤的新钥匙
免疫检查点抑制剂(ICIs)已彻底改变了肿瘤治疗格局,为多种肿瘤治疗提供了新策略。但在上消化道恶性肿瘤中,免疫治疗的临床获益主要局限于微卫星高度不稳定(MSI-H)和PD-L1阳性的亚群;即使在这些由生物标志物指导的患者群体中,仍有相当比例的患者会出现早期复发或对治疗无应答的情况。这种疗效的局限性反映了食管胃腺癌极具免疫抵抗性的肿瘤微环境(TME),其特点是间质致密、存在免疫抑制性的髓系细胞和调节性细胞群,以及效应T细胞浸润稀少。即便是在免疫原性相对较高的食管鳞状细胞癌中,PD-1或PD-L1抑制剂带来的获益也仅算中规中矩。
为了克服免疫屏障,研究重点已转向下一代ICI——尤其是TIGIT抑制剂。TIGIT是一种表达在活化T细胞和自然杀伤(NK)细胞表面的共抑制受体,可与其在肿瘤细胞和抗原递呈细胞上的配体CD155(PVR)及CD112相互作用。通过竞争性地抑制共刺激受体CD226,TIGIT的结合会削弱T细胞的增殖、细胞因子产生及细胞毒功能。在消化道肿瘤中,TIGIT常与PD-1在肿瘤浸润淋巴细胞上共同表达,从而加剧T细胞耗竭并促进免疫逃逸。其配体CD155在胃癌、食管癌和肝细胞癌的表皮及间质成分中通常呈高表达,放大了局部免疫抑制。TIGIT-CD155轴共同促成了定义许多消化道肿瘤的“免疫冷肿瘤”状态。
临床前模型表明,双重阻断TIGIT和PD-1可以恢复T细胞和NK细胞的效应功能,增强干扰素-γ信号传导,并产生比单用PD-1抑制剂更强效的抗肿瘤反应。因此,靶向TIGIT代表了扩大消化道肿瘤免疫治疗覆盖范围的策略——目前一系列早期临床试验正在探索这种检查点联合策略,旨在PD-1单药疗效不佳的领域重新点燃免疫反应。
试验:从 II 期的惊艳到 III 期的启示
尽管早期TIGIT抑制剂的表现令人振奋,但在III期研究中尚未转化为确切的获益。最初的II期研究数据提示其在肺癌、胃癌、食管癌和肝细胞癌等多种肿瘤中具有令人鼓舞的抗肿瘤活性,但目前尚并未转化为生存优势。
引人注目的早期信号来自EDGE-Gastric试验的A1组。在该研究中,Domvanalimab(抗TIGIT)联合Zimberelimab(抗PD-1)及FOLFOX方案,在未经治疗的HER2阴性胃癌、胃食管结合部癌及食管腺癌中,实现了59%的客观缓解率(ORR),中位总生存期(OS)接近27个月,中位无进展生存期(PFS)为12.9个月[1]。虽然结果数据优异,但该研究为单臂设计,样本量有限,该方案的明确获益有待进一步证实。期待正在进行的 STAR-221 III期研究结果,进一步揭示双重PD-1/TIGIT抑制是否能比现有标准方案显著延长患者生存。
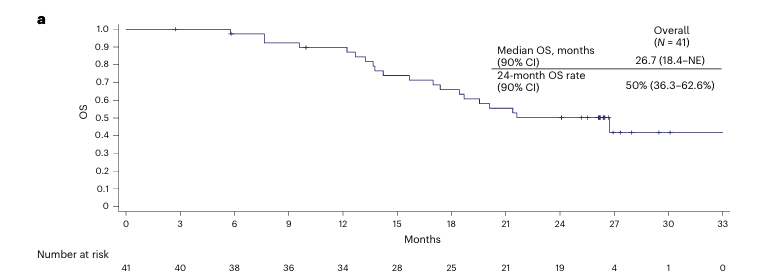
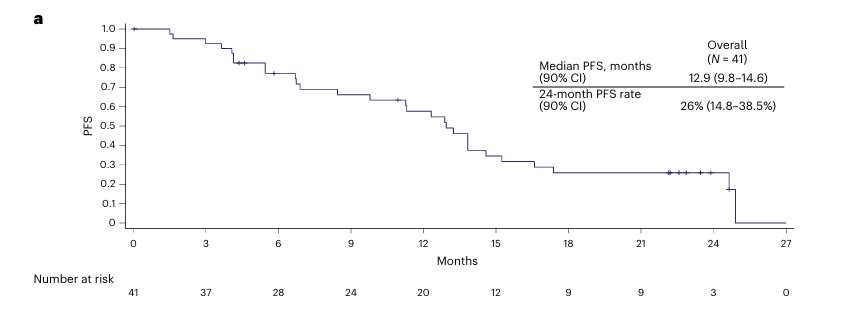
在晚期食管癌中,MORPHEUS-EC作为一项开放标签、多中心、随机的Ib/II期研究,其结果提示,在阿替利珠单抗联合化疗的基础上加入TIGIT抑制剂Tiragolumab,带来了增量获益。在初治的局部晚期不可切除或转移性食管癌患者中,ORR从单纯化疗的48%增加到化疗联合阿替利珠单抗方案的54%,而在加入TIGIT后的三联方案中进一步提升至68%。中位PFS也分别从4.1个月提高到6.8个月和6.9个月;中位OS分别为9.9个月 vs 13.1个月vs 16.0个月[2]。
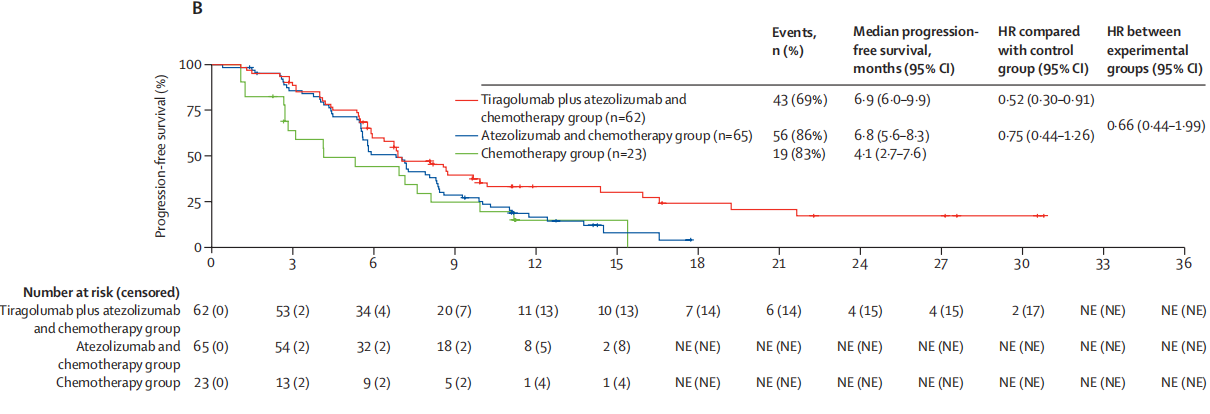
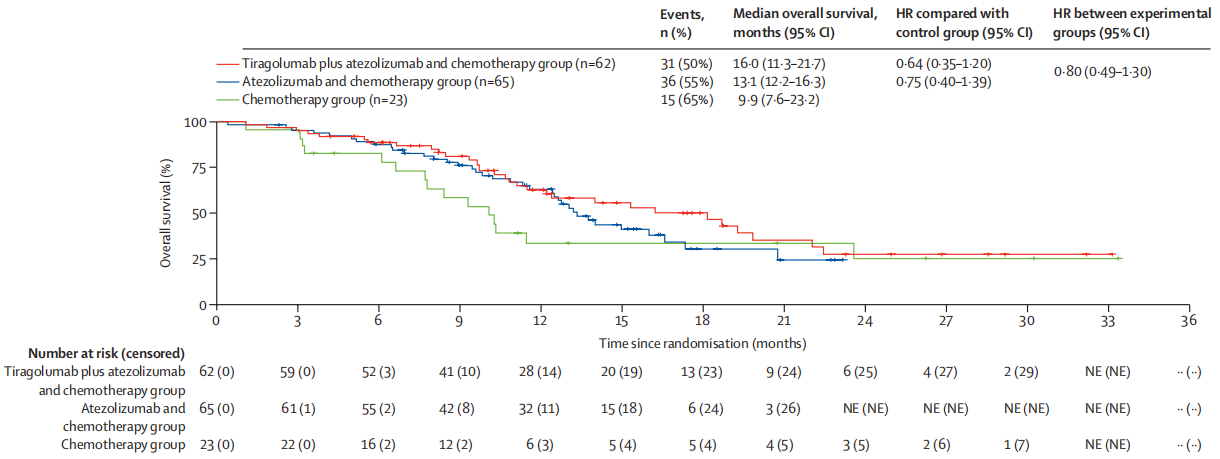
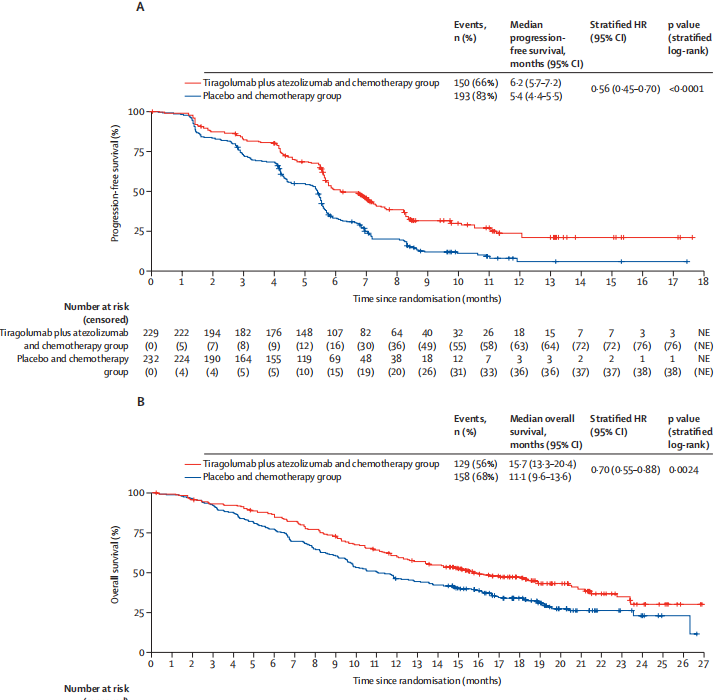
III期SKYSCRAPER-08的试验结果在全球范围内验证了这一策略。近日,该研究发表于《柳叶刀·肿瘤学》(The Lancet Oncology),表明对于不可切除局部晚期、不可切除复发或转移性食管鳞癌(ESCC)患者而言,相比于单纯化疗,Tiragolumab联合阿替利珠单抗和化疗治疗方案可显著延长PFS(6.2个月 vs. 5.4个月)和OS(15.7个月 vs. 11.1个月),降低患者疾病进展或死亡风险44%[3]。SKYSCRAPER-07试验评估了在局部晚期食管鳞癌中根治性放化疗后,采用阿替利珠单抗联合或不联合Tiragolumab进行维持治疗,未能显示出在PD-L1抑制剂基础上的额外获益。
在肝细胞癌领域,I/II期MORPHEUS-LIVER试验报告了Tiragolumab联合阿替利珠单抗和贝伐珠单抗具有显著疗效,但III期IMbrave-152/SKYSCRAPER-14试验未能确认其生存或缓解优势[4,5]。这可能反映了II期研究对效应规模的过高估计,以及II期对照组预后异常偏差和肝脏独特的免疫环境。这也凸显了将早期免疫信号转化为可重复结果的巨大挑战。
综合来看,这些研究反映了TIGIT领域的一个普遍模式:强劲的II期活性尚未在III期研究成功中得到复制。当前,其生物学机制依然具有说服力,但如何影响临床实践将取决于后续大型随机试验的数据。
进阶:TIGIT的优化之路——双抗与早研
基于此,研究领域正从广泛的晚期治疗转向更精细的策略——双特异性抗体、更早期疾病以及生物标志物驱动的选择。
Rilvegostomig是一种PD-1/TIGIT双特异性抗体,旨在优化两者的共同结合与信号协同效应。ARTEMIDE-Gastric-01研究正在探索 Rilvegostomig联合德曲妥珠单抗(T-DXd)或曲妥珠单抗联合化疗,对比帕博利珠单抗方案的对照组,用于HER2阳性胃及胃食管腺癌一线治疗[6]。其他研究还延伸至肝细胞癌(探讨Rilvegostomig联合或不联合Tremelimumab及贝伐珠单抗)和胆道癌(对比辅助治疗中Rilvegostomig联合化疗与单纯化疗,以及在晚期HER2阳性疾病中联用德曲妥珠单抗)。
与此同时,研究者们正将TIGIT抑制疗法推向更早期、可能对免疫反应更敏感的阶段。英国的ZODIAC试验正在评估一种围手术期减毒化疗策略,即在可手术切除的dMMR/MSI-H型胃癌及胃食管癌中使用Zimberelimab联合或不联合Domvanalimab[7]。
然而,要让 TIGIT 真正站稳脚跟,预测性生物标志物可能至关重要。到目前为止,PD-L1、TIGIT 或 CD155 的表达并未能一致地预测治疗反应。新兴研究转而关注免疫再激活的动态标志物、T细胞耗竭特征、干扰素-γ活性以及T细胞受体(TCR)克隆性等,这些正在EDGE、ZODIAC和ARTEMIDE等研究中通过多组学相关性分析进行探索。
总体而言,真正的免疫修复可能需要更广泛、整合的检查点调节,将TIGIT与PD-1、CTLA-4等靶点结合,并聚焦于免疫活跃的生态位,如dMMR疾病或围手术期阶段。相信凭借更精准的试验设计、更深层次的生物标志物洞察以及双特异性抗体的创新,TIGIT仍有望重塑消化道癌症的免疫治疗策略。
[1] Janjigian YY, Oh DY, Pelster M, Wainberg ZA, Prusty S, Nelson S, DuPage A, Thompson A, Koralek DO, Sison EAR, Rha SY. Domvanalimab and zimberelimab in advanced gastric, gastroesophageal junction or esophageal cancer: a phase 2 trial. Nat Med. 2025 Dec;31(12):4274-4280. doi: 10.1038/s41591-025-04022-w. Epub 2025 Oct 18. PMID: 41109921; PMCID: PMC12705419.
[2] Sun JM, Chao Y, Kim SB, Rha SY, Evans TRJ, Strickland AH, Wainberg Z, Chau I, Pelles-Avraham S, Ajani J, Malhotra R, Liu Q, Li S, Cha E, Kalaitzidou M, Huang X, Allen S, Hsu CH. First-line tiragolumab plus atezolizumab and chemotherapy in patients with previously untreated, locally advanced unresectable or metastatic oesophageal cancer (MORPHEUS-EC): a randomised, open-label, phase 1b/2 trial. Lancet Oncol. 2026 Jan;27(1):90-102. doi: 10.1016/S1470-2045(25)00402-4. PMID: 41449151.
[3] Hsu CH, Lu Z, Gao S, Wang J, Sun JM, Liu T, Fan Q, Cai J, Ge F, Li S, Zhang L, Cha E, Allen S, Shen L. Tiragolumab plus atezolizumab and chemotherapy as first-line treatment for patients with unresectable oesophageal squamous cell carcinoma (SKYSCRAPER-08): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2026 Jan;27(1):103-115. doi: 10.1016/S1470-2045(25)00401-2. PMID: 41449142.
[4] Finn RS, Ryoo B-Y, Hsu C-H, et al. Results from the MORPHEUS-liver study: phase Ib/II randomized evaluation of tiragolumab (tira) in combination with atezolizumab (atezo) and bevacizumab (bev) in patients with unresectable, locally advanced or metastatic hepatocellular carcinoma (uHCC). J Clin Oncol. 2023;41:16s (suppl; abstr 4010).
[5] Badhrinarayanan S, Cotter C, Zhu H, Lin Y-C, Kudo M, Li D. IMbrave152/SKYSCRAPER-14: a phase III study of atezolizumab, bevacizumab and tiragolumab in advanced hepatocellular carcinoma. Future Oncol. 2024;20(28):2049-2057.
[6] Xu R-H, Gomes DBD, Chen J-S, et al. ARTEMIDE-Gastric01: a phase 3 randomized study of rilvegostomig with fluoropyrimidine and trastuzumab deruxtecan (T-DXd) as first-line (1L) treatment for locally advanced or metastatic HER2-positive gastric or gastroesophageal junction cancer (GC/GEJC). J Clin Oncol. 2025;43:16s (suppl; abstr TPS4204).
[7] Keogh GA, Patel N, Crux R, et al. 477TiP A randomised phase II study of zimberelimab ± domvanalimab immunotherapy in resectable mismatch repair deficient (dMMR) gastric and gastroesophageal junctional (G/GOJ) adenocarcinoma (ZODIAC). Ann Oncol. 2025;36(1):S179-S180.
排版编辑:肿瘤资讯-AS











 苏公网安备32059002004080号
苏公网安备32059002004080号


