2026年1月29日,由中国临床肿瘤学会(CSCO)、浙江大学医学院附属第二医院主办的“How We Treat暨浙大二院肿瘤沙龙第43期”以线上直播的形式召开。本期会议以“从2026 ASCO GI再看:dMMR/MSI-H mCRC的治疗选择”为主题,由浙江大学医学院附属第二医院袁瑛教授担任大会主席,浙江大学医学院附属第二医院翁姗姗教授担任会议主持,邀请来自全国多家医院的消化肿瘤领域专家共同探讨dMMR/MSI-H转移性结直肠癌(mCRC)的治疗策略。【肿瘤资讯】特此整理会议精粹内容。

会议伊始,浙江大学医学院附属第二医院翁姗姗教授对参会专家表示热烈欢迎,并简要介绍了本次会议的主题背景。翁姗姗教授指出,对于dMMR/MSI-H转移性结直肠癌(mCRC)患者,免疫治疗的发展可谓一路高歌猛进。从2015年免疫检查点抑制剂(ICI)在该人群中初显疗效,到2020年KEYNOTE-177研究奠定了单药免疫治疗作为一线治疗的循证医学基础,再到CheckMate 8HW研究揭示双免联合可能优于单药免疫治疗,该领域的治疗格局持续演变。而COMMIT研究作为备受期待的临床试验,旨在回答在免疫治疗基础上联合标准化疗和靶向治疗能否进一步提升疗效这一关键问题。本次会议将由袁瑛教授以2026 ASCO GI大会最新发布的数据为切入点,梳理dMMR/MSI-H mCRC治疗格局的关键研究进展,并重点解读COMMIT研究。
从2026 ASCO GI再看:dMMR/MSI-H mCRC的治疗选择
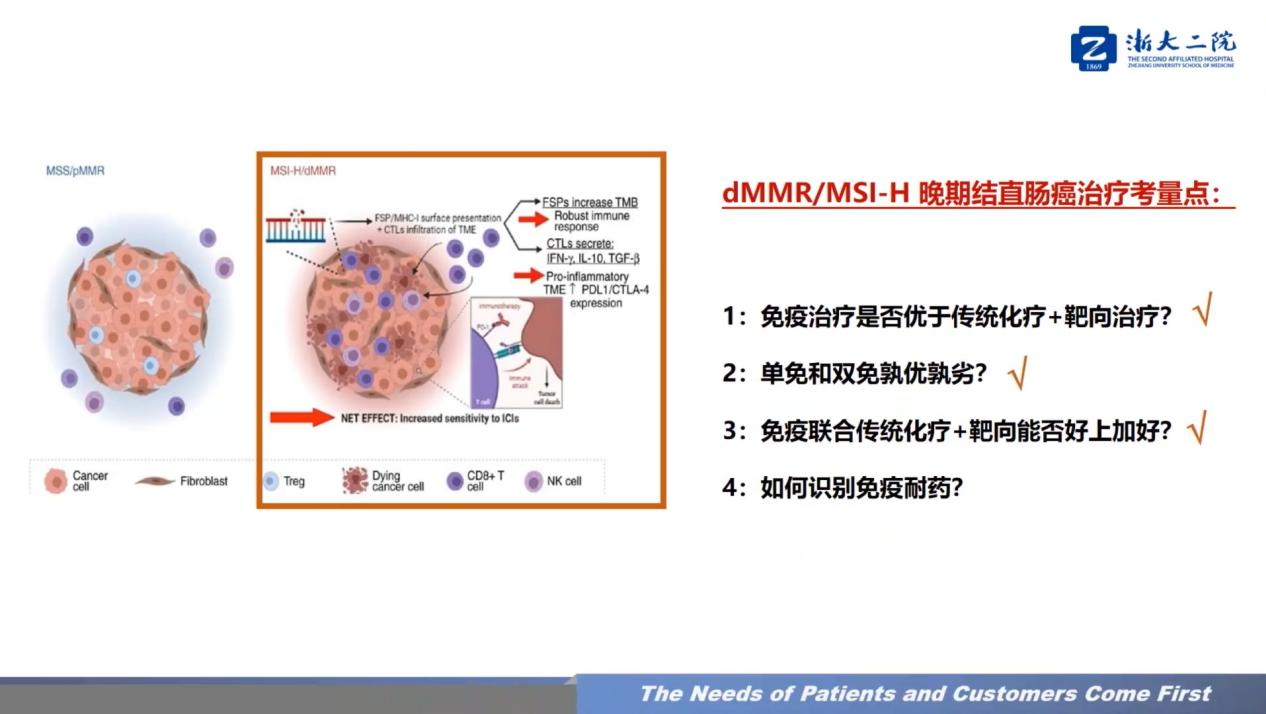
袁瑛教授首先梳理了dMMR/MSI-H mCRC治疗领域亟需回答的几个核心问题:免疫治疗是否优于传统化疗+靶向治疗?单免和双免孰优孰劣?免疫联合传统化疗+靶向能否好上加好?如何识别免疫耐药?
在回顾经典研究方面,袁瑛教授首先介绍了KEYNOTE-177研究。该研究纳入dMMR/MSI-H mCRC患者,一线随机接受帕博利珠单抗或标准化疗联合或不联合靶向治疗。结果显示,帕博利珠单抗组的中位无进展生存期(mPFS)达16.5个月,显著优于化疗+靶向组的8.2个月;客观缓解率(ORR)从33.1%提升至43.8%;尽管研究中约62%的患者发生交叉用药,帕博利珠单抗组在总体生存(OS)方面仍显示出获益趋势,死亡风险降低约27%。该研究奠定了单药免疫治疗在dMMR/MSI-H mCRC一线治疗中的标准地位。
随后,袁瑛教授解读了CheckMate 8HW研究。该研究入组对象为既往未接受过免疫治疗的dMMR/MSI-H mCRC患者,采用2:2:1的随机分组设计,比较纳武利尤单抗联合伊匹木单抗(双免组)、纳武利尤单抗单药组(单免组)与化疗联合或不联合靶向组的疗效。中位随访近4年的数据显示,双免组与化疗组的PFS曲线明显分离,且在多数亚组中均观察到免疫治疗带来的持续获益。单免组一线治疗的mPFS达到60.8个月,表现优异。双免组的ORR为73%,疾病进展(PD)率仅为11%;单免组ORR为61%,PD率为16%。在完全缓解(CR)比例相当的前提下,双免治疗进一步降低了疾病进展(PD)发生率,提示双免联合策略可能有助于降低MSI-H mCRC中存在的原发性免疫耐药风险。亚组分析提示,对于左半结肠、PD-L1≥1%、RAS/BRAF野生型及Lynch综合征患者,双免与单免一线治疗的PFS差异相对有限,这为临床在综合考虑疗效、安全性及经济因素时选择单药免疫治疗提供了参考依据。
袁瑛教授随后重点介绍了2026 ASCO GI大会上报告的COMMIT研究。该研究自2017年启动,在美国16家中心开展,旨在探索在免疫治疗基础上联合标准化疗及抗血管生成治疗,是否能够进一步改善dMMR/MSI-H转移性结直肠癌患者的疗效。基线特征分析显示,三组患者在主要临床和分子特征方面总体保持一致,具有良好的可比性。研究结果显示,FOLFOX联合贝伐珠单抗联合PD-L1抑制剂阿替利珠单抗组(n=41例)的mPFS为24.5个月,显著优于阿替利珠单抗单药组(n=41例)的5.3个月;化靶免联合组的ORR达86.1%,PR率50%,CR率36.1%,PD率仅为2.8%,相比之下单免组PD率达32.4%。尽管联合治疗在无进展生存和缓解率方面显示出优势,但在 24 个月 OS 方面,两组尚未观察到显著差异(HR = 1.04)。值得关注的是,在BRAF V600突变患者中,化疗、靶向联合免疫治疗相较于单药免疫治疗显示出更明显的疗效改善趋势,提示对于预后不良人群,免疫强化策略可能具有更大的临床价值。
安全性数据方面,化靶免联合组3-4级不良事件发生率为73.2%,高于单免组的41.5%。联合组41例患者中出现4例(9.8%)死亡,其中2例为突发死亡,分别发生在第16和第18个周期——此时FOLFOX已停药3~4个月,提示其中可能存在尚未明确的因素。在总结部分,袁瑛教授对上述三项关键研究的数据进行了梳理。在ORR方面,双免联合和化靶免联合表现更优;在PD率方面,单免相对较高,而双免和化靶免较低,尤其是化靶免仅为2.8%。在安全性方面,KEYNOTE-177中单免组无治疗相关死亡发生;CheckMate 8HW中单免组死亡风险低于1%,双免组为1%;COMMIT研究化靶免联合组即使排除2例肿瘤进展相关死亡,仍有约5%的突发死亡风险。袁瑛教授表示,未来研究方向应聚焦于如何识别免疫耐药患者,袁瑛教授团队正在分析本中心dMMR肠癌患者中接受免疫治疗后快速进展和超进展的病例,已发现一些潜在的分子标志物,正在进行后续机制研究,期望未来能够提前筛选出最可能发生免疫耐药的患者,为这部分患者制定个体化的治疗策略。

讨论环节
讨论环节由翁姗姗教授主持,六位特邀专家围绕COMMIT研究带来的新思考及临床实际选择展开了热烈探讨。

绍兴市人民医院陈遐林教授指出,随着多项研究结果的相继发表,dMMR/MSI-H mCRC患者的一线治疗选择日益丰富。目前临床需要考虑的关键问题是如何在单药免疫、双免及化靶免联合方案中进行合理选择。对于身体状况良好、能够耐受免疫治疗的患者,双免联合可能是更优选择;而对于免疫状态较差或需要快速控制肿瘤的患者,可以考虑COMMIT研究的化靶免联合方案,但需注意充分评估不良反应风险。此外,未来需要进一步探索生物标志物以实现精准分层,明确哪些患者更适合何种治疗方案。
无锡市惠山区人民医院丁宁教授表示,COMMIT研究结果呈现出几个核心问题:首先,PD-L1抑制剂单免组的mPFS为5.3个月,提示PD-1与PD-L1抑制剂在mCRC中的疗效差异值得进一步探讨;其次,该研究设计时选择单药PD-L1抑制剂作为对照组,未能与双免进行头对头比较,当然,考虑到该研究启动时间较早、有其历史合理性;第三,化靶免联合组虽然mPFS显著优于单免组,遗憾的是两组的mOS获益无显著差异,建议关注一些从该方案明显获益的亚组人群。丁宁教授认为,化靶免联合应优先考虑年轻、体能状态好、肿瘤负荷大、生物学行为更差的患者。
青岛大学附属医院吕静教授从不良反应管理的角度分享了观点。吕静教授指出,从单免到双免再到化靶免联合,疗效确实在提升,但毒性也在累加。虽然双免联合不良反应较单免增加,但仍属于免疫相关不良反应的同一反应谱;而化靶免联合则叠加了化疗、靶向和免疫三类药物的不良反应,目前临床经验相对有限。在不良反应管理方面,吕静教授强调应遵循CSCO指南的指导原则:用药前评估高风险因素、治疗过程中密切监测、及时发现并规范处理。吕静教授还提出了临床实践中的困惑:一线免疫治疗进展后,二线如何选择?尤其是使用双免或化靶免一线治疗后如何进行后续治疗?
针对吕静教授的问题,袁瑛教授进行了回应。袁瑛教授指出,COMMIT研究PFS差距显著但OS相近的原因,可能是因为化靶免联合组一线即使用了多种有效治疗手段,导致后续可选择的方案相对有限;而单免组在疾病进展后,仍可序贯使用化疗、靶向或双免联合等方案。袁瑛教授强调,临床决策应以治疗目标为导向:对于肿瘤负荷大、需要短期内快速缩瘤的患者,化靶免联合可作为一种选择,但需充分告知患者治疗相关风险;从临床经验来看,双免方案的成熟度相对更高。而对于肿瘤负荷不大、无NED机会的患者,可能更应以安全和延长生存期为主要考量。
宁波市第二医院徐建芬教授强调治疗决策需个体化:年轻、肿瘤负荷大、有望达到NED状态的患者,可考虑更强化的联合方案。对于一线免疫治疗进展后的二线治疗,建议根据进展模式制定方案:孤立性进展或缓慢进展可考虑局部联合免疫维持;也可在免疫治疗基础上联合抗血管生成药物或化疗药物。对于同时存在BRAF V600E突变和dMMR/MSI-H的mCRC患者,免疫治疗联合BRAF抑制剂可能是值得探索的方向。
淮安市第一人民医院仲小敏教授指出,随着错配修复蛋白检测的普及,dMMR/MSI-H患者的临床识别率已明显提高。在单免与双免的选择上,理论上双免优于单免,但需权衡不良反应增加的问题。根据CheckMate 8HW研究的亚组分析结果,左半结肠、RAS/BRAF野生型、PD-L1≥1%、Lynch综合征等亚组患者使用单免可能已经足够。然而,具体临床实践中哪类肠癌患者更适合单免、哪类更适合双免,目前仍缺乏明确的分层标准。仲小敏教授建议在制定治疗方案时应综合考虑药物可及性、经济因素及替代方案等。她还分享了小分子TKI联合免疫治疗在肠癌肺转移患者中取得良好疗效的经验,以及局部放疗联合免疫治疗肠癌肝转移的初步探索。
衢州市人民医院翁美玲教授认为,对于能够耐受治疗的年轻患者,双免联合可能是更优选择,因为其ORR更高,PD率更低。COMMIT研究的化靶免联合呈现出86.1%的高ORR和24.5个月的优异mPFS,对于肿瘤负荷大、症状明显、有转化治疗需求的患者具有吸引力。此外,翁美玲教授还提出了几个值得探索的方向:是否存在生物标志物可以早期识别免疫耐药患者?ctDNA动态监测能否帮助早期识别耐药?免疫治疗能否像抗血管生成治疗一样跨线持续使用?体能状态差的后线治疗患者能否考虑免疫联合多靶点TKI治疗?
答疑环节+大会总结
袁瑛教授在答疑环节中指出,KEYNOTE-177、CheckMate 8HW、COMMIT三项研究中BRAF V600E突变患者比例均在23%~28%,总体处于相近水平。这一数据与既往文献报道的欧美dMMR人群中约21%合并BRAF V600E突变的比例相吻合,说明各研究入组人群的分子特征具有可比性。
在总结中,袁瑛教授分享了一个重要的观察视角:临床研究的设计往往滞后于临床认知的发展。她以ATOMIC研究为例进行说明——该研究设计于2017年,彼时KEYNOTE-177研究尚未公布dMMR晚期CRC的免疫治疗数据,研究者在当时的认知背景下尚缺乏“去化疗”辅助治疗的信心,因此采用了化疗联合免疫的研究设计。相比之下,其团队与丁培荣教授团队合作开展的一项针对III期dMMR CRC术后患者的研究,则是在KEYNOTE-177数据公布后设计,比较“去化疗”的免疫辅助治疗与传统辅助治疗策略,体现了不同时代背景下研究设计理念的演进。袁瑛教授指出,尽管临床研究回答问题的速度相对滞后于临床需求,但学术界始终在持续努力推动该领域的探索与进步。
排版编辑:xiaodong











 苏公网安备32059002004080号
苏公网安备32059002004080号


