肝细胞癌(HCC)是全球第六大常见恶性肿瘤,每年导致超过80万人死亡,5年生存率不足15%。尽管手术、消融和免疫检查点抑制剂(ICIs)等治疗手段不断进步,但术后复发率高及免疫治疗原发耐药仍是临床面临的重大挑战。肿瘤免疫微环境(TIME)中M2型肿瘤相关巨噬细胞(TAMs)浸润与免疫逃逸密切相关,而代谢重编程作为肿瘤核心特征之一,在调控免疫细胞功能中发挥关键作用。本研究旨在阐明去泛素化酶USP2通过调控脂质代谢介导HCC细胞与M2巨噬细胞交互的分子机制,并评估其作为治疗靶点的临床转化价值。
研究背景
HCC的进展伴随着显著的代谢重编程,其中脂肪酸从头合成增强是维持肿瘤快速增殖的重要特征。去泛素化酶(DUBs)通过调控蛋白质稳定性参与肿瘤发生发展,但其在HCC代谢-免疫交互中的作用尚未充分阐明。泛素特异性蛋白酶2(USP2)作为DUB家族成员,已被报道在多种肿瘤中稳定PD-L1等关键蛋白,但其在HCC脂质代谢及巨噬细胞极化中的作用仍属未知。过氧化物酶体增殖物激活受体γ(PPARγ)是脂质代谢的核心转录因子,其蛋白稳定性受泛素化调控。研究假设USP2通过去泛素化稳定PPARγ,促进脂肪酸合成,进而通过分泌脂肪酸诱导M2巨噬细胞极化,形成促肿瘤正反馈环路。
研究方法
患者来源类器官(PDO)与细胞模型:收集6例HCC手术标本构建PDO模型,采用22种DUB抑制剂(10 μM)筛选关键靶点。使用7404、Hep3B、HepG2、PLC/PRF/5、LM3等7种HCC细胞系,通过慢病毒shRNA构建USP2稳定敲低细胞系,转染Flag-USP2质粒构建过表达模型。
动物模型:14日龄C57BL/6雄性小鼠腹腔注射二乙基亚硝胺(DEN, 25 mg/kg)诱导原发性HCC模型,16周龄起给予USP2抑制剂ML364(5 mg/kg, 每2天一次)或联合抗PD-1抗体(10 mg/kg, 每周2次)治疗12周。皮下移植瘤模型使用Hepa1-6细胞(1×106/只),观察21天。采用脂质体氯膦酸盐清除巨噬细胞验证USP2功能依赖性。
代谢组学与分子机制:对PDO进行LC-MS代谢组学分析,检测游离脂肪酸(FFA)和甘油三酯(TG)水平。免疫共沉淀-质谱(IP-MS)鉴定USP2互作蛋白,免疫荧光观察USP2-PPARγ共定位。CUT&RUN-qPCR验证PPARγ对ACSS2、ACLY、ACACA启动子的结合。使用环己酰亚胺(CHX, 10 μg/mL)追踪PPARγ半衰期,MG132(10 μM)阻断蛋白酶体降解。检测K48/K63连接泛素链明确去泛素化类型。
免疫表型分析:THP-1细胞经PMA(100 nM, 48小时)诱导为巨噬细胞,与HCC细胞Transwell共培养。流式细胞术检测CD206+ CD11b+ F4/80+ M2巨噬细胞比例及GZMB+ IFN-γ+ CD8+ T细胞浸润。多重免疫组化分析M2标志物CD163、ARG1、IL-10表达。
生物信息学分析:整合11个HCC scRNA-seq数据集(GSE125449, GSE149614等),基于USP2表达水平分为高/低组,t-SNE可视化免疫细胞浸润。从TCGA获取365例HCC患者数据,计算风险比(HR)及95%置信区间(95%CI)。Kaplan-Meier法绘制生存曲线,log-rank检验比较差异。
研究结果
USP2抑制剂ML364显著抑制HCC PDOs活性
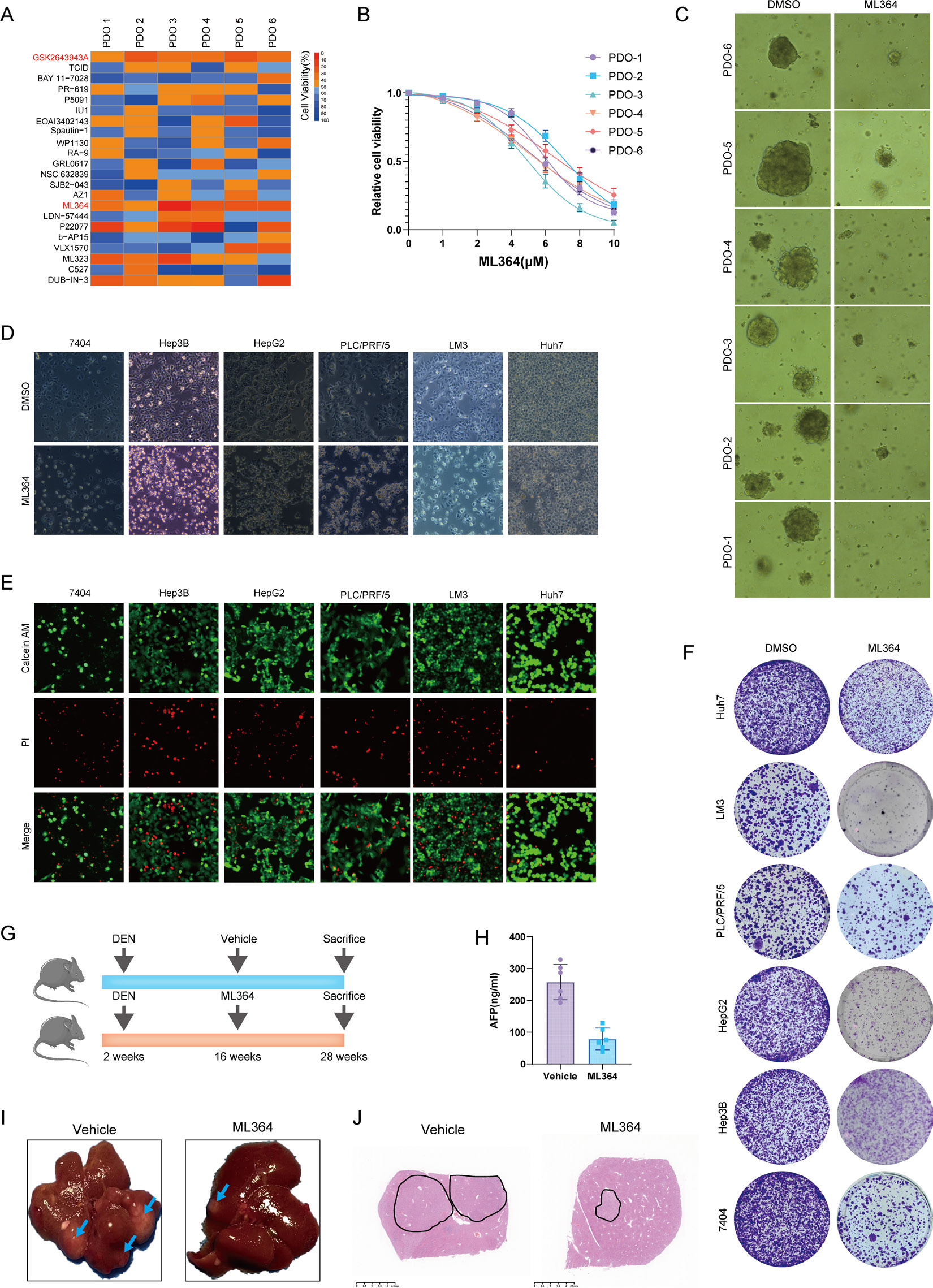
对6例HCC PDOs筛选22种DUB抑制剂,发现ML364(USP2选择性抑制剂)呈剂量依赖性抑制PDO活力(IC50 2-5 μM),10 μM处理48小时使细胞活力降低超过70%(P < 0.001)。在7404、Hep3B等细胞系中,ML364(5 μM)显著抑制克隆形成(抑制率>60%, P < 0.01)和侵袭能力(P < 0.001)。DEN诱导的原发性HCC模型中,ML364治疗组肝肿瘤数量较对照组减少58%(P < 0.01),血浆AFP水平下降62%(P < 0.001),证实USP2是HCC治疗的关键靶点。
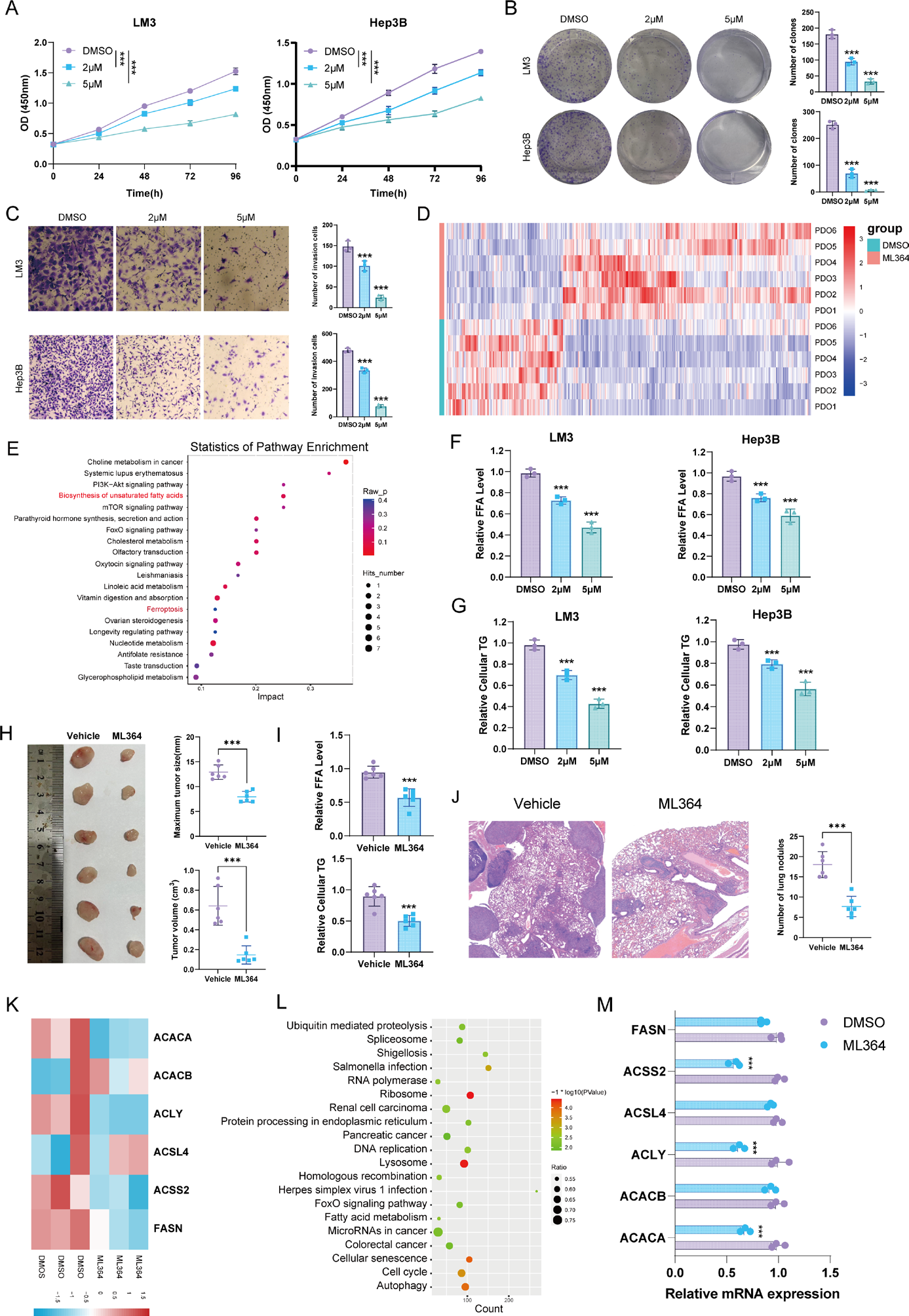
USP2通过PPARγ调控脂肪酸从头合成
代谢组学分析显示,ML364处理使PDO中不饱和脂肪酸合成通路显著抑制,其中油酸水平下降最显著(FC = 0.31, P < 0.001)。LM3细胞中,ML364(5 μM)使FFA和TG水平分别降低52%和48%(P < 0.01)。RT-qPCR证实ACSS2、ACLY、ACACA mRNA表达下调>60%(P < 0.001)。IP-MS鉴定PPARγ为USP2直接互作蛋白,分子对接显示USP2的S576/R270位点与PPARγ的D251/E351位点结合(结合能-12.3 kcal/mol)。Co-IP验证内源性USP2-PPARγ相互作用,免疫荧光显示二者部分共定位于胞质。
USP2通过K48连接去泛素化稳定PPARγ
USP2敲低使PPARγ蛋白水平下降70%(P < 0.001),而mRNA无变化。MG132处理可逆转此效应,表明其通过蛋白酶体途径降解。CHX追踪实验显示USP2敲低使PPARγ半衰期从8.2小时缩短至2.1小时(P < 0.001)。泛素化实验证实USP2野生型(WT)而非催化失活突变体(C276A)显著降低PPARγ多泛素化水平。使用K48/K63突变泛素显示,USP2特异性去除K48连接泛素链。通过构建PPARγ截断突变体,鉴定DBD结构域为USP2作用区段。进一步点突变筛选确定K142位点是USP2去泛素化的关键赖氨酸残基,K142R突变使PPARγ泛素化水平降低85%(P < 0.001)。
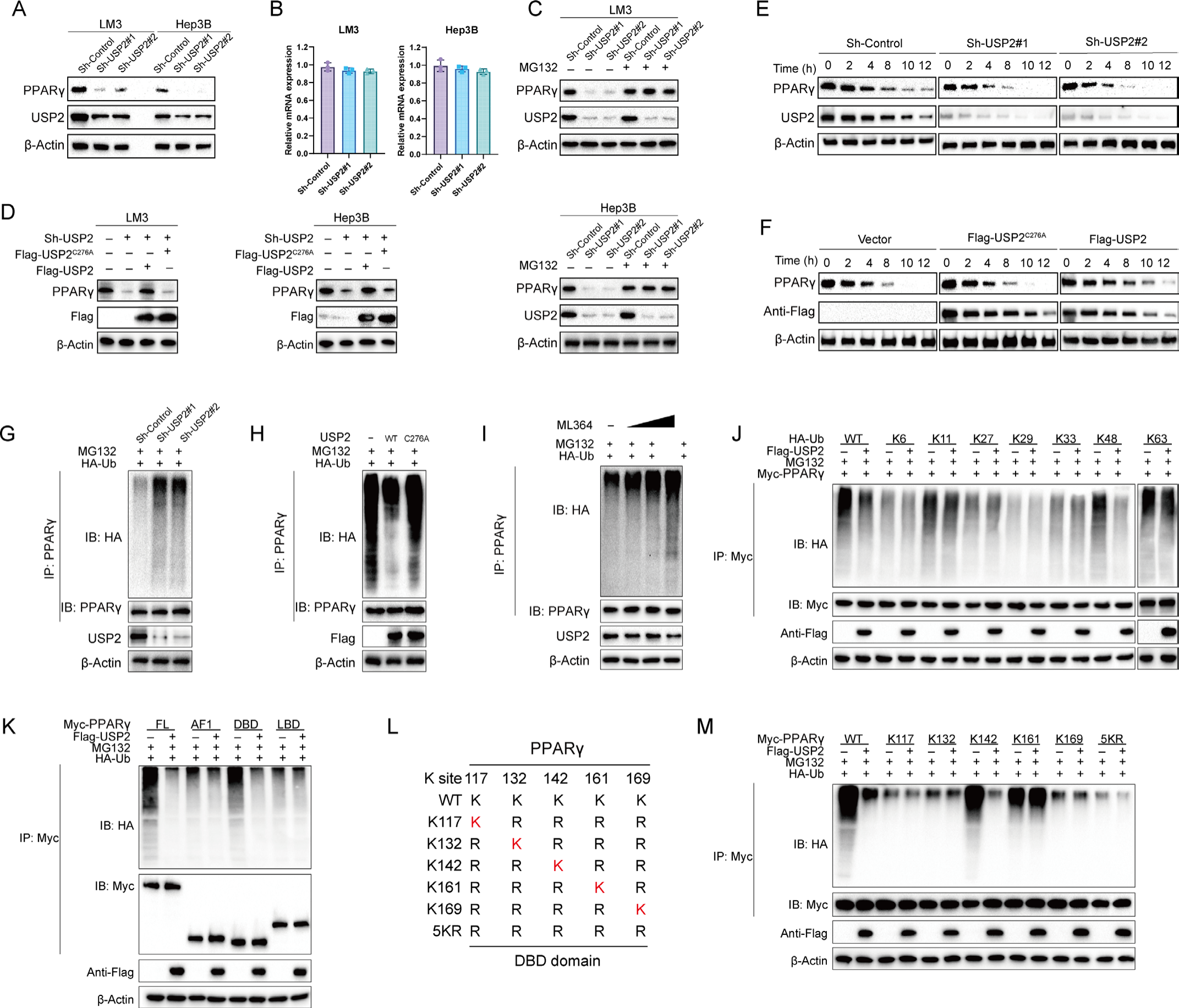 图3 USP2通过靶向K48连接的泛素化在PPARγ的K142位点稳定PPARγ蛋白
图3 USP2通过靶向K48连接的泛素化在PPARγ的K142位点稳定PPARγ蛋白
PPARγ转录激活脂肪酸合成基因
CUT&RUN-qPCR显示PPARγ直接结合ACLY启动子区(-427/-408)、ACACA启动子区(-801/-782)及ACSS2启动子区(-644/-625)。USP2敲低使PPARγ在这些区域的富集度下降>75%(P < 0.001)。双荧光素酶报告基因实验证实,PPARγ过表达使ACLY、ACACA、ACSS2启动子活性分别提升3.2倍、2.8倍和2.5倍(P < 0.001),而K142突变体丧失此功能。在USP2敲低细胞中过表达PPARγ-WT可恢复脂肪酸合成,而转录失活突变体PPARγ-ΔDBD无此作用,证实USP2-PPARγ轴以转录依赖方式调控代谢。
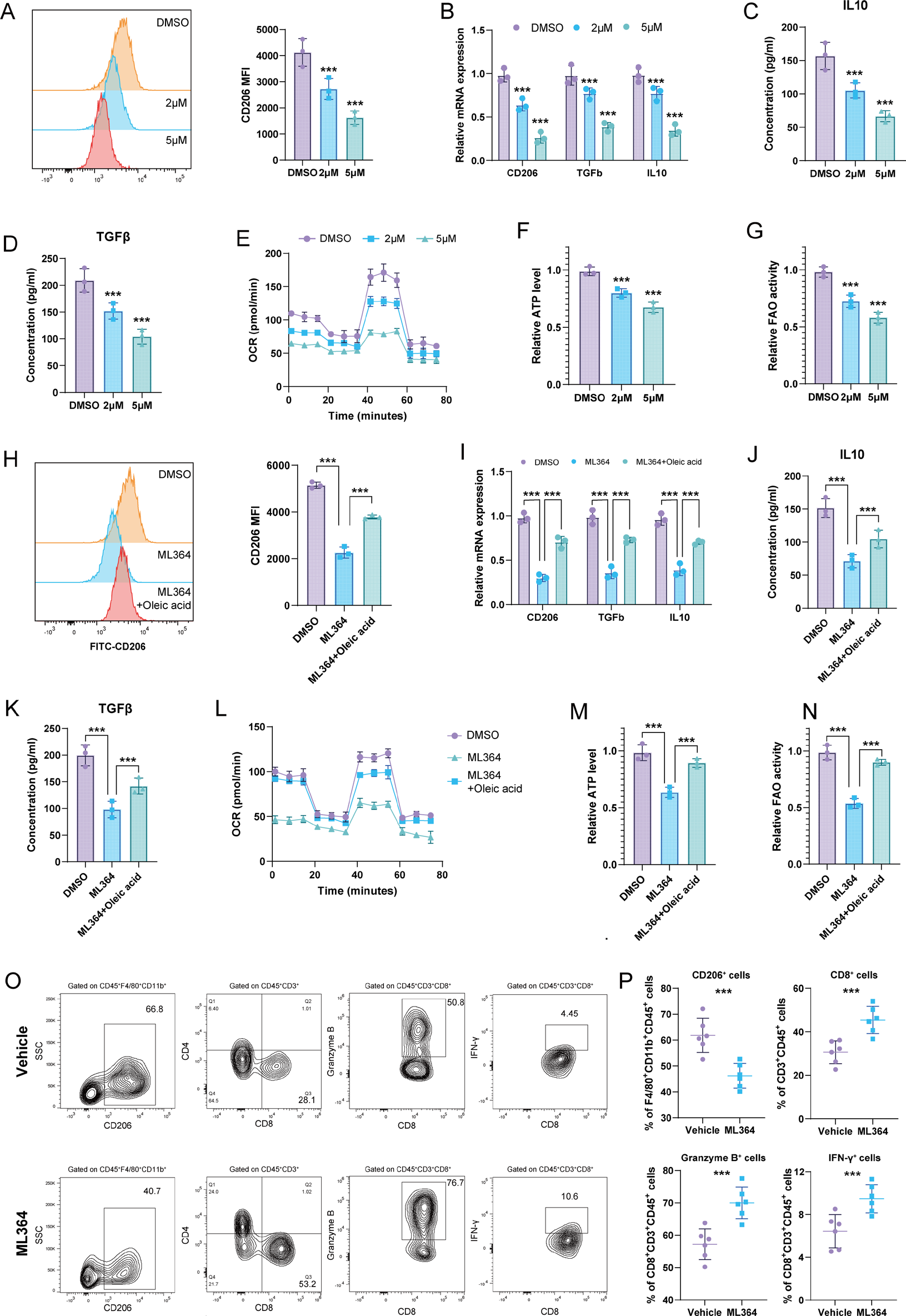
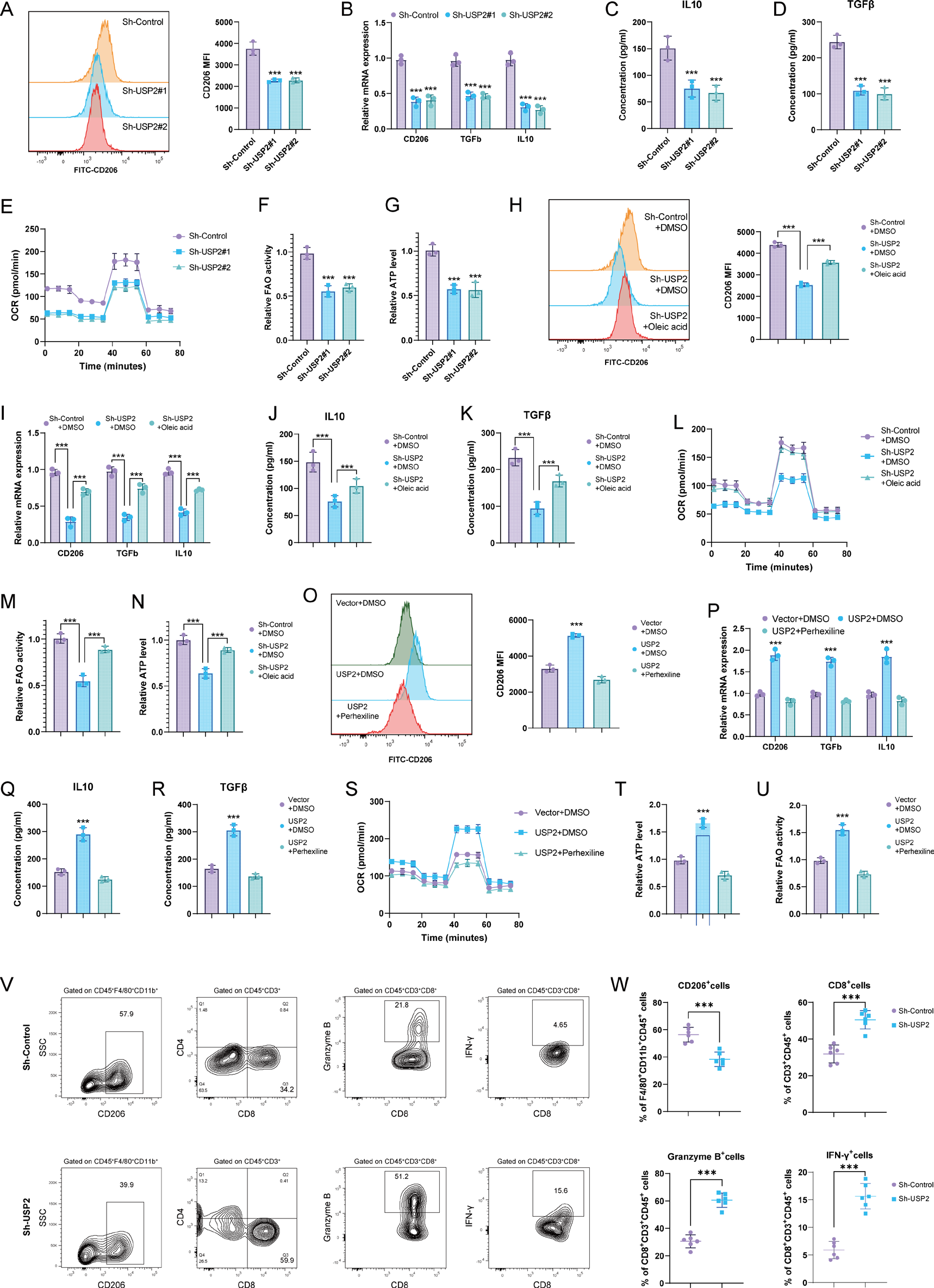
油酸通过增强脂肪酸氧化诱导M2巨噬细胞极化
将LM3细胞来源的油酸(100 μM)添加至THP-1巨噬细胞,使CD206+ M2比例从12%升至45%(P < 0.001),IL-10和TGF-β分泌增加2.5倍和1.8倍(P < 0.01)。Seahorse检测显示油酸使巨噬细胞氧消耗率(OCR)提升1.7倍,脂肪酸氧化(FAO)增加2.3倍,ATP产生增加1.9倍(P < 0.01)。FAO抑制剂perhexiline(5 μM)可阻断油酸诱导的M2极化,使CD206+比例恢复至15%(P < 0.001)。Transwell共培养实验显示,ML364处理的LM3细胞使共培养巨噬细胞CD206表达降低65%(P < 0.001),而补充油酸可逆转此效应,证实油酸是连接USP2与巨噬细胞极化的关键代谢物。
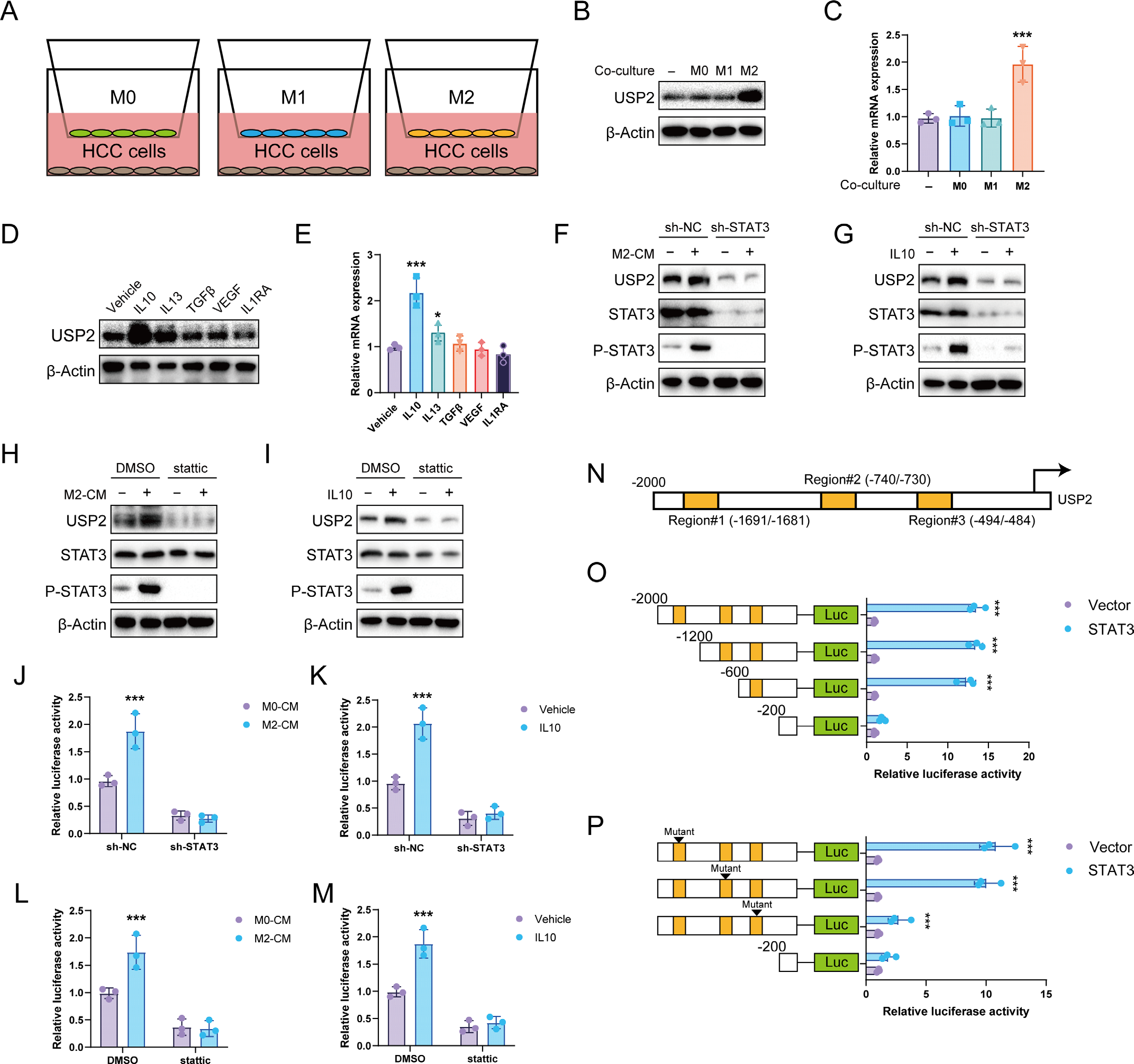
M2巨噬细胞分泌IL-10形成STAT3-USP2正反馈环路
M2巨噬细胞条件培养基使HCC细胞USP2 mRNA和蛋白表达分别上调2.8倍和2.4倍(P < 0.01),而M0/M1亚型无此作用。ELISA筛选显示IL-10(50 ng/mL)诱导USP2表达最强(P < 0.001)。IL-10激活STAT3磷酸化,sh-STAT3或抑制剂static(10 μM)可阻断M2条件培养基诱导的USP2上调。CUT&RUN-qPCR鉴定USP2启动子区-494/-484存在STAT3结合位点,突变该位点使IL-10诱导的USP2启动子活性降低78%(P < 0.001)。这形成“USP2-PPARγ-油酸-M2-IL-10-STAT3-USP2”正反馈环路,持续驱动肿瘤进展。
USP2高表达与M2浸润及不良预后相关
分析11个HCC单细胞数据集(n = 378),USP2高表达组M2标志物(CD163、ARG1、IL-10)阳性巨噬细胞比例较USP2低表达组增加2.1倍(P < 0.001),而CD8+ T细胞浸润减少58%(P < 0.01)。多色免疫组化显示USP2高表达肿瘤中CD206+ TAMs密度增加3.5倍(P < 0.001)。94例HCC切除队列中,USP2高表达(IHC评分>中位数)患者5年总生存率降低(HR = 2.31, 95%CI=1.18~4.52, P = 0.014),多因素Cox回归确认其为独立预后因素。
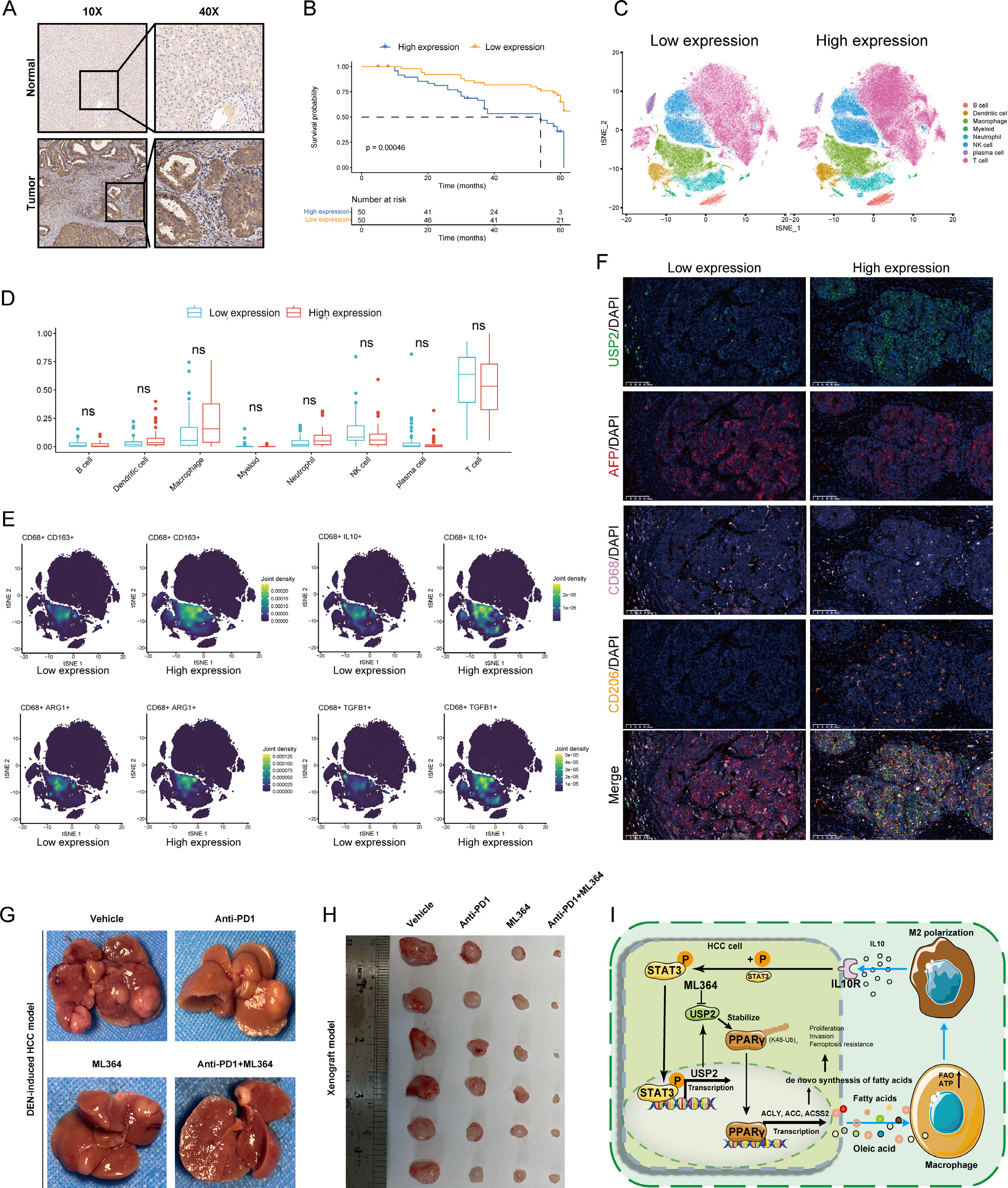
靶向USP2联合PD-1阻断增强抗肿瘤免疫
在DEN诱导HCC模型中,ML364联合抗PD-1抗体使肿瘤负荷较单药组进一步降低45%(P < 0.001),肿瘤内GZMB+ IFN-γ+ CD8+ T细胞浸润增加3.8倍(P < 0.001)。皮下移植瘤模型中,联合治疗组肿瘤重量较对照组减少82%(P < 0.001)。使用clodronate脂质体清除巨噬细胞后,USP2过表达的促肿瘤作用消失(P > 0.05),CD8+ T细胞功能恢复,证实USP2通过调控巨噬细胞影响免疫应答。
本研究系统阐明了USP2-PPARγ-油酸代谢轴在HCC进展与免疫抑制中的核心作用。USP2通过K48连接去泛素化稳定PPARγ K142位点,促进脂肪酸合成基因转录,导致油酸分泌增加。油酸作为代谢信号分子,增强巨噬细胞FAO推动M2极化,分泌的IL-10激活STAT3进一步上调USP2,形成正反馈环路。这一环路不仅驱动肿瘤代谢重编程,还抑制CD8+ T细胞功能,造成免疫逃逸。
本研究的临床意义在于:首先,USP2是HCC预后预测的生物标志物,高表达者需强化辅助治疗;其次,ML364联合ICIs显示协同效应,为克服免疫耐药提供新策略;最后,靶向代谢-免疫交互的联合方案代表精准治疗新方向。未来需开展ML364的临床转化研究,并探索USP2在复发监测中的应用价值。
Cao J, Chen K, Hu K, et al. USP2-mediated PPARγ stabilization promotes hepatocellular carcinoma progression and M2 macrophage polarization via oleic acid. J Immunother Cancer. 2025;13(11):e012721. Published 2025 Nov 4. doi:10.1136/jitc-2025-012721
审批号:CN-175729
审批时间:2025-12-23
有效期至:2026-12-23
声明:本材料由阿斯利康提供支持,仅供医疗卫生专业人士参考。
排版编辑:肿瘤资讯-李鑫











 苏公网安备32059002004080号
苏公网安备32059002004080号


