“沉舟侧畔千帆过,病树前头万木春”。以奥希替尼为代表的第三代表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)单药方案,虽已成为 EGFR 突变阳性晚期非小细胞肺癌(NSCLC)的标准治疗,但疗效仍有提升的空间。在此背景下,第三代 EGFR-TKI 联合治疗策略的优化、双特异性抗体(双抗)药物的广泛应用,均在为进一步提升这类患者的临床获益持续探索。耐药是疾病全程管理中的核心挑战,随着新药研发的推进及多种联合方案的不断探索,临床应对耐药的治疗手段日益丰富。本文将系统梳理 2025 年最新临床研究数据,重点阐述 EGFR 突变阳性晚期 NSCLC 一线及后线治疗的用药新进展,为临床实践提供参考。
一、EGFR 突变阳性 NSCLC 一线治疗盘点
(一)国内外指南一线治疗方案回顾
1. 2025 年非小细胞肺癌 CSCO 指南(Ⅳ 期 EGFR 敏感突变 NSCLC)
埃万妥单抗联合兰泽替尼的治疗方案被CSCO指南列为Ⅲ级推荐

2. NCCN NSCLC指南2026 V2(EGFR 外显子 19 缺失或 L858R 突变 NSCLC)
埃万妥单抗联合兰泽替尼的治疗方案被NCCN NSCLC指南推荐为首选(Preferred)

(二)EGFR 经典突变晚期 NSCLC 一线治疗新进展
1. EGFR/MET 双特异性抗体联合第三代 EGFR-TKI
MARIPOSA 研究是一项全球性随机对照 III 期临床试验,评估了EGFR/MET 双特异性抗体埃万妥单抗联合兰泽替尼一线治疗 EGFR 外显子 19 缺失(Ex19del)或 L858R 突变晚期 NSCLC 患者的疗效与安全性 [1,2]。
盲态独立中心审查(BICR)结果显示,埃万妥单抗联合兰泽替尼组的中位无进展生存期(mPFS)为23.7个月;亚洲亚组中,该联合方案的 mPFS 进一步提升至 27.5 个月[3,4]。中位随访 37.8 个月时,联合治疗组的中位总生存期(OS)尚未达到,但已[2] 展现出明确生存获益,mOS预计延长时间可超过一年,且生存曲线呈现 “长拖尾” 效应[5]。在刚刚结束的ESMO Asia 会议中更新了亚洲亚组OS数据,联合治疗组OS尚未达到,但已具有临床意义的显著获益[6]。
在脑转移患者中,联合治疗同样显示出显著临床获益:联合治疗组 icPFS 延长至 25.4 个月,3 年 icPFS 率达36%,中位颅内缓解持续时间(icDoR)亦达到35.7 个月[5]。在伴有脑转移、肝转移及 TP53 共突变等高风险因素亚组中,联合治疗组均展现出PFS 获益[7]。
机制层面,联合治疗改变了疾病生物学演化轨迹:治疗后 MET 扩增发生率显著降低(3.4% vs 13.1%, P=0.002),EGFR 继发耐药突变发生率亦明显下降(1.4% vs 7.6%, P=0.01)[8],这与使用其它三代EGFR TKI相比有着明显不同。安全性方面,联合治疗的不良事件(AE)以 1-2 级为主,且多发生于治疗前 4 个月。常见 AE 包括输液相关反应(IRR)、皮疹、甲沟炎及静脉血栓栓塞(VTE)等 [5];采用规范预防性管理策略(如 COCOON 研究探索的皮肤管理方案),可显著降低用药前12周的中重度 AE 发生率 [9-11],提高患者的生活质量并提升了用药依从性,令患者可以接受持续的、足量的治疗。
此外,PALOMA-2 研究队列 5 [12] 评估了皮下注射埃万妥单抗(Q4W)联合兰泽替尼的药代动力学、疗效及安全性,结果显示:研究者与独立审查中心评估的客观缓解率(ORR)分别为 82%(95% CI:71-90)和 87%(95% CI:77-94),经确认的 ORR 分别为 79%(95% CI:69-88)和 83%(95% CI:73-91);中位应答时间为 8.1 周(范围 7.0-16.5 周),目前中位 DoR、PFS 及 OS 尚未达到。
2. 化疗联合第三代 EGFR-TKI
FLAURA2 研究:评估奥希替尼联合含铂化疗一线治疗 EGFR 突变晚期 NSCLC 的疗效。最终 OS 分析显示,联合治疗组中位 OS 达 47.5 个月,较奥希替尼单药组(37.6 个月)提升 9.9 个月(HR=0.77)[13],为 EGFR 经典突变患者提供了另一种治疗选择。
ACROSS2 研究:聚焦伴有抑癌基因(如 TP53、RB1 等)共突变的 EGFR 突变阳性晚期患者,对比阿美替尼联合化疗与阿美替尼单药的疗效。中位随访 25.3 个月时,联合治疗组 mPFS 显著延长(19.8 个月 vs 16.5 个月,HR=0.55),OS 数据尚未成熟 [14]。该结果为这类预后相对较差的特殊人群提供了新的治疗方向。
3. 双抗 ADC 联合第三代 EGFR-TKI
BL-B01D1(Iza-Bren)是一款由 EGFR×HER3 双特异性抗体偶联而成的抗体偶联药物(ADC)。一项 II 期研究探索了其联合奥希替尼一线治疗 EGFR 敏感突变晚期 NSCLC 的潜力,初步数据显示该联合方案具有显著抗肿瘤活性:2.5 mg/kg 剂量组 ORR 达 100%,12 个月 PFS 率高达 92.1%;安全性方面,最常见 AE 为血液学毒性,整体可耐受 [15]。
(三)EGFR 非经典突变晚期 NSCLC 一线治疗新进展
EGFR 外显子 20 插入突变(Ex20ins)具有高度异质性,临床治疗难度较大。PAPILLON 研究证实,埃万妥单抗联合化疗一线治疗 EGFR Ex20ins 突变晚期 NSCLC 的疗效显著:联合治疗组 mPFS 较单纯化疗组延长 4.7 个月(11.4 个月 vs 6.7 个月),疾病进展或死亡风险降低 60%(HR=0.40, P<0.001)[16,17]。尽管对照组有 66% 的患者交叉接受埃万妥单抗治疗,中期 OS 分析仍显示联合治疗组存在明确获益趋势(HR=0.675)[17]。PALOMA-2 研究队列 2 的数据进一步验证了该联合方案的疗效,且皮下剂型埃万妥单抗联合化疗的安全性更优,给药相关反应(ARRs)发生率显著降低 [18]。
此外,一项 II 期临床试验初步探索了舒沃替尼联合安罗替尼治疗 EGFR Ex20ins 及其他非典型突变 NSCLC 的疗效,结果显示 ORR 达 84.6%,疾病控制率(DCR)为 100%,安全性可耐受 [19],为非经典突变患者提供了更多联合治疗选择。
二、EGFR 突变阳性 NSCLC 耐药后
治疗策略盘点
(一)国内外指南耐药后治疗方案回顾
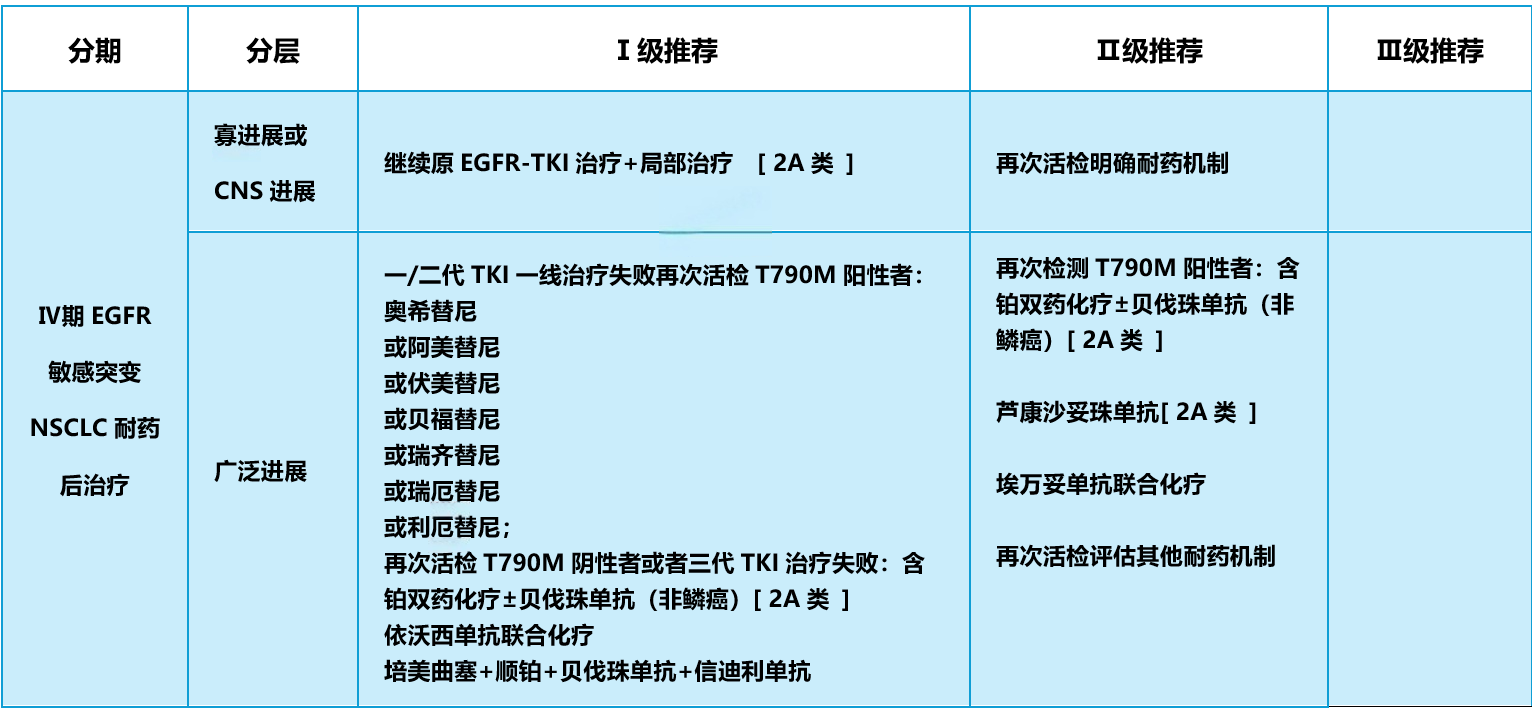
1. 2025 年非小细胞肺癌 CSCO 指南(IV 期 EGFR 敏感突变 NSCLC 耐药后)
埃万妥单抗联合化疗(铂类+紫杉醇)被CSCO指南列为Ⅱ级推荐
2. NCCN 指南 2026 V2(EGFR突变阳性 NSCLC 耐药后)
出现广泛进展时,埃万妥单抗联合化疗方案被NCCN NSCLC 指南列为首选(Preferred)

(二)耐药后关键治疗新进展
1. 双抗联合化疗
MARIPOSA-2 研究:一项 III 期、双盲、多中心随机对照临床研究,评估埃万妥单抗联合化疗(ACP 方案)在奥希替尼耐药患者中的疗效与安全性 [20-22]。结果显示,ACP 组 mPFS 较化疗组显著延长 4个月(8.2个月 vs 4.2 个月,HR=0.41, P<0.001);亚洲人群中,研究者评估的 ACP 组 mPFS 达10.3 个月(化疗组 4.2 个月,HR=0.39, P<0.0001),疾病进展和死亡风险降低 61%。客观缓解率方面,ACP 方案整体人群 ORR 达 64%,显著高于化疗组(36%);亚洲人群中 ACP 组 ORR 进一步提升至 66%[22]。中位随访 18.1 个月的二次期中分析显示,ACP 组中位 OS 较化疗组显著获益(HR=0.73,95% CI: 0.54-0.99,p=0.039)[20]。安全性方面,ACP 方案相关的 IRR、皮疹可通过预防性给药有效管理;PALOMA-2 和 PALOMA-3 研究数据显示,埃万妥单抗皮下注射剂可提升给药便利性,并降低 IRR 发生率 [23,24]。
HARMONi-A 研究:一项随机、双盲、多中心 III 期研究 [25],旨在评估 PD-1/VEGF 双特异性抗体依沃西单抗联合化疗,对比单纯化疗在 EGFR-TKI 经治失败的 EGFR 突变转移性 NSCLC 患者中的疗效与安全性。结果显示,依沃西单抗联合化疗可显著改善患者 mPFS(7.1 个月 vs 4.8 个月,HR=0.46),中位 OS 达 16.8 个月(HR=0.74),为 EGFR-TKI 耐药患者提供了新的免疫联合治疗选择。
2. 靶靶联合(针对明确耐药机制)
SAVANNAH 研究:II 期临床试验,评估赛沃替尼联合奥希替尼治疗奥希替尼一线经治后伴 MET 扩增和 / 或过表达的 NSCLC 患者的疗效与安全性 [26]。BICR 评估结果显示,联合治疗组 ORR 为 58%,显著高于对照组(16%);联合治疗组 mPFS 达 8.3 个月,对照组仅为 3.6 个月。在基线伴有 CNS 转移的患者中,联合治疗组确认的 CNS ORR 为 43%,对照组为 25%。安全性方面,联合治疗组≥3 级 AE 发生率为 57%,与 SACHI 研究结果一致。
3. ADC 药物
OptiTROP-Lung04 研究是一项全国多中心、随机、开放标签 III 期研究 [27],聚焦 EGFR-TKI 治疗失败但尚未接受含铂化疗的二线人群,对比芦康沙妥珠单抗与含铂化疗的疗效。结果显示:芦康沙妥珠单抗组 mPFS 为 8.3 个月,显著优于含铂化疗组(4.3 个月,HR=0.49,P<0.001),疾病进展或死亡风险降低 51%;但OS 数据尚未成熟。
总结
在 EGFR 突变晚期 NSCLC 的系统治疗演进中,第三代 EGFR-TKI 联合策略已成为突破现有疗效瓶颈的核心路径。对于 EGFR 经典突变患者,MARIPOSA 研究确立了埃万妥单抗联合兰泽替尼的 “去化疗” 联合方案,其在延长生存期、重塑耐药机制方面以及高危人群均看到显著优势,提示该模式有望成为未来一线治疗的重要方向;FLAURA2、ACROSS2 等研究则证实化疗联合第三代 EGFR-TKI 在广泛人群及特殊共突变人群中的价值。
在 EGFR 非经典突变领域,尤其是 Ex20ins 亚型,PAPILLON 研究证实埃万妥单抗联合化疗的关键治疗价值,填补了该人群的有效治疗空白;舒沃替尼联合安罗替尼等方案的初步数据亦显示出良好潜力。
耐药后治疗方面,MARIPOSA-2、HARMONi-A 等研究推动双抗联合化疗成为重要治疗选择;针对 MET 扩增等明确耐药机制的靶靶联合方案(如赛沃替尼 + 奥希替尼)展现出精准治疗优势;ADC 药物(芦康沙妥珠单抗)及免疫联合化疗 + 抗血管生成药物的探索,进一步丰富了耐药后治疗格局。
随着治疗范式的持续演进与创新药物的不断涌现,EGFR 突变晚期 NSCLC 的治疗正迈向更精准、个体化的阶段,患者的长期生存获益有望得到进一步延展与深化。
[1] Cho BC, et al. N Engl J Med. 2024;391(16):1486-1498.
[2] Cho BC, et al. 2023 ESMO. LBA14.
[3] Byoung C Cho, et al. N Engl J Med. 2024 Jun 26.
[4] Shun Lu, et al. 2023 ESMO Asia LBA10.
[5] James Chih-Hsin Yang, et al. ELCC 2025 4O.
[6] Hidetoshi Hayashi, et al. 2025 ESMO Asia 972O.
[7] Enriqueta Felip et al. 2024 ASCO Oral 8504.
[8] Hidetoshi Hayashi, et al. 2025 WCLC PT1.03.06.
[9] Girard N, et al. ELCC 2025 10MO.
[10] Byoung Chul Cho, et al. 2025 WCLC P3.12.46.
[11] Pei Jye Voon, et al. 2025 ESMO Asia. 991MO.
[12] Scott SC, et al. 2025 WCLC. MA.0805.
[13] David Planchard et al. 2025 WCLC PL02.06.
[14] Jie Wang et al, 2025 WCLC PL02.09.
[15] Fei Zhou et al, 2025 WCLC OA10.04.
[16] Caicun Zhou, et al. N Engl J Med. 2023 Nov 30;389(22):2039-2051.
[17] Ke-Jing Tang, et al. 2024 ASCO Abstract 8606.
[18] Sun Min Lim, et al. 2025 WCLC MA08.03.
[19] H. Shi et al. 2025 WCLC P3.12.43.
[20] Sanjay Popat, et al. 2024 ESMO LBA54.
[21] Passaro A, et al. Ann Oncol. 2024;35(1):77-90.
[22] Jin-Yuan Shih, et al. ESMO Asia. 2023. LBA11.
[23] Sun Min Lim et al. 2024 ASCO LBA 8612.
[24] Natasha B. Leighl, et al. 2024 ASCO. Oral LBA8505.
[25] Li Zhang, et al. SITC 2025 Presentation.
[26] Benjamin Levy, et al. 2025 ASCO, Abstract 8513.
[27] Zhang L, et al. OptiTROP-Lung04: A phase III study of sacituzumab govitecan versus platinum-pemetrexed chemotherapy in EGFR-mutant NSCLC after TKI failure. ESMO Presidential Symposium 2025
*截至发布日期
CRC Code:EM-196190
Approved Date: 2025-12-25
排版编辑:肿瘤资讯-Vickey
✅ “本资料仅用于医学、科学交流,可能涉及尚未在中国获批的产品和适应症。强生创新制药不支持、不鼓励任何未被批准的药品/适应症使用。”
✅ “本资料中涉及的AE/SS/PQC已按照公司的要求上报。”(适用于含AE/SS/PQC的资料)











 苏公网安备32059002004080号
苏公网安备32059002004080号


