引言:近年来,随着免疫检查点抑制剂的蓬勃发展,非小细胞肺癌(NSCLC)的治疗格局发生了深刻变革。免疫治疗从后线迈向前线,并进一步覆盖至围术期,为可手术切除的NSCLC患者带来了追求更高病理缓解率和更长生存期的希望。
CheckMate-816研究作为首个证实新辅助免疫联合化疗显著获益的III期临床研究,奠定了纳武利尤单抗联合化疗在NSCLC围术期治疗中的基石地位。本期肿瘤资讯特邀上海市胸科医院沈岚教授分享一例IIIA期(N2)肺鳞癌患者的诊疗经过。该患者经多学科团队(MDT)评估后,接受纳武利尤单抗联合化疗新辅助治疗,成功实施袖状切除术,并最终获得病理学完全缓解(pCR),为临床实践提供了宝贵的参考与启示。
上海市胸科医院肿瘤内科
毕业于上海交通大学医学院肿瘤学专业
长期从事胸部肿瘤疾病的诊断和治疗工作
CSCO青年专家委员会委员
中国胸部肿瘤研究协作组青年专家委员会(CTONG YOUNG)委员
《JCO中文版》青年编委
参与多项国内、国际多中心临床研究,并发表多篇SCI论文
病例介绍
基本情况
基本信息: 男性,54岁。
主诉: 因“间断咳嗽1个月,发现左上肺占位2周”入院。
既往史:高血压病史;青霉素过敏史。
个人史: 吸烟史20年,600支/年,戒烟2周,无饮酒史;工作及生长环境中无化学毒物接触史,无放射性物质接触史。
家族史: 家人体健。无传染病情况。无家族遗传性病史。
辅助检查
胸部CT(2021/11/03): 左肺占位,考虑恶性病变;左肺上叶炎性改变,左肺门淋巴结增大。
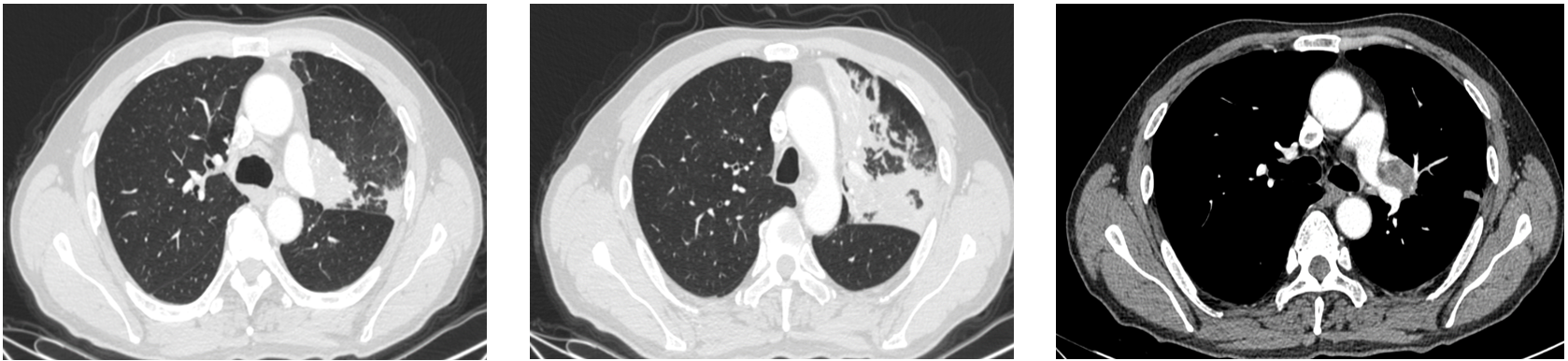
PET-CT(2021/11/10): 左肺上叶近肺门处占位(4.2x3.5cm),伴左肺上叶多发高密度影,FDG代谢增高;右肺中叶实性小结节,FDG代谢不高,考虑炎性结节可能;纵隔内(4L、8区)和左肺门淋巴结增大,FDG代谢增高。双侧胸膜局部增厚。
头颅MRI/骨扫描: 未见异常。
肺功能(2021/11/10 ):通气功能示气道阻塞,弥散功能正常,气道大致阻力正常。
心脏超声(2021/11/10 ):升主动脉增宽左室各节段收缩活动未见明显异常,左室舒张功能未见明显异常。
血常规:正常 凝血机制:正常
肝肾功能电解质:正常
肿瘤标志物:癌胚抗原 2.37ng/ml ,细胞角蛋白19片段:3.63ng/ml ,鳞状上皮细胞癌抗原:0.46ng/ml,神经元特异烯醇化酶 21.15ng/ml ,糖类抗原125:39.03U/ml↑, 胃泌素释放肽前体:41.32pg/ml。
ECG:正常
查体:神清,气平,锁骨上淋巴结未及肿大,双肺呼吸音清,未及罗音心率83次/分,律齐,未及杂音,腹软,肝脾肋下未及,神经系统(-)
EBUS-TBNA(2021/11/13):左上肺支气管开口新生物,余管腔通畅
病理及分子检测
病理:(左上叶新生物)鳞癌;(4L组淋巴结细胞块)鳞癌。
分子病理: 未见驱动基因突变。
PD-L1表达: 10%。
临床诊断
支气管肺癌(原发性 中央型 左肺 鳞癌);c-T2N2M0 IIIA期;PS 1分;PD-L1低表达(10%)。
治疗经过
MDT多学科会诊:依据CheckMate-816研究模式,决定行免疫联合化疗新辅助治疗。新辅助治疗:2021.11.16开始接受纳武利尤单抗(360mg)+白蛋白紫杉醇+卡铂方案治疗,每3周一次,共完成3个周期。
新辅助治疗疗效评估:
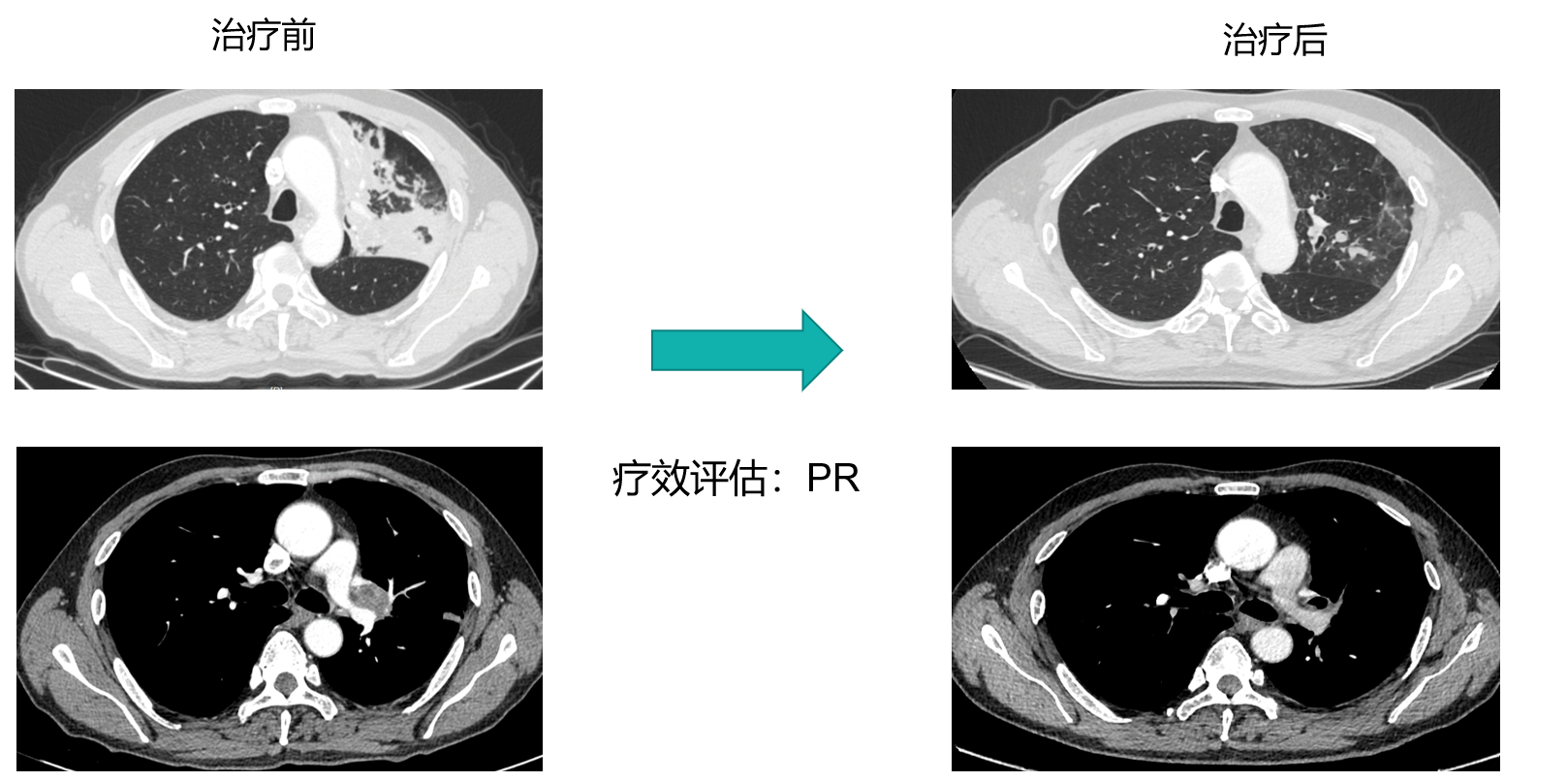
影像学评估: 治疗后复查胸部CT(2022/1/6)显示左肺门占位较前范围缩小(1.2x1cm),左肺门淋巴结缩小,炎性改变明显好转。疗效评估为部分缓解(PR)。
气管镜检查: 左上叶支气管开口黏膜充血水肿消退,管腔通畅。
手术及术后病理
手术实施: 2022年1月12日,患者在全麻下行胸腔镜下左肺上叶切除术(袖状切除)+淋巴结清扫术。手术过程顺利,未发生治疗相关不良反应,手术难度因肿瘤显著退缩而降低。
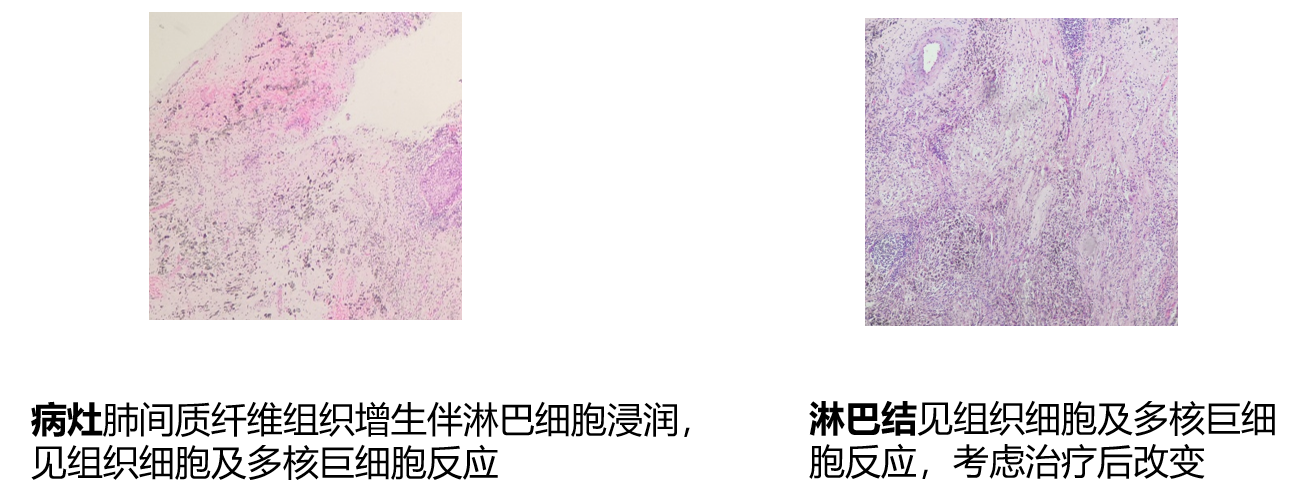
术后病理:左上叶袖形切除标本。镜下见纤维组织增生、伴淋巴细胞及浆细胞浸润,结合病史,符合治疗后改变,未见肿瘤残留,瘤床大小1.5x0.7x0.7(cm)。支气管上、下切端阴性。淋巴结(4L、5、6、7、8、9、10、11)共8组慢性炎,未见肿瘤。疗效评估pCR(病理学完全缓解)。
术后管理与随访:术后予以两次纳武利尤单抗联合白蛋白紫杉醇+卡铂;后纳武利尤单抗单药治疗一年于2023.3结束,期间出现甲状腺功能紊乱、对症治疗后稳定可控。后患者定期随访复查,疾病稳定。
专家点评
沈岚教授:本例患者为54岁男性,初诊即为IIIA期(N2)中央型肺鳞癌,属于局部晚期肺癌,治疗难度较大。MDT讨论制定了基于免疫联合化疗的新辅助治疗策略。患者在接受3周期纳武利尤单抗联合含铂双药化疗后,影像学显示肿瘤显著缩小,达到PR。后顺利实施了肺叶袖状切除术,无术中及术后不良并发症,最大程度保留了肺功能。术后病理提示原发灶及清扫淋巴结均无肿瘤残留,达到了pCR。这一结果不仅验证了该方案的卓越疗效、极大提高了生活质量,预示着良好的长期生存。
多学科诊疗(MDT)是局部晚期NSCLC治疗决策的关键
对于III期NSCLC患者,特别是N2期患者,治疗方案的选择往往充满挑战。是直接手术、同步放化疗还是围手术期治疗,需要综合考量。本病例中,MDT团队发挥了至关重要的作用。首先,基于影像学评估确认了病灶的“潜在可切除性”;然后结合最新指南与循证医学证据,为患者量身定制了围手术期治疗方案。MDT模式确保了诊疗的规范化与个体化,是可切除转化为完全切除(R0切除)的重要保障。
CheckMate-816奠定围术期治疗的标准地位
本病例的成功主要得益于CheckMate-816研究模式的应用。作为首个证实新辅助免疫联合化疗显著获益的III期研究,CheckMate-816研究确立了纳武利尤单抗联合化疗在可切除NSCLC新辅助治疗中的标准地位。最新随访数据显示,纳武利尤单抗联合化疗组的5年OS率高达65%,显著优于单用化疗组的55%;5年EFS率更是达到49% vs 34%。尤其值得注意的是,该方案在不同PD-L1表达水平(包括<1%人群)和不同组织学类型(鳞癌与非鳞癌)中均显示出一致的获益。本例PD-L1低表达的鳞癌患者获得pCR,正是这一广泛适用性的生动体现。该患者整个治疗期间未发生严重不良反应,手术难度未因新辅助治疗而增加,反而因肿瘤退缩变得更为可控。这一成功实践再次印证了免疫新辅助治疗在局部晚期NSCLC中的巨大潜力,为改善此类患者的长期预后提供了强有力的循证医学支持。随着随访时间的延长,我们期待该患者能获得长久的无瘤生存。
pCR是预测长期生存获益的“金标准”
本例患者经过 3 周期纳武利尤单抗联合化疗的新辅助治疗后,术后病理显示原发灶达到病理完全缓解(pCR),在新辅助治疗中,pCR被视为评估疗效和预测预后的重要早期指标。CheckMate-816研究的探索性分析表明,达到pCR的患者长期生存优势显著。在纳武利尤单抗联合化疗组中,达到pCR的患者5年OS率高达95%,5年EFS率高达88%,且疾病复发或死亡风险大幅降低。这意味着一旦患者通过新辅助治疗达到pCR,其实现“临床治愈”可能性进一步提高。
排版编辑:Niko











 苏公网安备32059002004080号
苏公网安备32059002004080号


