神经内分泌癌(NEC)作为神经内分泌肿瘤中分化差、恶性度高的亚型,其进展迅速、治疗棘手,对临床医生的诊断和治疗策略提出了严峻的挑战。本文分享一例胃神经内分泌癌伴肝转移的病例,详细介绍其诊断、治疗、及多学科讨论的全过程,旨在探讨此类高度恶性肿瘤的二线治疗策略选择、免疫治疗的潜在价值及生物标记物的指导意义,以期为临床实践提供借鉴与启示。
病例介绍
患者基本情况:男性,56岁。
主诉:胃神经内分泌癌肝转移
外院诊疗经过:患者于2022年10月体检时,MRI示:肝右叶占位,直径2.5cm。
18F-FDG-PET/CT示:肝右叶占位,FDG高代谢。
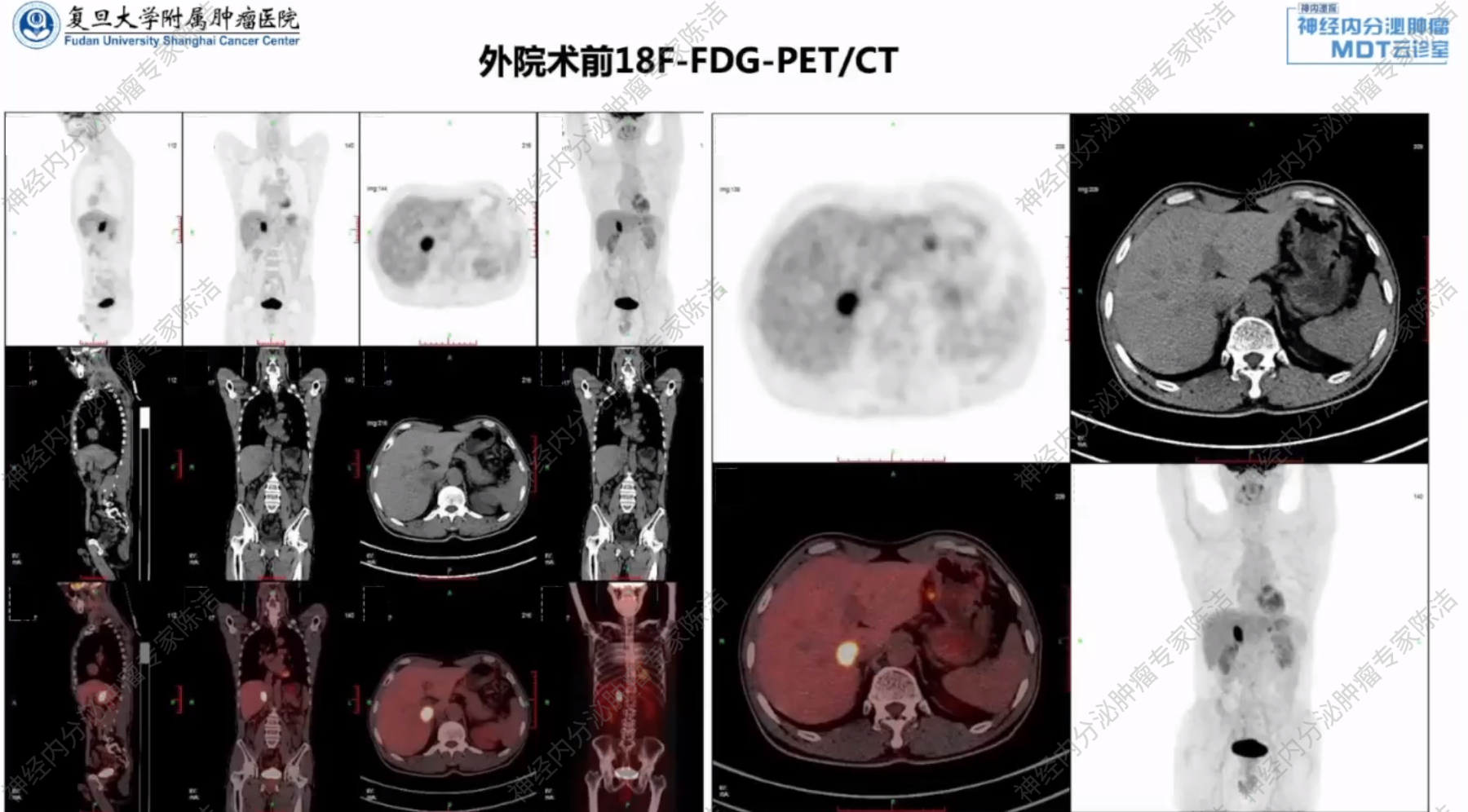
胃镜示:胃角黏膜凹陷,大小1.5cm,周围黏膜水肿;胃镜活检病理:中低分化腺癌。
患者于2022年10月27日在外院行“右肝肿瘤+胆囊切除术”,肝右叶术后病理:NET G3,3.5cm,核分裂>20/10HPF,Hep-1-, GPC3-, GS-, CK7-, Muc-1+, CD34+, CgA+, CD56部分+, Syn+, INSM1个别+, Ki-67 80%。
随后于2022年11月17日在外院行“胃大部切除术”,胃切除术后病理:NET G3, Ki-67 70%, Syn+, CD56部分+, P53缺失。
术后于2022年12月5日开始接受EP方案(依托泊苷+铂类)化疗3周期。
2023年1月外院复查MRI示:肝右后叶转移。
我院诊疗经过:为求进一步诊治,患者于2023年1月至我院就诊。
我院病理会诊:胃考虑为神经内分泌癌,肝右叶符合神经内分泌癌转移。

基因检测:PD-L1 CPS<1, TPS<1%,微卫星状态稳定(MSS),肿瘤突变负荷(TMB) 3.59Mut/Mb,CD8阳性浸润T淋巴细胞(CD8TILs) 653pcs/mm²。
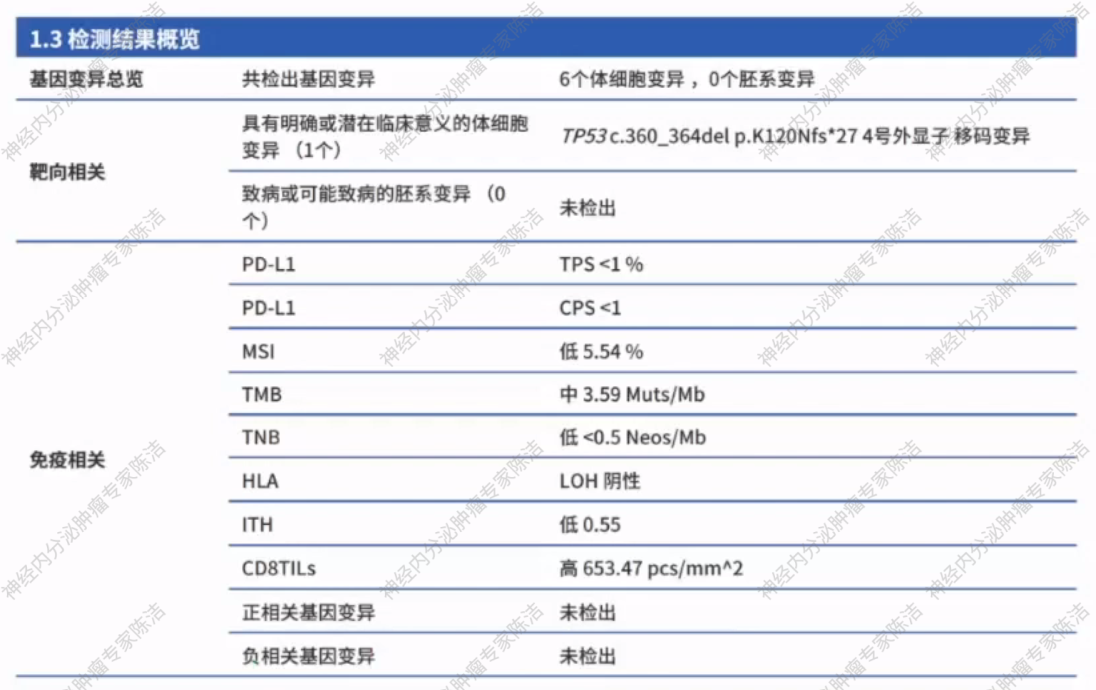
综合考虑患者为胃NEC,一线含铂方案治疗失败,且肿瘤微环境中CD8+ T细胞浸润密度高,提示可能对免疫治疗敏感。经MDT讨论后,于2023年2月18日开始行FOLFOX方案化疗联合PD-1单抗(斯鲁利单抗)治疗。
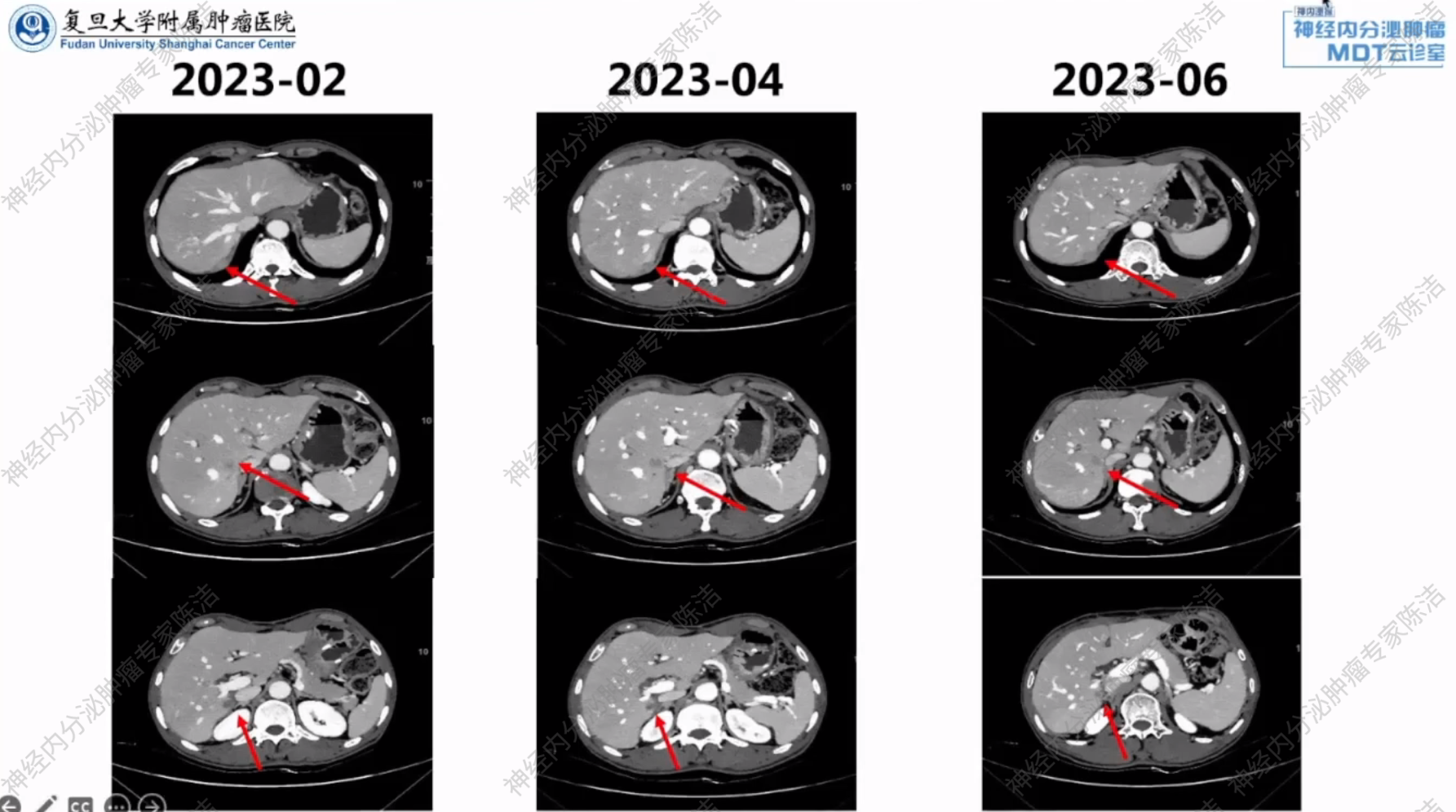
疗效评估:2023年4月(治疗4周期后):复查CT及MRI,疗效评估为疾病稳定(SD)。遂继续FOLFOX方案化疗联合斯鲁利单抗治疗。
2023年6月(继续治疗4周期后):再次复查CT及MRI,疗效评估为SD。

多学科团队(MDT)讨论
病理科李媛教授:本病例的Ki-67指数高(70%~80%),结合外院病理提示P53缺失,符合分化差的NEC,而非分化好的NET G3,这一鉴别诊断至关重要。在免疫治疗方面,虽然PD-L1和TMB等常规标志物不支持,但本例患者的CD8+ T细胞浸润密度相对较高,提示其属于“免疫浸润型”或“炎性”肿瘤微环境,这为联合免疫治疗提供了重要依据。
放射诊断科汤伟教授:从2023年2月至6月的系列影像对比来看,患者肝脏的转移灶在接受FOLFOX联合斯鲁利单抗治疗后,大小及形态保持稳定,部分病灶甚至有轻微缩小。证实了疾病得到了有效控制,疗效评估为SD。
核医学科徐俊彦教授:患者术前的18F-FDG PET/CT检查充分显示了病灶的糖代谢特征。对于Ki-67指数如此之高的NEC,肿瘤细胞增殖活跃,糖代谢也高,因此,FDG PET/CT是评估全身肿瘤负荷和病变范围的最佳选择。这类肿瘤的生长抑素受体(SSTR)通常为阴性,即使表达,其疾病进展速度也远非生长抑素类似物所能控制,故无需进行68Ga-SSTR PET/CT扫描。
陈洁教授总结
这是一例颇具启发性的胃神经内分泌癌病例。患者在一线含铂标准化疗方案快速进展后,面临着严峻的治疗挑战。
在二线治疗的决策上,虽然肿瘤PD-L1阴性、MSS以及低TMB状态,但肿瘤CD8+ T细胞浸润密度这一重要生物标志物发现较高的CD8+ T细胞浸润,提示肿瘤微环境中存在免疫应答的基础。基于此,我们选择了FOLFOX化疗联合斯鲁利单抗的化疗联合免疫治疗的策略。在近6个月的治疗期间,患者肿瘤保持稳定,这对于侵袭性强、二线治疗选择有限的胃NEC而言,实属不易。
此病例提醒我们,对于胃肠胰神经内分泌癌这类免疫治疗数据尚不充分的瘤种,不能完全依赖传统的生物标志物。深入探索肿瘤免疫微环境特征,如CD8+ T细胞浸润情况,可能为筛选潜在的免疫治疗获益人群提供重要参考依据。该案例为化疗联合免疫疗法在晚期胃NEC二线治疗中的应用提供了实践经验和探索方向。
更多精彩病例,可点击或复制以下链接,粘贴到浏览器查看神经内分泌肿瘤MDT云诊室-神经内分泌肿瘤免疫治疗专场回放:
https://doctor.liangyihui.net/#/doc/113808

本文仅供健康科普使用,不能作为诊断、治疗的依据,请谨慎参阅。












 苏公网安备32059002004080号
苏公网安备32059002004080号


