第28届中国临床肿瘤学会(CSCO)学术年会于2025年9月10日至14日在山东济南成功举办。本届年会以“规范诊疗,创新引领”为主题,汇聚全球肿瘤领域知名专家学者,分享前沿研究成果与临床经验,促进学术交流与合作,积极开展肿瘤学继续教育。在9月11日的NSCLC免疫治疗专场,陆军军医大学第二附属医院朱波教授分享《
肺癌免疫治疗困境与方向》的精彩汇报,【肿瘤资讯】特此整理,以飨读者。

肺癌免疫治疗现状和困境
肺癌免疫治疗已成为肺癌治疗的基石,具有全人群覆盖和全周期覆盖的特点。在非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)治疗中,免疫治疗展现显著疗效,相关临床试验如KEYNOTE系列、IMpower系列等为治疗方案的制定提供重要依据。
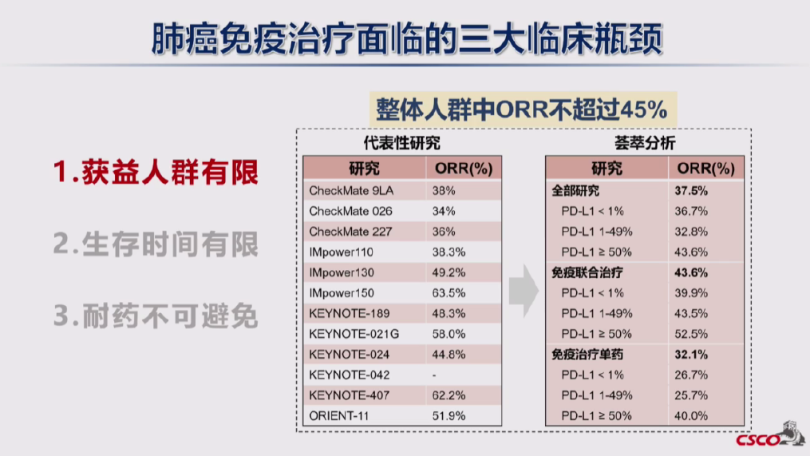
然而,肺癌免疫治疗仍面临三大临床瓶颈:
获益人群有限:整体人群中客观缓解率(ORR)不超过45%。不同研究结果显示,ORR在34%至63.5%之间波动,且PD-L1表达水平对疗效有显著影响。例如,CheckMate 9LA研究中ORR为38%,而KEYNOTE-024研究中ORR为44.8%。
生存时间有限:鳞癌患者的无进展生存期(PFS)为5.5-8.5个月,总生存期(OS)为18-25个月;非鳞癌患者的PFS为8.3-11个月,OS为19-25个月。即使在联合治疗方案中,生存期的延长仍有限。
耐药不可避免:免疫治疗耐药的决定因素包括宿主内源性因素(如肿瘤微环境、T细胞功能等)和宿主外源性因素(如环境暴露、生活方式等)。研究表明,肿瘤微环境中的免疫抑制细胞(如Tregs、MDSCs)和代谢产物(如腺苷、乳酸)均可能影响免疫治疗效果。
肺癌免疫治疗前沿进展
新型免疫治疗药物的研发为肺癌治疗带来新的希望。以下几类药物成为研究热点:
双特异性抗体(BsAbs):超过150项双特异性抗体临床试验在肺癌中开展,部分药物已获批肺癌适应症。例如,靶向PD-1×VEGFA的依沃西单抗在NSCLC一线和二线治疗中均显示出显著疗效,分别降低疾病进展风险49%和54%。此外,靶向PD-1×CTLA-4的抗体也显示出良好的耐受性和协同增效作用。
T细胞衔接器(TCE):如DeLLphi-301和DeLLphi-304研究显示,塔拉妥单抗在治疗经治SCLC患者中取得良好效果,10mg和100mg剂量组的中位OS分别为13.6个月和11.6个月。TCE通过桥接肿瘤抗原和T细胞受体,激活T细胞杀伤肿瘤细胞,展现独特的治疗机制。
T细胞调控因子:IL-2α-bias激动剂在免疫治疗耐药的肺癌患者中展现显著的抗肿瘤活性,鳞癌患者ORR达36.7%,腺癌患者ORR达24%。通过精准调控IL-2信号通路,可有效激活CD8+ T细胞并减少调节性T细胞(Tregs)的活化。
抗体偶联药物(ADC)联合免疫治疗:芦康沙妥珠(TROP2 ADC)联合塔戈利(PD-L1)一线治疗进展期NSCLC患者取得积极结果,队列1A的ORR为40%,PFS达15.4个月;队列1B的ORR高达67.7%。ADC药物通过将细胞毒性药物精准递送至肿瘤细胞,显著提升治疗效果并降低系统性毒性。
新药研发的启示与思考
新型免疫治疗药物的研发为肺癌治疗提供新的思路,但也暴露出一些问题:
双特异性抗体的减毒增效:αPD-1-αVEGFA抗体显著提升疗效,αPD-1-αCTLA-4抗体则降低毒性。研究显示,联合靶向VEGFA可改善肿瘤血管功能,增强免疫细胞浸润;而靶向CTLA-4可协同增强T细胞活化,同时减少免疫相关不良事件。
T cell engager药物的局限性:包括无效衔接、未考虑其他免疫成分的作用以及靶点选择有限等。当前TCE多以CD3为靶点,易与CD4+ T辅助细胞、调节性T细胞等建立无效衔接,导致治疗效果受限。
细胞因子改造的优化策略:强α激动IL2(IL2α-bias)能够有效激活CD8+ T细胞,提升抗肿瘤免疫反应。通过纳米技术或基因工程改造IL-2分子,可进一步优化其药代动力学特性和组织分布,增强局部治疗效果。
新药研发需关注前沿方向
细胞生态靶向药物:靶向“细胞生态”的新型免疫治疗策略,如αPD-1-DNase1L3药物,通过调节肿瘤免疫微环境增强治疗效果。研究表明,DNase1L3可降解肿瘤细胞释放的核糖核酸,减轻免疫抑制并促进T细胞功能恢复。
增强内源性T细胞功能:通过过表达CD200增强T_pex存续能力,提升免疫治疗疗效。CD200在肿瘤微环境中可抑制免疫细胞活化,而通过基因编辑或药物干预调节CD200表达,可有效增强耗竭前体T细胞(T_pex)的功能和持久性。
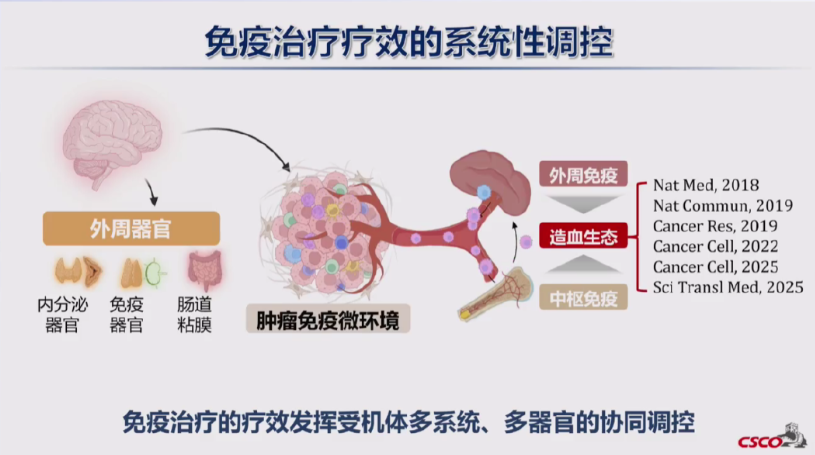
系统性调控免疫治疗疗效:免疫治疗的疗效受机体多系统、多器官的协同调控,未来研发应关注整体免疫调控机制。例如,肠道菌群、中枢神经系统、内分泌系统等均可能通过免疫代谢、神经免疫等途径影响肿瘤免疫微环境。
免疫治疗转化研究的范式革新
以临床问题为驱动的肿瘤免疫治疗研究新范式,正助力新靶点发现与创新药物研发,推动精准免疫治疗加速落地。其核心内涵包括:
基础与临床深度融合:从实验室到临床应用的转化过程中,强调多学科交叉合作,整合基础研究与临床资源,构建“从患者中来,到患者中去”的研究闭环。
全程动态观察与精准诊疗:通过聚焦个体、聚焦队列和动态监测,实现对疾病发生、发展及治疗响应的全程追踪,为个性化治疗方案的制定提供依据。
学科交叉融合与创新:打破单一学科局限,促进免疫学、肿瘤学、生物信息学、药学等多学科协同创新,探索新型治疗技术与策略。
注:本文图源CSCO照片直播及大会直播
排版编辑:肿瘤资讯-Bear











 苏公网安备32059002004080号
苏公网安备32059002004080号


