编译:肿瘤资讯
在亚洲非小细胞肺癌(NSCLC)患者中,表皮生长因子受体(EGFR)的突变率高达40-60%[1-3]。EGFR酪氨酸激酶抑制剂(EGFR-TKIs)的问世,极大地改变了EGFR突变阳性晚期NSCLC患者的治疗模式[4-6]。以奥希替尼为代表的第三代EGFR-TKI,作为一线治疗方案,显著延长了患者的无进展生存期(PFS)[7-9]。然而,获得性耐药的出现仍是不可避免的临床挑战,限制了患者的长期获益[10]。当前,应对奥希替尼耐药的研发方向主要包括开发第四代EGFR-TKI、EGFR-MET双特异性抗体,以及探索创新的联合治疗方案[11]。在这些新兴疗法中,抗体药物偶联物(ADC)作为一种新型的靶向治疗药物,为攻克三代TKI耐药难题带来了新的曙光,有望重塑耐药后的治疗格局。基于此,本文旨在结合最新的专家共识与前沿研究进展,系统性地探讨EGFR-TKI耐药后的ADC的临床应用价值。
ADC药物概述
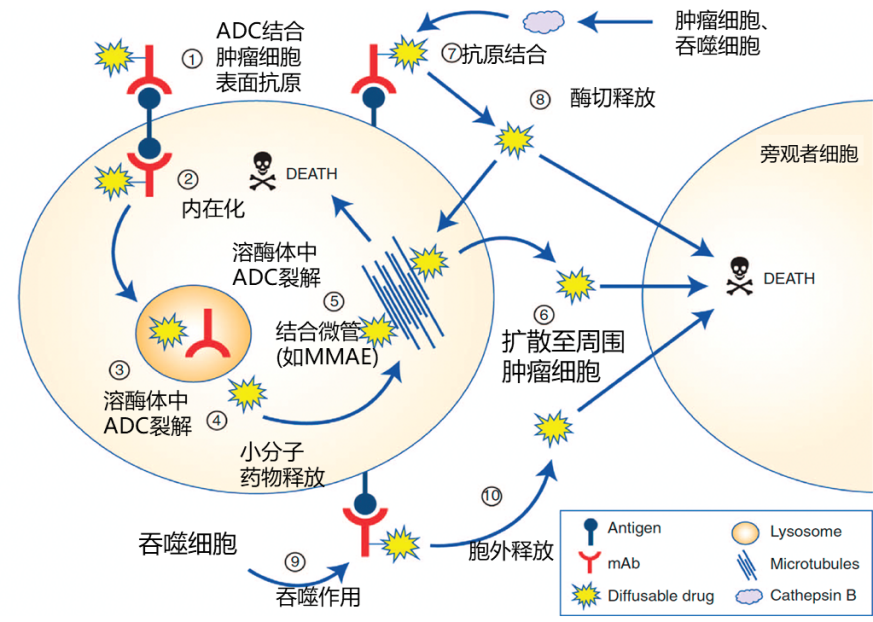
ADC药物是一种精密的靶向治疗制剂,它由三部分构成:一个能特异性识别人类肿瘤细胞表面抗原的单克隆抗体、一个高活性的小分子细胞毒性药物(即“有效载荷”)以及一个将两者稳定连接在一起的连接子(图1)。其作用机制如同“生物导弹”:单克隆抗体部分负责精准“导航”,将药物导向并结合至癌细胞表面的特定靶点;随后,癌细胞会将ADC复合物内吞,并在溶酶体内通过连接子的断裂释放出高活性的细胞毒性药物,从而在肿瘤内部实现“精准爆破”[12]。
这种设计赋予了ADC药物高靶向性和强杀伤力的双重优势。此外,一些先进的ADC药物(如德曲妥珠单抗)还具有强大的“旁观者效应”,即释放的细胞毒性药物可以穿透细胞膜,杀伤邻近的不表达靶点抗原的肿瘤细胞,从而克服肿瘤异质性[13]。这使其成为极具潜力的抗癌“魔法子弹”。
重塑TKI耐药后治疗格局的ADC药物
在三代EGFR-TKI耐药后,多种复杂的耐药机制被揭示,包括EGFR通路依赖的“靶内耐药”(如C797S突变)和旁路激活等“靶外耐药”机制(如MET或HER2扩增)[14, 15]。ADC通过攻击耐药后异常激活的旁路信号通路上的靶点,来绕开EGFR通路的限制[16]。
靶向HER2的ADC药物:德曲妥珠单抗 (T-DXd)
HER2(人表皮生长因子受体2)扩增或突变是EGFR-TKI耐药的机制之一[17]。HER2与HER3的异二聚化可以持续激活下游信号通路,导致对EGFR抑制剂的耐药[13]。T-DXd是一种靶向HER2的ADC药物。在关键的II期临床研究DESTINY-Lung02中,T-DXd用于治疗既往接受过系统治疗的HER2突变不可切除或转移性NSCLC患者。研究结果显示,接受德曲妥珠单抗 5.4 mg/kg 和 6.4 mg/kg 治疗的 HER2 突变转移性 NSCLC 患者,经盲法独立中心审查(BICR)确认的客观缓解率(cORR)分别为 50.0% 和 56.0%,中位缓解持续时间(DoR)分别为 12.6 和 12.2 个月,中位无进展生存期(PFS)分别为 10.0 和 12.9 个月,中位总生存期(OS)分别为 19.0 和 17.3 个月[18]。
在安全性方面,5.4和6.4 mg/kg组分别有40/101例(39.6%)和30/50例(60.0%)患者发生≥ 3级药物相关治疗期间出现的不良事件 (TEAE),其中最常见的不良事件为恶心(发生率分别为67.3% [68/101] 和 82.0% [41/50])。经独立委员会裁定的药物相关间质性肺疾病 (ILD) 的发生率分别为14.9% (15/101) 和 32.0% (16/50),大部分为1级或2级;每个治疗组各有1例5级事件发生[18]。
靶向TROP-2的ADC药物:德达博妥单抗 (Dato-DXd)
TROP-2(滋养层细胞表面抗原2)是在包括NSCLC在内的多种实体瘤中广泛高表达的蛋白。Dato-DXd 是一种以TROP-2为靶点的ADC药物。全球多中心的III期注册临床研究TROPION-Lung01纳入既往经治的伴或不伴可靶向基因改变(AGA)的局部晚期/转移性 NSCLC 患者,评估 Dato-DXd(6 mg/kg Q3W)单药治疗对比多西他赛的疗效和安全性。结果显示,与多西他赛组相比,Dato-DXd组显著改善了患者的PFS[12]。II期研究TROPION-Lung05则专门评估了Dato-DXd在经靶向治疗和化疗后进展的、携带AGA的晚期NSCLC患者中的疗效。在EGFR突变亚组中,确认的ORR为43.6%,mPFS达到5.8个月,既往接受过奥希替尼治疗的 EGFR 突变或 T790M 突变患者的 ORR 可达 49.1%进一步证实了其治疗潜力[19]。
在安全性方面,TROPION-Lung05研究中,28.5%的患者发生≥3级治疗相关不良事件(TRAE)。 最常见的TRAE为口腔炎(56.2%; ≥3级:9.5%)。 5例(3.6%)患者发生治疗相关间质性肺病/肺炎,1例(0.7%)为5级事件[19]。
靶向TROP-2的ADC药物:芦康沙妥珠单抗 (Sac-TMT)
OptiTROP-Lung03研究是一项开放标签、随机、多中心注册研究,旨在评估芦康沙妥珠单抗对比多西他赛在经EGFR-TKI和含铂化疗后进展的晚期EGFR突变NSCLC患者中的疗效和安全性。研究结果显示,经BIRC评估,芦康沙妥珠单抗组ORR达45.1%,显著高于多西他赛组的15.6%。疾病控制率(DCR)方面,芦康沙妥珠单抗组为82.4%,多西他赛组为60.0%。BIRC评估的mPFS分别是6.9个月和2.8个月。校正后,多西他赛组的mOS为9.3个月,芦康沙妥珠单抗组仍未达到;12个月OS率芦康沙妥珠单抗组为72.8%,多西他赛组为43.2%[20]。
安全性方面,治疗暴露的中位持续时间芦康沙妥珠单抗组为5.0个月,多西他赛组为2.8个月。芦康沙妥珠单抗组3级及以上TRAEs和严重TRAEs的发生率均低于多西他赛组。芦康沙妥珠单抗组无TRAEs导致停药和死亡的患者,且未报告间质性肺病[20]。
靶向HER3的ADC药物:Patritumab Deruxtecan (HER3-DXd)
HER3(人表皮生长因子受体3)在EGFR突变NSCLC中普遍表达,并与TKI耐药密切相关[16][21]。Patritumab deruxtecan (HER3-DXd) 是一种靶向HER3的ADC药物。关键的II期研究HERTHENA-Lung01评估了HER3-DXd在接受过EGFR-TKI和铂类化疗的EGFR突变NSCLC患者中的疗效。研究结果显示,ORR为29.8%,mPFS为5.5个月,mOS为11.9个月[22]。HER3-DXd的安全性特征可管理且可耐受,与既往观察结果一致。这些发现表明,HER3-DXd对于经多线治疗的EGFR突变NSCLC患者是一种有潜力的治疗选择。
结论与展望
ADC药物的崛起,为三代EGFR-TKI耐药后的NSCLC患者提供了强有力的治疗新选择[11]。无论是通过靶向HER2、TROP-2还是HER3,ADC药物都在临床研究中展现了令人鼓舞的疗效,真正意义上重塑了耐药后的治疗格局。然而,ADC药物的应用仍面临挑战,如如何通过生物标志物(如靶点表达水平)精准筛选获益人群、优化给药剂量以平衡疗效与毒性(如间质性肺病等)、以及探索ADC药物与其他疗法(如免疫治疗、新型TKI)的联合应用策略等。随着对耐药机制理解的不断深入和更多临床研究的开展,我们有理由相信,以ADC为代表的“魔法子弹”将在未来的肺癌精准治疗领域扮演越来越重要的角色,为更多患者带来生存希望。
排版编辑:肿瘤资讯-明小丽
[1] Zhang YL, Yuan JQ, Wang KF, et al. The prevalence of EGFR mutation in patients with non-small cell lung cancer: a systematic review and meta-analysis. Oncotarget, 2016 7(48):78985-78993.
[2] Araki T, Kanda S, Horinouchi H, Ohe Y. Current Treatment Strategies for EGFR-mutated Non-Small Cell Lung Cancer: From First Line to Beyond Osimertinib Resistance. Japanese Journal of Clinical Oncology. 2023;53(7):547-561.
[3] Zhou X, Zeng L, Huang Z, et al. Strategies Beyond 3rd EGFR-TKI Acquired Resistance: Opportunities and Challenges. Cancer Medicine. 2025;14(9):e70921.
[4] Qiu MZ, Zhang Y, Guo Y, et al. Evaluation of Safety of Treatment With Anti–Epidermal Growth Factor Receptor Antibody Drug Conjugate MRG003 in Patients With Advanced Solid Tumors: A Phase 1 Nonrandomized Clinical Trial. JAMA Oncology. 2022;8(7):1042-1046.
[5] Hsu R, Benjamin DJ. A Narrative Review of Antibody-Drug Conjugates in EGFR-mutated Non-Small Cell Lung Cancer. Frontiers in Oncology. 2023;13:1252652.
[6] Phillips AC, Boghaert ER, Vaidya KS, et al. ABT-414, an Antibody-Drug Conjugate Targeting a Tumor-Selective EGFR Epitope. Molecular Cancer Therapeutics. 2016;15(4):661-9.
[7] Lu S, Dong X, Jian H, et al. AENEAS: a randomized phase III trial of aumolertinib versus gefitinib as first-line therapy for locally advanced or Metastatic Non-small-cell lung cancer with EGFR exon 19 deletion or 1858R mutations. J Clin Oncol, 2022:40(27):3162-3171.
[8] Shi Y, Chen G, Wang X, et al. Furmonertinib (AST2818) versus gefitinib as first-line therapy for Chinese patients with locally advanced or metastatic EGFR mutation-positive non-small-cell lung cancer (FURLONG): a multicentre, double-blind, randomised phase 3 study. Lancet Respir Med. 2022:10(11):1019-1028.
[9] Soria JC, Ohe Y, Vansteenkiste J, et al. Osimertinib in untreated EGFR-mutated advanced non-small-cell lung cancer. N Engl J Med. 2018:378(2):113-125.
[10] Santos EDS, Nogueira KAB, Fernandes LCC, et al. EGFR Targeting for Cancer Therapy: Pharmacology and Immunoconjugates With Drugs and Nanoparticles. International Journal of Pharmaceutics. 2021;592:120082.
[11] Johnson M, Garassino MC, Mok T, Mitsudomi T. Treatment Strategies and Outcomes for Patients With EGFR-mutant Non-Small Cell Lung Cancer Resistant to EGFR Tyrosine Kinase Inhibitors: Focus on Novel Therapies. Lung Cancer (Amsterdam, Netherlands). 2022;170:41-51.
[12] Ahn M, Lisberg A, Paz-Ares L, et al. LBA12 Datopotamab deruxtecan (Dato-DXd) vs docetaxel in previously treated advanced/metastatic (adv/met) non-small cell lung cancer (NSCLC): results of the randomized phase III study TROPION-Lung01. Ann Oncol. 2023:34:S1305-S1306.
[13] Yonesaka K. HER2-/HER3-Targeting Antibody-Drug Conjugates for Treating Lung and Colorectal Cancers Resistant to EGFR Inhibitors. Cancers. 2021;13(5):1047.
[14] Leonetti A, Sharma S, Minari R, Perego P, Giovannetti E, Tiseo M. Resistance mechanisms to osimertinib in EGFR-mutated non-small cell lung cancer. Br J Cancer. 2019 121(9):725-737.
[15] Bertoli E, De Carlo E, Del Conte A, et al. Acquired resistance to osimertinib in EGFR-mutated non-small cell lung cancer: how do we overcome it? Int J Mol Sci. 2022:23(13).
[16] Lim SM, Kim CG, Cho BC. Antibody-Drug Conjugates: A New Addition to the Treatment Landscape of EGFR-Mutant Non-Small Cell Lung Cancer. Cancer Research. 2022;82(1):18-20.
[17] Gomatou G, Syrigos N, Kotteas E. Osimertinib resistance: molecular mechanisms and emerging treatment options. Cancers. 2023:15(3).
[18] Pasi A. Jänne, et al. Trastuzumab deruxtecan (T-DXd) in patients with HER2-mutant metastatic non–small cell lung cancer (mNSCLC): Final analysis results of DESTINY-Lung02. 2024 ASCO Abs 8543.
[19] Sands Jacob, Ahn Myung-Ju, Lisberg Aaron, et al. Datopotamab Deruxtecan in Advanced or Metastatic Non-Small Cell Lung Cancer With Actionable Genomic Alterations: Results From the Phase II TROPION-Lung05 Study.[J] .J Clin Oncol, 2025 Jan 6:JCO2401349.
[20] Zhang L, et al. ASCO 2025. Abstract 8507.
[21] High P, Guernsey C, Subramanian S, Jacob J, Carmon KS. The Evolving Paradigm of Antibody-Drug Conjugates Targeting the ErbB/HER Family of Receptor Tyrosine Kinases. Pharmaceutics. 2024;16(7):890.
[22] Yu HA, Goto Y, Hayashi H, et al. HERTHENA-Lung01, a phase II trial of patritumab deruxtecan (HER3-DXd) in epidermal growth factor receptor-mutated non-small-cell lung cancer after epidermal growth factor receptor tyrosine kinase inhibitor therapy and platinum-based chemotherapy. J Clin Oncol. 2023:41(35):5363-5375.











 苏公网安备32059002004080号
苏公网安备32059002004080号


