乳腺癌是女性最常见的恶性肿瘤。据世界卫生组织 GLOBOCAN[1]数据显示,全球乳腺癌年新发病例数从2018年的210万例增至2020年的226万例。在中国,2020 新发乳腺癌约1.6万例,高居女性恶性肿瘤的首位。其中,约70%的乳腺癌患者为激素受体(HR)阳性和人表皮因子生长受体2(HER2)阴性(HR+/HER2-)[2]。CDK4/抑制剂可通过与CDK4 和CDK6激酶的三磷酸腺苷(ATP)结合位点结合,抑制其活性,干扰网膜母细胞瘤(Rb)的磷酸化,阻断细胞周期从G1 期到S 期的进程,抑制肿瘤细胞增殖。此外,CDK4/6 抑制剂还能抑制上游雌激素受体信号通路的表达,与内分泌治疗之间存在协同效作用。迄今为止,已有5种CDK4/6抑制剂获批上市。国内外权威指南一致推荐 CDK4/6抑制剂联合芳香化酶抑制剂(AI)用于HR+/HER2-晚期乳腺癌一线治疗。然而,随着学界的不断探索,CDK4/6抑制剂于早期乳腺癌辅助治疗领域的研究也相继报阳,为HR+乳腺癌打开了全新治疗格局。
瑞波西利亮眼OS引领HR+乳腺癌晚期一线治疗
传统内分泌治疗是 HR+/HER2-乳腺癌的治疗基石,但几乎所有患者都会出现获得性耐药。CDK4/6抑制剂的出现,为HR+/HER2-晚期乳腺癌患者的临床治疗带来了革命性的转变。研究发现,联合CDK4/6抑制剂和内分泌治疗可克服或延缓内分泌抵抗的发生,延长晚期乳腺癌患者的生存时间,开启了HR+/HER2-晚期乳腺癌治疗的全新纪元。多项临床研究[3-5]证实,CDK4/6抑制剂联合内分泌治疗相比内分泌单药治疗可显著延长HR+/HER2-晚期乳腺癌患者的无进展生存期(PFS)。目前,CDK4/6抑制剂联合内分泌治疗已受到国内外主流指南的推荐,作为HR+晚期乳腺癌的标准一线治疗方案。
然而,并非所有CDK4/6抑制剂均能获得OS获益。瑞波西利无论在绝经前还是绝经后乳腺癌患者中均可显著延长OS,并改善患者生活质量,是国内首个在晚期乳腺癌一线治疗领域覆盖绝经前/围绝经期、绝经后人群的CDK4/6抑制剂:
对于绝经前乳腺癌患者,MONALEESA-7研究是首个且目前唯一专注于绝经前/围绝经期HR+晚期乳腺癌患者的大型III期研究,填补了完全针对晚期绝经前HR+乳腺癌领域CDK4/6i相关研究的空白。该研究全部纳入绝经前/围绝经期乳腺癌患者,评估瑞波西利联合内分泌治疗的获益,并证实了瑞波西利可为绝经前患者带来总生存和生活质量双重获益——研究结果显示,瑞波西利具有显著的抗肿瘤活性,瑞波西利组病灶可测量人群的客观缓解率(ORR)达50.9%、临床获益率(CBR)达79.9%,72%的患者8周即可快速缩瘤[6]。而且,瑞波西利的生存获益显著:与安慰剂组相比,瑞波西利组的中位PFS达到近2年,疾病进展或死亡风险降低45%[6];中位OS约5年,死亡风险降低24%[6]。
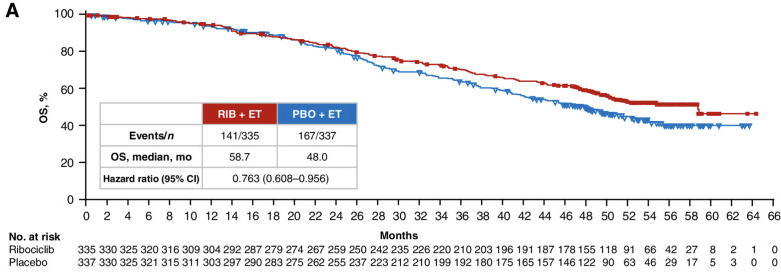
而对于绝经后HR+晚期乳腺癌患者,MONALEESA-2研究对瑞波西利联合内分泌药物作为一线治疗方案的疗效和安全性进行了探索,同样取得了积极结果。研究显示中位OS达到了63.9个月,与安慰剂组相比,OS延长超过12个月,相对死亡风险降低24%[7]。MONALEESA-2是绝经后人群中首个带来OS阳性结果的CDK4/6抑制剂III期临床研究。
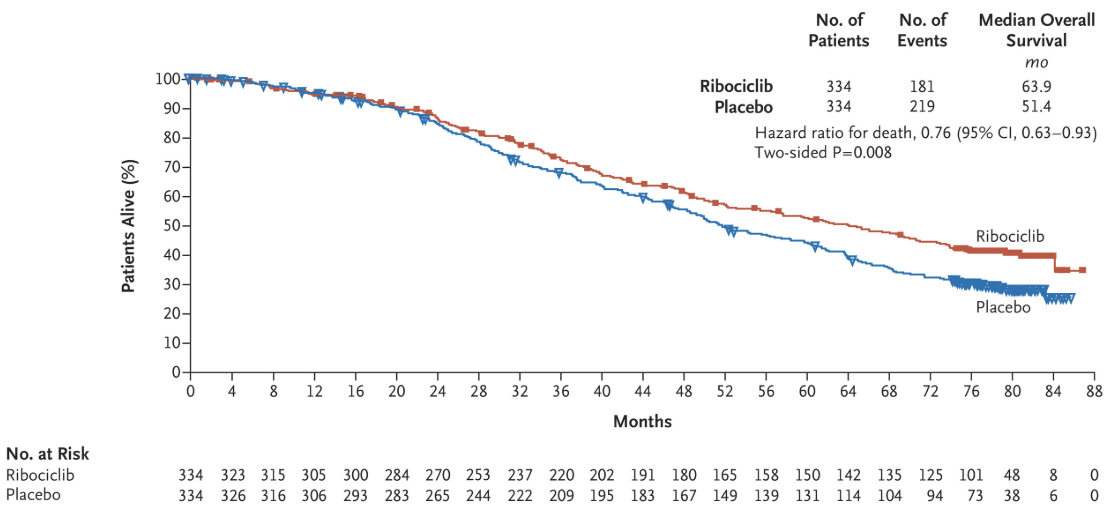
基于显著的疗效获益,NCCN指南中将瑞波西利联合AI一线治疗作为HR+/HER2-晚期乳腺癌1类推荐治疗方案。并且,凭借疗效显著且能改善患者生活质量的确切优势,瑞波西利成为唯一获得欧洲内科肿瘤学会临床获益量表(ESMO-MCBS)5分满分的CDK4/6抑制剂[8]。
至于 CDK4/6 抑制剂进展后的治疗策略,目前仍处在探索阶段,还需收集大量且更为长期的生存疗效数据,找到可靠的预测性生物指标,建立基于生物标志物的更为精准的治疗策略,从而对 CDK4/6抑制剂耐药后患者的治疗选择做出更清晰的指引。
早期强化治疗新篇:CDK4/6抑制剂对HR+早期乳腺癌的探索照入现实
HR+/HER2-早期乳腺癌的复发高峰在术后2~3年内[9],而经过5年的辅助内分泌治疗后, 远期复发的比例仍可达10%~41%[10]。因此,辅助治疗阶段的强化对于降低复发风险、提高患者远期生存率至关重要。近年来,无论是内分泌治疗药物的优化,还是卵巢功能抑制(OFS)的联合应用,抑或是辅助内分泌治疗的延长,均改善了患者的预 后。其中于近期落幕的2025 ASCO大会中,SOFT/TEXT研究经过15年随访后公布的最新疗效数据,以及ASTRRA研究关于淋巴结阳性患者联合2年OFS治疗效果的验证,这些结果均进一步巩固了OFS在绝经前HR+/HER2-乳腺癌患者中的治疗地位。
此外,CDK4/6抑制剂的加入更是为HR+/HER2-早期乳腺癌的治疗带来了突破——MonarchE研究与NATALEE研究,及2025 ASCO年会上亮相的DAWNA-A研究均提示了CDK4/6抑制剂在HR+早期乳腺癌患者中联合内分泌治疗的获益。其中,DAWNA-A研究中达尔西利于HR+早期乳腺癌辅助治疗领域尚未获批。
monarchE研究纳入了临床病理分期高危的HR+/HER2-早期乳腺癌患者,包括腋窝淋巴结≥4个阳性,或1-3个阳性腋窝淋巴结且T≥5cm/组织学分级为G3/Ki67≥20%的HR+/HER2-早期高危乳腺癌患者。结果显示,阿贝西利联合SERM/AI药物辅助治疗2年,可为HR+/HER2-早期高危乳腺癌患者带来iDFS获益,但其OS数据仍不成熟[11]。
相比于monarchE研究,NATALEE研究纳入了广泛Ⅱ-Ⅲ期HR+/HER2-早期乳腺癌患者,包括所有淋巴结阳性,以及淋巴结阴性伴有高危因素(N0且T3/T4,或N0且T2合并G3/G2且Ki-67≥20%/G2且多基因检测高复发风险)的早期乳腺癌患者[12]。中国国家癌症中心数据显示,符合NATALEE试验条件患者的复发风险是不符合NATALEE试验条件患者的3倍(5年rwiDFS:81.37% vs. 93.37%,HR=3.03,P<0.0001)[13]。NATALEE研究阳性成果的披露可为更多HR+/HER2-早期乳腺癌患者带来生存获益,提供辅助强化治疗新选择。结果显示,瑞波西利联合AI可显著降低意向治疗(ITT)人群28.5%的复发风险,瑞波西利联合AI辅助治疗3年后,iDFS获益持续扩大,4年iDFS绝对获益达4.9% [12]。当前瑞波西利联合AI的OS数据尚未成熟,但已显示出获益趋势,且积极趋势持续存在[12,14]。
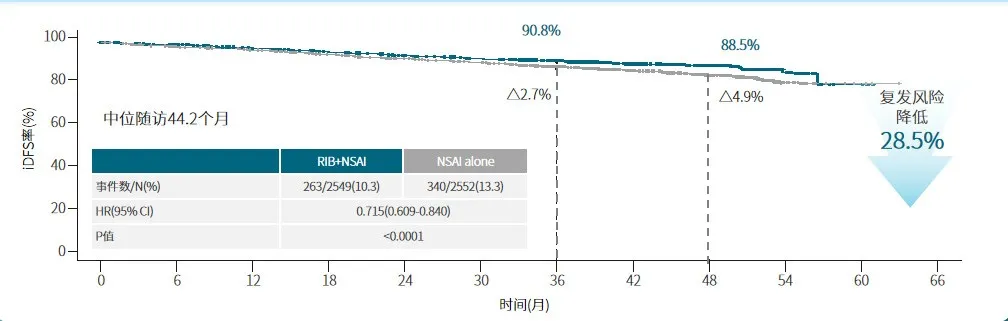
此次2025 ASCO大会上,进一步公布了NATALEE研究*基于绝经状态和年龄分层的数据,研究提示,无论患者的年龄或绝经状态如何,瑞波西利联合内分泌治疗都能带来一致的获益。这提示我们在临床实践中,对于符合临床研究入组标准的患者,应为其提供更优的早期强化辅助治疗机会。
小结
作为近十年来乳腺癌治疗领域最亮眼的创新药物之一,CDK4/6抑制剂在晚期乳腺癌治疗领域展现出显著疗效优势。以瑞波西利为例,该药物可用于HR+/HER2-乳腺癌晚期一线治疗,是目前唯一在绝经前、围绝经期及绝经后患者群体中均表现出 PFS和OS获益的CDK4/6抑制剂。基于其在晚期乳腺癌治疗中取得的疗效,研究者们将CDK4/6抑制剂治疗前移,在HR+/HER2-早期乳腺癌的辅助治疗领域开展深入探索,旨在与内分泌治疗协同作用,进一步降低患者的复发风险。展望未来,CDK4/6抑制剂研究成果的临床应用必将进一步推动乳腺癌诊疗水平的全面提升,为更多、更广泛的HR+乳腺癌患者带来治疗希望与生存获益。
*NATALEE试验ITT人群,入组标准为:1)所有淋巴结阳性;2)淋巴结阴性合并T3/T4;3)淋巴结阴性且肿瘤大小2-5cm合并G3,G2且Ki-67≥20%,或基因检测高危
[1] Sung H,Ferlay J,Siegel RL,et al. Global cancer sta- tistics 2020:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries [J]. CA Cancer J Clin,2021,71(3):209-249.
[2] 国家肿瘤质控中心乳腺癌专家委员会,中国抗癌协会肿瘤药物临床研究专业委员会 . CDK4/6 抑制剂治疗激素 受体阳性人表皮生长因子受体 2 阴性晚期乳腺癌的临床 应用共识 [J]. 中华肿瘤杂志,2021,43(4):405-413.
[3]Ribociclib as first-line therapy for HR-positive, advanced breast cancer[J]. N Engl J Med, 2018, 379(26): 2582.
[4] FINN R S, MARTIN M, RUGO H S, et al. Palbociclib and letrozole in advanced breast cancer[J]. N Engl J Med, 2016, 375(20): 1925-1936.
[5] GOETZ M P, TOI M, CAMPONE M, et al. MONARCH 3:abemaciclib as initial therapy for advanced breast cancer[J].J Clin Oncol, 2017, 35(32): 3638-3646.
[6] Yen-Shen Lu, et al. Updated Overall Survival of Ribociclib plus Endocrine Therapy versus Endocrine Therapy Alone in Pre- and Perimenopausal Patients with HR+/HER2- Advanced Breast Cancer in MONALEESA-7: A Phase III Randomized Clinical Trial.Clin Cancer Res. 2022 Mar 1;28(5):851-859.
[7]Gabriel N Hortobagyi , Salomon M Stemmer , Howard A Burris, et al. Overall Survival with Ribociclib plus Letrozole in Advanced Breast Cancer.N Engl J Med. 2022 Mar 10;386(10):942-950. doi: 10.1056/NEJMoa2114663.
[8]https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs-for-solid-tumours/esmo-mcbs-scorecards?mcbs_score_cards_form%5BsearchText%5D=ribociclib.
[9] SHEFFIELD K M, PEACHEY J R, METHOD M, et al. A real-world US study of recurrence risks using combined clinicopathological features in HR-positive, HER2-negative early breast cancer[J]. Future Oncol, 2022, 18(21): 2667- 2682.
[10] PAN H C, GRAY R, BRAYBROOKE J, et al. 20-year risks of breast-cancer recurrence after stopping endocrine therapy at 5 years[J]. N Engl J Med, 2017, 377(19): 1836-1846.
[11] Rastogi P, et al. J Clin Oncol 2024; 42(9):987-993.
[12] Peter A. Fasching, et al, 2024 ESMO, LBA13
[13] Li Q, Jiang M, Liu J, et al. The Breast, 2025, 80.
[14] Gabriel N. SABCS 2023, GS03-03.
排版编辑:肿瘤资讯-CYX











 苏公网安备32059002004080号
苏公网安备32059002004080号


