肺癌是全球癌症死亡的主要原因之一,非小细胞肺癌(NSCLC)占肺癌的大多数。目前,NSCLC 的治疗已经从传统的化疗发展到根据特定基因突变进行靶向治疗的时代。MET异常是NSCLC的关键驱动基因之一,MET 14号外显子(METex14)跳跃突变发生在约3-4%的NSCLC患者中[1]。针对该靶点的抑制剂开发为患者带来了新的希望,其中,卡马替尼作为一款高选择性MET抑制剂,在临床研究中展现了卓越的疗效与安全性,已成为METex14跳跃突变NSCLC治疗的重要药物。近期,中山大学肿瘤防治中心的李苏教授团队在Translational Lung Cancer Research发表了题为“The pharmacokinetics of capmatinib and its efficacy in non-small cell lung cancer treatment: a narrative review”的综述(doi: 10.21037/tlcr-2025-700),从药代动力学(PK)角度,深入剖析了卡马替尼优异临床表现背后的药理学基础。【肿瘤资讯】特邀中山大学肿瘤防治中心赵洪云教授,从临床医生的视角对该研究进行深度点评。
二级主任医师,博士生导师
中山大学肿瘤防治中心抗肿瘤新药I期病房主任,临床研究部副主任
广东省临床医学学会肺癌精准治疗及临床研究专委会主任委员
中国抗癌协会肿瘤药物临床研究专业委员会青年委员会副主任委员
中国抗癌协会肿瘤药物临床研究专业委员会常委
广东省抗癌协会化疗专业委员会青年委员会副主任委员
《健康中国2030》—肿瘤健康之“肺癌规范化诊疗”项目组专家顾问
教育部重点实验室、华南恶性肿瘤防治全国重点实验室PI,中山大学肿瘤防治中心高层次人才特殊支持计划“临床医学科学家”,广东省杰出青年医学人才,岭南名医,羊城好医生;在Nature medicine、Lancet Oncology 、Cancer cell、STTT、 JHO、CMI、JTO、Cell reports medicine等杂志发表SCI论文八十余篇;主持四项国家自然科学基金和一项广州市重点研发计划项目
文献解读
该综述纳入了2010年6月至2025年2月期间发表或公布的关于MET抑制剂在NSCLC中应用的文献,检索范围包括PubMed和外文医学信息资源检索平台(FMRS)公布的内容,也涵盖多个国际会议的发表内容,包括欧洲肺癌会议(ELCC)、美国癌症研究协会(AACR)年会、美国临床肿瘤学会(ASCO)年会、世界肺癌大会(WCLC)、欧洲肿瘤内科学会(ESMO)年会以及ESMO亚洲会议。基于检索获得的关键文献,该综述全面对比了卡马替尼与其他Ib型MET抑制剂(特泊替尼、赛沃替尼、谷美替尼)的PK特性及临床数据。
吸收与暴露
在多种MET抑制剂中,卡马替尼的吸收速度快,达峰时间(Tmax)仅为1.09–1.87小时,而特泊替尼为8.0小时,赛沃替尼为2.0–4.0小时,谷美替尼为4.0小时(表1)。卡马替尼的血药浓度峰值(Cmax)和曲线下面积(AUC)均处于较高水平,且稳态卡马替尼的AUC和Cmax在每日两次(BID)100至600mg的剂量范围内通常与剂量成比例,这确保了充分的药物暴露。
表1 MET抑制剂的PK参数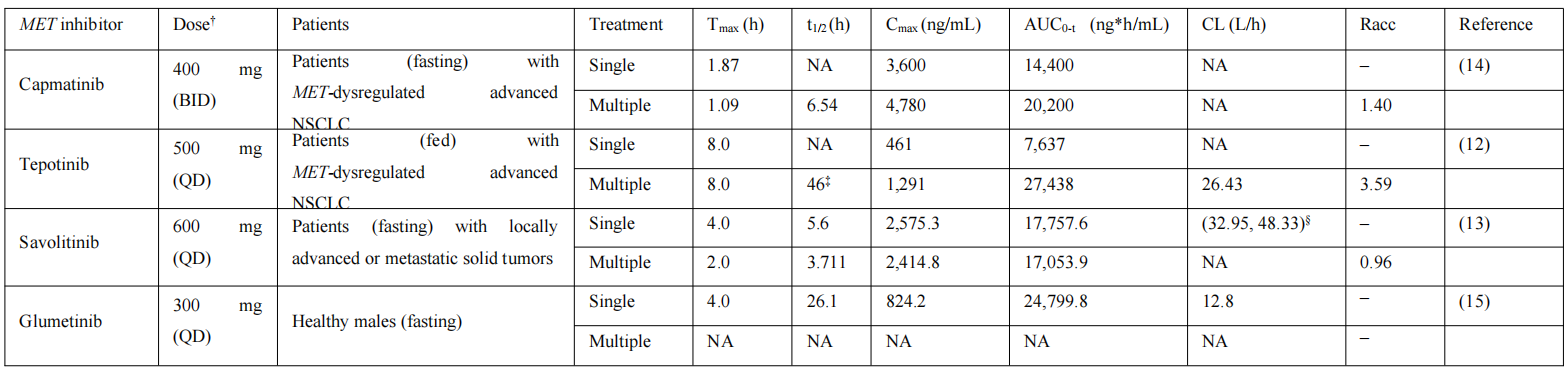
卡马替尼对METex14突变的半数最大抑制浓度(IC50)为0.6 nmol/L,体外抑制活性强,其他MET抑制剂的IC50分别为3.0 nmol/L(特泊替尼)、2.1 nmol/L(赛沃替尼)和2.45 nmol/L(谷美替尼)(表2)。快速吸收与强效抑制的结合,使卡马替尼能在短时间内达到有效治疗浓度,这是其临床快速起效的药理学基础。
表2 MET抑制剂的IC50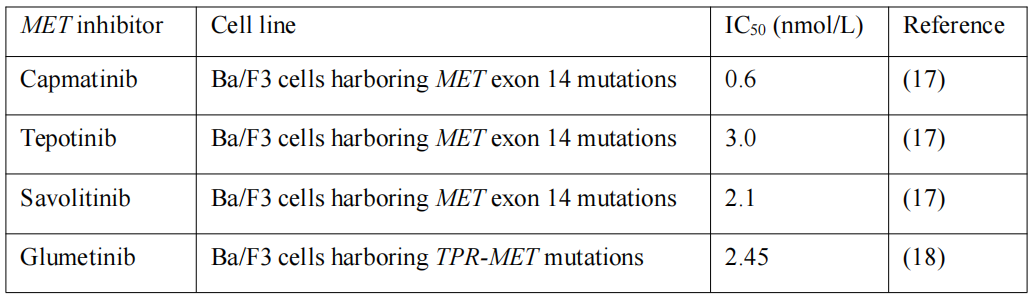
代谢与清除
MET抑制剂主要通过肝脏代谢,卡马替尼、特泊替尼、赛沃替尼和谷美替尼主要通过细胞色素P450(CYP)3A4和醛氧化酶代谢。研究表明,在轻度、中度和重度肝功能不全的受试者中均可适用,且无需调整剂量,表现出良好的耐受性。在空腹条件下,卡马替尼和赛沃替尼代谢迅速,多次给药后的半衰期(t1/2)分别为6.54和3.711小时。特泊替尼和谷美替尼的消除半衰期相对较长,约为1至2天(表1)。卡马替尼和赛沃替尼在人体内清除也快,卡马替尼、特泊替尼、赛沃替尼和谷美替尼的清除率分别为30.0–121 L/h、26.43 L/h 、32.95–48.33 L/h和12.8 L/h。此外,卡马替尼的蓄积比(Racc)低至1.40,表明其在连续给药后不易在体内过度蓄积,长期用药安全性高。
药物服用便利
食物摄入很可能改变许多抗肿瘤药物的PK,进而影响其安全性。 因此,评估食物和脂质摄入对新药PK的影响至关重要。食物对卡马替尼的生物利用度影响很小,随餐服用卡马替尼不会显著影响其暴露。而进食会影响特泊替尼、赛沃替尼和谷美替尼的药物暴露量。因此,临床上特泊替尼需与食物同服,赛沃替尼需要餐后即刻服用,谷美替尼在服药前至少2小时和用药后1小时内需禁食。在药物相互作用方面,卡马替尼无论是单药治疗还是与其他药物联合使用,都具有可控的安全性和疗效。
颅内渗透性
高达40%的NSCLC患者在病程中会发生脑转移,这类患者的预后较差,药物能否有效穿透血脑屏障(BBB)是决定颅内疗效的关键。卡马替尼药物化学结构中专门设计了用于选择性靶向MET的“DFG-in”构象,并通过π-π相互作用强效结合残基Y1230,良好的脂溶性、与血浆蛋白的高结合率以及被动渗透性,抑制P-gp/BCRP外排,使其能有效穿越血脑屏障治疗脑转移病灶。
专家点评
MET抑制剂的问世为METex14突变NSCLC患者带来了突破性的治疗进展。目前,已有多款同类药物获批上市,为MET变异的NSCLC患者提供了新的治疗选择。这篇综述对于临床医生的用药选择非常具有参考价值,该篇综述回归到药物的本质——药代动力学,揭示了MET抑制剂优越疗效的底层逻辑。从临床医生的角度看,一个药物优异的药代动力学特性,是其在真实世界中能否被患者长期、安全、方便地使用,并最终实现生存获益的基石。
临床上,许多晚期肺癌患者初诊时症状较重,亟需快速有效的治疗来控制病情。卡马替尼“Tmax短”(快速吸收)和“IC50低”(强效抑制)的特点,意味着药物口服后能迅速达到并维持有效的血药浓度来强力抑制肿瘤。这与其在GEOMETRY mono-1全球关键研究[2,3]中观察到的高效、快速、持久的缓解高度契合:卡马替尼一线治疗起效迅速,至缓解时间(TTR)为1.4个月,68.4%的患者在首次疗效评价时即出现肿瘤退缩。此外,卡马替尼一线治疗的客观缓解率(ORR)高达68.3%,疾病控制率(DCR)高达98.3%,中位无进展生存期(mPFS)达12.5个月,中位总生存期(mOS)达21.4个月,疗效远超传统化疗。卡马替尼的优异疗效在针对中国患者的GeoMETry-C研究[4]中进一步得到证实。此外,患者报告结局(PRO)研究[5]补充验证了卡马替尼的临床疗效,在接受卡马替尼治疗后的第7周患者咳嗽症状显著改善,在后续随访观察中,尤其在达到临床完全缓解(CR)或部分缓解(PR)的患者中,QLQ-LC13症状在所有周期均得到了改善,并延缓了咳嗽、胸痛等肺部症状的最终恶化时间(TTDD)。这种“快而强”的特性,对于需要尽快缓解症状、控制肿瘤进展的患者而言,意义重大。
靶向治疗是一个长期管理的过程,药物的安全性直接决定了患者能否坚持治疗并从中持续获益。卡马替尼清除快、蓄积风险低(Racc=1.40),这意味着由药物过度蓄积引发的慢性毒性风险更低,为患者的长期用药提供了更高的安全保障。在GEOMETRY mono-1研究中,最常见的不良事件为外周性水肿和恶心,且多为低级别、可管理。GEOMETRY-C研究也进一步证实,卡马替尼在中国人群中的安全性相较于全球人群更优,绝大多数不良反应为1-2级,所有级别外周水肿发生率为26.7%,ALT升高发生率为20%[4],无因AE导致的停药。2024年WCLC公布一项匹配调整间接比较(MAIC)显示[6],无论在全球人群还是亚洲人群中,卡马替尼相比于其他MET抑制剂有更低的TRAE发生风险,相比赛沃替尼、特泊替尼、谷美替尼,卡马替尼TRASE发生风险分别降低了11.4%、11.1%和12.6%(P<0.05)。多个真实世界研究[7-11]也证实了其在临床实践中良好的耐受性,使其成为患者可以长期信赖的治疗选择。
除了疗效和安全性,卡马替尼在临床应用上的巨大便利性也非常值得关注。首先,轻度、中度和重度肝功能不全的患者均可适用且无需调整剂量,这在临床实践中是一个巨大的优势。NSCLC患者,特别是老年患者,常常合并各种基础疾病或因肿瘤本身导致肝功能异常。无需因肝功能调整剂量,不仅极大地简化了医生的处方决策,更从根本上提升了这类特殊人群的用药安全性。其次,卡马替尼的服用不受食物摄入的显著影响。这一点看似微小,却直接关系到患者的用药依从性和生活质量。正是基于这些明确的临床优势和坚实的循证数据,卡马替尼最早于2020年就已被《NCCN非小细胞肺癌诊疗指南 》纳为METex14跳突变晚期NSCLC一线治疗的优先推荐,并获得《CSCO非小细胞肺癌诊疗指南2025》治疗IV期METex14跳跃突变NSCLC的I级推荐,成为全球公认的标准治疗方案。
此外,脑转移是NSCLC治疗中的“老大难”问题,预后极差。卡马替尼卓越的颅内渗透能力和在临床研究中得到验证的确切颅内疗效,使其成为伴有脑转移的METex14突变NSCLC患者的优选方案。GEOMETRY mono-1研究中,共纳入了28例基线有可评估脑转移病灶患者(包括接受过颅内放射治疗的13例和未接受颅内放射治疗的15例),总体颅内ORR为57%,颅内CR率32%,在未接受过颅内放射治疗的患者中,颅内ORR为67%,颅内CR率33.3%。在纳入中国患者的GeoMETry-C研究中,初治脑转移患者的颅内CR率高达50%,颅内DCR更是达到了100%。在一项纳入68例METex14跳突并伴有脑转移的NSCLC患者的美国真实世界研究显示[11],接受卡马替尼一线治疗的患者(N = 55)的全身rwORR为90.9%,颅内rwORR为87.3%,颅内DCR为96.4%,中位全身rwPFS为14.1个月,全身及颅内疗效同样优于以IO为基础的治疗方案。一篇卡马替尼的病例文章更印证了卡马替尼卓越的颅内疗效[12]。该例晚期METex14 跳跃突变NSCLC脑转移患者接受卡马替尼治疗后取得了显著的颅内缓解,即使存在往往预后不佳的脑膜转移,患者的颅内转移灶也几乎完全消失(图1)。此外,值得关注的是,该例患者在最初的常规分子检测未发现常见靶向治疗的靶点,而后续的血液基因检测成功检出METex14 跳跃突变,这也为患者的靶向治疗提供了有力的证据。这些数据为临床医生治疗这一最具挑战性的患者亚群提供了强有力的武器和信心。
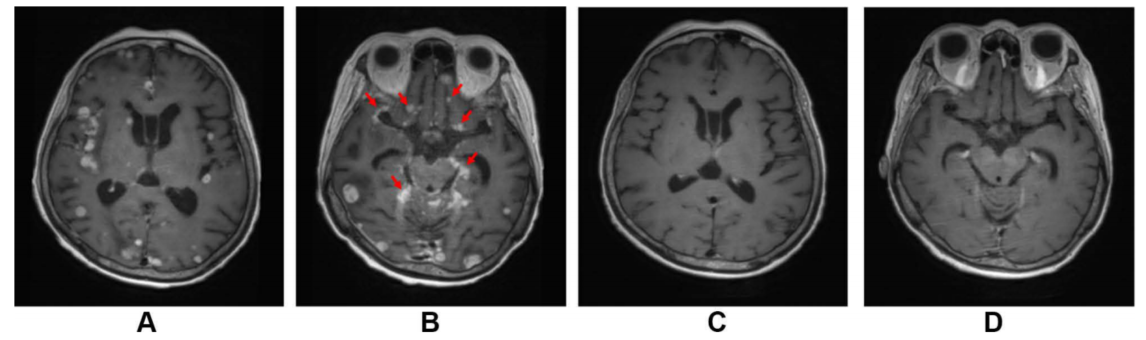
图1 METex14 跳跃突变NSCLC伴脑转移患者在卡马替尼治疗前后的脑MRI
(A) 治疗前:多发脑实质转移灶;(B) 治疗前:软脑膜转移(箭头所示);(C, D) 治疗后:脑实质及软脑膜转移灶几乎完全消失。
总而言之,卡马替尼凭借其吸收迅速、抑瘤活性强、临床疗效确切、安全性高(蓄积风险低、轻度、中度和重度肝功能不全患者均适用且无需调量)食物影响小,以及对脑转移病灶疗效优异等多重优势,已成为METex14跳跃突变NSCLC领域全球权威指南一致推荐的标准治疗。这些PK优势所构成的坚实药理学证据,为临床医生在制定个体化精准治疗方案时,提供了更为清晰和坚定的指引。
[1] Subramanian J, et al.. Expert Rev Anticancer Ther 2021; 21: 877-86.
[2] Wolf, Jürgen et al. The Lancet Oncology, 2024, Volume 25, Issue 10, 1357-1370.
[3] J. Wolf ,et al.. 2022 ELCC 26P .
[4] Yi-Long Wu, et al. 2022 ESMO AISA, 388P.
[5] Jurgen Wolf et al. Eur J Cance. 2023 Apr:183:98-108.
[6] Yi-Long Wu, et al. 2024 WCLC EP.12D.05.
[7] Ferreira M, et al.. Lung Cancer. 2024 Oct;196:107934.
[8] Illini O, et al. Ther Adv Med Oncol. 2022 Jun 13;14:17588359221103206
[9] Choi W, et al. Cancer Res Treat. 2021 Oct;53(4):1024-1032.
[10] Furqan M,et al. Future Oncol. 2024;20(22):1553-1563.
[11] Paik PK, et al. Future Oncol. 2023 Jan;19(3):217-228.
[12] Kim TW, et al. Onco Targets Ther. 2022 Aug 31;15:941-946.
审批码TAB0052088-109569,有效期为2025-08-14至2026-08-13,资料过期,视同作废
排版编辑:肿瘤资讯-CYX











 苏公网安备32059002004080号
苏公网安备32059002004080号


